
肝内胆管癌是原发性肝癌中恶性程度较高、治疗较困难、预后较差的一种类型,其发病率仅次于肝细胞癌,约占原发性肝癌的10%~15%[1,2]。肝切除术是较早期肝内胆管癌的有效且首选的治疗方法[1]。然而,大多数肝内胆管癌患者确诊时已处于晚期,缺乏有效治疗手段;即便是有机会实施根治性手术的患者,术后也极易复发和转移[1]。在此背景下,通过化疗、靶向治疗、免疫治疗等联合治疗策略实现降期转化手术,以及通过术后辅助治疗延缓肿瘤复发,成为了改善肝内胆管癌患者生存的关键和研究热点[1-3]。本期由郑州大学第一附属医院宗可医生为大家分享并解读一则病例,该病例为替雷利珠单抗联合GEMOX化疗(吉西他滨+奥沙利铂)成功转化治疗合并门静脉癌栓的IIIB期肝内胆管癌的真实案例,患者手术达到R0切除,实现病理学完全缓解(pCR),术后继续在系统化疗基础上(吉西他滨+替吉奥)采用替雷利珠单抗进行免疫治疗,目前该患者无复发生存期(RFS)已超18个月。
指导专家
肝胆胰外科(5)负责人
郑州大学第一附属医院
郑州大学第一附属医院
南院区肝胆胰外科负责人
教授、主任医师、外科学博士
分享专家
肝胆胰外科 主治医师
郑州大学第一附属医院
外科学博士
郑州大学第一附属医院肝胆胰外科 主治医师
中国医促会转移性肿瘤分会 委员
河南省医学会肠内肠外营养分会 秘书
研究方向为肝胆胰外科疾病的微创和转化治疗
病例详情
01基本情况
患者男性,62岁。
主诉:纳差1月余,腹胀10天。
现病史:患者于1月余前无明显诱因下出现纳差,未重视未治疗,10天前无明显诱因下出现进食后腹胀,无腹痛、发热、皮肤黏膜黄染,无胸痛、胸闷等,期间未治疗,我院行CT示:1.肝内占位,肝细胞癌?,肝右叶小结节,肝内转移?2.肝门部肿大淋巴结,考虑淋巴结转移。现患者一般情况可,今为求进一步诊治,门诊以“肝占位性病变”收入院。自发病以来,食欲正常,睡眠正常,大便稀,小便黄染,精神正常,体重下降2Kg。
既往史:无乙肝、酗酒等病史;余既往史无特殊。
体格检查:无特殊。
02辅助检查
肿瘤标志物:AFP:19.90 ng/mL,CEA:28.70 ng/mL,CA125:10.90 U/mL,CA19-9:116.00 U/mL。
余各项常规检查未见明显异常。
2021-06-17腹部 MRI示:1、肝左右叶交界区及尾状叶异常信号,考虑肝细胞癌,建议结合临床及病理;2、肝右前后叶异常信号,考虑转移;3、肝门部异常信号,考虑淋巴结转移;4、门静脉癌栓考虑。
 2021-06-17患者腹部MRI检查结果(治疗前),圆圈、箭头所示为占位病变
2021-06-17患者腹部MRI检查结果(治疗前),圆圈、箭头所示为占位病变
2021-06-27全腹增强CT示:1、肝内占位,肝细胞癌?肝右叶小结节,肝内转移?;2、肝门部肿大淋巴结,考虑淋巴结转移。
 2021-06-27全腹增强CT检查结果(治疗前),箭头所示为占位病变
2021-06-27全腹增强CT检查结果(治疗前),箭头所示为占位病变
病理检查:CT引导下肝占位穿刺活检提示:腺癌(全腹增强CT已排除消化道转移)。由此排除肝细胞癌,明确诊断为肝内胆管癌。
03临床诊断
肝内胆管癌(T2N1M0 IIIB,程式Ⅲ型PVTT)
04治疗经过
经全面评估患者病情,并经多学科会诊(MDT)讨论和患者及家属同意,制定总体治疗方案为:在基础化疗基础上,采取“靶向治疗+免疫治疗”的策略来积极转化治疗,以期降期后有机会实现R0切除;并给予术后辅助治疗来延缓肿瘤复发。
1、转化治疗阶段
制定转化治疗方案为:GEMOX(d1、d8 吉西他滨+d1奥沙利铂,21d)+替雷利珠单抗 200mg q3w+仑伐替尼 8mg qd,拟四药联合治疗6个周期后复查。
2021-09-10上腹部增强CT检查示:1、肝内占位并肝门部肿大淋巴结显示,多考虑恶性,较2021-06-27片肝内病灶及肝门淋巴结明显缩小,请结合临床进一步综合评估;2、肝右叶小结节,较前变化不大;3、肝胃间隙及腹膜后小淋巴结,较前相仿,建议随诊。

 治疗前(2021-06-27)、治疗6周期后(2021-09-10)CT影像检查对比,见瘤灶较前明显缩小
治疗前(2021-06-27)、治疗6周期后(2021-09-10)CT影像检查对比,见瘤灶较前明显缩小
2021-09-13上腹部增强MRI检查示:1、“肝内胆管癌化疗后”改变,对比2021-06-17片,肝左右叶交界区病变范围明显缩小,肝门部门静脉旁淋巴结较前缩小,请结合临床动态复查;2、老片门静脉癌栓此次检查显示不明确。


 治疗前(2021-06-17)、治疗6周期后(2021-09-13)MRI影像检查对比,见肝左右叶交界区瘤灶较前明显缩小,门静脉癌栓基本消失
治疗前(2021-06-17)、治疗6周期后(2021-09-13)MRI影像检查对比,见肝左右叶交界区瘤灶较前明显缩小,门静脉癌栓基本消失
经MDT讨论,认为患者转化治疗6周期后疗效评估为部分缓解(PR),目前有达到R1切除的可能,拟继续原方案化疗2周期后再评估。
在“GEMOX+替雷利珠单抗”转化治疗方案实施8个周期后,分别于2021-11-18和2021-11-19进行MRI和CT检查,结果显示:肿瘤缩小<30%,疗效评估为部分缓解(PR)。
 2021-11-18MR和2021-11-19CT检查结果,见病灶较前进一步缩小
2021-11-18MR和2021-11-19CT检查结果,见病灶较前进一步缩小
转化治疗期间肿瘤标记物变化趋势如下:
 转化治疗期间肿瘤标记物变化趋势图
转化治疗期间肿瘤标记物变化趋势图
MDT讨论认为目前有实施根治性手术达到R0切除的机会,拟择期安排手术切除肿瘤,术前停用靶向药物和免疫药物3周。
2、手术及术后辅助治疗阶段
于2021-11-22实施“左半肝切除术+胆囊切除术”,术中见肝脏呈奥沙利铂化疗后多发黑色点状改变。手术过程顺利,术中出血200mL,耗时约3h50min。
2021-11-23术后病理检查结果如下,见肿瘤细胞完全坏死,淋巴结检查(-),表明该患者达到了R0切除,病理疗效评估为pCR。
 左半肝切除术后送检标本病理报告结果
左半肝切除术后送检标本病理报告结果
术后第5天患者出现轻度胆漏,留置的引流管引流通畅。术后第11天准予患者带管出院。
术后1个月后复查CT证实胆漏已消失,遂拔除引流管
为遏制肿瘤复发,经病情评估,于术后6周开始给予“吉西他滨+替吉奥+替雷利珠单抗”进行术后辅助治疗。目前6个月的术后辅助治疗已结束,截至2023-05-21,影像学及实验室结果均未见肿瘤复发证据。
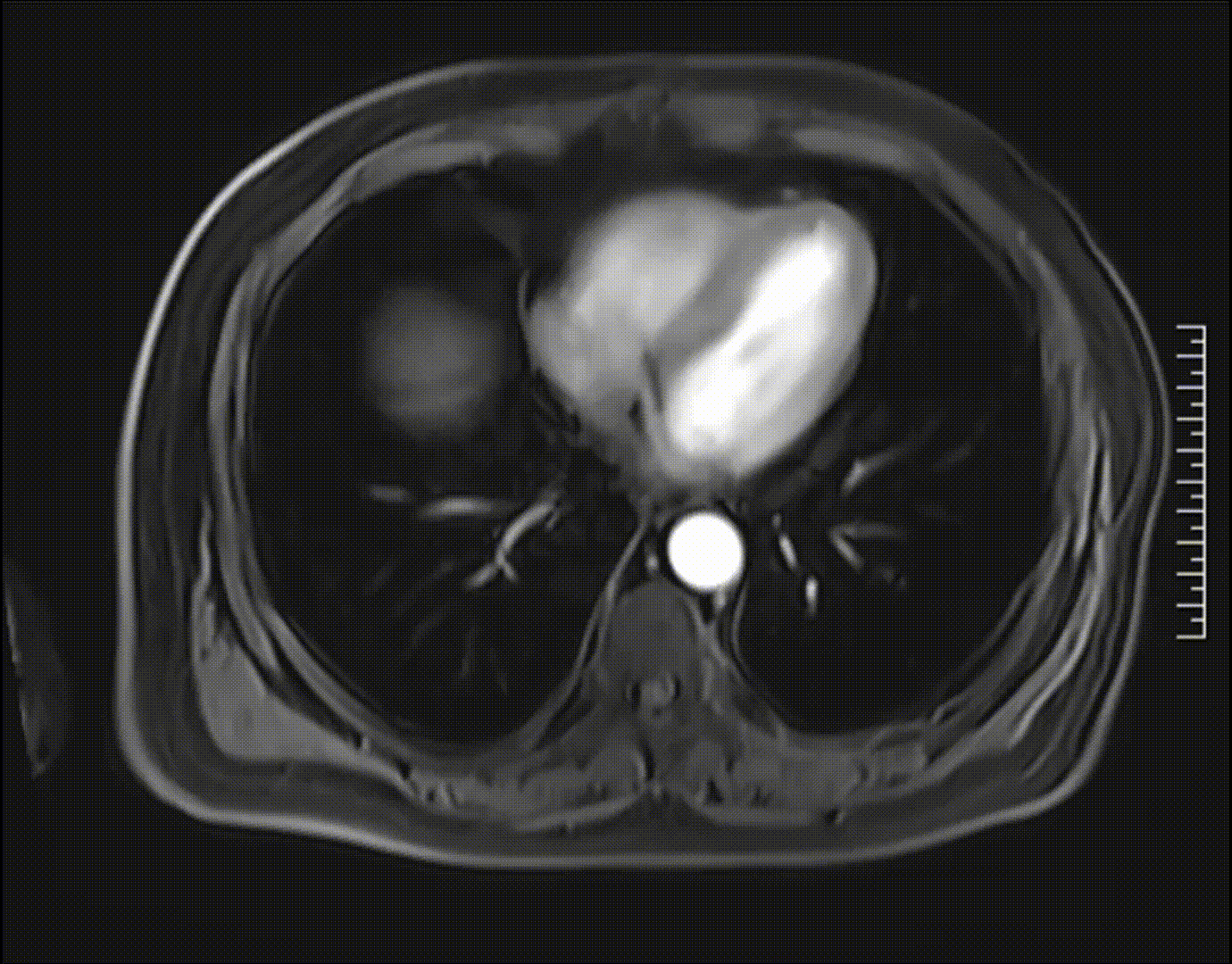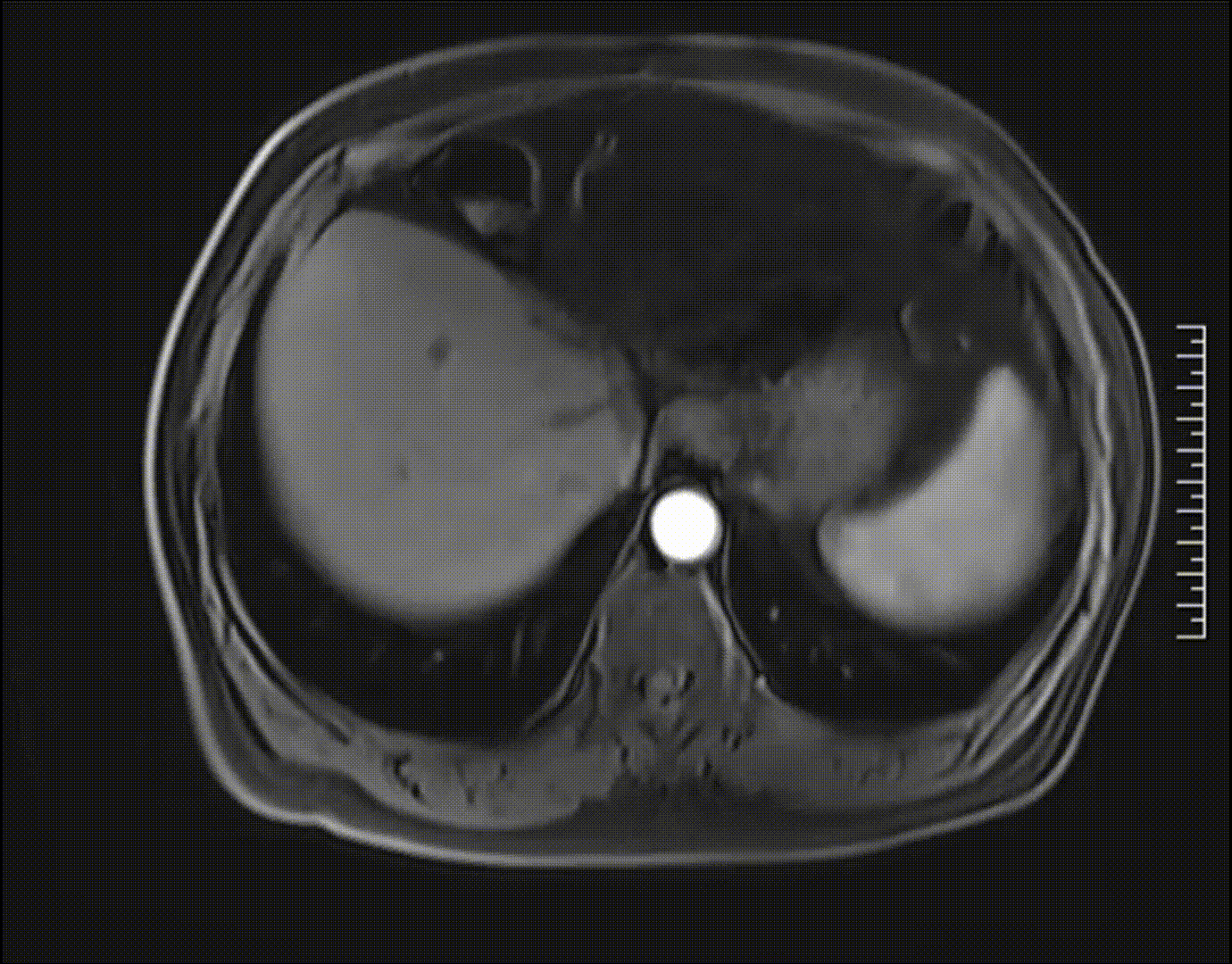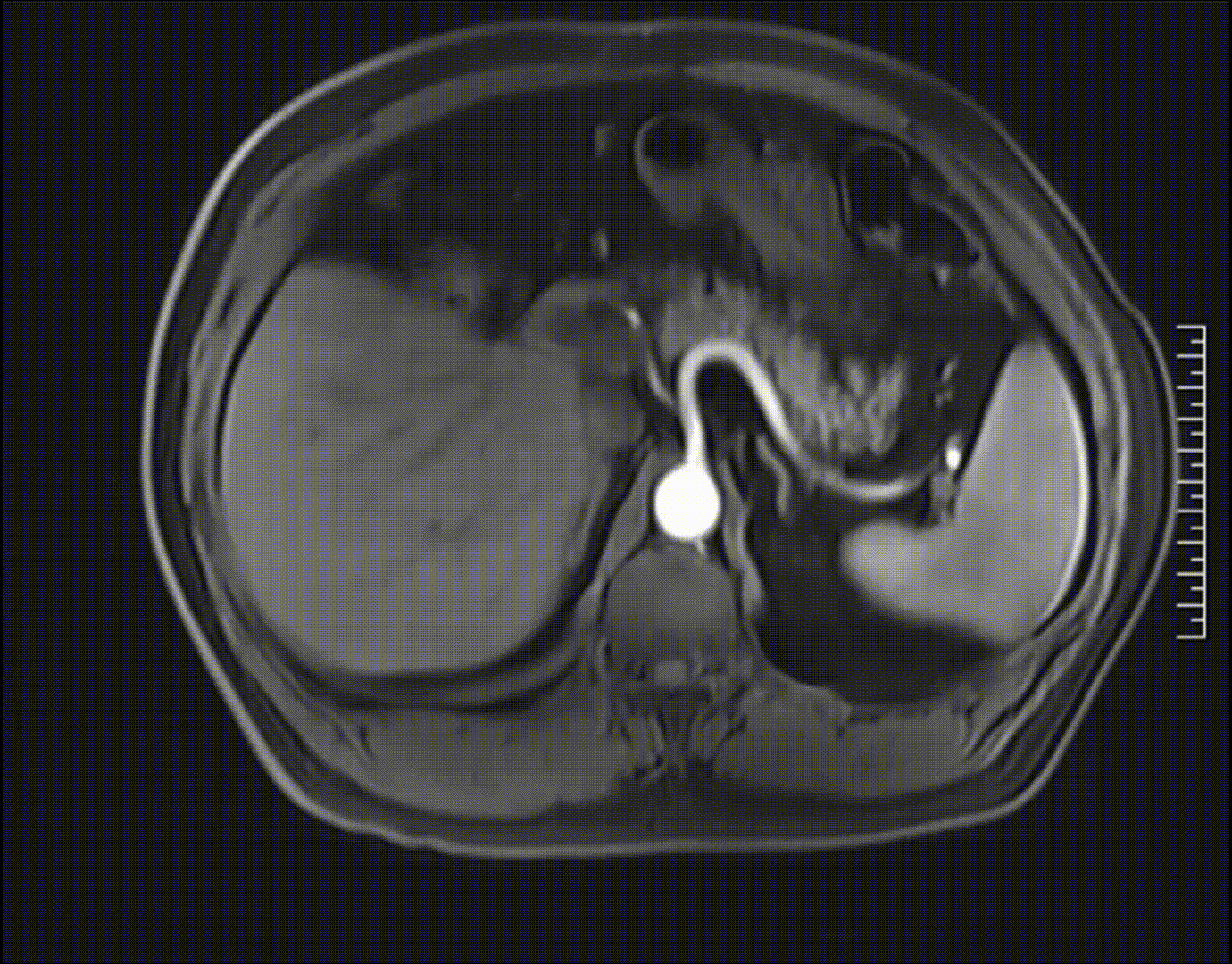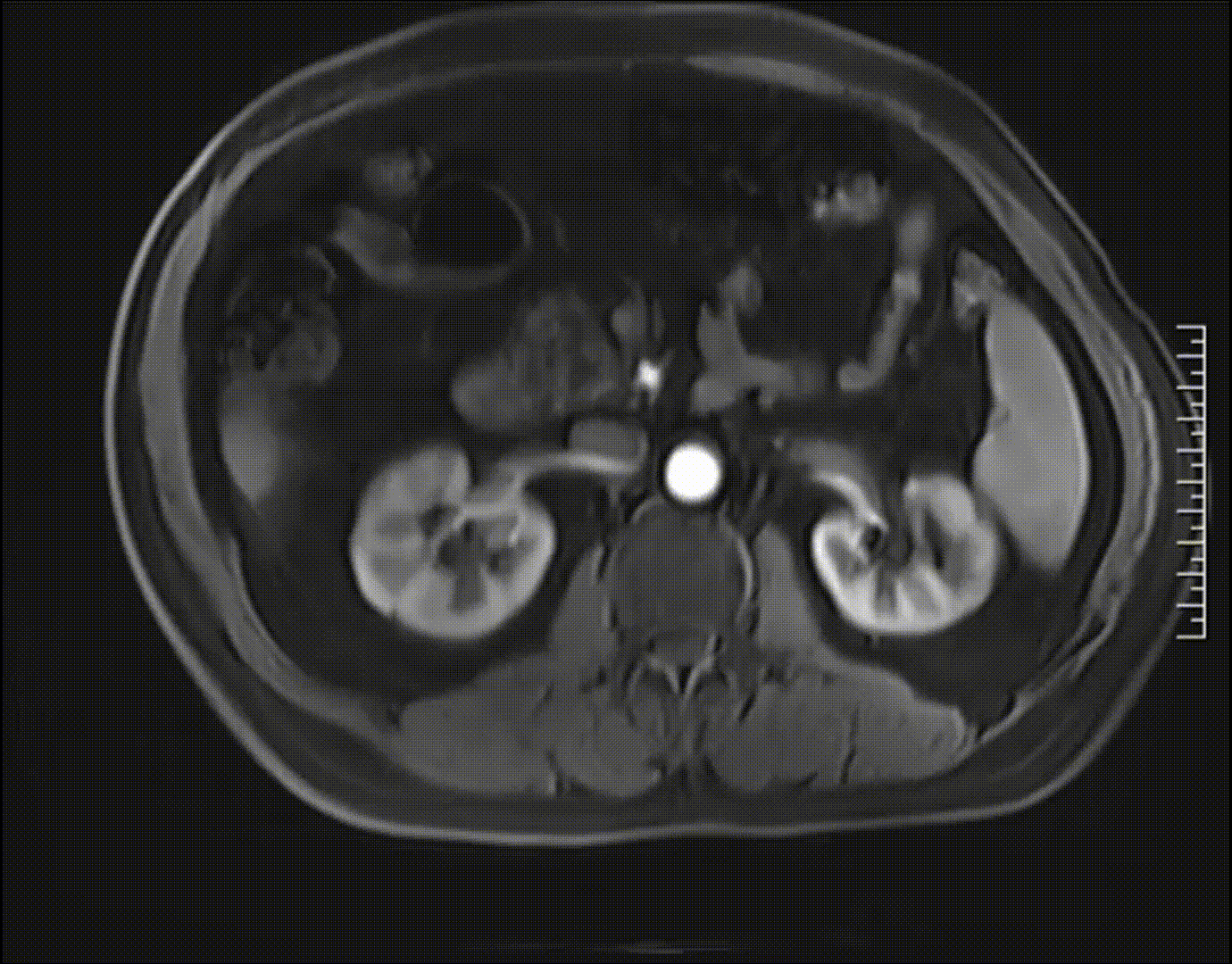

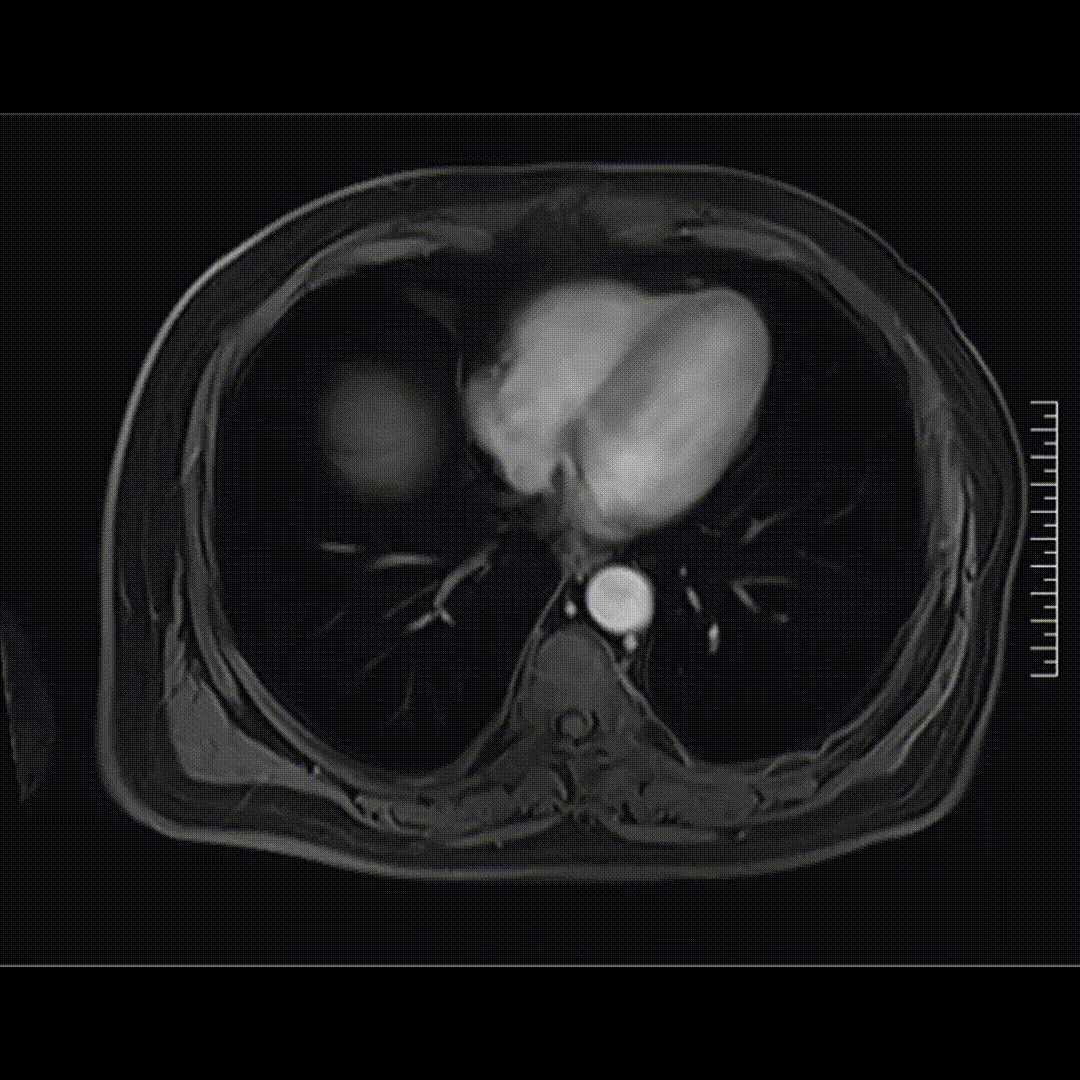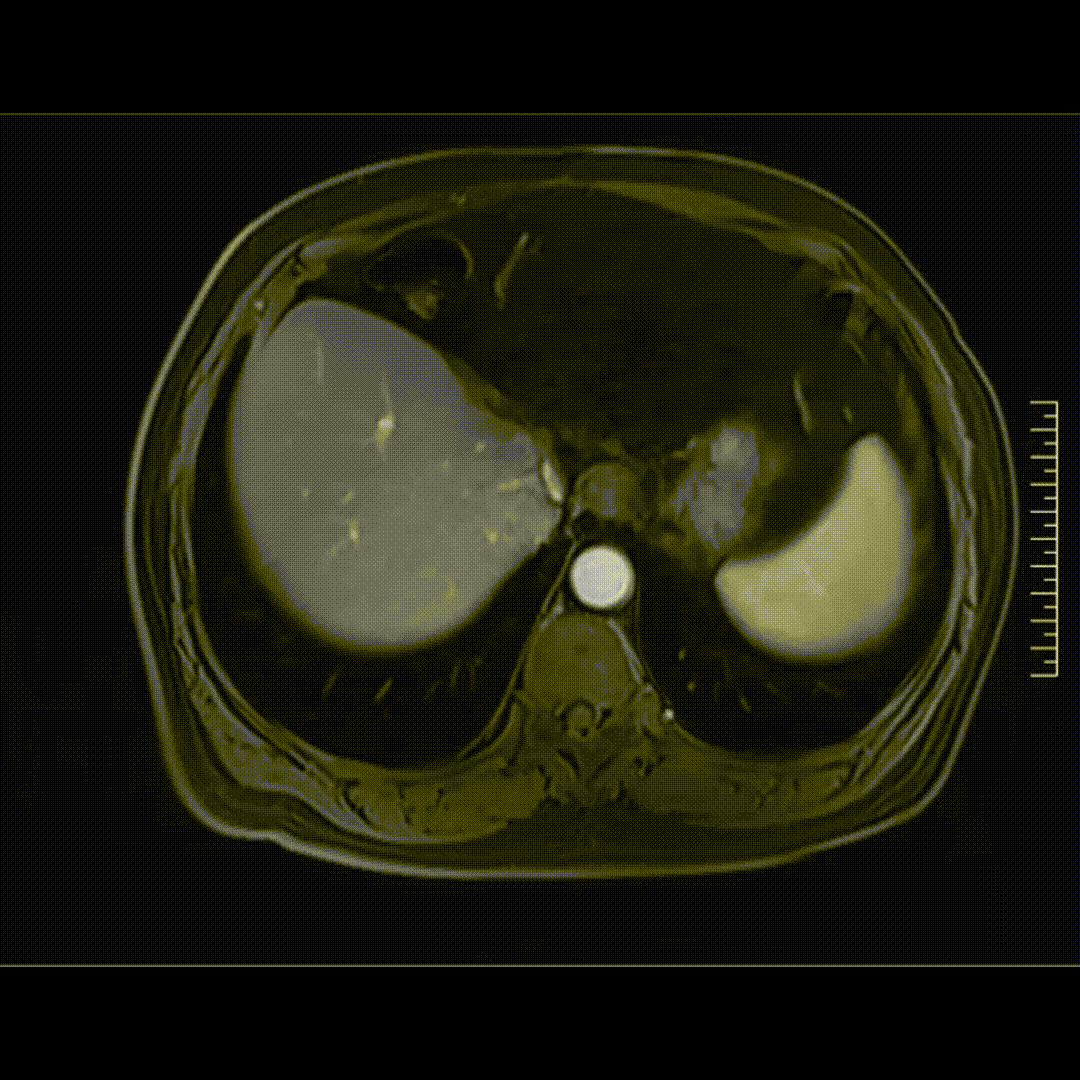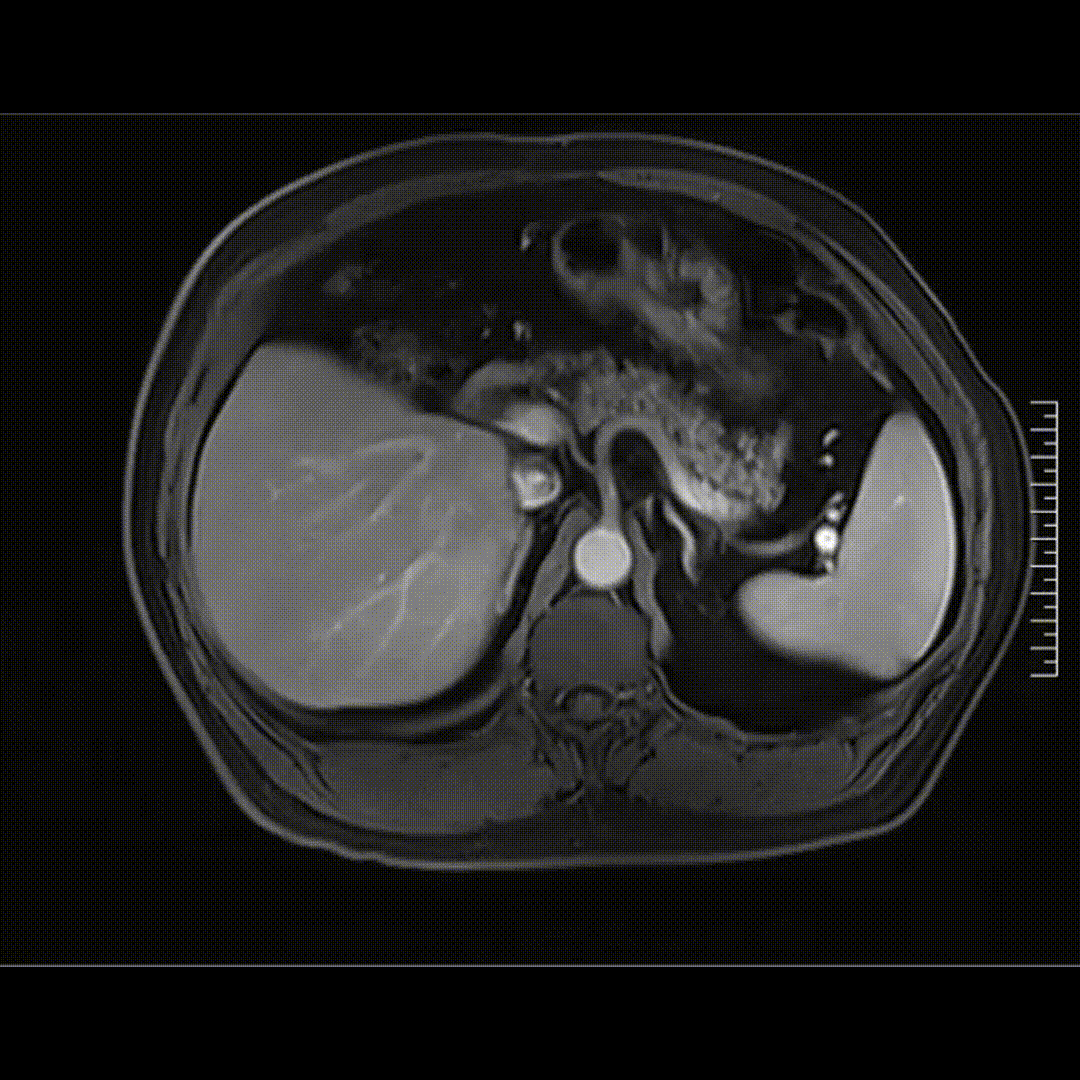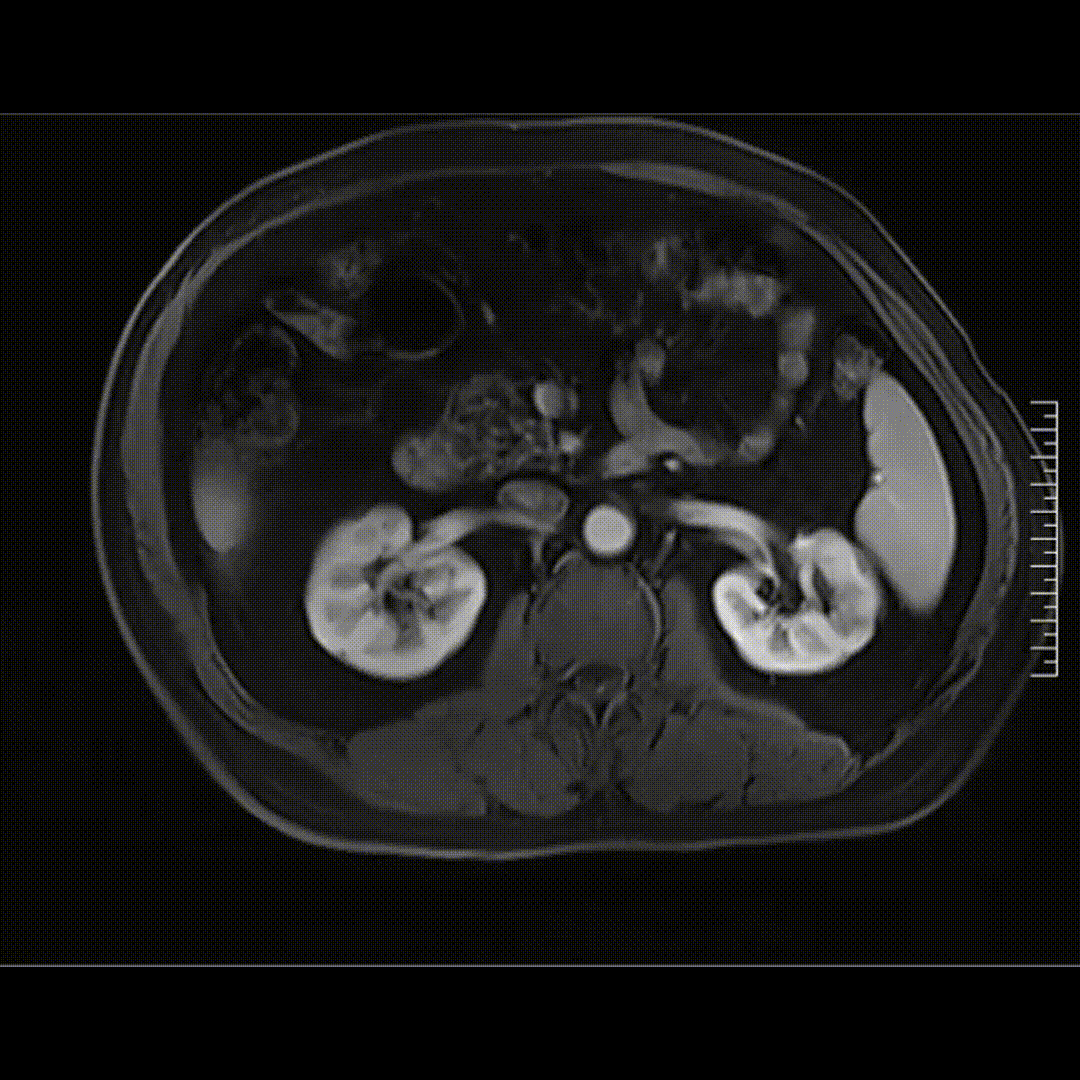 2023-05-21腹部MRI检查影像,未见肿瘤复发证据
2023-05-21腹部MRI检查影像,未见肿瘤复发证据
疗效评估:患者采用替雷利珠单抗联合GEMOX成功转化治疗IIIB期肝内胆管癌实现R0切除和病理学pCR,术后辅助治疗继续采用替雷利珠单抗免疫治疗,目前RFS已超18个月。
不良反应:整个治疗期间患者无明显不良反应发生。
讲堂点金
肝内胆管癌(intrahepatic cholangiocarcinoma,ICC)起源于肝内胆管上皮细胞,是人类第二常见的肝脏恶性肿瘤(占原发性肝癌的 10%~15%),发病率仅次于肝细胞癌[1,2,4]。目前根治性手术切除仍是唯一可能治愈ICC的首选治疗方式[2],但由于ICC发病隐匿、症状不典型、进展快,大多数患者(>65%)被诊断时病灶不可切除[3]。对于此类中晚期ICC患者,近年来以靶向治疗和免疫检查点抑制剂为代表的免疫治疗显示出了更有效的转化治疗潜力[4]。《原发性肝癌诊疗指南之肝内胆管癌诊疗中国专家共识(2022版)》也明确指出:对于拟行降期后手术切除的ICC,建议化疗联合靶向、免疫等多种治疗手段,针对患者进行个体化合理选择,并全程实施 MDT 策略[2]。本病例是一例典型的IIIB期肝内胆管癌伴门静脉癌栓案例,经全面评估病情和MDT讨论,决定在化疗基础上,采取“靶向治疗+免疫治疗”的策略来积极转化治疗,以期把不可切除肿瘤变为可切除,并争取实现R0切除。
一项前瞻性单中心探索性研究采用GEMOX联合多纳非尼和替雷利珠单抗一线治疗局部晚期或转移性胆道系统恶性肿瘤,结果显示:患者的6个月总生存期(OS)率高达90.9%,转化治疗成功率约23.1%;且整个研究期间,未观察到5级TRAE和非预期不良事件[5]。由此可见,替雷利珠单抗治疗胆道系统恶性肿瘤有效且安全。另一项单臂、开放标签、II期研究也显示,替雷利珠单抗联合仑伐替尼和GEMOX在潜在可切除的局部晚期胆道系统恶性肿瘤中能达到56%的客观缓解率(ORR),患者转化治疗成功率高达84%,约52%的患者实现了R0切除,其中1例(4%)患者达到pCR,且所有患者术后均未发生严重并发症[6]。这些数据充分显示了替雷利珠单抗在以化疗为基础的联合系统治疗中,具有强势而持久的肿瘤控制能力和可靠的安全性。
基于上述研究证据和相关指南共识推荐,本例患者在 MDT 团队的指导下,实施了8个周期的替雷利珠单抗联合GEMOX化疗方案,经转化治疗实现了手术R0切除,并达到了肿瘤的病理学pCR。从该案例中,我们能够感受到替雷利珠单抗帮助晚期ICC患者重获根治性手术机会的重要价值。
另外,高达60%~70%的术后复发率是ICC患者预后较差的另一个重要原因[7];针对该问题,目前各指南、共识普遍认为,可通过术后辅助治疗根除术后剩余肝脏、淋巴结、血液或其他器官中的肿瘤微转移[4]。鉴于吉西他滨、替吉奥(S-1)等单药或联合用药显著改善ICC术后患者的RFS和OS的表现[2],以及PD1/PD-L1免疫检查点抑制剂在肝癌术后辅助治疗中的重要价值[8],经MDT讨论,我们采取了“吉西他滨+替吉奥(S-1)+替雷利珠单抗”的术后辅助治疗方案。目前患者RFS已超18个月,而且整个治疗期间,患者无任何治疗药物相关不良反应发生。后续长期获益情况正随访评估中。
总而言之,本例患者的治疗策略对中晚期ICC的减瘤降期及防范术后复发等治疗具有一定的借鉴意义,希望替雷利珠单抗能够助力更多中晚期ICC患者成功转化实现R0切除,并在术后辅助治疗中持久发力、长期遏制肿瘤复发。
专家点评
根治性手术切除是目前可能治愈ICC的唯一方式,该患者肿瘤位置特殊,肿瘤较大,切缘不能保证,可疑血管侵犯,一期手术很难达到R0切除的目的,经MDT充分讨论,决定先进行转化治疗,再二期切除。
经采用替雷利珠单抗联合吉西他滨和奥沙利铂多周期治疗,肿瘤标记物逐步降低,肿瘤逐步缩小,达到了手术标准。术后病理提示完全缓解。且患者耐受性良好,结果满意。说明免疫治疗可以在肝内胆管癌的治疗中发挥更大的作用。
肝内胆管癌转化或者新辅助后的辅助治疗方案目前还缺乏证据。该病例继续采取替雷利珠加化疗辅助治疗6个月,随访至今取得了18个月的无复发生存期,说明替雷利珠单抗在胆管癌的作用值得进一步研究。
靶向治疗和免疫治疗在ICC的治疗及后续的探索治疗中已逐步显现出不错的疗效。进一步高级别的证据有利于临床的推广和扩大适应患者人群。
[1]科技部传染病防治重大专项课题“病毒性肝炎相关肝癌外科综合治疗的个体化和新策略研究”专家组. 肝内胆管癌外科治疗中国专家共识(2020版)[J]. 中华消化外科杂志, 2021, 20(1):1-15.
[2]中国抗癌协会肝癌专业委员会胆管癌协作组. 原发性肝癌诊疗指南之肝内胆管癌诊疗中国专家共识(2022版)[J]. 中华消化外科杂志,2022,21(10):1269-1301.
[3]赵海涛, 杨旭. 肝内胆管癌转化治疗[J]. 中国实用外科杂志, 2020, 40(6):732-737.
[4]喻彦熹, 吴忠均, 唐伟,等. 肝内胆管癌国际临床实践指南和共识的诊疗建议比较[J]. 中华外科杂志, 2023, 61(4):297-304.
[5]Lu Wang, et al. Efficacy and safety of sintilimab combined nab-paclitaxel and gemcitabine as first-line treatment for metastatic pancreatic ductal adenocarcinoma (PDAC): A retrospective analysis,2022 ESMO World GI ,p-110
[6]Huikai Li, et al. A single-arm, open-label, Phase II study of tislelizumab combined with lenvatinib and GEMOX regimen for conversion therapy of potentially resectable locally advanced biliary tract cancers.2022 ESMO 65P.
[7]王冲, 程石. 肝内胆管癌——国内外专家共识及指南解读[J]. 外科理论与实践, 2021, 26(2):124-129.
[8]肝癌术后辅助治疗中国专家共识协作组, 中国医师协会外科医师分会, 中国抗癌协会肝癌专业委员会, 等. 肝癌术后辅助治疗中国专家共识(2023版)[J]. 中华消化外科杂志, 2023, 22(4):437-448.
排版编辑:肿瘤资讯- Olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


