各位肿瘤资讯的网友大家好,我是陈功医生。正在西班牙马德里2017年ESMO大会现场为大家进行播报。今天是2017年的9月11日,距离ESMO闭会还有一天时间,本次大会结直肠癌第二个口头报告专场交流刚刚结束,本场包括四项研究,在此简单跟大家汇报一下。
摘要486O:转移性结直肠癌(mCRC)氟尿嘧啶(FP)联合贝伐单抗(BEV)序贯一线治疗方案对比初始FP+伊立替康(IRI)+BEV:德国AIO KRK0110 (ML22011)研究
背景 AIO KRK-0110研究评价初治mCRC患者FP+ BEV首次进展后序贯IRI+FP+BEV(A组)对比初始FP+IRI+BEV (B组)的效果。
方法 有效性主要终点指标为治疗方案失败时间(TFS)。非劣效界值90%可信区间风险比(HR)为0.8(效能70%,α = 0.05)。次要研究终点包括反应率、无进展生存(PFS)、总生存(OS)、不同分子型亚组的有效率及生活质量(EORTC QLQ C30)。
结果 全分析集(FAS)包括421例患者,A组212例,B组209例,平均年龄71岁。没有达到主要研究终点(TFS)(HR: 0.86 (0.73-1.02))。 关于TFS,RAS/BRAF 野生型(WT) mCRC患者从初始含伊立替康的治疗方案中获益更明显,但对于RAS 或 BRAF突变(MT)患者没有观察到这一点。Cox模型交互检验,不同研究组RAS状态存在差异(P = 0.03)。PFS及OS结果与TFS一致。客观缓解率显示B组更为获益(36.8% vs 53.6%,P = 0.005)。生活质量在基线及治疗结束时均没有显著性差异。
结论 本研究老年患者居多,初始FP+BEV vs FP+ IRI+BEV没有达到TFS非劣效性结果。序贯方案对于RAS/BRAF-WT mCRC患者显示劣势,因此更不推荐。但对于RAS MT mCRC老年患者,以BEV为基础的序贯方案仍可以作为可选方案。BRAF突变患者样本量较小不能评价。临床研究信息:NCT01249638。
附表
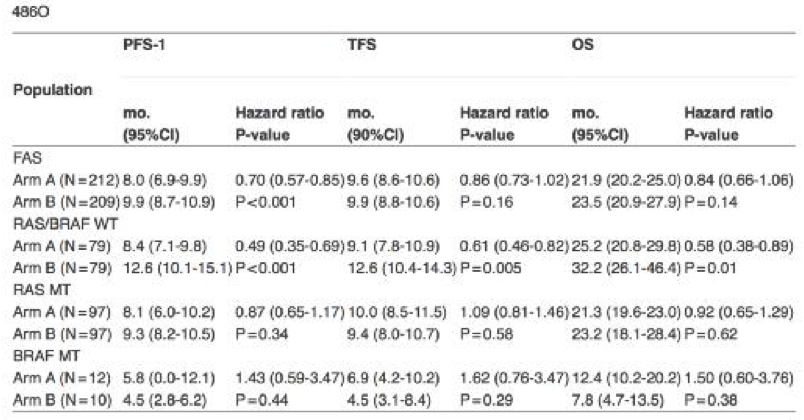
陈功教授:本篇报道是来自于德国AIO KRK0110 (ML22011)研究,摘要号为486O。研究目的是比较FP+BEV首次进展后加用伊立替康序贯治疗和FP+ IRI+BEV初始强化治疗的疗效及安全性,共计纳入434例未经治疗的晚期转移性结直肠癌患者,随机分为两组:第一组初始氟脲嘧啶制剂联合贝伐单抗治疗,进展以后加用伊立替康序贯治疗,观察第二次进展的时间;第二组初始应用FP+IRI+BEV的强化治疗方案,可见第一组采用序贯治疗方案,从弱到强,做加法治疗。而第二组采用初始强化治疗方案。研究设计初衷是想证明序贯治疗在疗效上不劣于初始强化治疗,非劣效比较的终点是治疗策略失败时间(time to failure of strategy,TFS),本质是达到第二次PD的时间。非劣效的介质是风险比HR不低于0.8。
具体结果:
1、客观缓解率ORR的统计结果显示,序贯治疗劣于初始强化治疗方案:
① RAS状态不明的患者的客观缓解率ORR,序贯治疗组是36.8,初始强化治疗组是53.8,组间具有显著的统计学差异;
② RAS/BRAF双野生患者,序贯组ORR 44.3,初始强化治疗组65.8,组间具有显著的统计学差异;
③ 单纯RAS野生型患者,序贯组ORR 33.0,初始强化治疗组46.4,组间统计学达到边界差异;
④ 单纯BRAF野生型的患者,序贯组ORR 25.8,初始强化治疗组30.8,组间无差异。
2、达到第一次PD的PFS1,初始强化治疗组优于序贯治疗组:
① 完全人群的统计结果是序贯组PFS1为8.0个月,初始强化治疗组为9.9个月,HR是0.7,具有统计学差异;
② RAS/BRAF双野生的患者,序贯组PFS1是8.4个月,初始强化治疗组是12.6个月,组间有显著统计学差异。
3、主要终点治疗策略失败时间(time to failure of strategy,TFS),TFS=PFS1+PFS2,结果显示:
① 所有人群的统计结果显示,序贯组TFS=9.6个月,初始强化治疗组为9.9个月,HR风险比是0.86,在0.73到1.02区间内,P值0.16,组间无统计学差异;
② RAS/BRAF双野生型患者的TFS统计结果,风险比是0.61,95%可信区间是0.46到0.82,提示初始强化治疗优于序贯治疗;
③ RAS突变型患者,风险比1.08,95%可信区间是0.81到1.46,组间达到非劣效。
综上所述,该研究并未达到主要终点,两种方案未达到非劣效。但如果按人群分层分析,RAS突变型的患者非劣效可以达成,而RAS/BRAF双野生型患者,ORR 、PFS1、TFS的统计结果都不支持序贯治疗方案。
该研究证明对绝大多数的人群来讲序贯治疗策略是不太适合的。现如今当临床上有了比较好的治疗药物,而病人身体状态也比较好的情况下,对绝大多数的患者来讲是不应该采用序贯治疗的。该研究的结论也很明确,序贯治疗方案仅能适用于RAS突变型的少数人群。而对于RAS/BRAF双野生型患者,只要患者的身体条件能够耐受初始强化治疗方案,都不应该选择序贯治疗方案。
摘要478O:Sym004对于抗EGFR获得性耐药型难治性结直肠癌的效果及安全性:随机II期研究(RP2S)结果
背景 Sym004是两种抗EGFR单克隆抗体(mAbs)的混合物,在前期的1、2期研究中显示出对难治性mCRC的有效性。由于其独特的作用机制,Sym004可以克服抗EGFR单抗的获得性耐药。
方法 国际、开放标签研究共纳入254例患者,按1:1:1随机分为3组,RP2S对比两种Sym004剂量方案(A组12 mg/kg Qw;B组 负荷剂量9mg/kg序贯6mg/kg Qw)及研究者选择(IC)(C组)5-FU、卡培他滨或最佳支持治疗的效果及安全性。主要入组标准为患者对化疗无效,对含抗EGFR mAbs的治疗方案有效但最终疾病进展、肿瘤样本RAS 2号外显子野生型。评价指标为3组治疗间隔3个月的总生存改善(6月 vs 9月)。
结果 人口学及基线参数水平均衡。Sym004不良事件(AE)非常典型,常见及严重AE为皮肤AEs及低镁血症,但是消化道AEs较其他抗EGFR mAbs 要低。B组较A组具有更好的耐受性。ITT分析OS并进行探索性亚组分析。由于C组出现意想不到的结果导致该研究主要研究终点为阴性。与A组相比,B组不仅耐受性良好而且改善了生存。生物标志物特异性分析,双阴性(DN)(循环肿瘤细胞[ct]DNA中RAS突变阴性等位基因频率>20%;无BRAF V600E)或三阴性(TN)(DN并且ctDNA中没有EGFR胞外区突变)患者生存改善,对B组治疗方案耐受良好并且OS延长(DNmCRC延长3.5月,TNmCRC延长5.5月)。
结论 尽管ITT分析结果为阴性,在与4线方案的对比中,Sym004对mCRC显示出非常好的治疗反应。通过分子分型筛选人群可以为下一步EGFR抑制剂治疗难治性mCRC研究设计提供指导。临床研究信息:NCT02083653或EMR200637-002。
附表
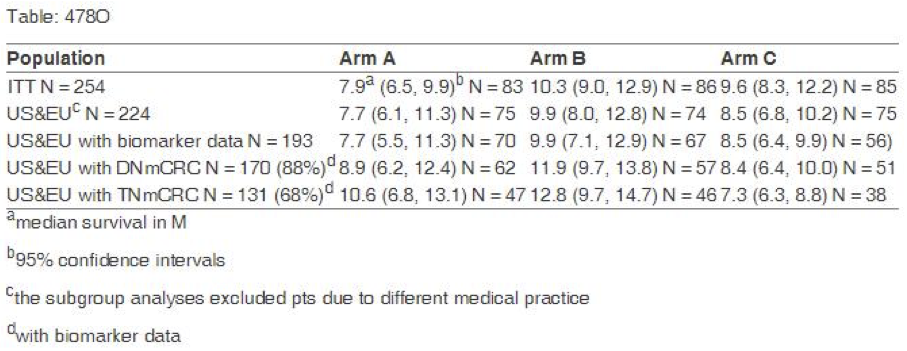
陈功教授:本项研究旨在验证一个新的抗癌药物Sym004治疗晚期结直肠癌的疗效及安全性。Sym004是一种由两种重组的、以非重叠性的EGFR-胞外域抗原表位为靶点的人-鼠嵌合型单克隆抗体的新型混合物,同西妥昔单抗、帕尼单抗属于同一大类,但又有所不同。该研究选择的研究对象是晚期至少接受过一线以上的化疗,必须接受过EGFR单抗治疗且EGFR单抗有效,治疗后又进展的患者,共计纳入254例,按1:1:1随机分为3组,Sym004A组12mg/kg Qw;B组Sym004负荷剂量9mg/kg序贯6mg/kg Qw及C组最佳支持治疗或是研究者根据病人的情况来给予单药卡培他滨,或单药5-FU。
研究结果显示:
1、主要终点是OS,ITT(intent-to-treat)分析的结果显示组间没有统计学差异,A、B、C三组OS分别是7.9个月,10.3个月,9.6个月;A、B组同最佳支持治疗相比,风险比分别为1.31和0.97,没有统计学差异。
2、三组PFS统计结果,分别是2.8个月,2.7个月跟2.6个月,风险比1.08和0.99,同样无统计学差异。
3、客观缓解率ORR,A组ORR为14%,B组ORR为9.6%,而C组只有1.4%。但不同剂量的Sym004治疗方案的客观缓解率有明显的好处提升,却并未获得更好的生存收益。
4、Sym004的不良反应较大。三度以上的皮疹,A组发生率为54%,B组为36.9%,而C组发生率仅为1.3%。对于Sym004如此高的变态反应发生率,绝大多数患者无法耐受。
该研究难能可贵的一点是往精准医学的角度迈进了一大步,研究选用二代测序技术NGS,检测以下内容:
1、RAS的两个等位基因的突变是否超过20%,以20%为一个cut-off值,分成突变超过20%和未超过20%;
2、ctDNA有没有B基因的突变;
3、EGFR胞外域ECD(extra—cell4Ilar domain)有无突变。
按检测结果分为两个亚组:
1、Double Negative,既RAS等位基因突变没有超过20%,又没有BRAF突变,这一组病人定义成双阴性,这一亚组患者OS总生存三个组分别是8.9个月,11.9个月还有8.5个月,风险比0.95、0.71,无统计学差异;但OS已经有一部分的延长,尤其是B组比C组总生存期延长了3.1个月,而且B总生存达到一年的患者约占50%,而C组只有29%。
2、NGS检测的三个指标全部阴性的患者的总生存分别是A组10.6个月,B组12.8个月,C组7.3个月,B、C两组风险比是0.95,95%可信区间0.35到0.99,有显著的统计学差异。B组全阴性患者56%能够活到一年,C组只有21%。
因此经过精准医学的筛选,对原来EGFR曾经耐药的患者,使用另外的EGFR单抗又能够获得有效率,这是该研究给临床带来的一个启示。目前晚期肠癌唯一称得上精准治疗的典范就是EGFR单抗,我们需要更精准地检测,把所有的耐药因素排除。众所周知EGFR单抗有很多耐药因素,譬如RAS突变,Her2的过表达等,而该研究提及的ECD也可能是导致EGFR单抗耐药的因素。
相信在未来Sym004如果能够上市,再经精准医疗的筛选,能够在三线应用,让50%的患者额外延长10个月也是非常有价值的。
摘要479O:共识分子亚型(CMS)作为转移性结直肠癌一线使用贝伐单抗获益的预测因子:MAX研究回顾性分析
背景 CMS是一种以转录物为基础的分型方法,对结直肠癌(CRC)的预后具有预测作用,但是它与治疗反应的相关性,尤其是转移方面尚不明确。本研究采用MAX 3期研究数据,评价CMS分型是否可以预测贝伐单抗的治疗效果。前期报道过贝伐单抗(B)联合化疗(卡培他滨(C)+/-丝裂霉素(M))治疗转移性CRC可以改善无进展生存(PFS)。
方法 256例患者(占总研究人群的54%)的肿瘤标本可以采用Almac Xcel芯片进行基因表达检测,将肿瘤分为CMS 1-4型,将CMS分组与MAX研究中PFS相关联。Cox风险模型发现CMS与贝伐单抗治疗效果相关,提示CMS具有预测价值。
结果 数据经质控后分析,239例(占总研究人群的51%)符合生存分析要求。CMS分型分布为CMS1 18%, CMS2 48%, CMS3 12%, CMS4 23%。C vs CB+CBMPFS风险比(HR)(95% CI)4个CMS亚型组分别为0.83 (0.43-1.62), 0.50 (0.33-0.76), 0.31 (0.13-0.75) 及1.24 (0.68-2.25)(p = 0.03)。调整预后因素后多因素分析显示,CMS仍然是PFS的独立预测因子(p = 0.04)。
结论 转移性CRC中,CMS 2、3亚型患者更容易从加入贝伐单抗的化疗方案中获益,需要进一步的独立队列研究来证实这一结果。一旦结果被证实,CMS分型可用于指导贝伐单抗治疗患者的选择。
陈功教授:这是来自澳大利亚的MAX研究,之前该研究的主要终点已经公布过,研究的目的是验证同单药卡培他滨相比卡培他滨+贝伐单抗或者卡培他滨+贝伐单抗+丝裂霉素C的疗效和安全性。之前披露的结果显示卡培他滨联合贝伐单抗明显优于单用卡培他滨。
本次大会MAX研究探讨了共识分子亚型CMS对患者预后以及靶向药物应用的指导价值。该研究纳入410例患者,很可惜最后能够通过NGS技术实现CMS分型的患者只有237例,原发瘤部位是左半的有67%,右半30%。MAX研究CMS分型从一型到四型的比例跟之前其他相关报道一致,分别是一型18%,二型47%,三型12%,四型23%;左半更多的是二型跟四型,右半更多的是一型跟三型。说明原发瘤部位左右半导致的差异背后一定是有分子事件推动。
该研究团队得出两个结论:
1、从预后的角度来讲,CMS一型是最差的,其次是CMS三型,CMS四跟二型比其他两型要好,最好是CMS二型,预后从差到好排列是1、3、4、2。CMS四型跟二型跟一型相比较具有显著的统计学差异,P值小于0.01,风险比是0.44跟0.57。很容易理解,因为这个研究左半是二跟四型,右半是一跟三型,我们知道左半比右半好,所以CMS二跟四型的预后好于一型跟三型。
2、MAX研究将患者分成两个群体,一个群体是单纯接受卡培他滨治疗的患者,第二个群体接受卡培他滨联合贝伐单抗或者是卡培他滨、贝伐单抗和丝裂霉素C的三联治疗。从贝伐单抗角度来讲分成两个亚型,使用贝伐单抗和未使用贝伐单抗的患者。结果研究者发现很有趣的现象,CMS二跟三型两个亚型患者应用贝伐单抗是有获益的,CMS二型患者的获益风险比为0.5,获益50%,P值是0.001;而CMS三型患者获益更大,风险比0.31,应用贝伐单抗的患者死亡风险降低了69%,P值0.04,具有统计学差异。CMS分子分型是否能用来预测贝伐单抗的疗效,尚待进一步探讨。
摘要480O:甲基化表型对奥沙利铂基础化疗方案辅助III期结肠癌患者治疗的预后价值
背景 关于甲基化表型(CIMP+ 代表“CpG岛甲基化表型)对非转移性结肠癌(CC)患者的预后价值始终充满争论。本研究评价这一表型对于R0切除术后III期CC患者的预后价值,根据MSI, RAS及BRAF突变状态,辅助治疗方案分层。
方法 PETACC-8辅助治疗3期研究中,有1910例患者的肿瘤样本纳入分析。采用特异性甲基化PCR技术检测,5个基因(IGF2, CACNA1G, NEUROG1, SOCS1 and RUNX3)中至少有3个存在甲基化被定义为CIMP+。Cox模型评价CIMP状态与总生存(OS), 无疾病生存(DFS)和复发后生存(SAR)的相关性,调整预后因素(MSI, BRAF及RAS突变状态)及治疗因素(FOLFOX or FOLFOX联合西妥昔单抗)。根据治疗有效性分析CIMP状态。
结果 1870例(98%)患者成功确定了CIMP状态,275例(14.7%)为典型CIMP+。与CIMP-患者相比,CIMP+患者年龄偏大(p = 0.002),女性更多(p = 0.04)。CIMP+肿瘤更常见于右侧(p < 0.0001),组织学3-4级(p < 0.0001),pN2 (p = 0.001),MSI (p < 10e-4),BRAF突变 (p < 0.0001) 及RAS野生型 (p < 0.0001)。多因素分析显示,CIMP+状态与OS缩短(HR:1.4; 95% CI 1.02-1.9; p = 0.04) 及SAR 缩短(HR:1.8; 95% CI 1.2-2.6;p < 0.0004)具有相关性;但是,CIMP+与CIMP-患者DFS没有统计学差异(HR:1.1;95% CI 0.8 1.5;p = 0.34)。这些结果不受治疗方案的影响。对于CIMP+患者,西妥昔单抗在OS及DFS方面均没有显示获益或不利影响。
结论 在这个大型临床及分子分型研究者中,确定了III期CC标准辅助治疗的人群,甲基化表型可以作为OS及SAR的预后标志。然而,没有观察到CIMP状态于DFS的相关性。没有发现CIMP状态对于FOLFOX vs FOLFOX联合西妥昔单抗疗效具有预测作用。临床研究信息:PETACC8 Trial (EuDRACT编号: 2005-003463-23)。
陈功教授:该研究是来自欧洲的一项辅助化疗的研究PETACC8,旨在证明三期结直肠癌患者应用FOLFOX6加或不加西妥昔单抗,最终结果是阴性的,不管是贝伐单抗还是西妥昔单抗都不能用在辅助化疗。
该研究后续进行了精准医学的探索,希望找到辅助化疗疗效预测的标志物。法国团队探讨CpG岛甲基化表型(CpGislandmethylatorphenotype,CIMP)预测预后及奥沙利铂辅助化疗疗效的价值。之前的研究一般都认为CIMP有预后预测价值,疗效的预测价值尚不清晰。PETACC8一共纳入两千多例患者,筛选其中1867例患者进行CIMP表型检测。
国内研究生想做科研的话,如何定义CIMP是阳性还是阴性?一共检测五个基因:IGF2,CACNAEG,NEUROG1,RUNX3,SOCS1,其中三个基因有突变,那么CIMP阳性,反之则是阴性。1867例患者,CIMP阳性的比例14.7%,CIMP阳性跟临床病理、分子病理都是有显著的相关性:
1、CIMP阳性的患者中有更多的MSI-H及BRAF突变,而且有更多的RAS是野生型的,所以CIMP跟分子病理有关系。
2、CIMP阳性同MSI-H的患者类似,更多见于女性、右半,T分期、N分期更加晚。因此CIMP的临床病理特征都跟MSI-H或者dMMR的分子表型、临床表型非常一致。
具体结果有两点:
第一点,毫无疑问CIMP有一定的预测价值,具体要看情况,关于无瘤生存DFS方面的统计结果显示CIMP没有影响,风险比1.1,P值0.34。说明CIMP是否阳性并未影响到无瘤生存。言下之意,既然未影响到无瘤生存,CIMP很有可能不能作为辅助化疗的疗效预测的标志物。
第二点,患者辅助化疗结束后一旦出现复发,复发后的生存同CIMP的分子表型密切相关,复发后CIMP阴性患者跟CIMP阳性患者的生存明显不同,风险比1.8,说明CIMP阳性的患者一旦复发,复发后死亡风险增加了80%,HR是1.8,95%可信区间1.2到2.6,P值0.04。
综上,迄今为止,仍未找到较好的标志物来预测奥沙利铂的辅助化疗的疗效。
上述内容就是今天结直肠癌口头报告专场的内容,今年ESMO大会所有的肠癌口头报告都已结束,一共八个摘要,第一个专场对临床实践帮助比较大,第二个专场内容更多涉及精准医学方面,到临床应用还有一定的距离。
对于上述内容各位同道后续如有问题,欢迎在肿瘤资讯线上留言讨论,谢谢各位。











 苏公网安备32059002004080号
苏公网安备32059002004080号


