在众多癌症中,卵巢癌是女性常见的恶性肿瘤之一,卵巢癌由于起病隐匿,缺乏典型症状,大多数患者确诊时已是中晚期,预后相对差,死亡率居妇科恶性肿瘤之首,因此被称为女性健康“第一杀手”。近期,Cancer Letters发布了一篇原创性研究文章,由山东大学齐鲁医院妇产科宋坤教授团队领衔[1],研究发现,STING抑制剂H-151能够抑制CAFs中的STING信号通路,减少IFNB1的释放,并增强卵巢癌细胞对顺铂的敏感性。这一发现为卵巢癌的治疗提供了新的策略,有助于验证STING抑制剂在临床治疗中的有效性和安全性。【肿瘤资讯】整理该研究要点,以飨读者。

卵巢癌在全球范围内是女性生殖系统中最常见的恶性肿瘤之一,其发病率和死亡率均居高不下[2,3]。由于卵巢癌早期症状不明显,大多数患者在确诊时已处于晚期,错过了最佳治疗时机[4]。即便在初期治疗中,卵巢癌显示出对铂类药物(如顺铂)的敏感性,但不幸的是,许多患者在治疗后会发展出药物耐药性,导致癌症复发和预后恶化[5]。
肿瘤微环境(TME)通过招募和转化周围细胞,对卵巢癌的存活、生长和扩散起着关键作用。TME中的相互作用涉及生长因子、趋化因子、细胞因子和炎症分子的复杂网络。靶向TME作为肿瘤治疗的方法因其在肿瘤进展和治疗反应中的关键作用而受到关注[6]。在这一微环境中,癌症相关成纤维细胞(CAFs)因其在促进肿瘤进展和调节治疗耐药性中的核心作用而受到关注。CAFs能够通过分泌细胞因子和生长因子,以及通过细胞外基质的改变,促进肿瘤细胞的增殖、迁移和免疫逃逸[7]。
近年来,STING(Stimulator of Interferon Gene)信号通路因其在调节先天免疫反应和抗肿瘤免疫中的关键作用而成为研究的热点[8]。STING是一种胞质蛋白,能够识别细胞内的DNA,并激活下游的信号通路,导致I型干扰素和其他炎症因子的产生。在肿瘤治疗中,STING信号通路的激活可以促进肿瘤细胞的免疫识别和清除[9]。然而,一些研究表明,STING信号通路可能在促进抗肿瘤免疫反应方面发挥作用,而在其他情况下,它可能有助于肿瘤生长和转移。这种双向作用使得STING信号通路成为一个具有挑战性的治疗靶点[10]。
因此,深入了解STING信号通路在卵巢癌中的具体作用,特别是在CAFs中的作用,对于开发新的治疗策略至关重要。STING抑制剂作为一种潜在的治疗手段,可能通过调节肿瘤微环境中的信号传导,提高肿瘤细胞对化疗药物的敏感性,从而克服治疗耐药性。
本研究旨在探索STING抑制剂在卵巢癌治疗中的潜力,特别是在提高铂类药物化疗敏感性方面的作用,以期为卵巢癌患者带来更有效的治疗选择。
研究方法
本研究采用体外细胞培养和体内小鼠模型,通过STING抑制剂H-151处理CAFs,评估其对卵巢癌细胞对顺铂敏感性的影响。同时,通过免疫荧光、Western Blot和流式细胞术等技术,分析STING信号通路在CAFs中的活化状态及其对卵巢癌细胞行为的影响。
研究结果
研究团队首先观察到,顺铂能够促进卵巢癌细胞的DNA转移到CAFs中,进而激活CAFs内的CGAS-STING-IFNB1信号通路,这一过程导致癌细胞对铂类药物的耐药性增强。研究进一步发现,肿瘤基质中STING表达水平的升高与患者的不良预后相关联。
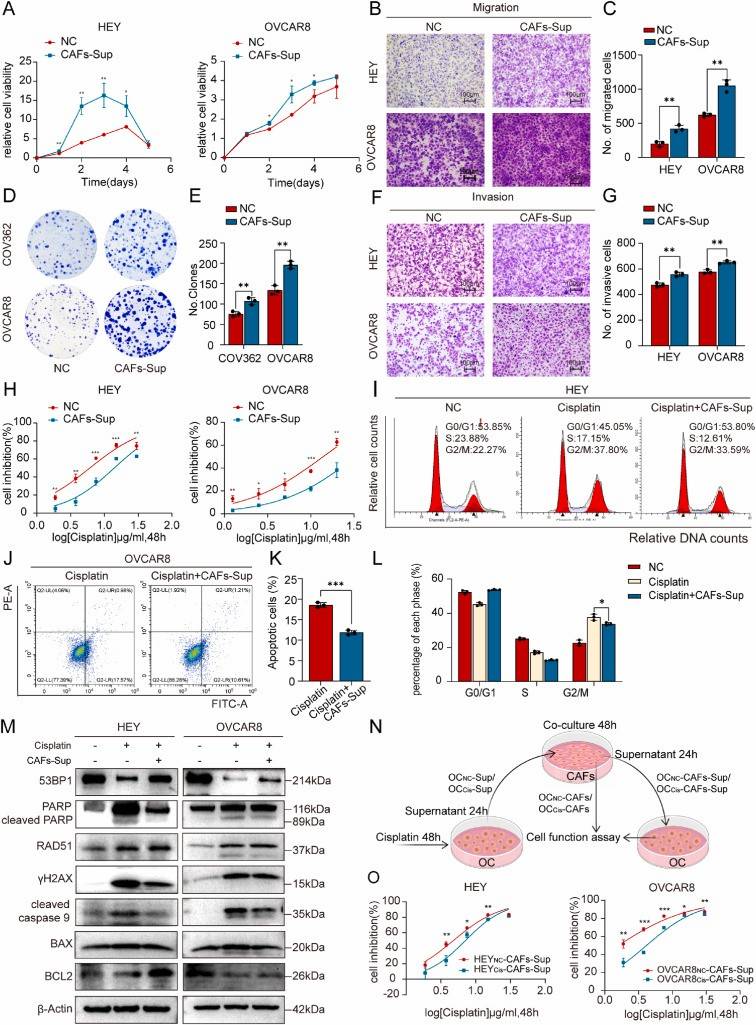
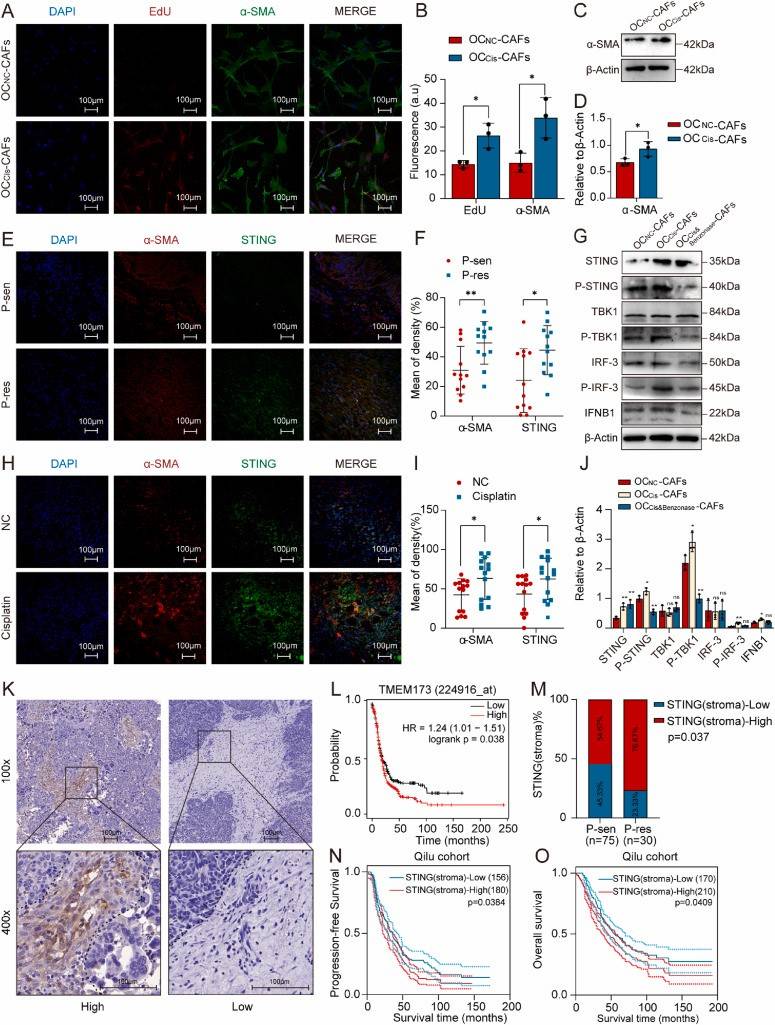
图 1.顺铂治疗后的卵巢癌进一步增强了CAFs促进卵巢癌细胞顺铂耐药性的能力
基于这些发现,研究者们使用了STING抑制剂H-151来抑制CAFs中的STING信号通路。实验结果显示,H-151能够有效地增强卵巢癌对顺铂的敏感性(图2),减少癌细胞的增殖和侵袭能力,并通过促进DNA损伤修复来增强铂类药物的杀伤效果。此外,在体内小鼠模型中,H-151与顺铂联合治疗显著减小了肿瘤体积,并延长了生存时间(图3)。
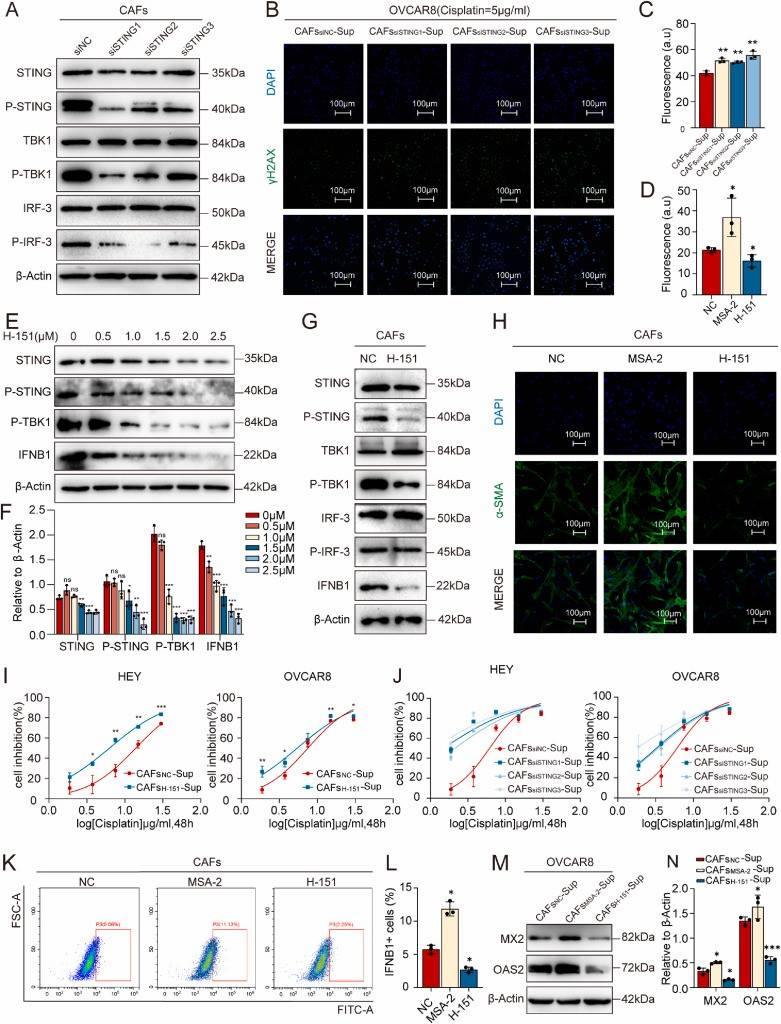 图2. Western blot实验表明H-151有效抑制了CAFs中CGAS-STING通路的表达
图2. Western blot实验表明H-151有效抑制了CAFs中CGAS-STING通路的表达
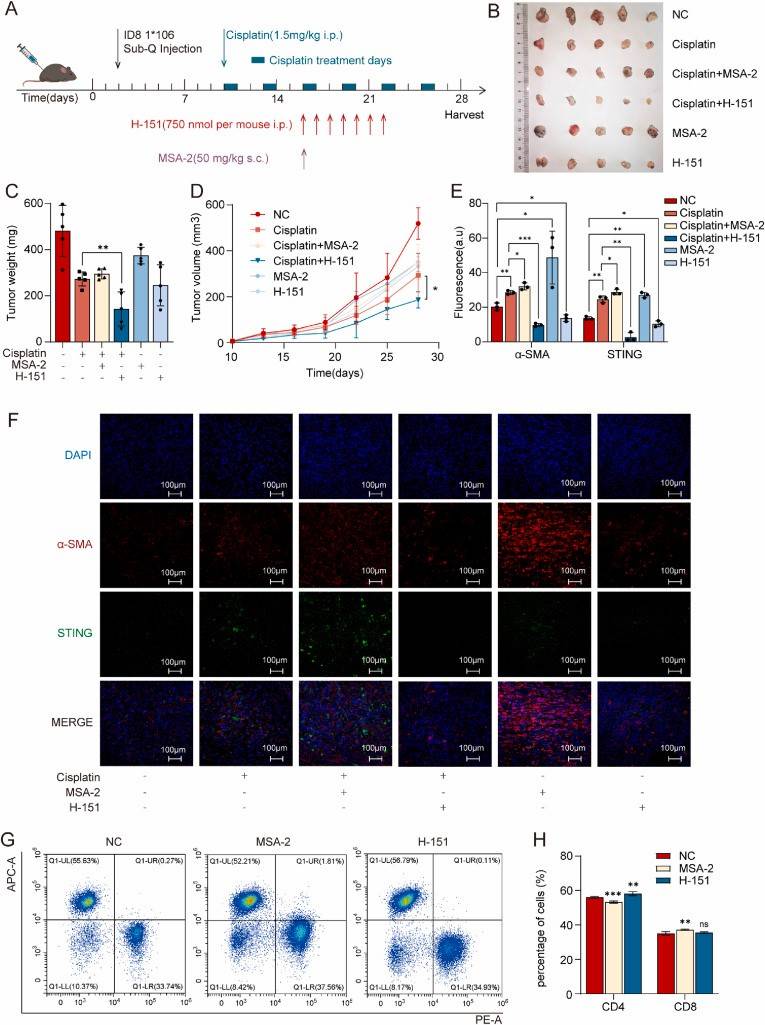
图 3.H-151的联合给药增加了顺铂的体内抗肿瘤功效
这些结果表明,STING抑制剂H-151有潜力成为一种新的治疗策略,用于提高卵巢癌患者对铂类药物的敏感性。此外,这项研究还为其他类型的癌症治疗提供了新的靶点和研究方向。
研究者们表示,未来的工作将集中在进一步验证STING抑制剂在临床治疗中的有效性,并探索其与其他治疗方法的联合使用潜力。这一发现为卵巢癌的治疗提供了新的策略,并为未来的临床研究和药物开发指明了方向。进一步的研究将有助于验证STING抑制剂在临床治疗中的有效性和安全性,为卵巢癌患者带来新的希望。
1.Liu J, Liu C, Ma Y, et al. STING inhibitors sensitize platinum chemotherapy in ovarian cancer by inhibiting the CGAS-STING pathway in cancer-associated fibroblasts (CAFs). Cancer Lett. 2024;588:216700.
2.Siegel, R. L., Miller, K. D., Wagle, N. S., & Jemal, A. (2023). Cancer statistics, 2023. CA: A Cancer Journal for Clinicians, 73, 17–48.
3.Lheureux, S., Gourley, C., Vergote, I., & Oza, A. M. (2019). Epithelial ovarian cancer. Lancet, 393, 1240–1253
4.Pitt, J. M., Marabelle, A., Eggermont, A., Soria, J. C., & Kroemer, G. (2016). Targeting the tumor microenvironment: removing obstruction to anticancer immune responses and immunotherapy. Annals of Oncology, 27, 1482–1492.
5.Bogani, G., Matteucci, L., Tamberi, S., Arcangeli, V., Ditto, A., Maltese, G., ... & Raspagliesi, F. (2017). The impact of number of cycles of neoadjuvant chemotherapy on survival of patients undergoing interval debulking surgery for stage IIIC–IV unresectable ovarian cancer: results from a multi-institutional study. International Journal of Gynecological Cancer, 27, 1856–1862.
6.Hinshaw, D. C., & Shevde, L. A. (2019). The tumor microenvironment innately modulates cancer progression. Cancer Research, 79, 4557–4566.
7.Papait, A., Romoli, J., Stefani, F. R., Chiodelli, P., Montresor, M. C., Agoni, A. R., ... & Parolini, O. (2022). Fight the cancer, hit the CAF. Cancers, 14.
8.Zhang, X., Bai, X. C., & Chen, Z. J. (2020). Structures and mechanisms in the cGAS-STING innate immunity pathway. Immunity, 53, 43–53.
9.Knelson, E. H., Ivanova, E. V., Tarannum, M., Campisi, M., Lizotte, P. H., Booker, M. A., ... & Mahadevan, N. R. (2022). A shared and distinct functions of type I and type III interferons. Immunity, 50, 907–923.
10.Bakhoum, S. F., Ngo, B., Laughney, A. M., Cavallo, J. A., Murphy, P., Ly, P., ... & Cantley, L. C. (2018). Chromosomal instability drives metastasis through a cytosolic DNA response. Nature, 553, 467–472.
声明:材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批号:CN-133828
排版编辑:肿瘤资讯-Rex











 苏公网安备32059002004080号
苏公网安备32059002004080号


