年轻乳腺癌是指患病年龄在 40 岁以下乳腺癌患者[1]。与年长患者相比,年轻乳腺癌患者组织学分级更高,Ki-67高表达比例更高,脉管浸润的比例更高,因而年轻乳腺癌患者复发转移风险较高、总体生存较差[1]。此外,约 70% 乳腺癌患者为 HR+:年轻患者由于卵巢功能活跃导致体内雌激素水平较高,可能刺激 HR+ 的乳腺癌细胞生长,从而与年长患者相比有更高的复发风险[1]。日前,ESMO Open 发表一项研究,通过对全球三大数据库 56 万例乳腺癌患者分析,提示亚洲年轻女性(<40 岁)中 HR+/HER2- 亚型患者存在显著生存劣势,且经 15 年随访,这种生存劣势仍持续存在[2]。
CDK4/6 抑制剂联合内分泌治疗(ET)是 HR+/HER2- 晚期乳腺癌一线标准治疗方案[3]。 MONALEESA-7 研究证实,瑞波西利联合 ET 可有效改善绝经前 HR+/HER2- 晚期乳腺癌患者的无进展生存期(PFS)和总生存期(OS)[4]。本期浙江省肿瘤医院李广亮医生带来一例 37 岁确诊 HR+/HER2- 晚期乳腺癌伴肝、腋窝淋巴结转移患者,一线治疗使用瑞波西利联合 ET 肿瘤退缩的病例,并邀请到浙江省肿瘤医院王晓稼教授对该病例诊治经过进行点评。
浙江省肿瘤医院乳腺内科主任医师/第五届人民名医“卓越建树“
浙江省免疫学会副理事长
浙江省肿瘤智能诊断和分子技术研究中心副主任
浙江省肿瘤诊治质控中心副主任兼乳腺癌质控专家委员会主任委员
中国临床肿瘤学会(CSCO)乳腺癌专家委员会副主任委员
中国抗癌协会乳腺癌专业委员会常委、医学伦理委员会常委
中国民族卫生协会卫生 健康技术推广专家委员会副主委/乳腺癌推广组组长
浙江省医学会肿瘤内科分会前任主任委员
浙江省抗癌协会乳腺癌专业委员会主任委员、肿瘤内科专委会前任主委
浙江省转化医学学会副会长
乳腺肿瘤MDT秘书
中国抗癌协会肿瘤营养专业委员会肿瘤营养诊断专家协作组委员;
浙江省转化医学会精准医学分会委员兼秘书;
浙江省抗癌协会肿瘤营养与支持治疗专委会青委;
浙江省免疫学会肿瘤免疫与生物治疗专委会青委;
院“人才振兴30计划”培养对象。
2021年度登峰之旅·西湖杯:肿瘤病例 MDT(乳腺癌) 菁英赛冠军
主持完成国家自然科学基金1项,省、厅级基金项目2项;主参国家及省级基金项目十余项。
作为Sub-I参与数十项国内外多中心临床研究。
以第一作者及通讯作者身份发表SCI论文十余篇。
参编专著2部、译著2部。
病例简介
基本情况
基本信息:患者,女性,37 岁。
主诉:发现右乳肿块 2 年,确诊右乳癌半月余。
现病史:
患者自述 2 年前哺乳期外伤后发现右乳肿块,约鸡蛋大小,于当地医院就诊考虑炎症,具体不详,予对症治疗后未见明显好转。患者当时未予重视,未继续诊治。后患者因右乳肿块逐渐增大,于 2024 年 7 月 19 日,至外院就诊。
2024 年 7 月 24 日行右乳肿块及右腋窝淋巴结穿刺术。右乳肿块穿刺病理示:右乳浸润性导管癌,WHO II级,局部见导管内癌,免疫组化:ER(90%,+++),PR (80%,+++),Her-2(浸润区2+,FISH阴性),Ki-67(约20%+)。右腋窝淋巴结病理示:上皮性癌浸润或转移,结合病史及免疫组化结果乳腺来源首先考虑。免疫组化:ER(>90%,+++),PR (80%,+++),Her-2(2+,FISH阴性),Ki-67(热点区约60%+)。
2024 年 7 月 26 日,外院 PET-CT 示:1、右乳外侧象限占位(3.1×1.6cm),伴右腋窝多发肿大淋巴结(大者约1.4cm),FDG 摄取增高,符合右乳腺癌伴右腋窝淋巴结转移。2、肝左内叶低密度,延迟显像 FDG 摄取轻度增高,不除外肝转移瘤,建议进一步增强CT或MRI检查。3、全身骨骼密度欠均伴弥漫性小班点状高密度影,FDG摄取轻中度增高,考虑代谢性骨病可能,请结合临床并密切随访,骨转移瘤待排。4、双锁骨上小淋巴结,FDG 摄取未见增高,左腋窝稍肿大淋巴结,FDG 摄取轻度增高,考虑炎性淋巴结可能性大,建议随访。5、盆腔双侧附件增大,密度欠均伴FDG摄取局部增高,考虑炎症可能性大,建议专科定期复查。宫腔少量积液伴生理性FDG摄取。盆腔少量积液。6、双肺数枚微小结节,FDG摄取未见增高,胸部CT随访。双肺散在少许炎症。双肺门、纵隔炎性小淋巴结。心包少量积液。双侧胸腔少量积液。7、其余双侧乳腺多发小结节,FDG摄取未见异常,专科随访。8、胃炎。胆囊炎,胆囊小结石。脾大。副脾。双肾孟、肾盏扩张积水。腹盆腔、腹膜后及双腹股沟炎性小淋巴结。9、甲状腺左右叶密度欠均,FDG摄取增高,考虑甲状腺炎可能性大,请结合专科检查。双侧筛窦炎。双侧扁桃体炎。双颌下、颏下及颈部炎性淋巴结。10、脊柱轻度退变。L3~S1椎间盘轻度膨突。
2024 年 7 月 28 日 ,外院肝脏增强 MR 示:1.肝脏数个小结节,考虑转移瘤可能性大。2.胆囊壁增厚毛糙。3.双肾盂扩张积水。4.肝门部及腹膜后多发淋巴结,部分增大。
既往史: 甲状腺功能减退症 4 年,平素口服优甲乐 25ug qd。
月经史:15 岁初潮,平素月经规律,末次月经时间:2024 年 7 月 29 日。
婚育史:22 岁结婚,育有 1 子 1 女。
个人史、家族史无特殊。
体格检查:
右乳外侧肿块,大小约 3.5×3.5cm,质中偏硬,边界一般,右腋窝可及大小约 2.5×2.5cm质硬淋巴结。左乳未触及明显肿块,左侧腋窝及双侧锁骨上未及明显肿大淋巴结。
实验室检查:
2024-8-9 血常规:白细胞:4.1×109/L,中性粒细胞绝对值:2.8×109/L,血红蛋白:105↓g/L,血小板:157×109/L;
影像学检查:
2024 年7 月 31 日,双乳 + 腋窝及锁骨上淋巴结 B 超:右乳外上低回声团,较大的约42mm×16mm×45mm (BI-RADS分类 6类);右乳外上结节(BI-RADS分类 4A类);左乳片状低回声区左乳外上见低回声区,范围约26mm×25mm×10mm(性质待定,请结合其他检查)。双侧腋窝多发淋巴结肿大(转移性考虑),双锁骨上淋巴结(性质待定)。
2024 年 8 月 1 日,肝脏增强MR:肝实质内多发结节,结合病史考虑转移瘤(约14枚)。肝门区及腹膜后多发增大淋巴结,建议复查。胆囊壁稍增厚,建议超声检查。
2024 年 8 月 5 日,骨显像:1、右侧第10后肋及双侧耻骨代谢稍活跃,建议定期复查。2、双肾及右侧输尿管腹段示踪剂滞留,请结合临床。
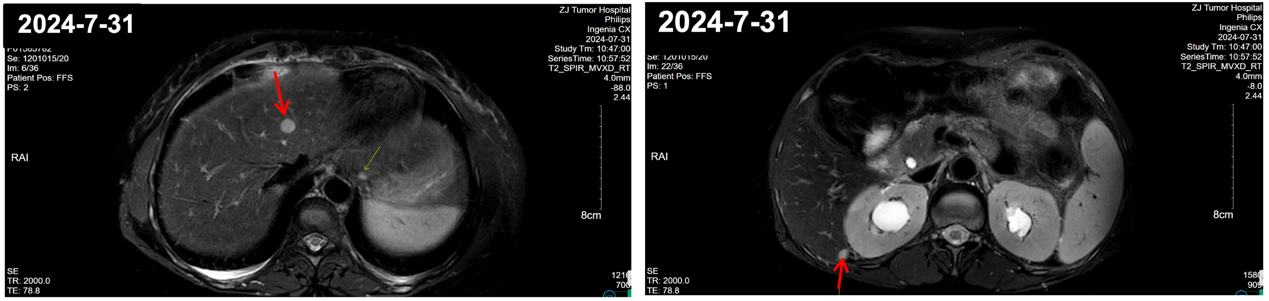
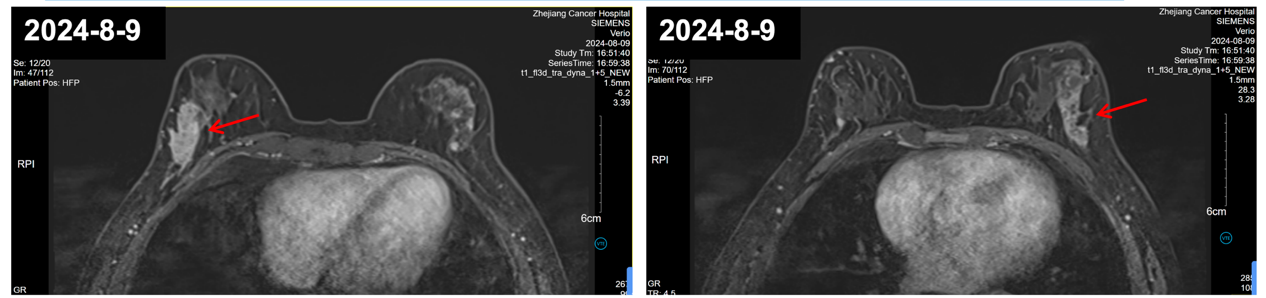
2024 年 8 月 9 日,乳腺 MR 增强:右乳外侧肿块,乳腺癌符合,BI-RADS 6级。右侧腋窝增大淋巴结,转移考虑。双乳外上象限非肿块样强化灶伴双乳导管局部扩张,导管内病变可能,BI-RADS 4A级。双乳散在强化小肿块,BI-RADS 3 级。
病理学检查:
2024 年 8 月 2 日,患者接受双侧乳房肿块麦默通旋切术。术后病理提示:
1.(左乳肿块)乳腺浸润性癌(WHO I级)。 免疫组化:(左):ER(+++,90%)、PR(+++,>90%)、AR(++,90%)、Her2(BC)(1+)、Ki-67(+,5%)、TRPS1(+)、GATA3(+)、E-cad(+)、P120catenin(膜+)。
2.(右乳肿块)乳腺浸润性癌(WHO I级)。免疫组化:(右):ER(+++,>90%)、PR(+++,>90%)、AR(++,90%)、 Her2(BC)(1+)、 Ki-67(+,10%)、E-cad(+)、P120catenin(膜+)。
临床诊断:双侧乳腺癌伴肝、腋窝淋巴结转移,IV期(luminal A型,HER2阴性)
治疗方案
2024 年 8 月 9 日起,予以患者 CDK4/6 抑制剂联合内分泌治疗至今。具体方案:瑞波西利 600mg po D1-21,来曲唑 2.5mg po qd,戈舍瑞林 3.6mg 皮下注射 q4w。
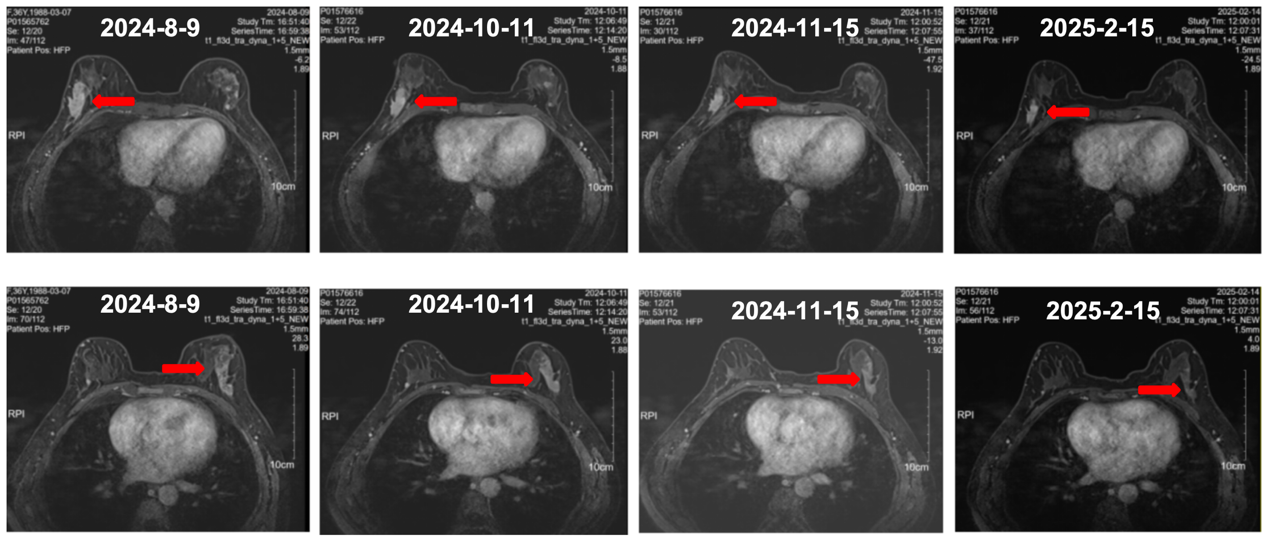
疗效评价:
乳腺 MR 增强显示,双侧乳腺癌病灶明显退缩。
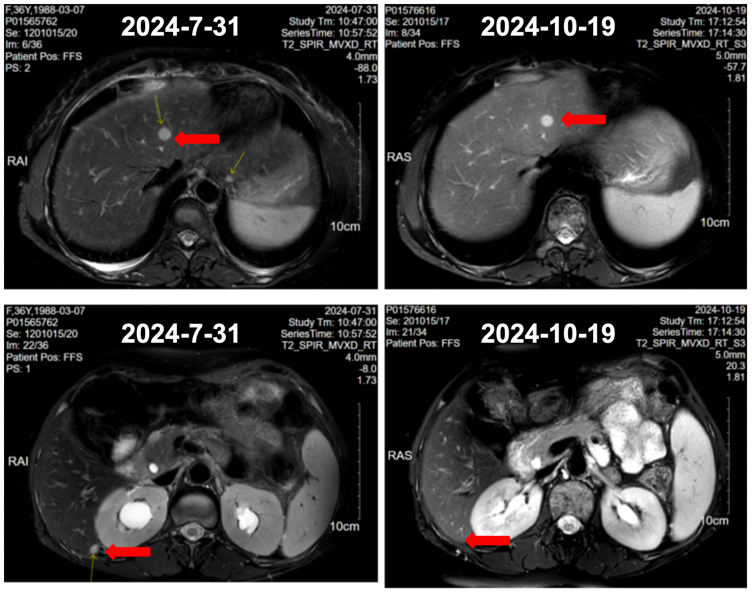
肝 CT 显示,肝多发转移病灶明显缩小。
治疗 2 周期后,肿瘤标志物癌胚抗原(CEA)、CA125、CA153持续下降。
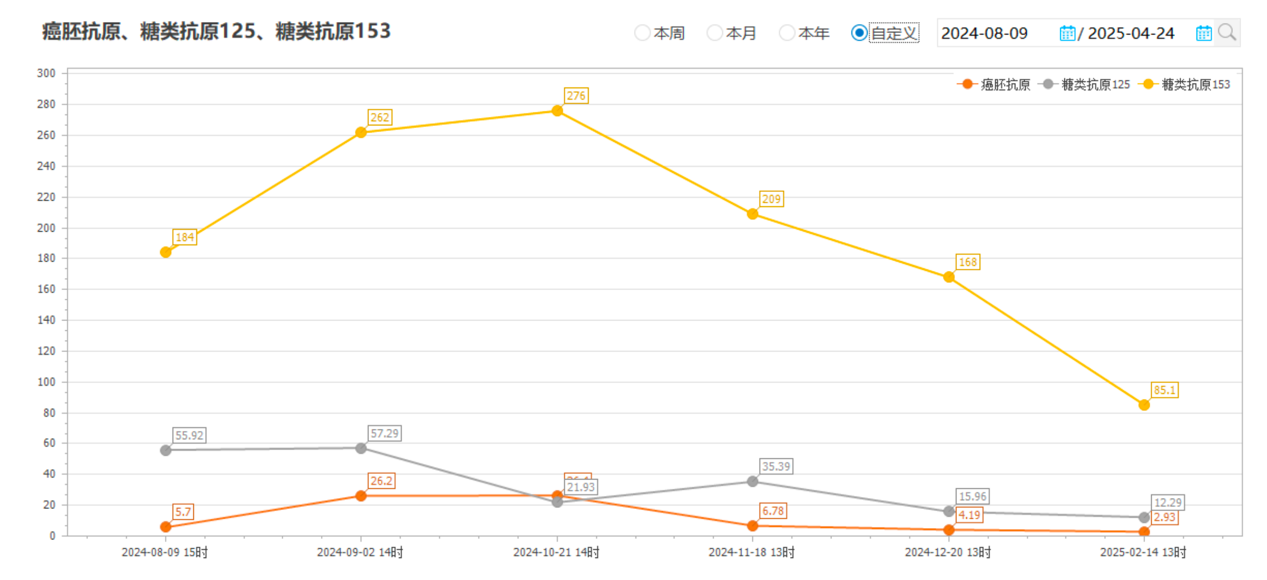
安全性评价:
治疗期间,患者曾出现白细胞、中性粒细胞下降,整体安全性可控。
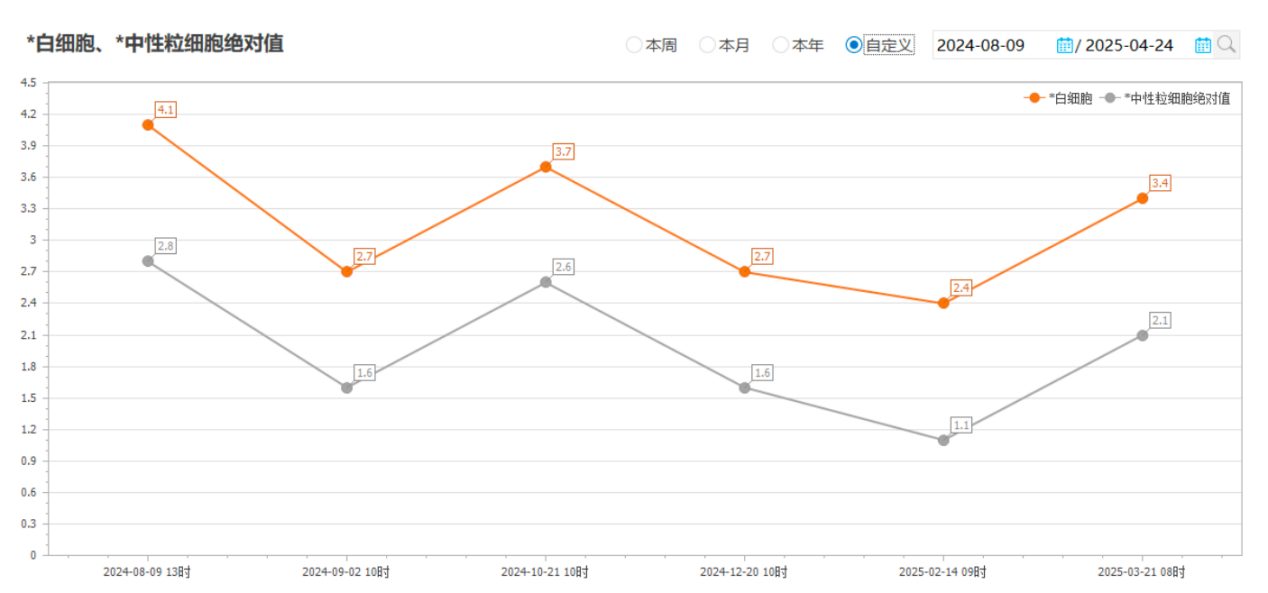
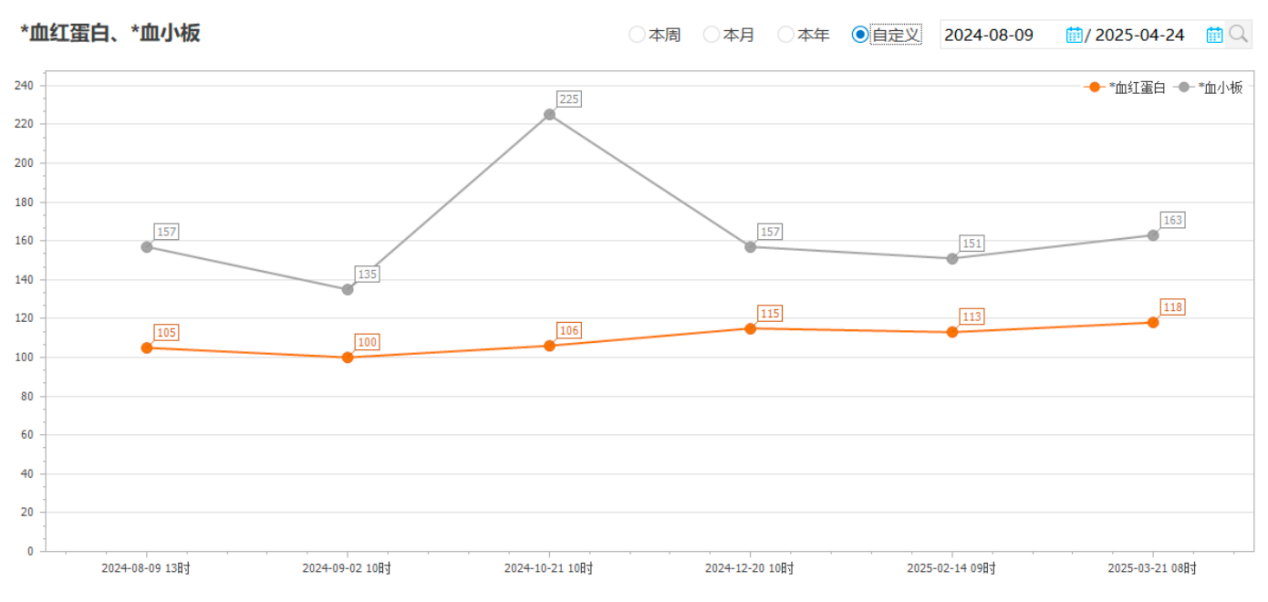
专家点评
这是一例初诊 IV 期的年轻 HR+/HER2- 晚期乳腺癌病例。患者于 2022 年发现右侧乳房肿块,未予重视。2024 年确诊时,乳腺癌细胞已经转移至肝脏。晚期一线治疗采用瑞波西利联合来曲唑联合卵巢功能抑制剂(OFS),肿瘤退缩情况较为理想,整体安全性可控。
在我国,65% 乳腺癌患者在确诊时处于绝经前或围绝经期状态[5]。值得注意的是,在HR+/HER2- 晚期乳腺癌患者群体中,绝经前患者比例高达 53%[5]。全球大型数据库的数据显示,绝经前 HR+/HER2- 乳腺癌患者的复发风险更高,生存预后更差[2]。对于 HR+/HER2- 晚期乳腺癌患者,一线治疗选择合适的治疗方案,将有利于延长整体生存期,改善生存预后。CDK4/6 抑制剂的出现,为 HR+/HER2- 乳腺癌带来了治疗新希望。
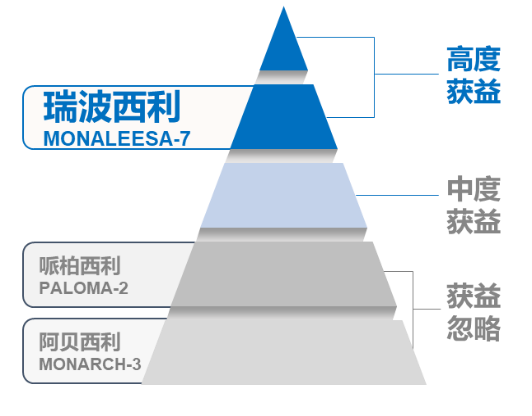
在所有CDK4/6 抑制剂中,MONALEESA-7 研究是目前唯一完全聚焦于绝经前 HR+/HER2- 晚期乳腺癌患者,且唯一取得确切OS获益的大型 III 期临床研究[4]。结果表明,瑞波西利联合 ET 能显著延长意向治疗(ITT)人群 mPFS 至 23.8 个月(安慰剂组仅 13.0 个月),中位 OS 延长至 58.7 个月(安慰剂组仅 48.0 个月)[4],提示瑞波西利联合 ET 可为绝经前 HR+/HER2- 晚期乳腺癌患者带来PFS、OS的双重获益。其中对于年龄 <40 岁亚组,瑞波西利组的 mPFS 为 29.7 个月(安慰剂组仅 10.8 个月),mOS 为 51.3 个月(安慰剂组仅 40.5 个月),进一步证实对于雌激素分泌更旺盛、复发风险更高的年轻乳腺癌患者,瑞波西利联合 ET 同样可显著降低患者复发风险,并带来超10月的OS获益[4]。此外,MONALEESA-7 研究的事后分析显示,瑞波西利联合 ET 可有效抑制绝经前 HR+/HER2- 晚期乳腺癌的雌二醇水平,降低卵巢逃逸概率,改善生存预后[6]。基于PFS及OS的双重获益,瑞波西利联合内分泌治疗已经成为HR+/HER2-晚期乳腺癌患者的一线优选治疗方案,获得NCCN乳腺癌指南的1类推荐[7]。
在此基础上,由于本例患者发病时年龄尚轻,有更多参与职场的机会和需求,承担的社会和家庭角色功能更多更复杂。研究显示,年轻患者生活质量明显更差,而该类患者对生活质量亦有更高预期[8],需在临床实践中加以关注。患者报告结局同样显示,瑞波西利能显著改善总体健康状态、身体功能、情感状态和工作效率[9],这意味着在生活质量维度上,瑞波西利联合内分泌治疗方案同样能满足本例患者的治疗需求。
对于本例患者存在的肝转移病灶,瑞波西利联合 ET 方案仍展现出理想的疗效。RIGHT Choice 研究*为本病例患者的内分泌治疗提供了有力证据[10]。该研究探索了瑞波西利联合 ET 对比双药化疗用于具有侵袭性疾病特征的 HR+/HER2- 晚期乳腺癌的疗效和安全性。研究纳入 67.6% 有症状的内脏转移患者。结果显示,瑞波西利联合内分泌治疗与化疗相比,中位 PFS 延长近 1 年(24.0 个月 vs. 12.3 个月),疾病进展或死亡风险降低 46%(HR = 0.54,95%CI:0.36~0.79,P=0.0007),且安全性更佳[10]。
总的来说,对于绝经前 HR+/HER2- 晚期乳腺癌患者,尤其是年轻患者,有效的治疗策略不仅能延长其总生存期,还可帮助患者尽早恢复正常生活。该患者在瑞波西利联合 ET 治疗期间,双乳病灶、肝转移病灶均明显退缩,且整体安全性较好。这提示对于绝经前伴有肝转移 HR+/HER2- 晚期乳腺癌患者,瑞波西利联合 ET 方案为这类患者提供了兼顾疗效与安全性的治疗选择。
*声明:瑞波西利的注册研究结果未涉及侵袭性疾病患者的有效性和安全性数据
[1] 龚畅,刘强.《中国年轻乳腺癌诊疗专家共识(2022)》解读[J].中国普通外科杂志,2023,32(11):1648-1656.
[2] Kim J, et al. Survival outcomes of young-age female patients with early breast cancer: an international multicenter cohort study. ESMO Open. 2024 Nov;9(11):103732.
[3] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)乳腺癌诊疗指南 2025[M].
[4] Lu YS, et al. Updated Overall Survival of Ribociclib plus Endocrine Therapy versus Endocrine Therapy Alone in Pre- and Perimenopausal Patients with HR+/HER2- Advanced Breast Cancer in MONALEESA-7: A Phase III Randomized Clinical Trial. Clin Cancer Res. 2022 Mar 1;28(5):851-859.
[5] Li Y, Mo H, Guan X, et al. Real world initial palliative treatment patterns and clinical outcomes in premenopausal patients with hormone receptor-positive, HER2-negative metastatic breast cancer: A study of the National Cancer Center, China. Breast. 2022;61:129-135.
[6] Estradiol suppression in premenopausal patients with hormone receptor-positive advanced breast cancer: MONALEESA-7 post-hoc analysis. 2024 ESMO ASIA P39.
[7] NCCN Guidelines Breast Cancer.
[8]中国临床肿瘤学会乳腺癌专家委员会,中国抗癌协会乳腺癌专业委员会,中华医学会外科学分会乳腺外科学组. 中国年轻乳腺癌诊疗专家共识(2022)[J]. 中华医学杂志,2023,103(6):387-403.
[9]Harbeck N,et al.Ther Adv Med Oncol . 2020;12:1758835920943065.
[10]Yen-Shen Lu et al. Final Results of RIGHT Choice: Ribociclib Plus Endocrine Therapy Versus Combination Chemotherapy in Premenopausal Women With Clinically Aggressive Hormone Receptor–Positive/Human Epidermal Growth Factor Receptor 2–Negative Advanced Breast Cancer. JCO 42, 2812-2821(2024).
[11]US Food and Drug Administration. Clinical trial endpoints for the approval of cancer drugs and biologics. Available at: https://www.fda.gov/media/71195/download. Accessed December.
[12]Johnston S, et al. NPJ Breast Cancer. 2019 Jan 17;5:5.
[13]Hortobagyi GN, et al. N Engl J Med. 2022;386(10):942-950.
[14]Dickler MN, et al. J Clin Oncol. 2016 Aug 1;34(22):2602-9.
[15]Bishal Gyawali, et al. Nat Rev Clin Oncol. 2022 Oct;19(10):613-614.
[16]Oosting SF, et al. Ann Oncol. 2023 Apr;34(4):431-439.
[17]https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-for-solid-tumours/esmo-mcbs-scorecards/scorecard-338-1.
[18] https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-scorecards/scorecard-158-1. [MONALEESA-7].
[19]https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-scorecards/scorecard-7-1. [PALOMA-2].
[20]https://www.esmo.org/guidelines/esmo-mcbs/esmo-mcbs-scorecards/scorecard-159-1. [MONARCH 3].
排版编辑:肿瘤资讯-CYX












 苏公网安备32059002004080号
苏公网安备32059002004080号


