肺癌是全球癌症死亡的首要原因,其中非小细胞肺癌(NSCLC)占80%以上。尽管指南推荐晚期NSCLC患者均需进行表皮生长因子受体(EGFR)突变检测以指导精准治疗,但真实世界中检测率和治疗选择仍存在显著差距。本文基于美国大型电子健康记录数据库(覆盖280余家癌症中心),分析了2015-2020年间16,309例晚期NSCLC患者的EGFR检测实践、治疗模式及临床结局,揭示检测不足、治疗延迟对生存的影响,相关成果已于2025年3月发表于Lung Cancer杂志。
研究背景
表皮生长因子受体(EGFR)突变是晚期非小细胞肺癌(NSCLC)的重要治疗靶点,约10%-20%的欧美患者携带EGFR敏感突变(如ex19del和L858R)。国际指南明确建议:所有晚期非鳞NSCLC患者应在治疗前完成EGFR检测,阳性者首选EGFR酪氨酸激酶抑制剂(EGFR-TKI)作为一线治疗。然而,真实世界数据显示,美国EGFR检测率虽从2010年的18%提升至2016年的61%,仍存在显著不足,且检测结果周转时间(TAT,中位20天)和治疗延迟可能影响生存获益。第三代EGFR-TKI奥希替尼等靶向药虽显著延长生存,但约25%突变患者未及时接受一线靶向治疗,反而选择化疗或免疫治疗(后者对EGFR突变患者疗效有限)。本研究通过分析美国大型真实世界数据库,揭示检测实践与治疗选择的差距,为优化临床决策提供证据。
研究方法
纳入Flatiron Health数据库中2015年1月至2020年1月诊断为IIIB-IV期NSCLC且接受一线治疗的16,309例患者,随访至2021年3月。通过电子病历提取人口学特征、EGFR检测时间与方法、一线治疗方案及生存数据。主要终点包括:EGFR检测率、检测至结果报告时间、一线治疗分布、至治疗终止/死亡时间(TTD)、至后续治疗/死亡时间(TTNTD)、总生存期(OS)。采用多变量Cox模型评估治疗选择和时间因素对预后的影响。
研究结果
1、EGFR检测率与患者特征
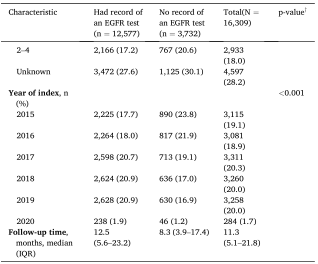
研究共纳入16,309例晚期NSCLC患者,其中12,577例(77%)有EGFR检测记录,3,732例(23%)未检测。接受检测的患者中位年龄为68岁(四分位距[IQR]:60-75),未检测组为69岁(IQR:62-75)。女性患者占比在检测组显著更高(48.8% vs 38.7%, p<0.001)。组织学类型差异明显:检测组中85.2%为非鳞癌,而未检测组仅38.1%为非鳞癌(p<0.001)。吸烟史方面,检测组无吸烟史患者比例更高(15.9% vs 4.8%, p<0.001)。从疾病分期看,检测组86.9%为转移性肿瘤(vs 未检测组68.9%),且ECOG 0-1分患者占比更高(55.2% vs 49.3%, p<0.001)(表1)。多因素分析显示,非鳞癌、转移性肿瘤及无吸烟史是接受EGFR检测的独立预测因素(p<0.001)。此外,检测率随时间显著提升:2015年仅71%患者接受检测,2019年升至81%(p<0.001)。

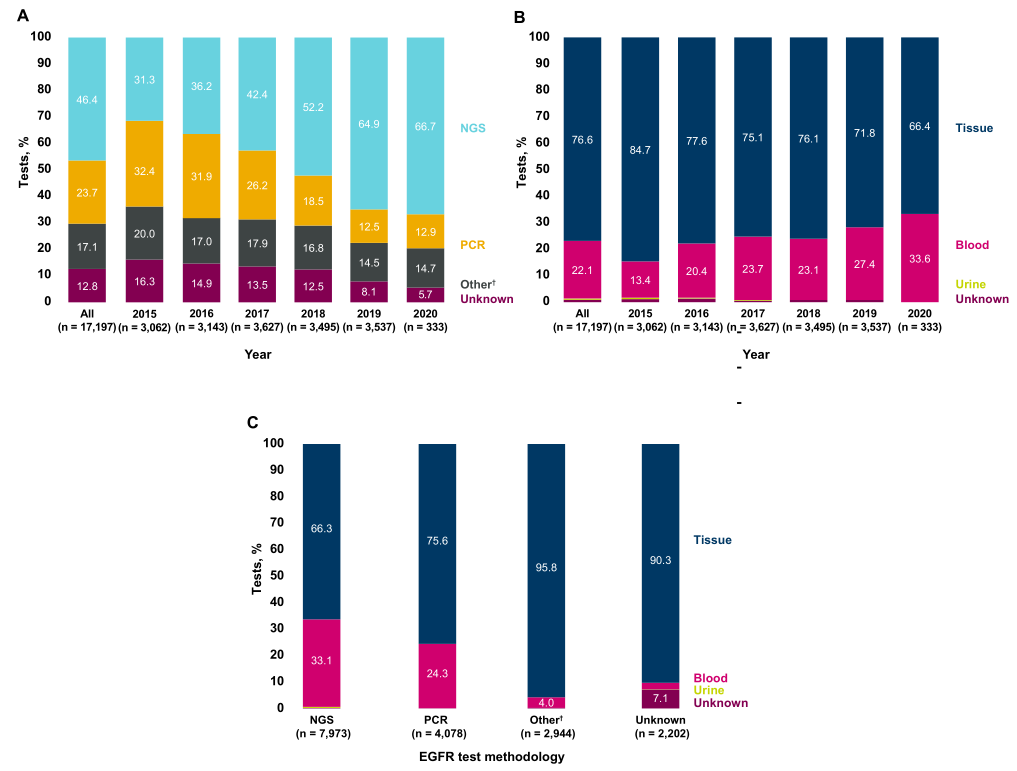
2、检测方法与时间趋势
EGFR检测标本来源中,组织样本占86%,血液样本占比从2015年的6%升至2020年的34%。二代测序(NGS)使用率逐年增加,2020年占67%,而传统PCR占比从2015年的32%降至2020年的19%(图1)。值得注意的是,使用血液样本检测的患者中,NGS占比达65%,反映液态活检与NGS技术的协同应用趋势。
3、治疗选择与检测时间的关系
EGFR突变阳性率为15%(1,914/12,577),其中93%在治疗前获知检测结果。治疗前检测的中位时间为诊断后20天(IQR:13-35天),而治疗后检测延迟诊断后276天(IQR:109-391天)。
EGFR突变阳性且治疗前获知结果的患者中,75%接受一线EGFR-TKI(奥希替尼占主导),11%选择化疗,9%免疫治疗(表2)。若检测结果发布时间延迟至治疗后,仅13%切换为EGFR-TKI,50%继续化疗。未接受EGFR-TKI的患者中,53%携带敏感突变(ex19del/L858R),提示治疗决策与检测时效密切相关。此外,136例一线治疗后检出EGFR突变的患者中,仅17例(12.5%)在后续治疗中接受了EGFR-TKI,中位切换时间为3.7个月,提示部分患者因病情进展或毒性无法继续非靶向治疗。EGFR突变阳性率为15%(1,914/12,577),其中93%在治疗前获知检测结果。治疗前检测的中位时间为诊断后20天(IQR:13-35天),而治疗后检测延迟诊断后276天(IQR:109-391天)。
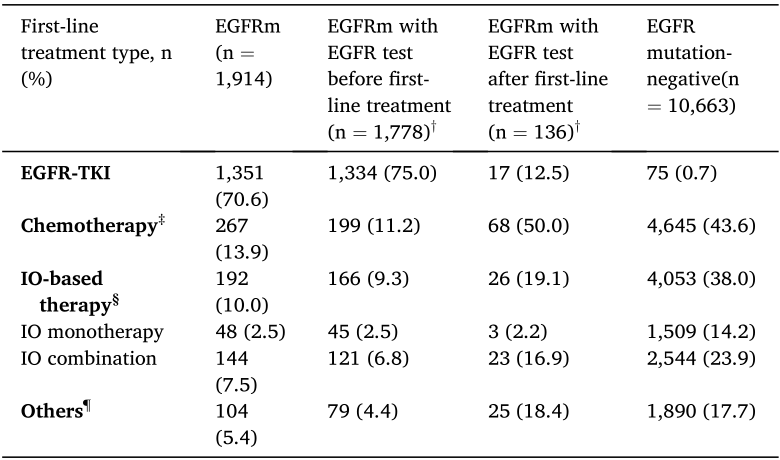
表2. 接受EGFR检测患者的一线治疗类型分布(按EGFR检测结果及检测时间分类,n=12,577)
4、生存分析
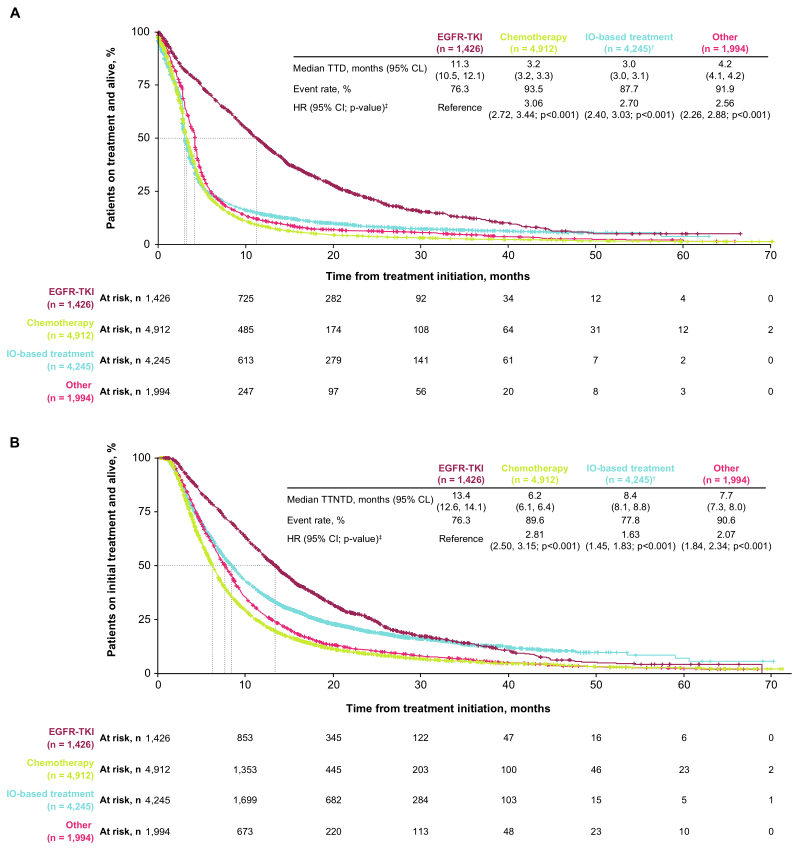
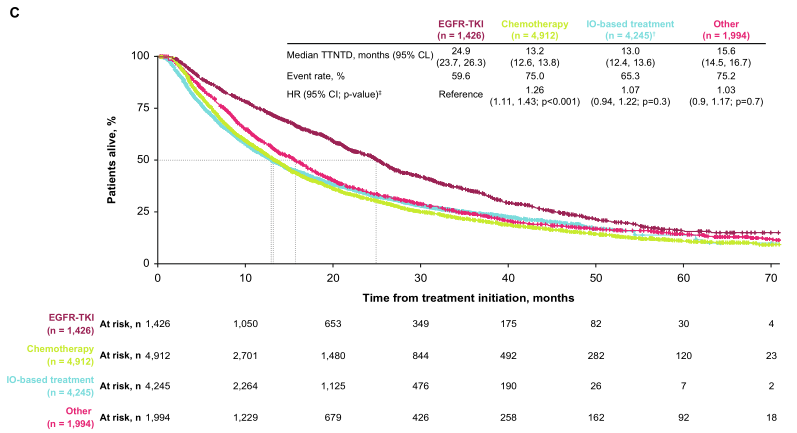
一线EGFR-TKI的TTD(中位11.3月)和TTNTD(中位13.4月)显著优于化疗(3.2月/6.2月)和免疫治疗(3.0月/8.4月)(图2)。调整基线特征后,EGFR-TKI的死亡风险较化疗降低48%(HR=0.52, 95%CI 0.48-0.57, p<0.001)。此外,诊断后≥21天启动治疗的患者OS更长(15.1 vs 12.9月,HR=0.79, 95%CI 0.72-0.88, p<0.001),可能与充分等待检测结果后选择靶向治疗相关。值得注意的是,EGFR-TKI治疗组内,诊断至治疗时间≥21天的患者OS(25.7月)与<21天(25.9月)无显著差异(HR=0.87, p=0.2),表明靶向治疗疗效不受短时间延迟影响。
5、EGFR未检测人群的特征与结局
在3,732例(23%)未接受EGFR检测的患者中,鳞癌占比62%,吸烟史高达95%,ECOG≥2分比例(20.6%)高于检测组(17.2%)。该人群一线治疗以化疗(42%)和免疫治疗(38%)为主,中位OS仅8.3月,显著低于检测组(11.3月)。提示未检测人群可能因临床状况差或认知偏差错失靶向治疗机会。
研究结论
本研究揭示了真实世界晚期NSCLC患者EGFR检测和治疗的三大关键问题:近1/4患者未接受EGFR检测,检测周转时间影响一线治疗选择,约25%突变患者未及时使用EGFR-TKI。数据表明,缩短检测时间、提高检测率(尤其鳞癌/吸烟人群)和强化指南依从性,可显著改善患者生存。血液NGS的普及为快速检测提供新方向,而治疗延迟患者的生存优势提示精准检测的优先级高于盲目抢先治疗。未来需推动多学科协作和检测流程标准化,确保患者从靶向治疗中最大获益。
Subramanian J, Gregg J, Berktas M, Li J, Leighl NB. EGFR testing practices, treatment choice and clinical outcomes in advanced NSCLC in a real-world setting: A retrospective analysis of a US-based electronic health records database. Lung Cancer. 2025;201:108412. doi:10.1016/j.lungcan.2025.108412。
审批编号:CN-158261
过期日期:2025-07-15
本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考
排版编辑:肿瘤资讯-Sally











 苏公网安备32059002004080号
苏公网安备32059002004080号


