激素受体阳性(HR+)HER2阴性(HER2-)晚期乳腺癌的治疗策略已因细胞周期依赖性激酶(CDK)4/6抑制剂的引入而发生变革,显著提升了患者的生存期。2024年1月19日,国际期刊Breast Cancer Research and Treatment在线刊登了一篇研究结果[1]。通过系统回顾和荟萃分析,研究团队探讨了HER2低表达状态与使用CDK 4/6抑制剂治疗的HR+转移性乳腺癌患者的生存率之间的关系。结果表明,HER2低表达患者的进展或死亡风险显著高于HER2阴性患者。【肿瘤资讯】特梳理综述主要内容如下,以飨读者。

引言
CDK 4/6抑制剂显著改变了HR+、HER2-转移性乳腺癌(MBC)的治疗格局[2]。CDK 4/6抑制剂联合内分泌治疗成为一线和二线标准治疗方案,提高了无进展生存期(PFS)和总生存期(OS)[3,4]。目前,这些药物在临床中被广泛使用,但并非所有患者均能从中受益。研究发现,约15%的患者在一线治疗中也会出现疾病进展[5,6]。因此,迫切需要能够预测长期受益和早期进展的生物标志物。
HER2受体家族在内分泌治疗耐药中起着关键作用,针对该途径的靶向治疗已应用于HER2+乳腺癌超过20年[7]。近年来, “HER2低表达乳腺癌”的概念引起广泛关注,其对患者预后的影响尚未明确[8,9],并且,现有的研究在研究设计、患者群体、样本量以及结局方面存在差异。本研究旨在系统评价HER2低表达对接受CDK 4/6抑制剂治疗的HR+MBC患者疗效的影响。
研究方法
文献检索:遵循PRISMA指南,系统检索Pubmed、Web of Science和Scopus数据库,筛选截至2023年8月8日发表的相关研究。使用的检索术语包括“HER2 low、“low HER2”、“ERBB2 low”、“low ERBB2”、“CDK”、“细胞周期蛋白依赖性激酶”和“CDK 4/6抑制剂”。
纳入标准包括:(1)前瞻性或回顾性研究,评估HER2低表达与CDK 4/6抑制剂治疗的PFS或OS的关联;(2)提供HER2低表达与HER2零表达组比较的(风险比)HR和95% 置信区间(CI);(3)英文全文或摘要。排除标准包括重复文章、综述、病例报告、指南、动物和细胞研究、儿童患者研究、不提供PFS或OS数据的研究、试验方案等。
研究结果
本研究纳入了9项研究,共2705名患者。其中,5项为多中心研究,4项为单中心研究。8项研究是回顾性研究,仅有1项是前瞻性研究。所有研究均纳入了接受芳香化酶抑制剂或氟维司群联合CDK 4/6抑制剂治疗的患者。各研究的样本量在84到1084之间不等,其中5项研究的样本量少于200名患者,中位随访时间范围在15至36个月之间。综合分析显示,HER2低表达组的进展和/或死亡风险显著更高(HR: 1.22, 95% CI 1.10–1.35, p < 0.001),如图1所示。
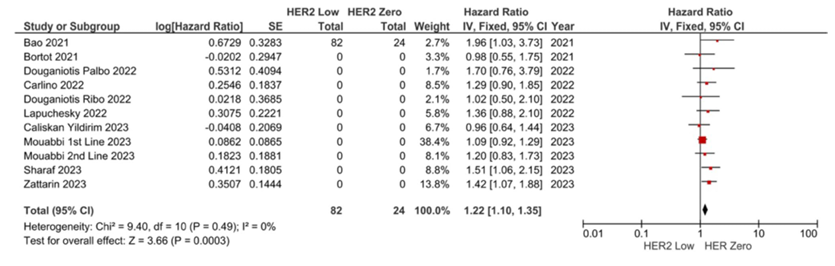
图1. PFS的荟萃分析结果,菱形表示综合效应值
在5项研究的综合分析中(图2),HER2低表达组的死亡风险较高(HR: 1.22, 95% CI 1.04–1.44, p = 0.010),所纳入的研究异质性较低(I² = 0%),剔除个别研究后进行的敏感性分析显示出一致的结果。
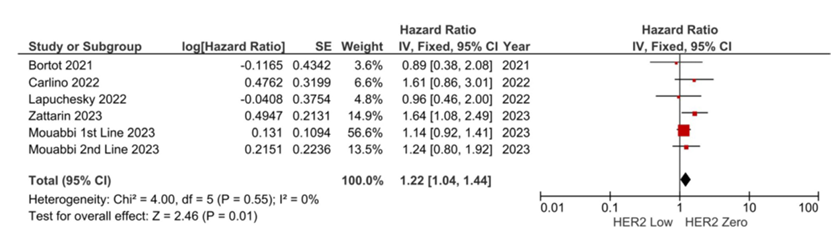 图2. OS的荟萃分析结果,菱形表示综合效应值
图2. OS的荟萃分析结果,菱形表示综合效应值
在基因表达水平上,观察到基底样相关基因/PAM50标记和免疫基因(如CD8A、PDCD1和CD274)的显著上调,以及CD4、ROR-P评分、乳腺相关和增殖相关基因/PAM50标记的显著下调(图 2C)。
此外,3项研究还分析了ORR,结果显示,HER2低表达组和HER2阴性组的ORR相似(HR: 0.80, 95% CI 0.44–1.44, p = 0.460) (图3)。
 图3. ORR的荟萃分析结果
图3. ORR的荟萃分析结果
研究讨论
本研究结果表明,HER2低表达状态可能通过增强内分泌耐药性,降低CDK 4/6抑制剂的疗效。CDK 4/6抑制剂治疗后早期进展患者的特征是当前研究的关键领域。既往数据表明,内脏转移和ECOG状态等临床特征,以及RB1和CCNE1等分子生物标志物与更高的进展风险相关[2]。此外,考虑到基于RNA的HER2富集分析的成本问题,通过免疫组织化学评估HER2低表达状态可能是在接受CDK 4/6抑制剂治疗的患者中评估ErbB2通路激活的替代指标。已有研究表明,HER2低表达肿瘤具有更高的ESR1[10]和AKT表达[11],这些特征与对CDK 4/6抑制剂的耐药性相关。因此,将HER2低表达状态作为接受CDK 4/6抑制剂治疗患者的疗效生物标志物是有益的,具有重要的生物学意义。
本荟萃分析存在一些局限性。首先,纳入的大多数研究为回顾性,样本量有限。研究队列在治疗线和内分泌治疗方面存在异质性,限制了亚组分析的统计功效。大多数研究的随访时间较短,影响了总生存期结果的可靠性。由于大多数研究为回顾性,无法确定HER2低表达状态对生存结局的因果关系,因此研究者使用“关联”一词而非“效应”。 尽管存在这些局限性,但在超过2700名患者的汇总队列中,研究者观察到HER2低表达对生存结果的负面影响。如果这些结果得到长期随访的前瞻性研究的支持,晚期HR+ HER2低表达乳腺癌患者可能受益于新型联合疗法,从而改善CDK 4/6抑制剂的预后。
研究结论
本研究表明,HER2低表达患者使用CDK 4/6抑制剂的进展或死亡风险显著更高。尽管CDK 4/6抑制剂联合内分泌治疗是标准治疗方案,但需要进一步研究以改善HR+HER2低表达肿瘤患者的预后。
1. Guven DC, Sahin TK. The association between HER2-low status and survival in patients with metastatic breast cancer treated with Cyclin-dependent kinases 4 and 6 inhibitors: a systematic review and meta-analysis. Breast Cancer Res Treat. 2024;204(3):443-452. doi:10.1007/s10549-023-07226-1
2. Finn RS, Martin M, Rugo HS, et al. Palbociclib and letrozole in advanced breast cancer. N Engl J Med. 2016;375:1925–1936. doi: 10.1056/NEJMoa1607303.
3. Tripathy D, Im SA, Colleoni M, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone-receptor-positive, advanced breast cancer (MONALEESA-7): a randomised phase 3 trial. Lancet Oncol. 2018;19:904–915. doi: 10.1016/s1470-2045(18)30292-4.
4. Finn RS, Crown JP, Lang I, et al. The cyclin-dependent kinase 4/6 inhibitor palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptor-positive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18): a randomised phase 2 study. Lancet Oncol. 2015;16:25–35. doi: 10.1016/s1470-2045(14)71159-3.
5. Hortobagyi GN, Stemmer SM, Burris HA, et al. Updated results from MONALEESA-2, a phase III trial of first-line ribociclib plus letrozole versus placebo plus letrozole in hormone receptor-positive, HER2-negative advanced breast cancer. Ann Oncol. 2018;29:1541–1547. doi: 10.1093/annonc/mdy155.
6. Goetz MP, Toi M, Campone M, et al. MONARCH 3: abemaciclib as initial therapy for advanced breast cancer. J Clin Oncol. 2017;35:3638–3646. doi: 10.1200/jco.2017.75.6155.
7. Alataki A, Dowsett M. Human epidermal growth factor receptor-2 and endocrine resistance in hormone-dependent breast cancer. Endocr Relat Cancer. 2022;29:R105–r122. doi: 10.1530/erc-21-0293.
8. Guven DC, Kaya MB, Fedai B, et al. HER2-low breast cancer could be associated with an increased risk of brain metastasis. Int J Clin Oncol. 2022;27:332–339. doi: 10.1007/s10147-021-02049-w.
9. Yang C, Zhang X, Chen Y, et al. Survival differences between HER2-0 and HER2-low-expressing breast cancer − a meta-analysis of early breast cancer patients. Crit Rev Oncol Hematol. 2023;185:103962. doi: 10.1016/j.critrevonc.2023.103962.
10. Hui T, Li S, Wang H, et al. An analysis of clinical and pathologic features, recurindex genomic profiles, and survival outcomes in HER2-low breast cancer. Oncologist. 2023 doi: 10.1093/oncolo/oyad159.
11. Li Y, Tsang JY, Tam F, et al. Comprehensive characterization of HER2-low breast cancers: implications in prognosis and treatment. EBioMedicine. 2023;91:104571. doi: 10.1016/j.ebiom.2023.104571.
声明:材料由阿斯利康支持,仅供医疗卫生专业人士参考
审批号:CN-140378
排版编辑:肿瘤资讯-Ale











 苏公网安备32059002004080号
苏公网安备32059002004080号


