既往十年见证了晚期肝细胞癌(HCC)的系统治疗进展。精准治疗代表着肿瘤治疗格局的改变,使用特定分子特征制定个体化治疗模式,旨在实现治疗疗效最大化。然而精准治疗在HCC中依旧处于起步阶段。近期,中国学者在国际知名肿瘤期刊Cancer Cell(IF 50.3)上发表的综述,对HCC精准治疗的生物标志物、分子分类、肿瘤微环境异质性等方面的前沿进展进行了梳理。
既往酪氨酸激酶抑制剂(TKI)一直是HCC的唯一治疗选择。随着IMbrave150等研究成果的公布,免疫检查点抑制剂(ICI)开启了晚期HCC一线治疗新纪元。
然而大多数患者依旧会发生耐药,筛选能够从特定治疗中获益的患者才能最大化获益、减小毒性和节约医疗资源。但是目前还没有应用于临床的生物标志物。此外,明确肿瘤微环境(TME)和免疫治疗结局的关系也十分重要。
获批疗法的生物标志物
分子靶向治疗
索拉非尼具有靶向抑制肿瘤细胞增殖和肿瘤血管生成的作用,因此MAPK通路的替代指标p-ERK是索拉非尼敏感性的潜在生物标志物。DKK1可抑制WNT信号通路,有研究发现DKK1表达和索拉非尼敏感性具有强相关性。
血浆生物标志物如VEGF、ANG2、FGF19、FGF21等和仑伐替尼反应具有相关性。还有研究发现了白蛋白-胆红素评分和瑞戈非尼、基线AFP和卡博替尼等的相关性。AFP可预测卡博替尼、雷莫西尤单抗、阿替利珠单抗+贝伐珠单抗等疗法的疗效,显示其作为治疗相关生物标志物的潜力。
免疫检查点阻滞疗法
PD-L1表达和免疫治疗反应的相关性还不清楚。免疫细胞特异性生物标志物可作为潜在免疫生物标志物,如更高的CD8评分、CXCL13+TH和PD-1hiCD8+效应T细胞等和免疫反应相关,而PD-1hiCD8+终末耗竭T细胞主要见于无反应患者。肿瘤突变负荷(TMB)和HCC免疫反应不相关。CTNNB1突变患者常对免疫治疗耐药。
外周血标志物或可预测疗效。更低的治疗前中性粒细胞-淋巴细胞比值(NLR)和更高的反应率相关。更高的基线CD14+和CD16+单核细胞水平和缺乏反应相关。此外,循环CXCR3+CD8+效应记忆T细胞和CD11c+HLADRhi抗原呈递细胞等可能也具有一定作用。
此外,部分免疫治疗相关不良事件(irAE)的发生也和ICI疗效相关。肠道微生物也可作为疗效预测性标志物和有潜力的治疗靶点。
病因对于治疗结局的影响
目前的证据显示不同病因导致的HCC具有显著不同的临床病理学和治疗差异。索拉非尼在丙型肝炎相关HCC中更有效。病毒相关HCC患者接受仑伐替尼具有更差的生存结局,而在非酒精性脂肪肝病(NAFLD)患者中疗效更佳,治疗乙型肝炎相关患者结局优于丙型肝炎患者。
非酒精性脂肪性肝炎(NASH)相关鼠肿瘤模型中,ICI常无效。临床数据显示ICI在非病毒性HCC患者中结局较差。这些病因导致的临床和生物学异质性可能和生物标志物变异相关。
具有治疗启示的分子分类
综合分类揭示亚类特异性药物反应
HCC具有多种分类系统。目前各种分类系统为发展亚类特异性治疗策略提供了理论基础(图1A)。其中,Hoshida提出的分类系统(S1-S3)是研究最为广泛的分类。S1亚类具有TGF-β和WNT通路活化,对SRC/ABL抑制剂敏感。S2亚类FGFR3/4表达增加和MYC/AKT活化,对FGFR抑制剂和BET溴区结构域抑制剂敏感。此外,基于众多亚型的药物开发也在进行中。
蛋白组学分类发现潜在治疗靶点
蛋白组学研究发现代谢和免疫因素在分类中具有重要作用。目前各研究的蛋白组学分类具有高度一致性,显示其反映HCC生物异质性具有更高准确性(图1B)。
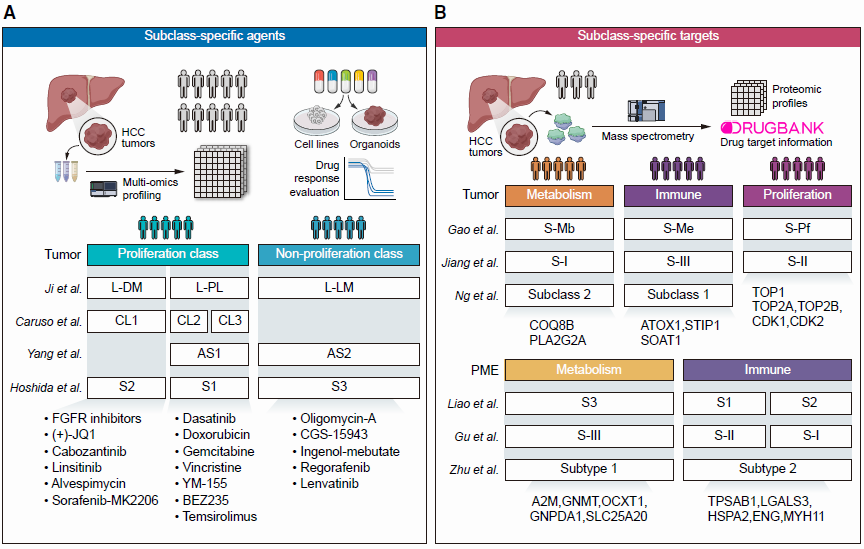
图1 分子分类(A)多组学分类(B)蛋白组学为基础的分类
HCC微环境对免疫反应的影响
基于TME进行的分类,将炎症组包括免疫亚类(22%)和免疫样亚类(15%),非炎症组分为豁免亚类(20%)和中间亚类(43%)(图2A)。而单细胞测序分类可反映细胞组成和功能(图2B)。TME细胞的空间分布可显著影响肿瘤免疫动态,不同表型具有不同的CD8+T细胞空间分布(图2C),这对于破译TME复杂性和追踪免疫耐药十分重要。
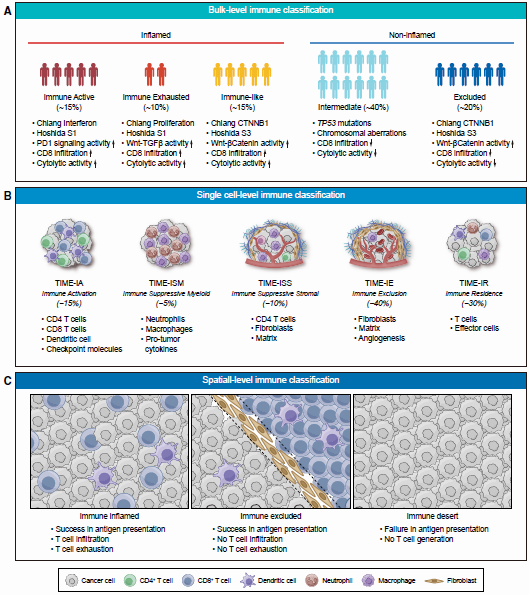
图2 微环境分类(A)大体水平;(B)单细胞水平;(C)空间分布水平
临床前与临床之间的桥梁
液体活检是一种前沿微创技术,可提供肿瘤分子特征“快照”。影像学为基础的人工智能分析同样对于HCC分型具有巨大潜力。
单细胞测序和空间组学在发现生物标志物、进行患者分层、早期诊断和监测微小残留病等方面具有希望。
总之,需要积极发展新型技术进展来桥接临床前研究和临床应用。
肝癌精准治疗未来发展方向
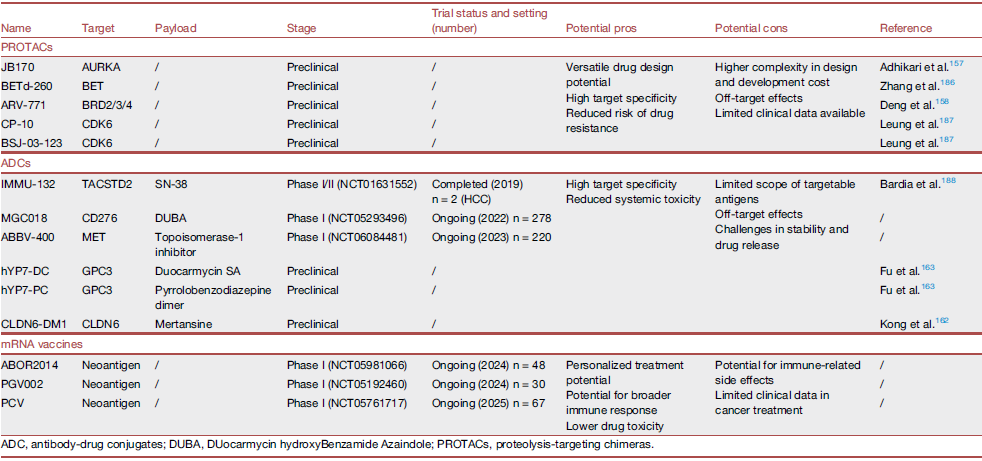
治疗策略方面,蛋白裂解靶向嵌合体(PROTACs)、抗体偶联药物(ADCs)和mRNA疫苗是具有吸引力/前景的发展方向(图3A,表1)。
生物标志物驱动临床试验可将异质性患者分层,进而优化资源(图3B)。越来越多此类试验正在进行,如REACH-2研究了评估雷莫西尤单抗在AFP≥400ng/mL HCC患者中的疗效。有必要在未来研究中将不同病因学患者分类进行治疗探索。
功能分析指导的个体化治疗是提高有效治疗的新型方法(图3C)。通过使用患者来源肿瘤模型可进行药物筛选,指导后续治疗选择。
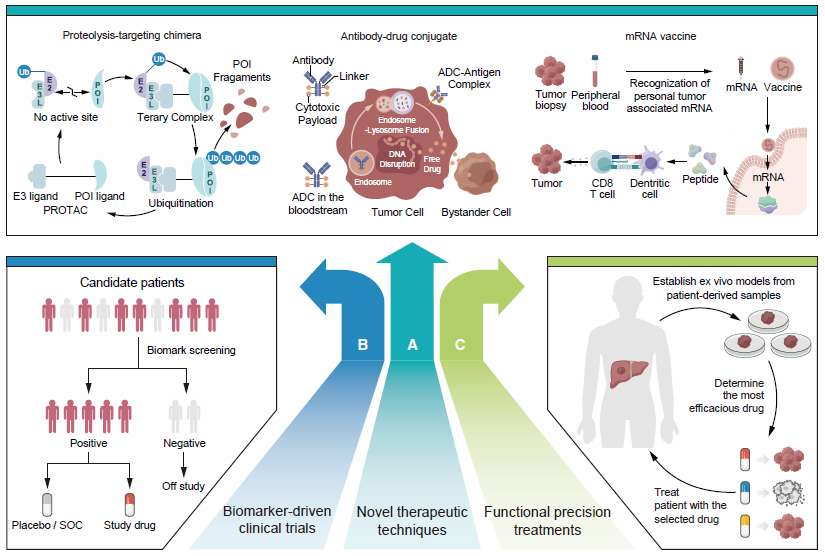
图3 精准治疗的未来方向
表1 HCC新型治疗技术
总结
生物标志物的发现可促进HCC个体化治疗发展。分子分型指导治疗决策是另一个有效方法,但是临床前研究和临床研究还存在差距。未来发展方向中,功能分析指导治疗最令人振奋,有助于将临床获益最大化。总之,治疗应强调个体化,促进HCC患者生存不断延长。
Yang X, et al. Precision treatment in advanced hepatocellular carcinoma. Cancer Cell. 2024;42(2):180-197.
排版编辑:肿瘤资讯-Marie











 苏公网安备32059002004080号
苏公网安备32059002004080号


