近年来,全球食管癌新辅助治疗和辅助治疗取得了卓越疗效和进展,但仍缺乏进一步的高质量研究探索更佳的食管癌围术期治疗模式。多项小样本研究显示,食管癌新辅助免疫治疗具有良好的应用前景,但尚无大型的前瞻性III期研究证实。在刚刚落幕的2024 ASCO GI会议上,由李印教授牵头开展、全国24家中心共同参与的一项“卡瑞利珠单抗联合化疗对比化疗新辅助治疗可切除局晚期食管鳞癌(ESCC)”的全国多中心、随机、平行对照III期研究(ESCORT-NEO/NCCES01)1成功入选LBA,成为全球首个食管癌围术期免疫治疗III期研究,研究结果显示,卡瑞利珠单抗+白蛋白紫杉醇+顺铂组(A组)和卡瑞利珠单抗+紫杉醇+顺铂组(B组)病理完全缓解(pCR)率均显著优于紫杉醇+顺铂组(C组)(A组 vs C组,28.0% vs 4.7%,p<0.0001;B组 vs C组,15.4% vs 4.7%,p=0.0034),两组均达到了主要终点,且未增加手术风险,安全性良好。ESCORT-NEO研究为中国乃至世界食管癌的临床实践和治疗策略提供了重要参考证据。
为第一时间了解全球首个食管癌围术期免疫III期研究结果,探索食管癌围术期治疗的未来发展趋势,“耀新生·愈食光”栏目组诚挚邀请中国医学科学院肿瘤医院康晓征教授作为主持,日本国立癌症研究中心医院的Ken Kato教授、中国医学科学院肿瘤医院李印教授和秦建军教授作为“ESCORT-NEO中外面对面”的访谈嘉宾,共同解读ESCORT-NEO研究首发数据,探讨全球食管癌围术期免疫治疗现状与趋势,展望中外食管癌研究合作的未来。
中外食管癌新辅助治疗模式多元与特色并存,求同存异,和而不同
康晓征教授:食管癌作为全球十大恶性肿瘤之一,其治疗是医学界重要课题。目前,局晚期可切除食管癌新辅助治疗为更多患者提供了更好手术及生存机会,新辅助治疗已呈现出并行发展的多元模式,李印教授和Ken Kato教授能否先分别谈谈中外食管癌的新辅助治疗现状?
李印教授:食管癌是中国特色癌种,与西方国家相比,中国食管癌以鳞状细胞癌为主,且多数患者确诊时已为局部晚期或晚期2。根据中国、欧美、日本等国家临床诊疗指南,针对局晚期可切除食管癌这一群体,新辅助治疗是标准的治疗手段,然而,具体的治疗模式却有所差异。以中国临床肿瘤学会(CSCO)食管癌诊疗指南为例,新辅助放化疗与新辅助化疗均被认定为标准的治疗方案3。这些治疗模式的制定并非仅基于国内研究,还汲取了欧美和日本的研究成果。目前在中国,新辅助化疗是主流选择,大约占到60%。随着近两年新辅助免疫联合化疗II期临床试验数据的陆续发布4-8,这一新兴治疗方案受到了医疗界的青睐,尤其在一些大型医疗中心,其应用比例超过了新辅助放化疗和新辅助化疗方案。
Ken Kato教授:日本与中国食管癌发病率相似,但由于实施了针对消化道肿瘤的筛查计划,因此日本食管癌患者在疾病早期阶段被诊断的概率更高,20%的患者处于I期,60%的患者处于II期或III期。在日本,基于JCOG1109 III期临床研究结果,新辅助化疗联合手术的治疗模式被定为日本的标准新辅助治疗方案,化疗方案采用DCF(多西他赛、顺铂和5-氟尿嘧啶)三联疗法9。而在西方国家,基于CROSS试验结果,新辅助放化疗加手术治疗局晚期可切除食管癌的模式占主导,具体方案为紫杉醇加卡铂联合放疗10。
ESCC在亚洲比例更高且备受关注,亚洲研究者肩负着提供更多本土化循证医学证据的重任,这些经验对改善食管癌治疗策略具有重要的借鉴意义。
李印教授:中日在新辅助化疗方案上呈现出明显差异。在我国TP(紫杉醇和顺铂)方案被广泛采用,日本却对DCF方案推崇备至。鉴于两种方案在疗效和安全性上有不同的优势,如果开展新辅助TP与DCF方案的比较研究,可以为实现个体化治疗提供更为扎实的科学依据,提升患者的总体治愈率和生活质量。
艾瑞卡开启食管癌围术期免疫治疗新食代,实现疗效安全双保障
康晓征教授:近年来食管癌免疫治疗发展迅猛,重磅研究层出不穷,本次ASCO GI发布的ESCORT-NEO/NCCES01研究是全球首个食管癌围术期免疫治疗III期研究,为局晚期食管癌治疗选择提供了重要的证据基础。可否请秦建军教授介绍下ESCORT-NEO/NCCES01研究的设计亮点?并详细解读下该研究的疗效和安全性结果?
秦建军教授:ESCORT-NEO/NCCES01研究是一项前瞻性、多中心、三臂、III期临床研究,共纳入391例T1b-3N1-3M0或T3N0M0可切除的ESCC患者。患者被随机分配为三组进行2个周期新辅助治疗:试验A组为卡瑞利珠单抗联合白蛋白紫杉醇和顺铂,B组为卡瑞利珠单抗联合紫杉醇和顺铂;对照C组为紫杉醇和顺铂。研究主要终点是经盲态独立审查委员会(BIRC)评估的意向治疗(ITT)人群pCR率和研究者评估的无事件生存期(EFS);次要终点包括R0切除率、主要病理缓解(MPR)率、总生存期(OS)、安全性等;探索性终点包括生物标志物探索和患者报告结局。
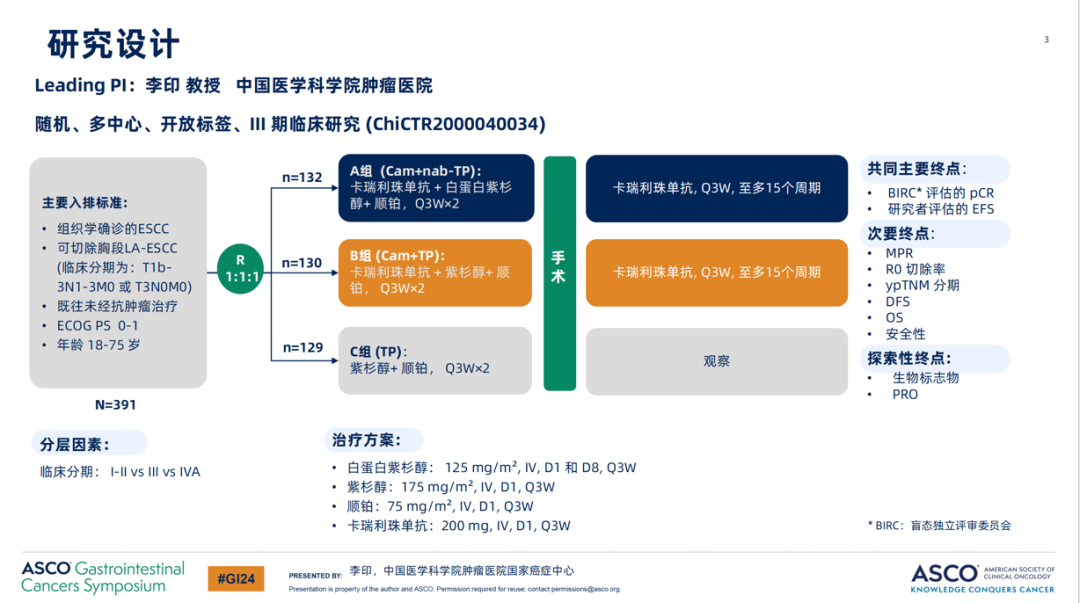 图1. ESCORT-NEO/NCCES01研究设计
图1. ESCORT-NEO/NCCES01研究设计
研究结果表明,新辅助卡瑞利珠单抗联合化疗较新辅助化疗显著提高局晚期可切除食管癌患者的pCR率。A组(卡瑞利珠单抗+nab-TP) vs C组(TP)的pCR率为28.0% vs 4.7%(p<0.0001);B组(卡瑞利珠单抗+ TP) vs C组(TP)的pCR率为15.4% vs 4.7%(p=0.0034),两组均取得了统计学显著差异。三组的MPR率分别为59.1%,36.2%和20.9%。在进行根治性手术患者人群中,R0切除率亦微有差异:A组(卡瑞利珠单抗+nab-TP)为99.1%,B组(卡瑞利珠单抗+TP)为95.7%,C组(TP)为92.2%;三组术后并发症发生率分别是:34.2%,38.8%,32.0%;安全性方面,新辅助治疗期间,≥3级不良事件的发生率与化疗组相近,分别为34.1%,29.2%,28.8%。包括EFS和OS在内的长期生存获益目前正在持续评估中1。以上数据揭示了卡瑞利珠单抗联合化疗作为局晚期可切除食管癌新辅助治疗的有效性和安全性, ESCORT-NEO/NCCES01研究为食管癌围术期免疫治疗提供了有力的临床依据,并为未来的治疗决策提供重要参考。
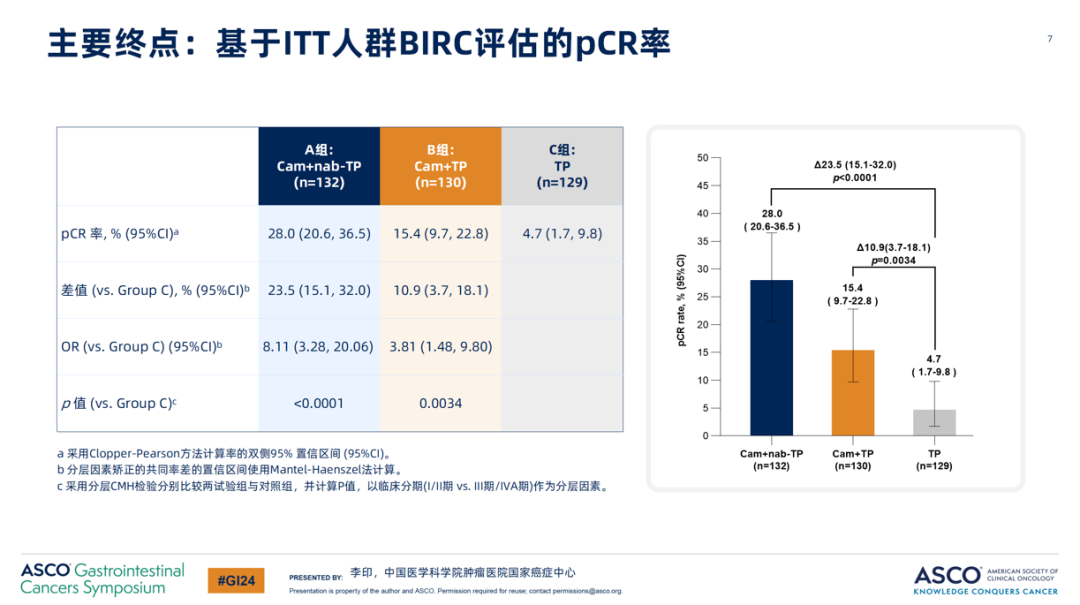 图2. BIRC评估的ITT人群pCR率
图2. BIRC评估的ITT人群pCR率
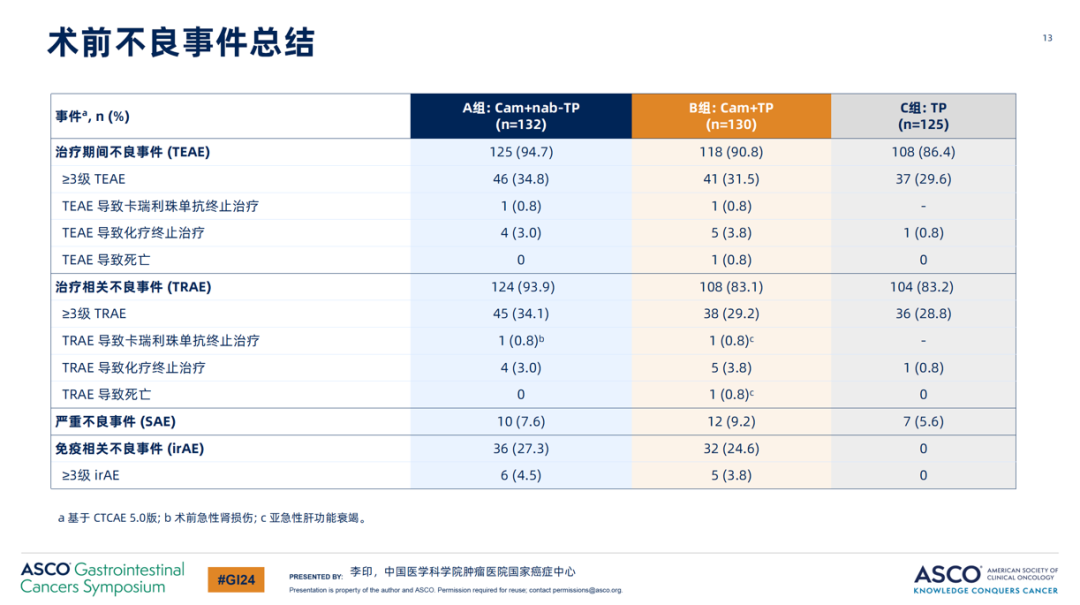 图3. 术前不良事件总结
图3. 术前不良事件总结
MDT视角下食管癌围术期免疫治疗的未来前景
康晓征教授:基于ESCORT-NEO/NCCES01研究结果,我们看到新辅助免疫联合化疗治疗局晚期可切除食管癌优越的疗效及可控的安全性。三位教授如何看待食管癌围术期免疫治疗的未来应用前景?围术期免疫治疗又会为食管外科带来哪些新挑战?
李印教授:前期我们进行了新辅助免疫联合化疗的II期试验,初步探明了该方案的疗效和安全性11。随后ESCORT-NEO/NCCES01 III期研究扩大了样本量并进行多中心协作,新辅助卡瑞利珠单抗联合白蛋白紫杉醇和顺铂方案体现出的有效性和安全性给了我们很大的信心。然而,也浮现出一些新的关键临床问题:第一,既往新辅助治疗后的手术时间间隔是化疗后的三到四周12,新辅助免疫联合化疗治疗模式下,最佳的手术时间间隔是什么?第二,新辅助免疫联合化疗的最佳周期数仍需深入探索。第三,新辅助免疫联合化疗安全性良好,多数情况下未对手术产生不利影响,然而少数患者在手术中出现炎症反应,如水肿等,因此我们将继续研究优势人群及哪些患者可能遭遇严重不良反应等,从而指导临床实践,优化患者治疗效果。
秦建军教授:食管癌治疗迎来了免疫疗法的新纪元,这一方法在围手术期治疗中展现出巨大潜力。随着ESCORT-NEO/NCCES01研究初步结果的发布,我们非常期待未来证实新辅助免疫联合化疗在局晚期可切除ESCC当中能否取得生存获益。肺癌等其他癌种研究已证实,pCR率和MPR率的提高与远期生存获益存在正相关13。因此,我们热切期盼李印教授未来能够带来更多关于生存结果的积极报告。
Ken Kato教授:我们迫切需要一种能迅速缩减肿瘤大小并显著延长缓解持续时间的新辅助治疗手段,新辅助免疫联合化疗实现了这一目标。在此过程中,我们需严格监控治疗安全性,确保不会增加手术并发症的风险。值得庆幸的是,新辅助阶段免疫治疗的加入并未引起额外的手术并发症,有望为局晚期可切除食管癌患者带来更加有效和安全的治疗方案。
多方求索持续开拓食管癌围术期免疫治疗蓝图
康晓征教授:Ken Kato教授既往参与并发表过多项免疫检查点抑制剂在晚期及围术期食管癌治疗的相关研究,您认为食管癌围术期免疫治疗未来还有哪些探索的方向?
Ken Kato教授:在晚期食管癌治疗中免疫治疗的作用已得到了证实,并预期会在未来围术期的治疗中发挥更大作用。随着新辅助治疗的重要性日益凸显,我们正致力于强化新辅助治疗方案,如通过优化药物组合和治疗周期,利用生物标志物如循环肿瘤细胞DNA(ctDNA)和微小残留病灶(MRD)指导用药,以提高治疗的精准度。此外,保器官治疗也是研究方向之一,目前新辅助免疫治疗展现的疗效与安全性已经在结直肠癌中实现了器官保留的目标。
百家争鸣,个体化策略引领食管癌围术期精准治疗
康晓征教授:目前全球食管癌围术期治疗相关研究如火如荼地开展,对食管癌围术期治疗模式探索越来越深入,可否请三位教授谈谈对围术期不同治疗模式的见解和选择策略?
李印教授:在探讨围术期治疗方法时,不同地域和医疗中心持有不同的观点。这些方法基于深厚的理论依据和众多临床研究,旨在达到更优的治疗结果。然而,新辅助治疗策略的优化并非通过简单增加或者减少治疗方式实现,新辅助放化疗、化疗以及免疫疗法等联合治疗均可给局晚期可切除食管癌患者带来显著的疗效和可控的安全性,尽管有些患者可能遭受严重副作用,但治疗的关键在于科学匹配,比如考虑降低新辅助放疗剂量或者减少靶区来减轻放疗引起的副作用,或是在手术前采取综合治疗措施以提升疗效。在处理大T分期肿瘤时,单纯手术往往无法解决问题,局部放疗可能是必要的补充手段。另外,对于T小N大的患者,全身治疗可能更为关键。这些策略表明,我们需要寻求不同治疗方法之间的有机结合,但这些治疗方案都亟需进一步研究和数据支持。
秦建军教授:新辅助化疗与新辅助放化疗并驾齐驱,但孰优孰劣尚未给出定论。免疫治疗的崛起使得新辅助治疗模式百花齐放,但不会出现一种包打天下的方案。相反,未来还需要更多基础和转化研究方面的探索,若能准确识别每种治疗方案的预测性生物标志物,定能开辟一条明晰之道。
局晚期可切除非小细胞肺癌(NSCLC)研究提示术前免疫治疗较术后辅助免疫可为患者带来更大的益处,至于目前食管癌新辅助免疫治疗后辅助免疫治疗的角色,价值和地位仍需要未来研究进一步证实。
Ken Kato教授:目前,免疫治疗在新辅助治疗中的重要性不言而喻,日本此前开展的JCOG 1804E I期研究初步证实了新辅助DCF或CF联合免疫治疗的安全性和有效性14。本次会议上公布的队列E结果显示,FLOT方案联合免疫治疗的安全性与疗效也得到初步结果,pCR率达到42%15。当前,我们面临的挑战是如何确定最有效的新辅助治疗,免疫治疗对于新辅助治疗非常重要,但日本的研究结果证明三药化疗对于新辅助也是有效的。未来,我们可能会开展新辅助三药化疗联合免疫治疗的临床研究,期待能为患者带来更优获益。
中日携手,共启食管癌治疗新篇章
康晓征教授:在全球食管癌领域,中日专家对局晚期食管癌治疗的探索贡献了卓越的研究成果,请李教授和Ken Kato教授谈谈中日团队有哪些可以相互学习和借鉴的方向,两位教授对未来国际临床研究合作和探索有何预期?
李印教授:中日食管癌拥有诸多相似点,组织学类型以ESCC为主。中国的优势在于庞大的患者量为临床研究提供了宝贵资源。日本的优势在于JCOG系列研究及对研究的严格质量控制,以及日本独立的分期系统和以自主研究为基础的指南体系,均值得我们学习与借鉴,并为我们建立中国自己的分期系统提供了范例。我们期待未来中日能深入合作促进ESCC标准治疗模式的探索,缩短研究周期并通过加强临床研究与质量控制培训合作,共同造福中日两国的食管癌患者。
Ken Kato教授:中日食管癌面临着相似的挑战和治疗难题。众所周知多学科团队协作(MDT)在食管癌的治疗中不可或缺,合作显得尤为关键。我们期待与中国外科、肿瘤内科、内镜科等专家展开合作。随着新疗法和药物的不断涌现,我认为现在是加速创新、强化中日合作的关键时刻。我们热切期望与中国的研究者们共同迈进,探索食管癌治疗的新篇章。
国家癌症中心、中国医学科学院肿瘤医院食管及纵隔外科主任
北京协和医学院教授、主任医师、博士研究生导师
享受国务院政府特殊津贴专家
英国皇家外科学院院士
国家癌症中心食管癌诊疗质控专家委员会副组长兼秘书长
中国食管疾病协会CSDE主席
中国医师协会胸外科医师分会食管外科专家委员会主任委员
中华医学会胸心血管外科学分会食管疾病学组组长
中国临床肿瘤学会CSCO食管癌专委会侯任主任委员
中国抗癌协会食管癌专业委员会副主任委员
中国医疗保健国际交流促进会胸外科分会食管癌学组组长
大中华胸腔镜发展及推动委员会培训专家
卫生部胸外科医师定期考核编委会委员
《Annuals of Esophagus》杂志主编
《中国肺癌杂志》常委编委
2020-2022年,国立癌症中心医院头颈科、食管肿瘤内科、胃肠道肿瘤内科主任国立癌症中心医院临床研究支持室临床研究协调科生物样本库转化研究支持科科长
JCOG日本食管肿瘤学组的小组协调员
食管癌相关研究:JCOG0502、JCOG1109、Checkmate-648(通讯作者);Checkmate-577、KEYNOTE-590等食管癌临床研究研究者
教授中国医学科学院肿瘤医院 胸外科
博士,主任医师
中国抗癌协会食管癌专委会委员
中国医师协会胸外科分会食管外科专家委员会委员
中华医学会胸心分会食管疾病学组委员
中华医学会肠外肠内营养分会胸部疾病协作组副组长
CSCO食管癌诊治指南执笔专家成员
中国胸心血管外科临床杂志青年编委
中国肺癌杂志编委
Annals of Esophagus编委
教授
国家癌症中心/中国医学科学院肿瘤医院 胸外科 副主任医师
中国临床肿瘤学会(CSCO)青委会常委,秘书长
中国抗癌协会(CACA)食管癌专委会青年委员
国际食管疾病学会中国分会(CSDE)青年委员会委员
美国杜克大学胸外科/癌症中心访问学者
美国临床肿瘤学会(ASCO)会员
美国胸外科医师学会(STS)会员
擅长食管癌多学科综合治疗,微创胸外科治疗,加速康复外科
以共同第一或通讯作者分别发表原创性临床及转化研究于Theranostics,Carcinogenesis, Journal of Biological Chemistry及Annals of Thoracic Surgery等专业高影响力期刊
2017年入选北京市医管局“青苗计划”人才培养项目
1.Yin Li, et al. 2024 ASCO GI LBA 244.
2.文龙,等.医学信息,2022,35(18):165-168.
3.中国临床肿瘤学会.2023CSCO食管癌诊疗指南.
4.Liu J, et al. J Immunother Cancer. 2022;10(3):e004291.
5.Yang W, et al. J Immunother Cancer. 2022;10(1):e003497.
6.Liu J, et al. Int J Cancer. 2022;151(1):128-137.
7.Yang G, et al. J Transl Med. 2023;21(1):411.
8.Wang Z, et al. J Natl Cancer Cent, 2022, 2(2): 98-105.
9.Ken Kato, et al. 2022 ASCO GI Abstract: 238.
10.Eyck BM, et al. J Clin Oncol. 2021 Jun 20;39(18):1995-2004.
11.Yang Y, et al. J Thorac Cardiovasc Surg. 2023 Sep 9:S0022-5223(23)00782-1.
12.国家癌症中心,等.中华消化外科杂志,2023,22(11):1272-1290.
13.C. Wang, et al. 2023 ESMO LBA58.
14.Yamamoto S,et al.Future Oncol. 2020Jul;16(19):1351-1357.
15.Rana R. et al. 2024 ASCO GI Abstract 326.
排版编辑:肿瘤资讯-Vicky











 苏公网安备32059002004080号
苏公网安备32059002004080号


