ALK基因重排在肺腺癌患者中的发生率为5%。相比于第一代ALK TKI克唑替尼,第二代药物表现出更长的无进展生存期(PFS)和更优的颅内疗效。ALK阳性患者可能同时合并其他共变异基因,从而影响ALK TKI的疗效。既往研究发现,一些共变异基因会影响患者接受第二代ALK TKI治疗的疗效。近日,Journal of Thoracic Oncology发表了一项来自拉丁美洲的前瞻性队列研究,在接受第二代ALK TKI治疗的患者中评估共变异基因对患者治疗疗效和预后的影响。
研究背景
在ALEX和ALTA-1L研究中,约20%的患者在接受阿来替尼或布格替尼治疗后6个月内会出现疾病进展;此外,30%患者会在治疗12个月内出现进展。这提示,有部分患者表现为更为恶性的肿瘤学特征,可能合并其他的耐药机制。目前,已有研究提示合并共变异基因的患者,接受ALK TKI治疗时表现为更短的PFS。在ALK阳性患者中,最常见的共变异基因为TP53,文献报道的发生率为43.8%。细胞周期蛋白依赖激酶抑制剂2A和2B(CDKN2A/B)是负责调节细胞周期的关键蛋白。这一基因缺失表现为蛋白表达下调,可引发肺癌的早期基因变异。该蛋白的缺失会加速细胞增殖、侵袭和迁移。既往一项单中心研究发现,合并CDKN2A/B蛋白缺失的ALK阳性NSCLC患者预后更差。这些研究结果均提示,共变异基因会影响ALK阳性NSCLC患者的预后。
ALK阳性患者表现为更高的脑转移风险,且在其他实体瘤中观察到CDKN2A/B基因缺失也会增加颅内进展风险和复发风险。类似研究可为ALK阳性NSCLC一线治疗的选择提供重要信息。本研究旨在接受第二代ALK TKI治疗的患者中评估共变异基因,尤其是TP53和CDKN2A/B基因对患者治疗和预后的影响。
研究方法
2017年12月至2022年12月期间,研究前瞻性的纳入5家拉丁美洲癌症中心经病理和分子确认的ALK阳性NSCLC患者。采用Foundation One CDX平台进行高通量测序,包括324个基因的碱基缺失、插入、拷贝数变异以及部分基因的重排检测。所有患者均接受了第二代ALK TKI治疗,可作为一线治疗或至多2线化疗后接受ALK TKI。ALK TKI包括阿来替尼、布格替尼和塞瑞替尼,治疗直至疾病进展或出现不可耐受的毒性。主要研究终点为PFS。其他研究终点包括客观缓解率(ORR)、疗效持续时间(DoR)和总生存期(OS)。
研究结果
患者临床特征
研究纳入116例患者,中位年龄为52.5岁,59.5%为女性,大多数(75%%)为非吸烟者,85.3%的患者ECOG PS为0-1分。所有的肿瘤标本均进行了ALK基因状态评估,83例(71.6%)患者采用VENTANA ALK D5F3平台检测为ALK蛋白阳性,且得到NGS确认。38例(30.4%)患者因为标本有限,仅采用NGS平台检测ALK基因重排。EML4是最常见的融合伴侣(76.8%)。整个队列中,患者的中位肿瘤突变负荷(TMB)为1,3例患者为高水平TMB(≥10mpb)。80例进行微卫星状态检测的患者,5例(6.2%)为MSI。
首诊时,62.4%的患者检测到共变异基因,中位体细胞共突变数为2个,最常见的共突变为TP53(27%),主要表现为错义突变;另一常见共变异基因为CDKN2A/B基因拷贝数(CNV)变化和基因缺失。ALK阳性患者中共变异基因谱总结见下图1。
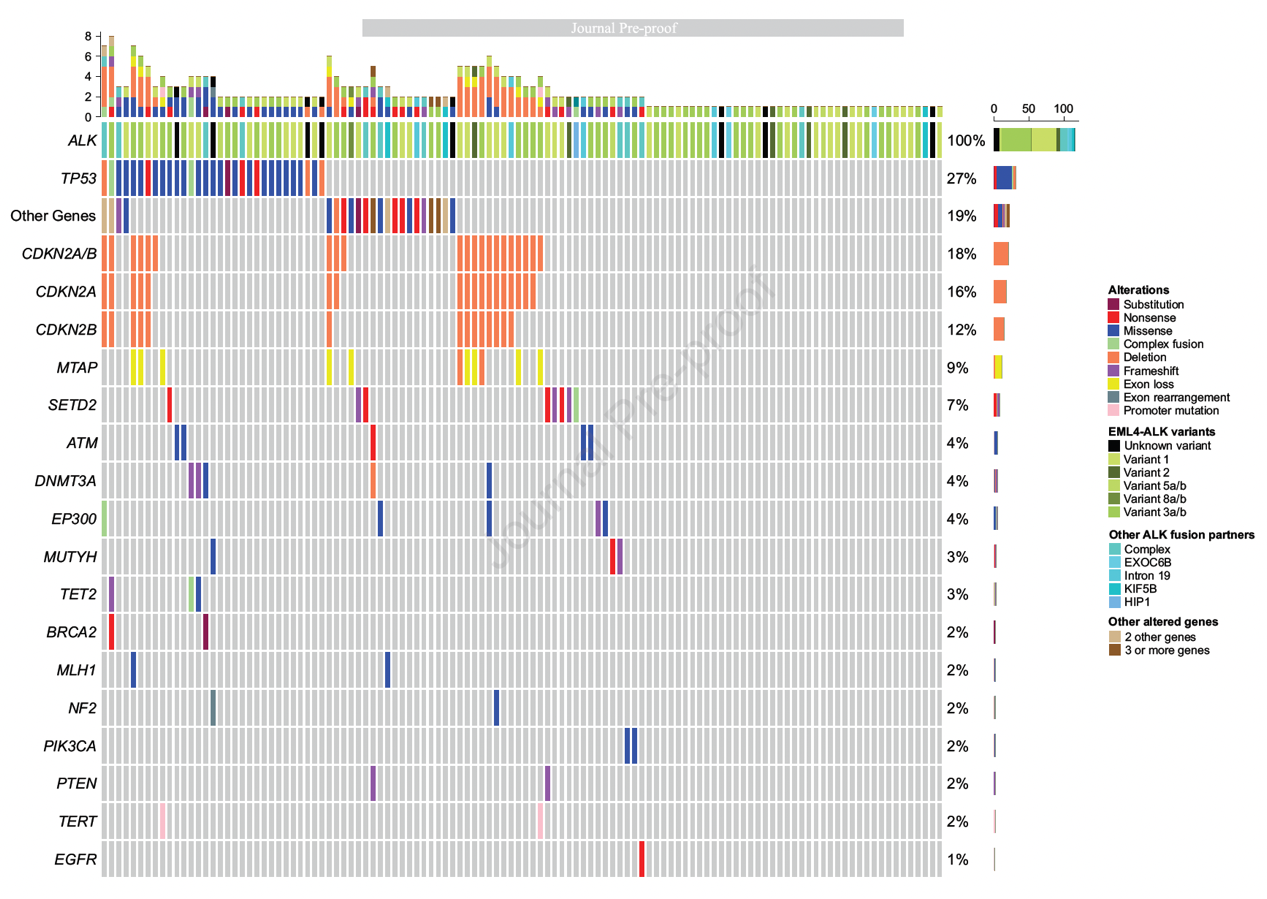 图1. ALK阳性患者的共变异基因谱
图1. ALK阳性患者的共变异基因谱
单因素分析显示,CDKN2A/B基因缺失的患者,出现首诊脑转移和ECOG PS≥2分的风险更高。此外,CDKN2A/B基因缺失的患者相比于未携带该共变异基因的患者,在治疗过程中,更容易出现中枢神经系统(CNS)转移(OR 6.28,95% CI (1.9-20.6);p=0.002)。
临床结局
所有患者均接受了第二代ALK TKI治疗,分别为阿来替尼(86.2%)、布格替尼(6.0%)和塞瑞替尼(7.8%)。其中,99例(85.3%)患者为一线治疗,其余14.7%的患者在一线或二线化疗后接受ALK TKI治疗。
ORR分析:总体人群的ORR为88.1%,其中13.6%的患者获得完全缓解(CR)。临床获益率(CBR)为94.1%,7例患者出现疾病进展(PD)。对比合并和未合并CDKN2A/B基因缺失的患者,发现合并CDKN2A/B基因缺失的患者治疗的ORR显著更低70% vs. 92.1%, p=0.006),部分缓解率更低(60% vs. 77.5%),且有很大比例患者出现疾病进展(25% vs. 1.1%,p<0.001)。
CNS有效率分析:无CDKN2A/B基因缺失的患者,CNS有效率显著更高80.9% vs. 35.7%;即便在接受了脑局部治疗的患者中,也观察到相似的现象(57.1% vs. 38.0%)。此外,在CDKN2A/B基因缺失的患者中,50%的患者出现颅内进展。
PFS分析:
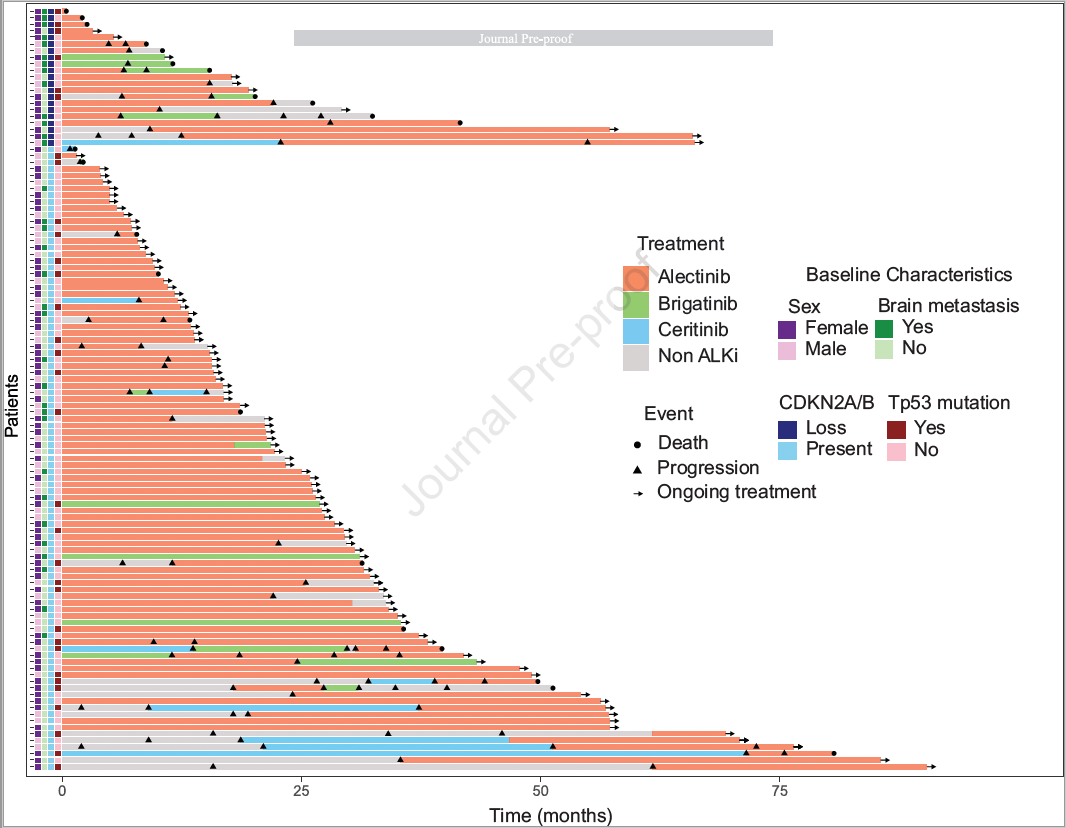
图2. 接受ALK TKI治疗的疗效以及患者的临床和分子特征
中位随访时间为21.3个月,中位PFS为28.7个月(图3A)。根据患者是否携带共变异基因进行分组,相比于未合并共变异基因的患者,至少合并1个变异基因的患者,中位PFS显著更短(24.6个月 vs. NR,p=0.002,图3C);36个月PFS率分别为74.2%和26.2%。在同时合并CDKN2A/B 基因缺失的患者中(n=21),也表现为中位PFS显著更短,中位PFS为10.2个月,而未合并CDKN2A/B 基因缺失的患者中,中位PFS为34.2个月(HR 3.85,p<0.001;图3E)。
在单因素分析中,TP53共突变是预测PFS的负性预测因素;此外,在校正了DKN2A/B基因缺失这一因素后,TP53对PFS的负性预测价值更明显。多因素分析还显示,在校正了患者的ECOG PS评分,肺腺癌亚型以及其他共突变基因和TP53突变状态后,CDKN2A/B基因缺失与更高的疾病进展或死亡风险显著相关(HR 4.0;p= 0.002)。
OS分析:整个队列的中位OS(mOS)为80.6个月,见图3B。与PFS分析类似,在至少合并1个共变异基因的患者中,中位OS显著更短(51.3 vs. NR, HR 10.8, p<0.020)。未合并共变异基因患者的5年OS率为96.6%;而携带共变异基因的患者,5年OS率为48.5%,见图3D。在合并共变异患者中,将CDKN2A/B基因缺失的患者排除,发现上述两组患者的OS无显著差异,合并共变异基因患者预估mOS为80.6个月,而未合并组mOS尚未达到(OS HR 6.6; p=0.072)。进一步对比合并和未合并CDKN2A/B基因缺失的患者,两组的mOS分别为26.2个月和80.7个月(HR 5.2;p<0.001)。
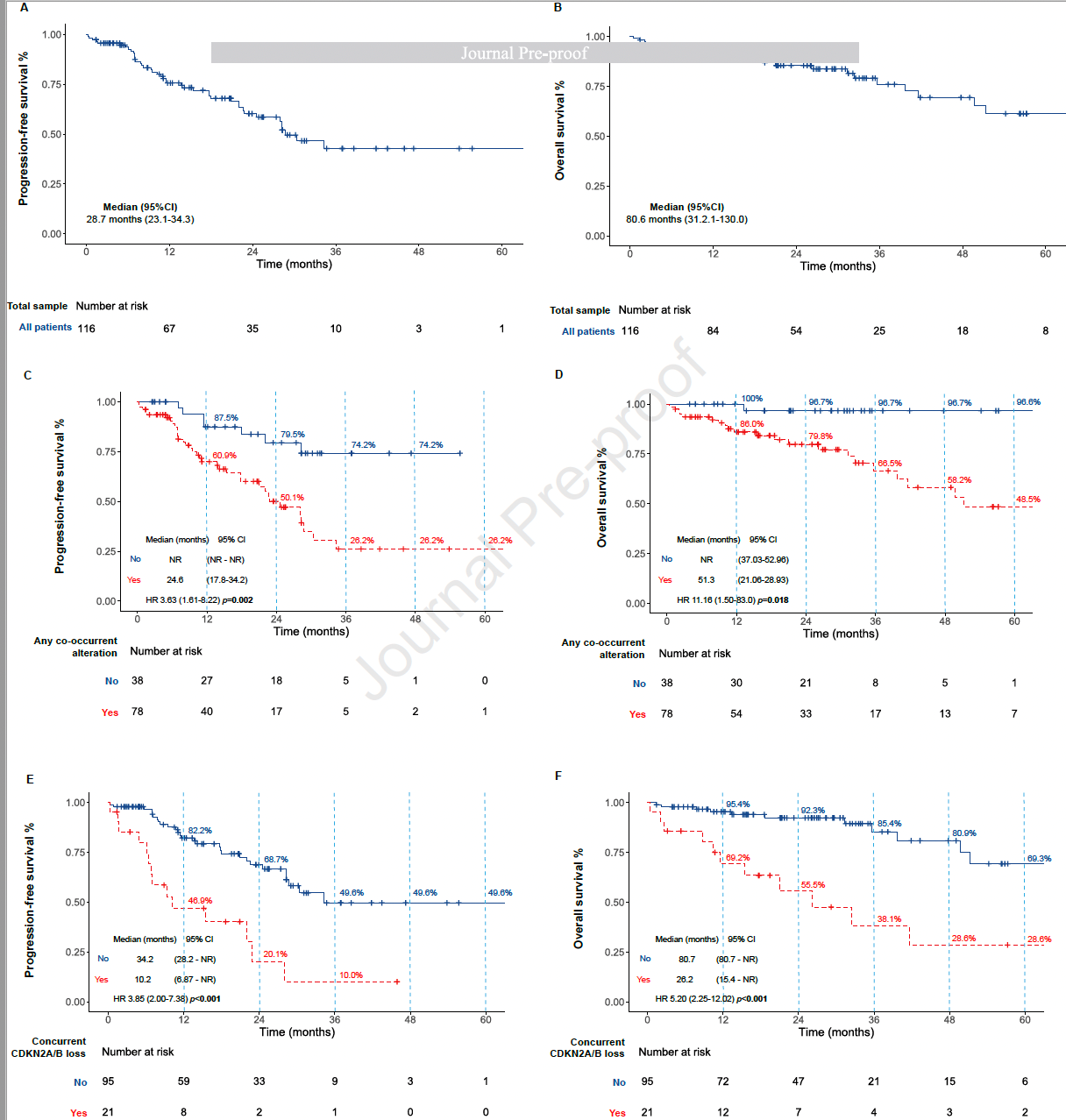
图3. 总体人群以及不同分组患者的PFS和OS分析
总结
这一队列研究结果显示,在ALK阳性的晚期NSCLC患者中,有62%的患者合并共突变。CDKN2A/B 基因缺失会影响二代ALK TKI的疗效,同时也增加首诊以及治疗过程中的脑转移风险。目前,对于ALK阳性患者的一线治疗,可以选择二代或三代ALK TKI。明确患者的耐药机制,同时在基线治疗时检测患者的共突变基因谱,可指导临床决策。接受ALK TKI治疗的ALK阳性患者中,大约有1/3患者会出现原发耐药(定义为治疗3个月内进展)。研究结果也部分解释了原发耐药和早期继发耐药患者可能的机制。
在研究队列中,62%的ALK阳性患者存在共突变,每个患者的中位共突变基因数为2个。与既往研究相似,相比于未携带突变患者,合并共突变基因的患者会更早出现疾病进展或死亡。多因素校正后发现,TP53共突变和CDKN2A/B基因缺失相比于总的体细胞共突变数,在预测治疗结局和预后上具有更重要的意义,携带这些基因变异ALK阳性患者的治疗结局和预后更差。
总体而言,这一研究结果证实,在接受二代ALK TKI治疗的ALK阳性NSCLC患者中,一些共突变基因会影响患者的治疗疗效。在ALK阳性患者中,CDKN2A/B基因缺失是第二常见的共变异基因;在校正了其他已知的预后因素后发现,同时携带CDKN2A/B基因缺失的患者,接受二代ALK TKI治疗,表现为更差的ORR,更短的PFS和OS。这一研究结果具有重要的临床意义,明确影响患者治疗疗效的因素,可以为后续探寻联合疗法或寻找克服耐药的新一代疗法提供重要思路。
Impact of concurrent genomic alterations on clinical outcomes in patients with ALK rearranged non-small cell lung cancer. [J]. Journal of Thoracic Oncology, 2023, S1556-0864(23)00727-X
CN-125589
过期日:2024-3-1
*本文由阿斯利康提供支持,仅供医疗专业人士参考
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


