肺癌是肿瘤相关死亡率最高的恶性肿瘤[1]。小细胞肺癌是肺癌中侵袭性最强的亚型,此类肿瘤恶性程度高、倍增时间短、易发生远处转移,初次就诊时即有约 2/3 患者被诊为广泛期,约占所有肺癌患者的15-20%,与吸烟关系密切。广泛期小细胞肺癌(extensive-stage SCLC, ES-SCLC)的有效治疗方案有限。既往一线标准治疗方案为依托泊苷或伊立替康联合铂类药物化疗,有效率高达60-80%,但患者往往短期内出现复发、转移,中位生存期仅有10个月左右[2,3],5年总生存率仅为1%左右。但近几年来,随着PD-1和PD-L1等多种免疫检查点抑制剂(Immune checkpoint inhibitors, ICIs)相继应用于临床,ES-SCLC的治疗模式发生了改变,免疫联合化疗成为ES-SCLC患者新的治疗选择。 PD-L1抑制剂联合化疗较单纯化疗可使ES-SCLC患者中位OS[2-4]延长2-2.5个月,斯鲁利单抗作为上海复宏汉霖首款自主研发的创新生物药PD-1抑制剂,也是首个在ES-SCLC治疗中获得成功的PD-1抑制剂,为患者带来的生存获益更加明显。2022年ESMO Asia上公布了更新的ASTRUM-005研究结果,斯鲁利单抗联合化疗组患者中位OS达15.8个月,较化疗组(11.1个月)延长了4.7个月[5]。本文通过分享一例伴脑转移ES-SCLC一线使用斯鲁利单抗联合化疗的用药经验,探讨免疫治疗在ES-SCLC中的应用与药物选择。
病例介绍
基本情况:男,67岁。
首诊日期:2022-06。
主诉:咳嗽,咳白痰半月余。
既往无基础疾病;无吸烟、饮酒史;无肿瘤家族史。
查体:PS评分1分,颈部淋巴结未触及,双肺未见异常。
肿瘤标志物(2022-06):
CEA:36.69 ug/L↑;CA125:138.3 ug/L↑; NSE:49.97 ug/L↑;ProGRP:5000 pg/↑。
影像学检查(2022-06 ):
胸部CT(见图1):右上肺叶不规则团块影,大小约4.4x3.3cm,伴轻度阻塞性肺炎,左下肺叶局部支气管扩张;纵隔内可见肿大淋巴结,增强扫描明显强化;双肺局限性气肿。
腹部CT(见图1):右肾上腺低密度影,大小约:4.0 x 3.7cm,考虑转移。
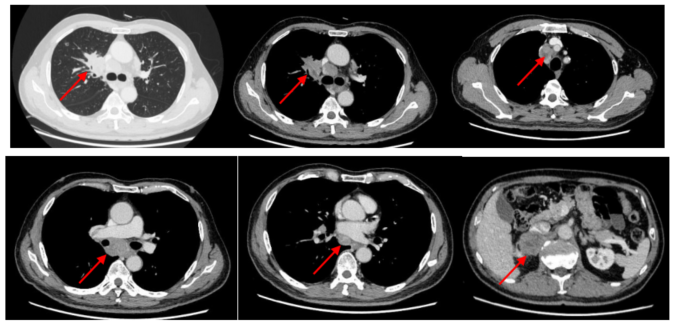 图 1
图 1
骨扫描:未见骨转移特征性表现。
颅脑MR(见图2):右侧额叶、双侧枕叶、小脑多发小圆形长T2信号影,较大者位于左侧小脑,大小约0.8x0.7cm,增强扫描可见环形强化。结合病史,考虑转移。
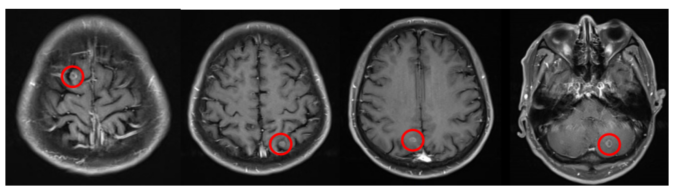 图 2
图 2
2022-06 行经皮CT引导下右肾上腺穿刺术。
病理结果:小细胞癌,结合病史符合肺来源。 免疫组化:CK (+),CK7 (-),P40 (-),Napsin-A (-),TTF-1 (+),CD56 (+),Synaptophysin (+),Chromogranin A (弱+),Ki-67(>50 %),PAX8 (-),S-100 (-)。
初步诊断
1.右上肺小细胞癌(cT2N2M1c ⅣB期,广泛期);多发脑转移;右肾上腺转移
2.双肺局限性气肿
治疗经过
一线治疗:
• 2022-06至2022-11行EC方案化疗联合斯鲁利单抗免疫治疗6周期,具体为:依托泊苷150mg d1-d3 ivd+卡铂200mg d1-d2 ivd+斯鲁利单抗300mg d1 ivd,Q3W。
• 2022-11至2023-09接受单药斯鲁利单抗免疫维持治疗,具体用药方案为:斯鲁利单抗300mg d1 ivd,Q3W。
• 2022-12行全脑放疗,放疗剂量为30Gy/10f。
• 2023-10于外院呼吸科诊断左肺下叶感染性肺炎,抗炎治疗后好转,暂停免疫,观察中。
一线治疗疗效评价:
化疗联合免疫治疗2周期后,患者咳嗽症状明显缓解。
实验室检查(见图3):一线治疗2周期后,肿瘤标志物即恢复至正常范围内。
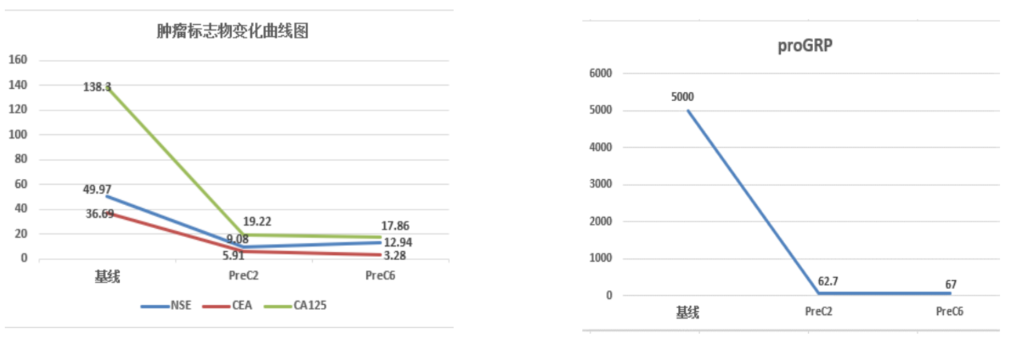 图 3
图 3
影像学评估(见图4):
• 2周期后(2022-08)复查CT:右肺上叶占位性病变(大小约为1.0 x 0.8cm)伴阻塞性炎症,对比2022-06原片范围明显缩小。右肾上腺病灶明显缩小。颅脑MR:对比2022-06前片,脑内强化灶明显减小。
依据RECIST1.1,疗效评价:PR。
• 4周期后(2022-10)复查 维持PR。
后规律复查,维持PR。

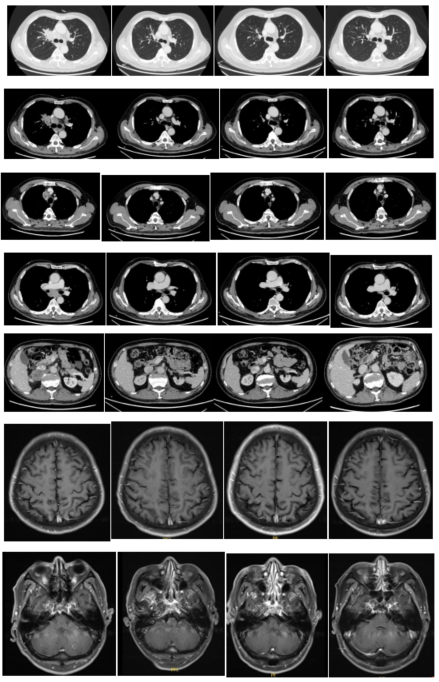 图 4
图 4
安全性评价
治疗过程中患者出现1°白细胞降低、轻度脱发,以及反酸、恶心等胃肠反应,给予对症处理,未影响后续治疗,治疗期间患者未发生irAE。
病例作者
MD Anderson Cancer Center 访问学者
中国医科大学附属第一医院肿瘤内科
中国抗癌协会化疗专业委员会青委
中国抗癌协会抗癌药物专业委员会青委
中国研究型医院学会精准医学与肿瘤MDT专业委员会青委
中国医药教育协会肿瘤化疗专业青委会常委
辽宁省细胞生物学学会肺癌细胞靶向和免疫治疗专委会副主任委员
辽宁省细胞生物学学会纵隔肿瘤细胞学专委会副主任委员
辽宁省免疫学会肿瘤免疫分会常委兼秘书
辽宁省细胞生物学学会肿瘤MDT和细胞学研究专委会常委
辽宁省预防医学会肿瘤防治专业委员会常委
北京整合医学会肺癌专委会副主任委员
北京肿瘤防治研究会青委会常委
辽宁省预防医学会肿瘤防治专委会肿瘤罕见突变学组委员
《中华肿瘤杂志》第一届青年编委,中国医科大学青年拔尖人才
主持国家自然基金青年基金及辽宁省科技厅各一项;参与多项国家、省级课题;
以第一作者或通讯作者在JCO等杂志发表SCI论文10余篇;
辽宁省自然科学成果奖一等奖(第一完成人)辽宁省科技进步一等奖(主要完成人)
病例小结
该患者为广泛期小细胞肺癌,初诊时伴脑转移及右肾上腺转移。
依据2022年CSCO小细胞肺癌诊疗指南相关推荐,该患者于2022年6月开始行斯鲁利单抗联合依托泊苷、顺铂治疗,用药2周期后肿瘤标志物明显下降, 恢复至正常范围,CT显示原发灶、区域转移淋巴结及脑转移灶均明显缩小,疗效达到PR(原发灶↓77%)。斯鲁利单抗单药维持治疗期间,影像学显示肿瘤维持PR,且无新发病灶。目前该患者一线PFS已达17个月。在整个治疗过程中,患者未出现明显免疫相关不良事件(irAE),安全性良好。此病例提示,斯鲁利单抗可为ES-SCLC带来持久生存获益,是ES-SCLC一线治疗优选方案。目前斯鲁利单抗在肺癌领域设有多项研究布局,期待研究数据进一步披露,为临床治疗提供更多的选择,惠及更多肺癌患者。
病例点评
点评专家
主任医师 博士生导师
国务院特殊津贴获得者
中国医科大学附属第一医院
中国临床肿瘤学会(CSCO )常务理事
中国临床肿瘤学会(CSCO )结直肠癌专委会副主委
中国老年医学学会肿瘤分会会长、精准医疗专委会副主委
中国医师协会肿瘤医师分会副会长
中国抗癌协会胃癌专委会常委、临床研究专委会常委
中国医药教育协会腹部肿瘤结直肠癌分会主委
国家结直肠肿瘤质控中心副秘书长、 肺癌指控中心委员
作为通信作者发表于JCO等杂志的SCI论文90余篇
主持国家科技重大专项2项和国家自然科学基金课题5项
获得中国抗癌协会科技二等奖1项;辽宁省科技进步一、二等奖各1项
获得全国五一奖章;首届“辽宁名医”、省优秀专家、省优秀科技工作者;
市劳动模范、市创新型领军人才
小细胞肺癌占肺癌的15%-20%,其发展呈侵袭性,脑部是小细胞肺癌患者发生转移的主要部位,也是患者死亡的重要原因。在放化疗作为标准治疗的时代,小细胞肺癌患者发生脑转移后,中位生存期仅有4-6个月。近些年,随着免疫治疗、抗血管治疗等综合治疗模式在小细胞肺癌中的应用,伴有脑转移的ES-SCLC患者生存期较前显著延长。但由于SCLC脑转移机制尚未完全明确,小细胞肺癌脑转移的治疗问题仍然是目前影响SCLC患者生活质量和生存期的重大挑战之一。
多项研究提示,免疫治疗能够给肺癌脑转移患者带来获益。2020年发表于Clinical Cancer Research的一篇综述阐述了肺癌脑转移免疫治疗的机制。颅外病灶内被ICIs激活的T细胞进入中枢神经系统,通过机体免疫系统及免疫细胞发挥抗肿瘤效应,这是脑转移肿瘤产生免疫应答的关键原因。同时,颅内活化的CD4+T细胞可通过局部生成IFN-γ,后者可使血脑屏障松弛,有利于循环中的ICIs进入颅内,从而增强ICIs的抗肿瘤活性。此外基础研究发现,免疫治疗并非促进颅内病灶淋巴细胞的增殖,而是通过调节颅外CD8+T细胞进入颅内病灶,从而发挥杀伤作用。这是颅内病灶患者发生应答的主要原因[6]。
该患者确诊ES-SCLC时伴有脑转移、右肾上腺转移,依据2022CSCO小细胞肺癌诊疗指南给予患者免疫联合化疗的一线标准治疗方案,患者在接受斯鲁利单抗联合化疗治疗2周期后,影像学显示肿瘤原发灶及脑转移灶、右肾上腺转移灶均明显缩小。免疫维持治疗期间联合脑部放疗进一步巩固疗效。ASTRUM-005 研究中,基线伴脑转移患者占比12.9%,亚组分析结果显示,斯鲁利单抗联合化疗组脑转移患者OS达 13.9个月,而对照组仅为9.1个月,HR 0.73(95% CI 0.42-1.25)[7]。
2023 WCLC大会上公布了IMpower 133研究5年随访数据[8],免疫联合化疗组的中位随访时间59.4个月,对照组26.4个月,结果显示免疫治疗联合化疗组的5年OS率为12%,相较于既往化疗方案的5年生存率显著提升,免疫治疗使更多患者生存期达到甚至超过5年。该病例充分证实了免疫联合化疗在ES-SCLC一线治疗中的长期疗效,夯实了免疫联合化疗在ES-SCLC治疗中的一线标准治疗地位。由于小细胞肺癌具有恶性程度高、增殖快和转移早等特点,该人群的生存仍不容乐观。因此,解决SCLC耐药、复发问题,进一步延长患者生存期成为目前临床诊疗的难点与重点,个体化治疗策略仍需探索。
[1] Siegel R L, Miller K D, Jemal A. Cancer statistics, 2020[J]. CA Cancer J Clin, 2020, 70(1): 7-30.
[2] Goldman J W, Dvorkin M, Chen Y, et al. Durvalumab, with or without tremelimumab, plus platinum-etoposide versus platinum-etoposide alone in first-line treatment of extensive-stage small-cell lung cancer (CASPIAN): updated results from a randomised, controlled, open-label, phase 3 trial[J]. Lancet Oncol, 2021, 22(1): 51-65.
[3] Liu S V, Reck M, Mansfield A S, et al. Updated Overall Survival and PD-L1 Subgroup Analysis of Patients With Extensive-Stage Small-Cell Lung Cancer Treated With Atezolizumab, Carboplatin, and Etoposide (IMpower133) [J]. J Clin Oncol, 2021, 39(6): 619-630.
[4] Wang J, Zhou C, Yao W, et al. CAPSTONE-1 Study Group. Adebrelimab or placebo plus carboplatin and etoposide as first-line treatment for extensive-stage small-cell lung cancer (CAPSTONE-1): a multicentre, randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2022 Jun;23(6):739-747.
[5] Ying Cheng, Liang Han, Lin Wu, et al. Updated results of first-Line Serplulimab vs Placebo Added to Chemotherapy on Survival in Patients With Extensive-Stage Small Cell Lung Cancer. 2022 EMSO ASIA[6] Iñaki Eguren-Santamaria , Miguel F Sanmamed Sarah B Goldberg et al. PD-1/PD-L1 Blockers in NSCLC Brain Metastases: Challenging Paradigms and Clinical Practice. Clin Cancer Res 2020 Aug 15 ; 26(16) : 4186-4197.
[7] Cheng Y,et al. 2023 ESMO
[8] IMPower 133. 2023 WCLC
排版编辑:DND











 苏公网安备32059002004080号
苏公网安备32059002004080号


