免疫检查点抑制剂(ICIs)是一类新型、广谱抗肿瘤药物,显著改善了肿瘤患者的生存,但同时也可能造成全身多个器官、组织损伤,部分严重免疫检查点抑制剂相关不良反应(irAEs)甚至危及生命,已成为全球肿瘤领域关注的焦点。东部战区总医院肿瘤科是国内最早一批应用ICIs的医学中心,并率先成立了irAEs多学科专家团队(MDT),在irAEs管理方面积累了非常丰富的经验。为系统性分享诊治经验,专家组特在肿瘤资讯平台开设专栏,其核心特色在于:1. 全程追踪疑难案例 专栏深度展示具有代表性的疑难病例从诊断、治疗到随访的完整过程,传递不同系统irAEs的精准诊治思路与前沿进展;2. 汇聚多学科智慧 真实记录MDT讨论精华,融合肿瘤、心脏、肝脏、呼吸、消化、内分泌、皮肤、影像、病理等多学科视角,分享跨学科的理论知识、指南共识与实战经验;3. 系统连载即时更新 病例采取定期连载形式发布,确保内容的时效性、系统性与持续的高品质输出。本专栏力求为同行提供实用参考,然学海无涯,文中疏漏之处在所难免,恳请各位同道不吝批评指正,共同推动irAEs管理水平的提升。
参加人员:东部战区总医院免疫相关不良反应多学科专家组
病例介绍
陈歆妮(主管医生):汇报患者病情经过。
患者于2017年11月1日外院CT检查提示“肝占位”;次日(11月2日)MRI检查示肝右叶占位,伴肝右叶胆管轻度扩张,临床诊断为原发性肝癌CNLCⅠb期,先后接受2次TACE治疗。2018年3月5日在外院行右肝肿瘤(Ⅷ段)切除术联合胆囊切除术,术后病理确诊为肝细胞癌,术后接受1次TACE治疗。2019年9月2日因肾上腺转移,在外院接受腹腔镜下右侧肾上腺肿瘤切除术。2020年9月27日MRI检查示:1.右肾及右肾周多发异常强化结节,与肝右叶分界欠清,考虑转移瘤;2.右下肺多发结节,不排除转移瘤可能。2020年10月起患者开始口服索拉非尼(400mg,2/日)。
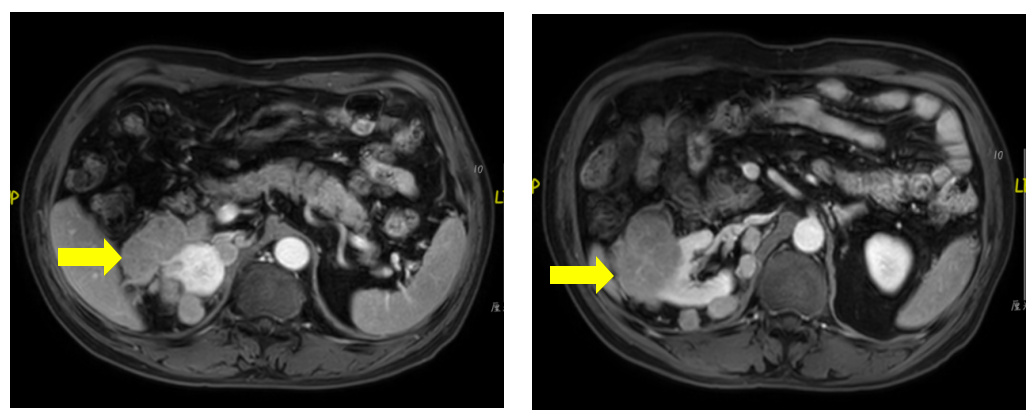
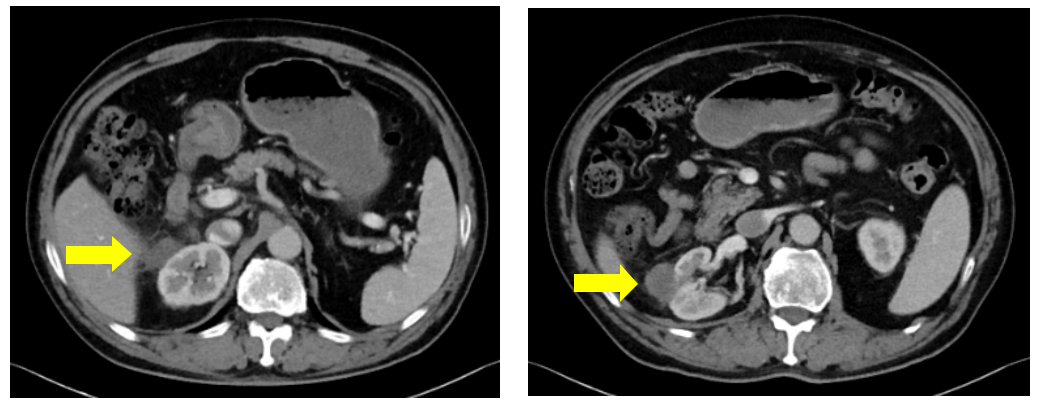
2021年5月18日患者外院MRI检查示:1.右肾及肾周多发转移灶较前增大(见图1);2.腹膜多发转移灶部分较前稍饱满;3.双肺多发转移灶较前增大。诊断为肝细胞癌术后Ⅲb期(肾周、双肺转移)。后转至我院,查AFP 84μg/L(正常值范围0~10μg/L)。2021年5月31日接受mFOLFOX4联合PD-1抑制剂治疗1周期;6月16日查肌酐125μmol/L,考虑肾损伤,予金水宝片口服,同时出现1级胸壁反应性皮肤毛细血管增生症(RCCEP)。继续予原方案治疗2周期。2021年8月10日CT检查示:1.肝细胞癌切除术后改变,肝左叶见点状低密度影;2.右肾、肾周及后缘肾周筋膜处多发结节及片絮状低密度影,侵犯右肾,考虑转移,较前明显缩小,部分病灶消失(见图2);3.右肺及左肺上叶多发点状影,较前缩小。查AFP降至正常范围。疗效评估为部分缓解(PR),继续原方案治疗2周期。2021年9月25日患者出现2级肝功能损伤、1级肌酐升高,予保肝、护肾治疗后停用免疫治疗及静脉化疗,改为口服卡培他滨2周期。2021年12月23日起患者接受PD-1抑制剂联合卡培他滨治疗3周期;2022年2月28日我院CT检查评估维持PR,但因肿瘤标志物AFP、CA50、CA19-9较前升高,于2022年3月28日调整为PD-1抑制剂联合酪氨酸激酶抑制剂(TKI)治疗,治疗后RCCEP结节缩小、范围减少,肿瘤标志物逐渐降至正常,定期行影像学检查评估为维持PR。
患者于2021年5月PD-1抑制剂治疗前测血皮质醇、促肾上腺皮质激素(ACTH)、泌乳素、TSH、FT3、FT4均正常,首次PD-1抑制剂治疗后测皮质醇3.6μg/dl(正常值范围7.2~32μg/dl),2021年5月至2023年1月多次测皮质醇降低(偶尔正常),但ACTH一直在正常范围,泌乳素轻度升高,TSH、FT3、FT4正常。因患者无临床症状,未做特殊干预。2024年6月患者出现乏力、头晕、视物模糊、排尿无力及食欲不佳,MRI检查示:T1相双侧基底节区对称片状略高信号,不排除肝性脑病可能;双侧大脑半球缺血灶,右侧侧脑室后角旁软化灶,透明隔增宽,双侧筛窦及上颌窦粘膜增厚,右侧乳突炎。查血氨正常,排除肝性脑病。后症状逐渐加重,2024年8月5日查皮质醇为0.08μg/dl,泌乳素923.62mIU/L(正常值范围72.66~407.4mIU/L),ACTH未测,甲状腺TSH、FT3、FT4正常,诊断为免疫相关性肾上腺皮质功能减退,予甲泼尼龙/强的松治疗后,乏力、头晕、排尿无力症状消失,食欲改善,后续长期口服强的松(5mg,2/日)。2024年9月13日恢复PD-1抑制剂联合TKI治疗,患者逐渐出现满月脸、面部痤疮样皮疹、肥胖及体重增加。2025年4月上旬患者自行停用强的松,出现严重乏力、纳差、嗜睡,症状进行性加重。2025年4月23日测皮质醇0.03μg/dl,ACTH<0.50pg/ml(正常值范围5.10~32.8pg/ml)。住院予激素治疗后症状消失,继续口服强的松(5mg,2/日),后停用PD-1抑制剂,维持TKI口服。2025年5月起肿瘤标志物PIVKA-Ⅱ升高,提示肿瘤进展可能,于2025年6月12日恢复予PD-1抑制剂联合TKI治疗。
2025年6月18日患者再次出现乏力、头晕、反应迟钝,急诊予甲泼尼龙静脉治疗后症状略有改善;同时出现口干、多饮、多食症状,测空腹血糖8.3mmol/L,餐后血糖15.0mmol/L,遂收入内分泌科。
辅助检查
2025年6月12日8时皮质醇1.38μg/dl,8时ACTH 0.53pg/ml;2025年6月22日测8时皮质醇22.30μg/dl(激素使用后),8时ACTH <0.50pg/ml;糖化血红蛋白正常;尿糖,尿酮体阴性。醛固酮、C肽水平正常;抗谷氨酸脱羧酶抗体、抗胰岛素抗体均为阴性;甲状腺功能:T4 55.47nmol/L(正常值范围66.92-163.45nmol/L),FT3 2.63pmol/L(正常值范围3.08-6.47pmol/L),TSH、FT4、T3正常,抗甲状腺球蛋白抗体、甲状腺过氧化物酶抗体、促甲状腺激素受体抗体阴性;血常规、肝肾功能及电解质基本正常。
MDT会诊内容
王锋(肿瘤科):针对该病例,我们主要围绕以下四个问题展开讨论:1. 免疫相关肾上腺皮质功能减退的诊断是否成立?2. 血糖升高是否与免疫药物相关?3. 肾上腺皮质功能减退应如何治疗?4. 待肾上腺皮质功能减退好转后,是否可重启免疫治疗?
王锋(肿瘤科):彭主任您好,请问该患者免疫相关肾上腺皮质功能减退的诊断是否成立?
彭晓韧(内分泌科):患者于2021年5月开始使用PD-1抑制剂,2024年6月出现乏力、头晕、视物模糊、排尿无力、食欲不振等症状。2024年8月实验室检查显示皮质醇显著降低,因此诊断为免疫相关肾上腺皮质功能减退。经甲泼尼龙治疗后症状明显改善,随后长期口服强的松。2025年4月,患者再次出现严重乏力、头晕、反应迟钝、排尿无力,症状与前次相似。经询问得知,患者在出现症状前自行停服强的松半个月余,考虑为自行停用激素后再次出现肾上腺皮质功能减退相关症状。
王锋(肿瘤科):肾上腺皮质功能减退属于常见的免疫相关不良反应吗?
彭晓韧(内分泌科):免疫药物引起的不良反应可累及全身多个脏器或组织,其中最常见的是皮肤毒性,其次为内分泌系统毒性。肾上腺皮质功能减退属于内分泌系统毒性,其发生率仅次于甲状腺功能减退。文献报道显示,PD-1/PD-L1抑制剂引起肾上腺皮质功能减退的发生率为0.8%~2%,而CTLA-4抑制剂联合PD-1抑制剂的发生率更高,达4.2%~7.9%。在实际临床工作中,由于不常规监测皮质醇水平,免疫检查点抑制剂(ICIs)引起肾上腺皮质功能减退的真实发生率可能被低估。
王锋(肿瘤科):内分泌系统毒性大约发生在ICIs用药后多长时间?
彭晓韧(内分泌科):ICIs相关内分泌系统毒性的发生时间跨度较大,通常比其他免疫毒性更晚。PD-1抑制剂单药引起的内分泌毒性一般发生在用药第10~24周,双免联合治疗时内分泌毒性发生时间显著提前,平均约在第12周左右。肾上腺皮质功能减退多发生于PD-1/PD-L1抑制剂单药治疗数月后,而CTLA-4抑制剂单药或联合用药时出现时间更早。该患者首次用药时间为2021年5月,首次出现肾上腺皮质功能减退相关症状为2024年6月,即用药3年后发病,明显晚于平均发生时间。
王锋(肿瘤科):肾上腺皮质功能减退常见的临床表现有哪些?
彭晓韧(内分泌科):若患者在ICIs用药后出现难以解释的严重乏力、意识障碍(如嗜睡、精神萎靡、反应迟钝等)、食欲不振等症状,同时伴有难以纠正的低钠血症,部分患者还伴有低血压(升压药治疗效果不佳),结合晨8时皮质醇水平明显降低,则提示免疫相关肾上腺皮质功能减退的可能性较大。
王锋(肿瘤科):如何区分原发性与继发性肾上腺皮质功能减退?
彭晓韧(内分泌科):原发性与继发性肾上腺皮质功能减退的核心区别在于器官损伤部位及激素水平的变化。原发性肾上腺皮质功能减退的原因是过强的免疫反应直接攻击肾上腺,导致皮质醇分泌不足,进而引起乏力、意识障碍、食欲不振等症状;而醛固酮不足则会导致肾脏排钠保钾功能异常,常表现为低钠血症、高钾血症。
免疫性垂体炎是免疫药物引起部分或全部垂体前叶功能受损所致,最常见的表现为继发性甲状腺功能减退(约占93%),其次为低促性腺激素引起的性腺功能减退(86%),再次为继发性肾上腺皮质功能减退(75%),对生长激素和泌乳素分泌的影响相对较小。因垂体功能障碍可能导致促肾上腺皮质激素(ACTH)减少,进而引起肾上腺皮质萎缩,以皮质醇缺乏为主,电解质异常程度较轻。免疫性垂体炎在国外报道较多,但国内病例数较少,这与中国医生较少使用CTLA-4抑制剂或双免联合治疗有关。PD-1/PD-L1抑制剂相关垂体炎的总体发生率约为0.4%,其中CTLA-4抑制剂单药治疗的垂体炎发生率高达3.2%,而CTLA-4联合PD-1抑制剂治疗时,这一比例进一步升至6.4%。垂体炎的主要临床症状包括持续性头痛和/或视觉障碍,需与脑转移癌、软脑膜疾病及脑血管疾病相鉴别;垂体MRI检查可显示垂体肿胀或增大,确诊则需完善促肾上腺皮质激素(ACTH)、促甲状腺激素(TSH)、游离甲状腺素(FT4)、游离三碘甲状腺原氨酸(FT3)、三碘甲状腺原氨酸(T3)、甲状腺素(T4)、黄体生成素(LH)、卵泡刺激素(FSH)、睾酮(T)、泌乳素(PRL)及晨起皮质醇(COR)等相关化验检查。
王锋(肿瘤科):这位患者考虑为继发性肾上腺皮质功能减退,还是原发性肾上腺皮质功能减退?
彭晓韧(内分泌科):从专科角度看,原发性肾上腺皮质功能减退的损伤部位在肾上腺本身,继发性则源于中枢,多由免疫性垂体炎引发。激素水平变化方面,典型的原发性肾上腺皮质功能减退表现为皮质醇降低、ACTH升高,而继发性则呈现皮质醇降低、ACTH降低。
该患者初次接受PD-1抑制剂治疗后,皮质醇降低但ACTH未出现反馈性升高,提示垂体可能存在损伤;此外,泌乳素轻度升高也进一步支持垂体损伤的可能性,同时不排除存在轻微免疫性肾上腺损伤,导致垂体未受到强烈负反馈刺激。但由于患者当时无相关临床症状,未进行特殊干预。2024年6月,患者出现乏力、头晕、视物模糊、排尿无力、食欲不振等症状,但无头痛及视神经压迫表现,影像学检查也未发现垂体异常;2024年8月的实验室检查显示皮质醇明显降低、泌乳素升高,但未检测ACTH。此后患者长期接受糖皮质激素治疗,2025年6月起多次检测提示ACTH水平明显降低,推测可能随着用药次数增加,垂体损伤加重,导致ACTH分泌减少,因此该患者应考虑诊断为继发性肾上腺皮质功能减退。后续仍需定期复查皮质醇、ACTH等指标,也可检测FSH、LH、T等,以明确是否存在多系统内分泌毒性。
王锋(肿瘤科):免疫性甲状腺功能减退应如何诊断和治疗?
彭晓韧(内分泌科):免疫性甲状腺功能减退是最常见的内分泌毒性反应,但绝大多数患者无明显症状,通过血清检查发现TSH升高、FT4降低即可确诊。因此,在免疫检查点抑制剂(ICIs)用药前进行基线检查,以及用药后定期监测甲状腺功能至关重要。甲状腺过氧化物酶抗体(TPO-Ab)、促甲状腺激素受体抗体(TRAb)等甲状腺自身抗体可协助鉴别病因。当甲状腺功能减退有相关临床症状或TSH>10 IU/ml时,应接受左旋甲状腺素治疗,推荐剂量为1~1.6μg/Kg/d,起始剂量为25~50μg/d;对于高龄或合并心血管疾病的患者,起始剂量可调整为12.5μg/d。甲状腺素的剂量需根据甲状腺功能检查结果进行调整,少数患者甚至需要150μg/d才能使TSH降至正常范围。
需要注意的是,部分患者在ICIs治疗后会出现破坏性甲状腺炎,早期表现为甲状腺毒症,即甲状腺激素增高,TSH降低,这种情况与甲状腺滤泡细胞被破坏后,滤泡内甲状腺素短期大量释放入血有关。随着时间推移,1~2月后甲状腺功能可出现下降或恢复正常。ICIs引起的“甲状腺功能亢进”无需抗甲状腺治疗,仅予对症处理即可。因此,ICIs治疗后出现的甲状腺功能异常需要进行严密的鉴别诊断,明确是真正的甲状腺功能亢进,还是一过性的甲亢(即破坏性甲状腺炎),可通过甲状腺摄碘率或甲状腺静态显像予以明确。破坏性甲状腺炎的摄碘率是降低的,静态显像表现为摄取减少,甲状腺不显影。这位患者甲状腺功能轻度异常,可继续随访观察,暂不作特殊处理。
王锋(肿瘤科):夏主任您好,免疫性垂体炎患者的临床表现似乎缺乏特异性,应如何与脑血管疾病鉴别?
夏磊(神经内科):肿瘤患者多为中老年人群,或多或少存在脑血管病变基础,若医生经验不足,免疫性垂体炎患者很容易被当作脑血管疾病在神经内科接受治疗。当患者接受神经内科常规处理后,乏力、意识障碍、食欲不振、低钠血症等症状迟迟无法纠正,部分患者可能因诊断延迟或并发症而危及生命。此外,垂体MRI并非临床常规检查项目,部分患者仅在垂体炎早期见垂体体积轻或中度增大,可伴垂体柄增粗,但大多数患者垂体MRI没有明显异常,容易导致漏诊或诊断延迟。因此,大多数免疫性垂体炎患者需要结合ICIs用药史、临床表现及垂体相关激素检测结果进行综合判断。
王锋(肿瘤科):该患者血糖显著高于正常水平,究竟是免疫药物所致的血糖升高,还是1型糖尿病或长期使用激素引发的不良反应?
彭晓韧(内分泌科):不少肿瘤患者本身存在2型糖尿病或糖耐量异常。免疫药物可损伤胰岛β细胞,导致胰岛素分泌不足,进而使血糖明显升高——这种情况在临床并不少见,却易被误诊为饮食不当、降糖药使用不规律引起的血糖波动,或其他药物的副作用。此类患者停用ICIs后,经短期强化降糖治疗,血糖通常可恢复至基线水平。
1型糖尿病95%由免疫系统异常引发,患者体内存在抗谷氨酸脱羧酶抗体、胰岛细胞抗体等针对β细胞的自身抗体,同时受遗传因素影响(如HLA-DQ、HLA-DR基因型会增加患病风险),但通常需病毒感染、饮食等环境因素共同作用才会发病。
ICIs治疗引发的糖尿病较为罕见,发病率不足1%,且多呈暴发性起病。此类患者通常无2型糖尿病病史或糖耐量异常,发病时间多在ICIs用药后数周至1年内,平均约20周。起病后,患者胰岛素及C肽水平常迅速降至正常值的三分之一以下,结合空腹血糖≥7.0mmol/L、餐后血糖≥11.1mmol/L即可确诊为ICIs相关糖尿病。其典型症状包括多尿、口渴、体重下降、恶心、呕吐等,严重者可合并酮症酸中毒。ICIs相关糖尿病与典型的暴发性或急性发作性1型糖尿病在临床特征上存在诸多差异,这类患者的胰岛功能往往难以逆转,需尽早启动长期胰岛素治疗,即使停用ICIs后也应持续进行糖尿病管理与随访。文献报道显示,约50%的ICIs相关糖尿病患者存在胰岛素抗体阳性,抗谷氨酸脱羧酶抗体可呈持续阳性;但我院收治的数例暴发性糖尿病患者中,抗谷氨酸脱羧酶抗体及胰岛细胞抗体均为阴性,这一现象有待进一步观察研究。
类固醇性糖尿病是指长期或大剂量使用糖皮质激素类药物导致的血糖异常,属于继发性糖尿病。其核心机制为激素干扰胰岛素的作用或分泌,造成胰岛素抵抗或胰岛β细胞功能受损,进而表现为空腹或餐后血糖升高。本例患者既往无糖尿病病史及糖耐量异常,因并发免疫相关肾上腺皮质功能减退需长期使用类固醇激素,导致空腹及餐后血糖明显升高,符合类固醇性糖尿病的诊断。目前患者为治疗肾上腺皮质功能减退,每日服用强的松10mg,剂量已超过生理水平,需考虑类固醇性糖尿病的可能,因此在使用激素的同时应给予降糖治疗。鉴于患者目前血糖仅轻度升高,可先采用口服降糖药治疗;若血糖控制不佳,再酌情给予胰岛素治疗。
王锋(肿瘤科):ICIs引起的垂体功能障碍也可能导致多尿、烦渴等症状,该如何与免疫性糖尿病酮症酸中毒鉴别?
彭晓韧(内分泌科):垂体是调节多种激素分泌的中枢,免疫性垂体损伤可能引发激素紊乱。垂体前叶功能减退可导致ACTH、TSH、LH/FSH分泌不足,进而表现出相应症状;而垂体后叶功能异常则可能造成抗利尿激素(ADH)分泌减少,引发多尿、极度烦渴、频繁夜尿等症状,但这种“尿崩症”在免疫毒性反应中十分罕见,可通过检测尿比重、禁水加压实验进一步明确诊断。
ICIs引起的糖尿病酮症酸中毒属于急症,其核心机制为胰岛素分泌严重不足,脂肪分解加速导致酮体生成量超过代谢能力,酸性物质蓄积引发酸中毒。患者除多饮多尿、恶心呕吐、呼吸深快外,严重时可出现意识障碍或休克,易被误诊为脑血管疾病,可通过空腹及餐后血糖测定、尿酮体测定等明确诊断。需要注意的是,部分糖尿病酮症酸中毒患者因严重脱水、电解质紊乱可导致多系统损伤,如心肌损伤(肌钙蛋白、CK-MB、Mb升高)、肾脏损伤(Cr、BUN升高)等,易被误诊为多系统免疫毒性而采用大剂量激素治疗,反而会进一步加重血糖升高,最终导致不良结局。
王锋(肿瘤科):免疫相关肾上腺皮质功能减退该如何治疗?这位患者长期使用强的松,出现了轻度满月脸、皮肤痤疮样皮疹、肥胖及体重增加的情况,是否由激素过量导致?
彭晓韧(内分泌科):免疫相关肾上腺皮质功能减退的难点在于诊断不明确,治疗本身并不复杂,核心是使用糖皮质激素,且起效较快,多数患者用药后1~3天症状即可明显缓解。急性期可每8小时静脉注射氢化可的松50~100mg;病情稳定后转为口服给药。虽然强的松与氢化可的松均可用于肾上腺皮质功能减退的治疗,但权威内分泌学会指南均推荐氢化可的松作为一线替代治疗药物,而非强的松。氢化可的松是人体肾上腺分泌的天然糖皮质激素(即皮质醇),生物活性与内源性皮质醇完全一致;强的松则为合成糖皮质激素,需经肝脏代谢转化为泼尼松龙才能发挥作用,而氢化可的松无需转化即可直接起效。此外,氢化可的松半衰期较短(约8~12小时),更贴近人体生理分泌节律,对下丘脑-垂体-肾上腺(HPA)轴的负反馈抑制相对较轻;强的松作用时间较长(12~36小时),长期使用更易抑制HPA轴,增加肾上腺萎缩风险。最后,替代治疗的核心是模拟生理性激素波动,而非强效抗炎——强的松的抗炎作用较氢化可的松更强,长期作为替代治疗可能引发过度抑制及代谢紊乱。该患者长期口服强的松(5mg/次,2/日),剂量已超出生理需求,其轻度满月脸、皮肤痤疮样皮疹、肥胖及体重增加可能与此相关,建议调整为氢化可的松治疗。
王锋(肿瘤科):针对ICIs相关肾上腺皮质功能减退,《CSCO免疫检查点抑制剂相关的毒性管理指南2023版》推荐氢化可的松的用法为早晨20mg、下午10mg。临床实践中,氢化可的松的常用剂量是多少?
彭晓韧(内分泌科):每日30mg的氢化可的松其实已超出生理需要量,易引发满月脸、向心性肥胖等激素相关症状,还会增加感染、高血糖风险。《免疫检查点抑制剂引起的内分泌系统免疫相关不良反应专家共识2020版》推荐氢化可的松每日总量为15~20mg,分2~3次服用,可根据患者症状变化酌情调整。
王锋(肿瘤科):部分患者使用激素后,抽血检测皮质醇仍偏低,是否考虑激素用量不足?
彭晓韧(内分泌科):这是临床中较为常见的认知误区。外源性激素替代无法完全模拟人体生理节律与反馈调节机制,长期使用还可能抑制下丘脑-垂体-肾上腺(HPA)轴功能,导致自身皮质醇分泌减少。因此,即便补充外源性激素,抽血检测的皮质醇仍可能低于正常水平,且增加剂量也无法使血液皮质醇恢复至正常范围。临床上不以皮质醇数值达标为目标,而应以乏力、意识障碍、食欲不振等症状得到有效缓解为核心,切忌因皮质醇未达正常范围而盲目加大激素用量。
王锋(肿瘤科):该患者曾因肿瘤侵及一侧肾上腺接受手术切除,后续出现的肾上腺皮质功能减退是否与手术相关?
彭晓韧(内分泌科):单侧肾上腺切除一般不会引发肾上腺皮质功能减退。该患者于2019年9月2日行腹腔镜下右侧肾上腺肿瘤切除术,术后未出现相关症状;2021年5月启动ICIs治疗前,皮质醇水平检测正常,直至ICIs用药后才出现皮质醇降低。由此可见,其肾上腺皮质功能减退与手术无关,而与ICIs治疗相关。
王锋(肿瘤科):患者已确诊为ICIs相关肾上腺皮质功能减退,若停用ICIs治疗,是否可同步停用氢化可的松?
彭晓韧(内分泌科):ICIs引发的内分泌毒性对肾上腺、甲状腺的损伤多为不可逆,因此需长期替代治疗。其中,肾上腺皮质功能减退需要长期服用氢化可的松,大多数甲状腺功能减退患者也需长期服用甲状腺素片,贸然停药或服药不规律可能导致症状复发。
李祥(药学科):晚期肝细胞癌(HCC)的治疗一直是临床难题,现有药物的疗效与无进展生存期(PFS)均不够理想。文献报道ICIs联合TKI一线治疗的PFS在4~9个月之间,而这位患者在索拉非尼一线治疗失败后,改用PD-1抑制剂联合方案,PFS却长达4年余,其原因是什么?
王锋(肿瘤科):这正是ICIs治疗的独特优势所在。该患者初始接受免疫联合化疗后达到部分缓解(PR),但因并发肝炎、肾功能损伤等不良反应而停止化疗,随后采用免疫联合TKI方案长期维持治疗,PFS较平均水平显著延长,主要得益于免疫治疗特有的“长拖尾效应”。临床观察发现,部分患者免疫治疗疗效佳且持续时间长,一方面与患者自身肿瘤负荷较低相关,另一方面可能与其肿瘤组织中PD-L1或肿瘤突变负荷(TMB)高表达有关。不过,由于该患者的原始手术标本不在我院,未进行相关基因检测,具体机制尚无法明确。
李祥(药学科):这位HCC患者采用免疫联合mFOLFOX4方案治疗获得PR,说明其可能对化疗也较为敏感,但当前国内外指南中,HCC的推荐药物主要为免疫药物和靶向药物,静脉化疗似乎未在临床广泛应用,究竟是什么原因?
王锋(肿瘤科):本院肿瘤中心曾牵头开展一项亚洲多中心Ⅲ期临床研究(EACH),研究结果于2013年发表在国际著名期刊《Journal of Clinical Oncology》,证明了FOLFOX4方案在晚期HCC一线治疗中的价值,FOLFOX4方案也被国内肝癌指南推荐用于晚期HCC。本中心部分患者经FOLFOX4方案治疗后获得完全缓解(CR)或PR,并实现长期生存,表明该方案具有一定疗效,尤其对伴有多发肺转移的HCC患者效果较好。目前国内正在开展化疗联合免疫、靶向药物的全国多中心Ⅲ期临床研究,以进一步明确化疗联合治疗的疗效与安全性。
当然,中国HCC患者常合并慢性乙型肝炎、肝硬化、脾功能亢进,部分患者还伴有门静脉高压、肝功能储备不足等问题,治疗期间易出现白细胞降低、血小板减少、消化道反应及肝功能异常等不良反应,导致患者对静脉化疗的耐受性普遍较差,这在一定程度上限制了化疗的广泛应用。因此,化疗前需完善充分的基线评估,化疗期间应加强监测与预防性处理,一旦出现不良反应需及时干预。近年来,国内部分肝癌中心尝试采用肝动脉灌注化疗(HAIC)方式给予FOLFOX4或其改良方案治疗,取得了较好疗效,相关高质量研究成果已陆续发表,值得进一步探索与推广。
陈歆妮(肿瘤科):该患者出现严重肾上腺皮质功能减退,若治疗有效,能否重启ICIs治疗?
王锋(肿瘤科):临床上部分肾上腺皮质功能减退患者虽症状严重,但经激素治疗后可快速完全缓解,通常不会危及生命,关键在于加强健康宣教,叮嘱患者切勿自行停用激素。该患者接受以免疫治疗为主的方案后,肿瘤长期维持部分缓解(PR)状态,但因不良反应停用免疫治疗后,肿瘤标志物一度显著升高,提示肿瘤仍处于活动期,不宜终止ICIs治疗。建议待患者肾上腺皮质功能减退症状缓解、血糖得到有效控制后,继续采用ICIs联合TKI治疗,并酌情延长用药间隔。
MDT小结:
1. 患者明确诊断为免疫相关肾上腺皮质功能减退(继发性)、类固醇性糖尿病;
2. 停用强的松,改为口服氢化可的松,积极控制血糖,定期监测皮质醇、ACTH及血糖变化;
3. 待患者相关症状缓解后,继续予PD-1抑制剂联合TKI治疗,酌情延长用药间隔。
治疗及随访结果:
1. 经内分泌科诊断为“类固醇性糖尿病”,予脯氨酸恒格列净(10mg,每日1次)降糖治疗,同时指导患者调整饮食结构并适当运动。治疗后血糖控制良好,口干、多饮、多食症状消失。
2. 停用强的松片,改为氢化可的松治疗(10mg,每日早8时服用;5mg,每日中午服用;5mg,下午15时服用)。患者满月脸、面部痤疮样皮疹逐渐消退,体重恢复至正常水平。
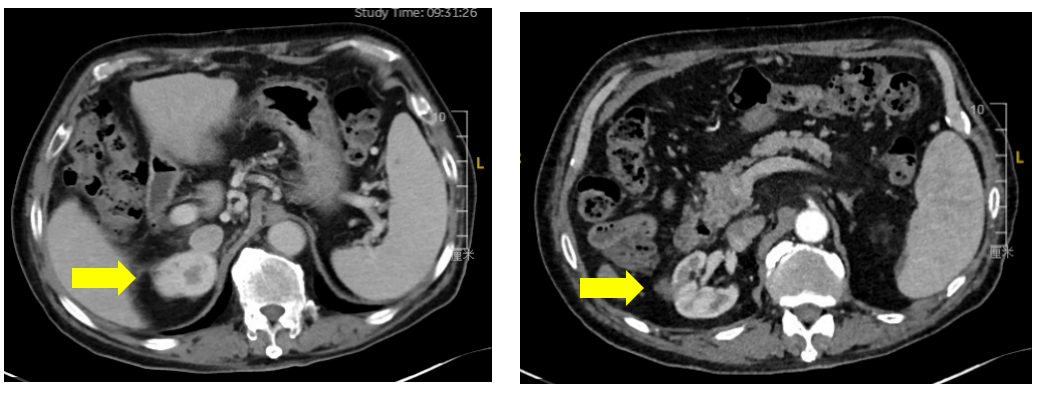
3. 2024年9月13日恢复PD-1抑制剂联合TKI治疗至今,用药间隔延长至5~6周,PD-1抑制剂末次用药时间为2026年4月21日。定期行影像学检查,评估为维持PR,末次检查日期为2026年2月6日(见图3)。
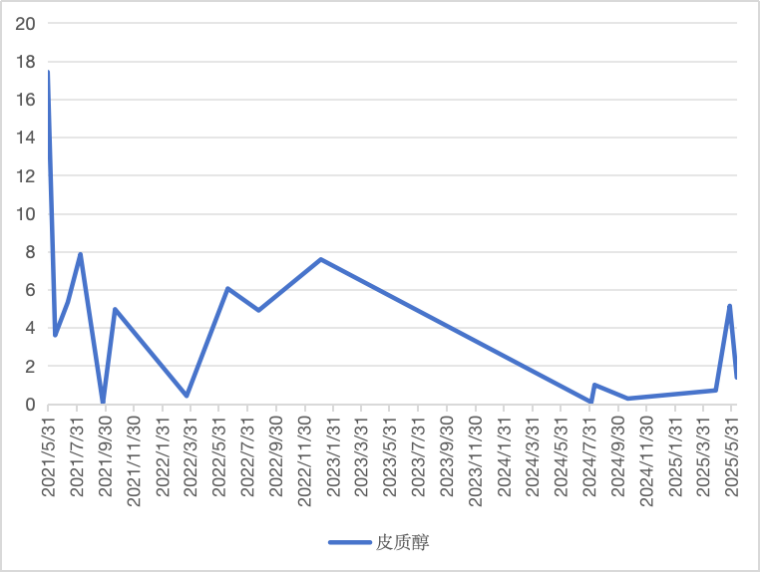
4. 患者ICIs治疗前、后的皮质醇变化情况见图4。


附“免疫治疗相关不良反应顺口溜”
免疫家族新军起,
数十瘤种显神奇。
不良反应少而轻,
多个系统可累及。
三早处理多逆转,
致死毒性须警惕。
激素王牌足量用,
专科会诊莫忘记。
注释:免疫检查点抑制剂作为抗肿瘤免疫药物家族的新生力量,为无数癌症患者带来了新的希望,部分患者因此获得强效且持久的神奇疗效。短短十余年间,全球已上市20余种免疫检查点抑制剂,获批用于数十个瘤种、100多项适应证。与化疗和靶向药物相比,免疫检查点抑制剂单药治疗的总体不良反应相对较少、程度较轻,但可能累及全身多个器官或组织,容易造成误诊或漏诊。
若能做到早期发现、早期诊断与早期治疗,大多数免疫相关不良反应可得到有效控制,但需警惕免疫性肺炎、免疫性肝炎、免疫性心肌炎、免疫性肠炎等可能危及生命的毒性;在内分泌系统毒性中,免疫性肾上腺皮质功能减退、免疫性垂体炎、1型糖尿病往往症状严重且难以鉴别。糖皮质激素常作为首选治疗药物(甲状腺功能减退需补充甲状腺素,肾上腺皮质功能减退优选氢化可的松),且需足量、足疗程使用。由于免疫不良反应可能累及全身多个器官或组织,单一科室在认知水平和管理能力上存在局限,因此有必要成立多学科诊疗团队(MDT);一旦发生免疫治疗相关不良反应,及时请专科医生协助诊治,才能确保患者得到及时诊断、精准治疗并快速康复。
本期专家组成员

排版编辑:XF











 苏公网安备32059002004080号
苏公网安备32059002004080号


