随着胃癌精准治疗的不断推进,FGFR2b作为新兴靶点正逐步受到临床关注。FIGHT II期研究显示,在晚期胃/胃食管结合部(G/GEJ)腺癌一线治疗中,靶向FGFR2b的贝玛妥珠单抗联合化疗为患者带来显著的生存获益。目前,两项III期临床试验正在进一步评估其在晚期G/GEJ腺癌中的疗效与安全性,其中FORTITUDE-101研究已公布达到了总生存期(OS)主要终点,详细结果值得期待。然而,FGFR2b过表达在胃癌临床实践中的发生率、其与胃癌已知靶点(HER2、MMR、PD-L1、CLDN18.2)之间的表达重叠情况、其临床特征及预后价值以及真实世界精准检测过程中需关注的关键因素,仍有待深入探索。【肿瘤资讯】特邀北京大学肿瘤医院张小田教授,深度解读由胃癌专家Kohei Shitara教授团队开展的一项关于晚期胃及胃食管结合部腺癌患者FGFR2b表达特征的研究,并围绕相关临床问题展开深入探讨。
北京大学肿瘤医院内蒙古医院 执行院长
主任医师、教授、博士生导师
科研方向:消化系统肿瘤(胃癌)防诊治一体化的临床与基础研究
北京市“登峰”人才培养计划团队负责人
消化系肿瘤整合防治全国重点实验室PI
中国临床肿瘤学会 理事胃癌专家委员会 副主任委员等
中国抗癌协会 理事 肿瘤信息化管理专业委员会 主任委员等
中国女医师协会 临床肿瘤学专家委员会 秘书长
北京癌症防治学会 胃癌防治专家委员会主任委员
致力于推动我国胃癌等消化系统恶性肿瘤精准诊疗水平走向国际前沿,牵头临床研究推动10种药物/方案进入临床实践,获批专利10项;近5年以第一或通讯作者(含共同)在JAMA、Nature、Lancet、JCO等主刊/子刊发表文章33篇,总影响因子447分,单篇最高引用371次;撰写指南27项, 24项研究改写33项国内外指南。
研究背景简介
这篇文章由 Kohei Shitara 教授团队发表在 ESMO Open,分析了胃癌领域临床医生高度关注的重要标志物——FGFR2b。文章探讨了 FGFR2b 表达型胃癌的临床病理特征,以及在多个关键标志物共表达的情况下,如何解读其病理特点,并在临床实践中如何评估和应用这一生物标志物。
成纤维细胞生长因子受体2b(FGFR2b)是一种新型蛋白质生物标志物,在G/GEJ腺癌中表达。FIGHT II期研究显示,在晚期G/GEJ腺癌一线治疗中,靶向FGFR2b的贝玛妥珠单抗联合化疗在无进展生存期(9.5个月 vs 7.4个月,HR=0.72)和总生存期(19.2个月 vs 13.5个月,HR=0.77)方面均优于安慰剂联合化疗[1,2]。目前,两项III期临床试验[FORTITUDE-101 (NCT05052801) 和FORTITUDE-102 (NCT05111626) ]正在进一步评估其在晚期G/GEJ腺癌中的疗效与安全性,其中FORTITUDE-101研究已公布达到了OS主要终点,详细数据会在今年ESMO大会上公布,结果值得期待。然而,FGFR2b表达肿瘤的特征以及其与目前可靶向治疗的胃癌生物标志物的重叠情况仍不清楚。
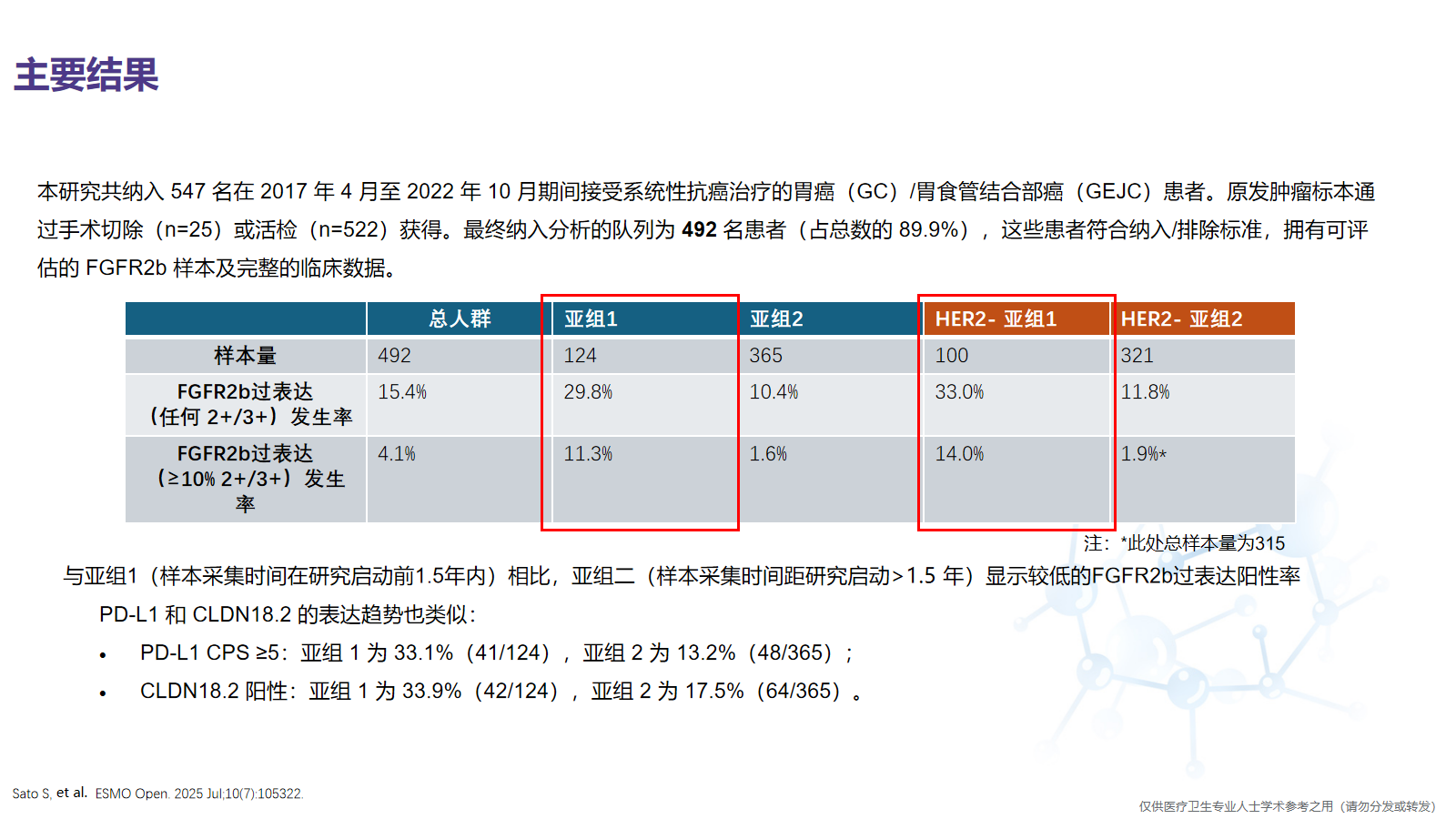
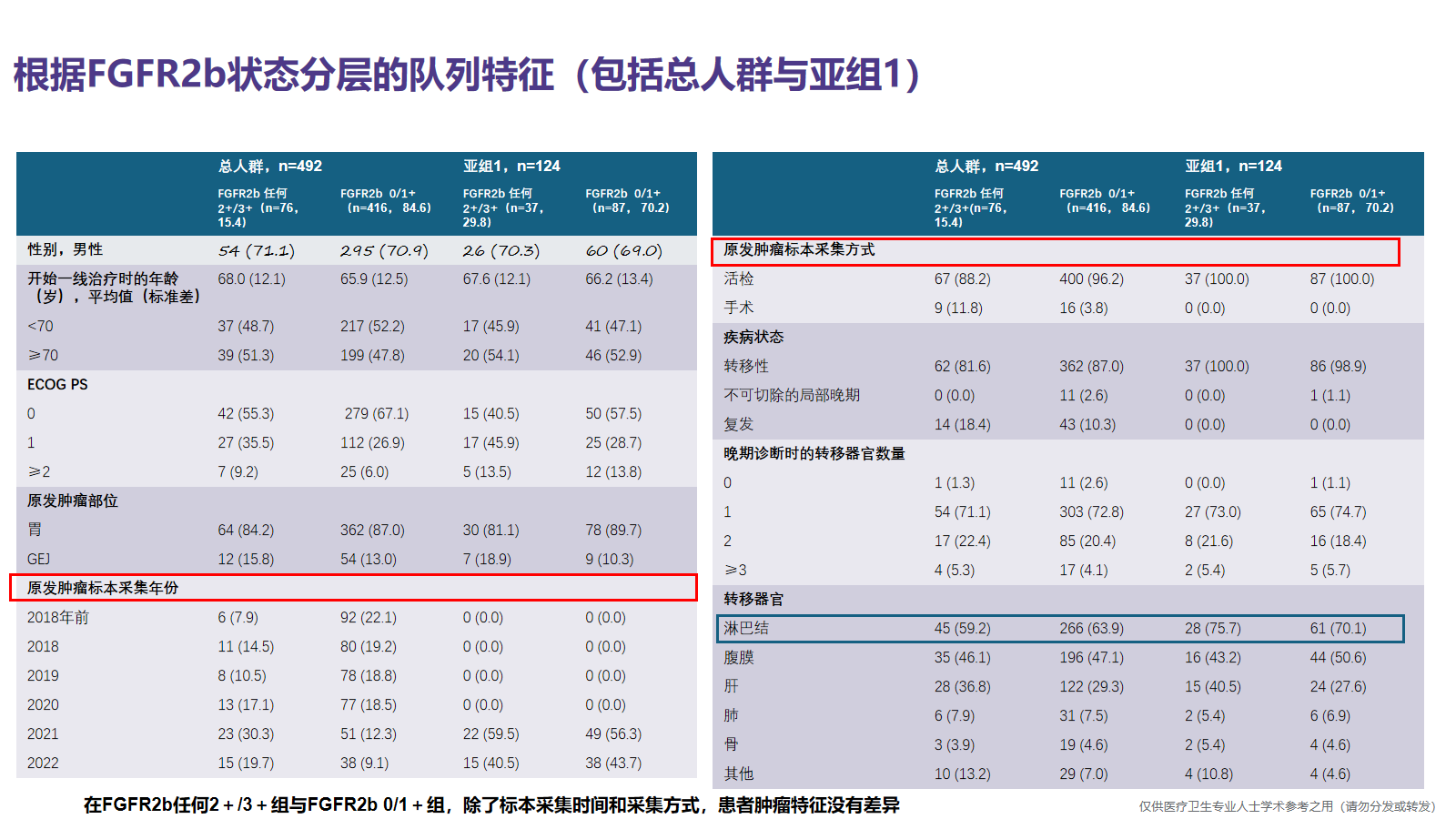
本研究是一项单中心回顾性分析[3],研究共纳入了492例G/GEJ腺癌患者,作为总人群,这些患者符合纳入/排除标准,具备可评估FGFR2b 的样本及完整的临床数据。研究根据样本采集时间将患者分为两个亚组:亚组1(n=124),样本采集时间距研究启动≤1.5年;亚组2(n=365),样本采集时间距研究启动>1.5年。研究进行描述性分析,以总结不同FGFR2b状态下的临床特征、生物标志物特征以及一线治疗方案。采用单变量和多变量Cox比例风险回归模型估算OS的风险比(HR)及其95%置信区间(CI)。多变量分析的预设协变量包括:年龄(≥70岁 vs <70岁)、性别(男性 vs 女性)、东部肿瘤协作组(ECOG)体能评分(≥1 vs <1)、转移器官数量(≥2个 vs <2个)、是否接受过胃切除术(是 vs 否)、碱性磷酸酶(ALP)水平(≥正常上限 vs <正常上限)、Lauren分型(弥漫型 vs 肠型/不确定型)、一线系统治疗类型(化疗联合免疫治疗 vs 单纯化疗,以及曲妥珠单抗或其他治疗 vs 单纯化疗)。
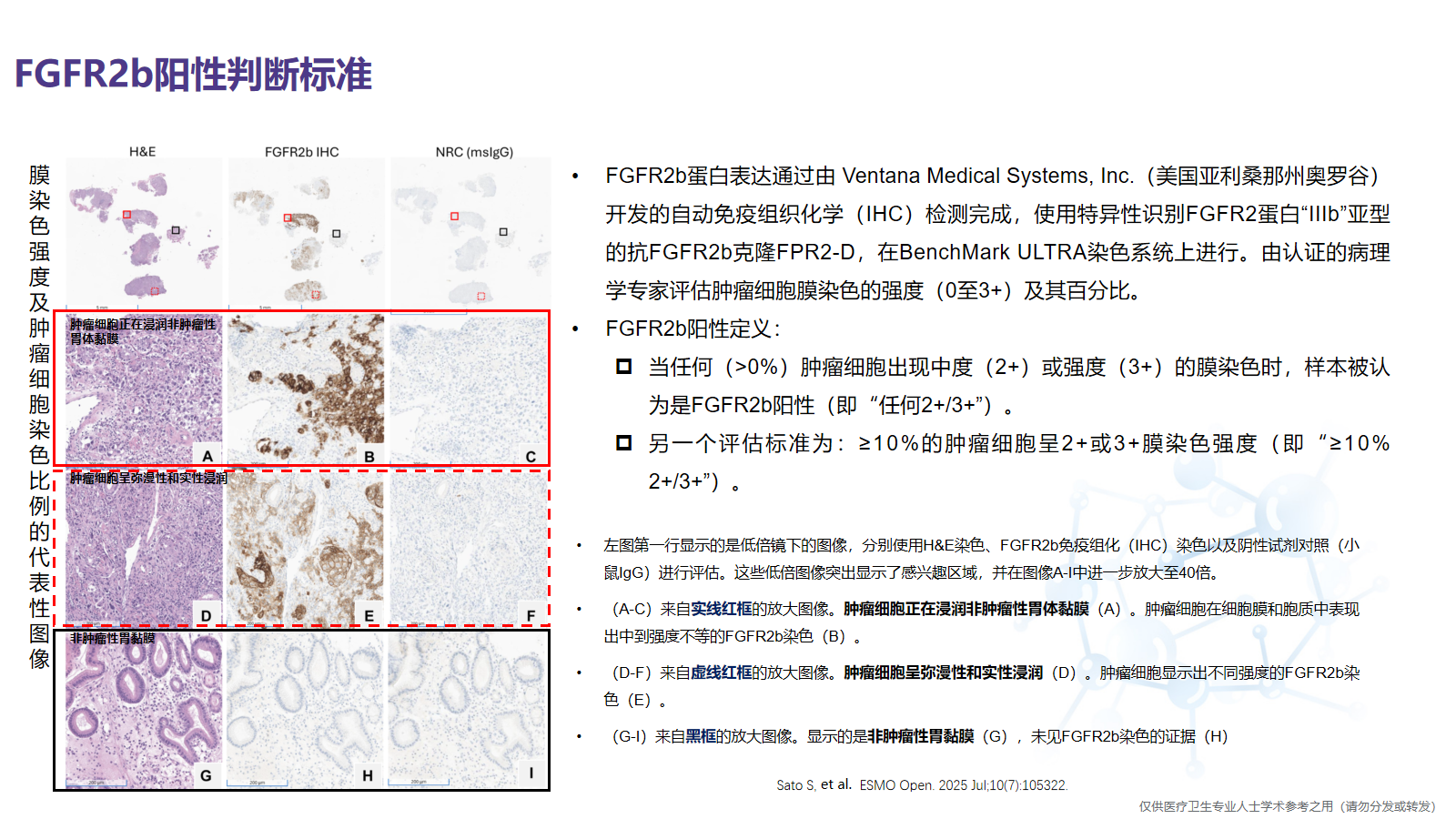
FGFR2b蛋白表达通过由 Ventana Medical Systems, Inc.(美国亚利桑那州奥罗谷)开发的自动免疫组织化学(IHC)检测完成,使用特异性识别FGFR2蛋白“IIIb”亚型的抗FGFR2b克隆FPR2-D,在BenchMark ULTRA染色系统上进行。由认证的病理学专家评估肿瘤细胞膜染色的强度(0至3+)及其百分比。FGFR2b阳性定义:当任何(>0%)肿瘤细胞出现中度(2+)或强度(3+)的膜染色时,样本被认为是FGFR2b阳性(即“任何2+/3+”)。另一个评估标准为:≥10%的肿瘤细胞呈2+或3+膜染色强度(即“≥10% 2+/3+”)。其他生物标志物(HER2、MMR、PD-L1、CLDN18.2)的评估依据当前临床指南。
本研究亚组1中的FGFR2b过表达发生率和既往临床研究报道的一致
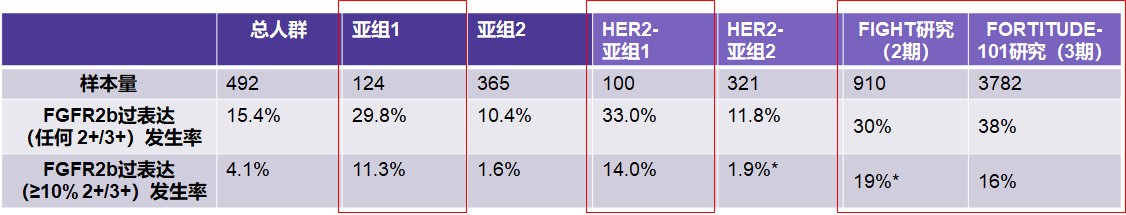
结果显示,总人群中,FGFR2b过表达(任何 2+/3+)发生率为15.4%,FGFR2b过表达(≥10% 2+/3+)发生率为4.1%。亚组1 中,FGFR2b过表达(任何 2+/3+)发生率为29.8%,FGFR2b过表达(≥10% 2+/3+)发生率为11.3%,而亚组2 中,这两个发生率分别为10.4%和1.6%。我们还可以看到,在亚组1中,HER2阴性患者的FGFR2b过表达率似乎更高(任何2+/3+为33.0%,≥10% 2+/3+为14.0%)。基于总人群和亚组1之间的FGFR2b过表达发生率的差异,可以理解是因为亚组二,即距离研究开始时标本时间过长的那一个亚组,影响了FGFR2b过表达的阳性率。FIGHT II期研究报道,FGFR2b过表达(任何2+/3+)发生率约为30%[2];FORTITUDE-101 III期研究3782例样本中,FGFR2b过表达(任何2+/3+)发生率为38%,FGFR2b过表达(≥10% 2+/3+)发生率为16%[4]。需要注意的是,临床研究中所采用的均为新鲜肿瘤组织,或入组前 ≤6 个月内采集的存档组织样本,从而确保了检测阳性率的可靠性。本研究亚组1中FGFR2b过表达发生率与临床研究中报道的大概相似。
与现有靶点重叠有限,FGFR2b在胃癌精准诊疗中具有重要价值
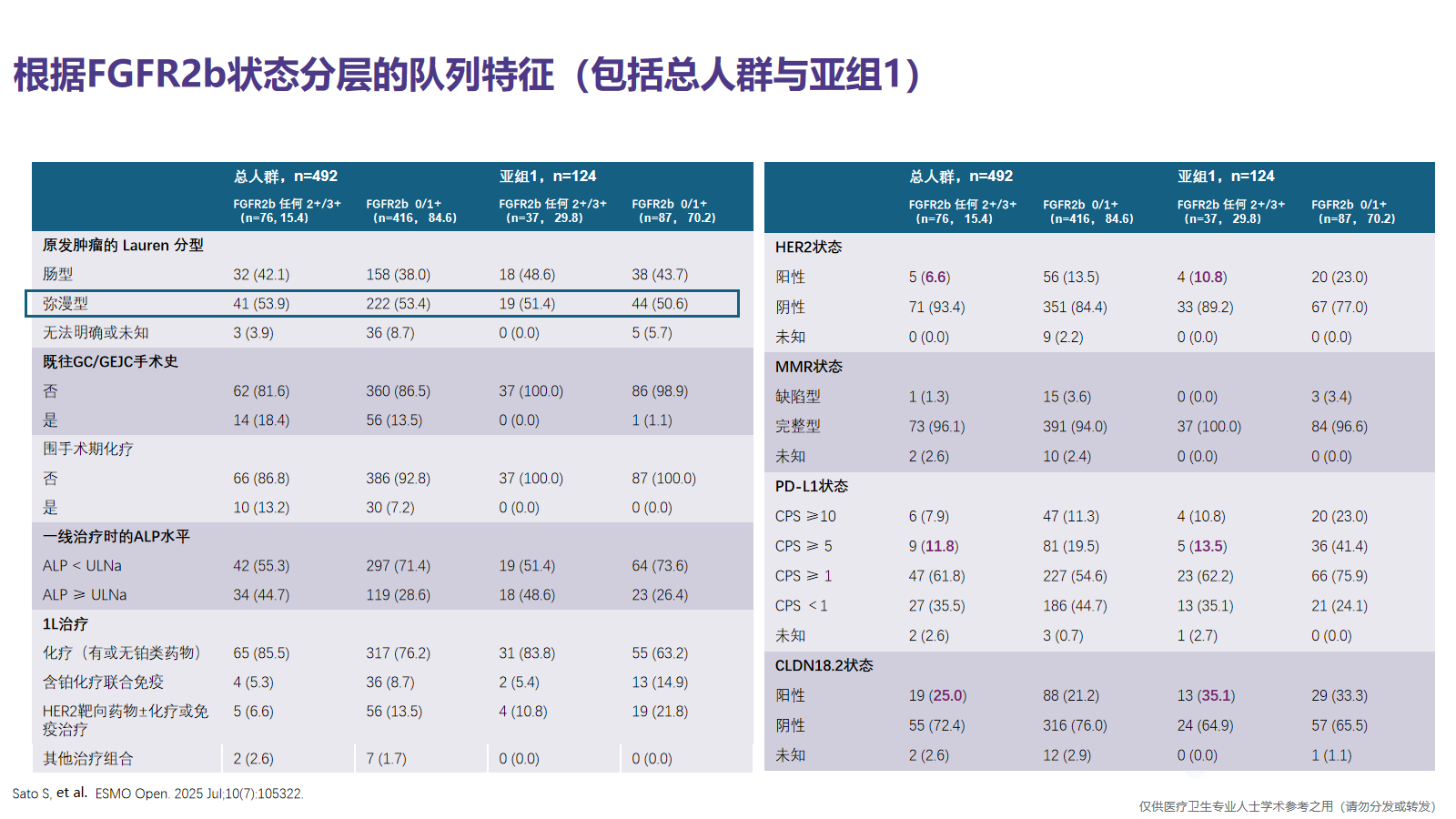
本研究关注了 FGFR2b 过表达与其他生物标志物的重叠情况,重点包括 HER2、MMR、PD-L1 和 CLDN18.2。
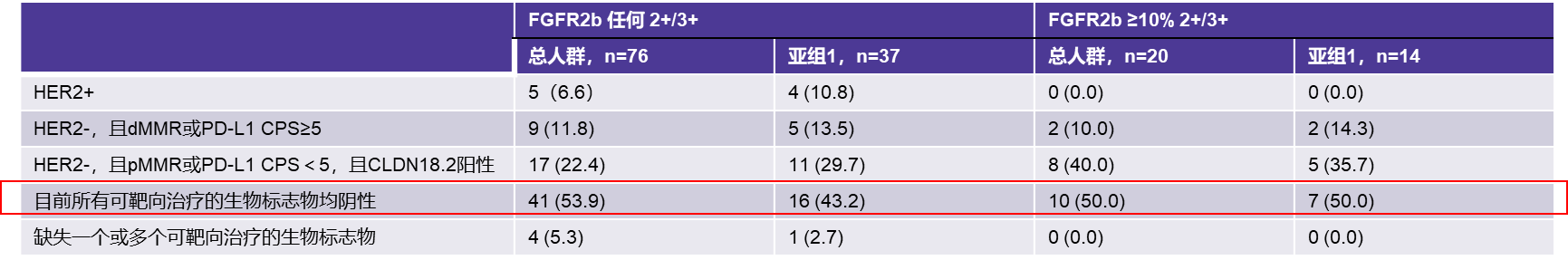
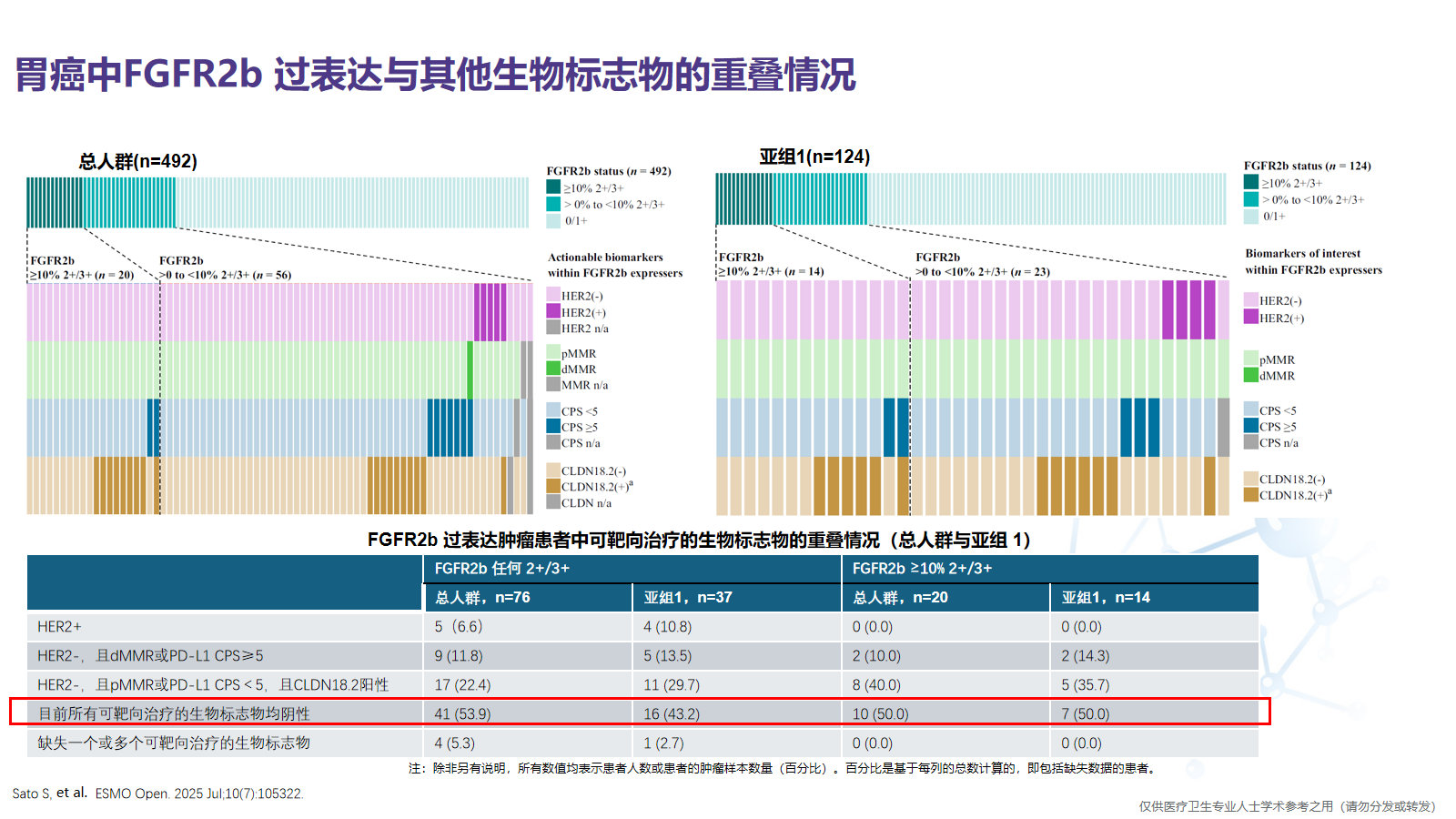
在总人群(n=492)中检测到76例患者存在FGFR2b蛋白过表达(任何2+/3+)。这76例FGFR2b阳性患者中,其共表达情况如下:
·HER2阳性:6.6%;
·HER2-,且dMMR或PD-L1 CPS≥5: 11.8%
·HER2-,且pMMR或PD-L1 CPS<5,且CLDN18.2阳性:22.4%
可以看到,以PD-L1 CPS ≥5为界限,53.9%(41/76; 95% CI:42.1%~65.5%)的FGFR2b阳性样本,其他生物标志物均为阴性
在亚组1(n=124)中,共检测到37例FGFR2b阳性(任何2+/3+)患者,其共表达情况如下:
·HER2阳性:10.8%;
·HER2-,且dMMR或PD-L1 CPS≥5: 13.5%
·HER2-,且pMMR或PD-L1 CPS<5,且CLDN18.2阳性:29.7%
在该亚组中,以PD-L1 CPS ≥5为界限,43.2%(16/37;95% CI:27.1%-60.5%)的
FGFR2b阳性样本,其他生物标志物均为阴性。
值得注意的是,无论在总人群还是亚组1中,若以FGFR2b ≥10% 2+/3+及PD-L1 CPS ≥5为界限,均有约50%的FGFR2b阳性患者,其他生物标志物的检测结果均为阴性。
FGFR2b 过表达肿瘤患者中可靶向治疗的生物标志物的重叠情况(总人群与亚组 1)如下图:
本研究结果表明FGFR2b是胃癌中一个非常重要的靶点,未来可以把这一部分人群先挑出来,对其进行精准治疗。但是,胃癌是一个时间和空间异质性都很强的肿瘤,所以我们也应该继续关注FGFR2b在不同的转移器官和不同的部位当中的差异,以及在治疗过程中的差异。
FGFR2b在胃癌预后评估中的潜在价值仍有待进一步探索
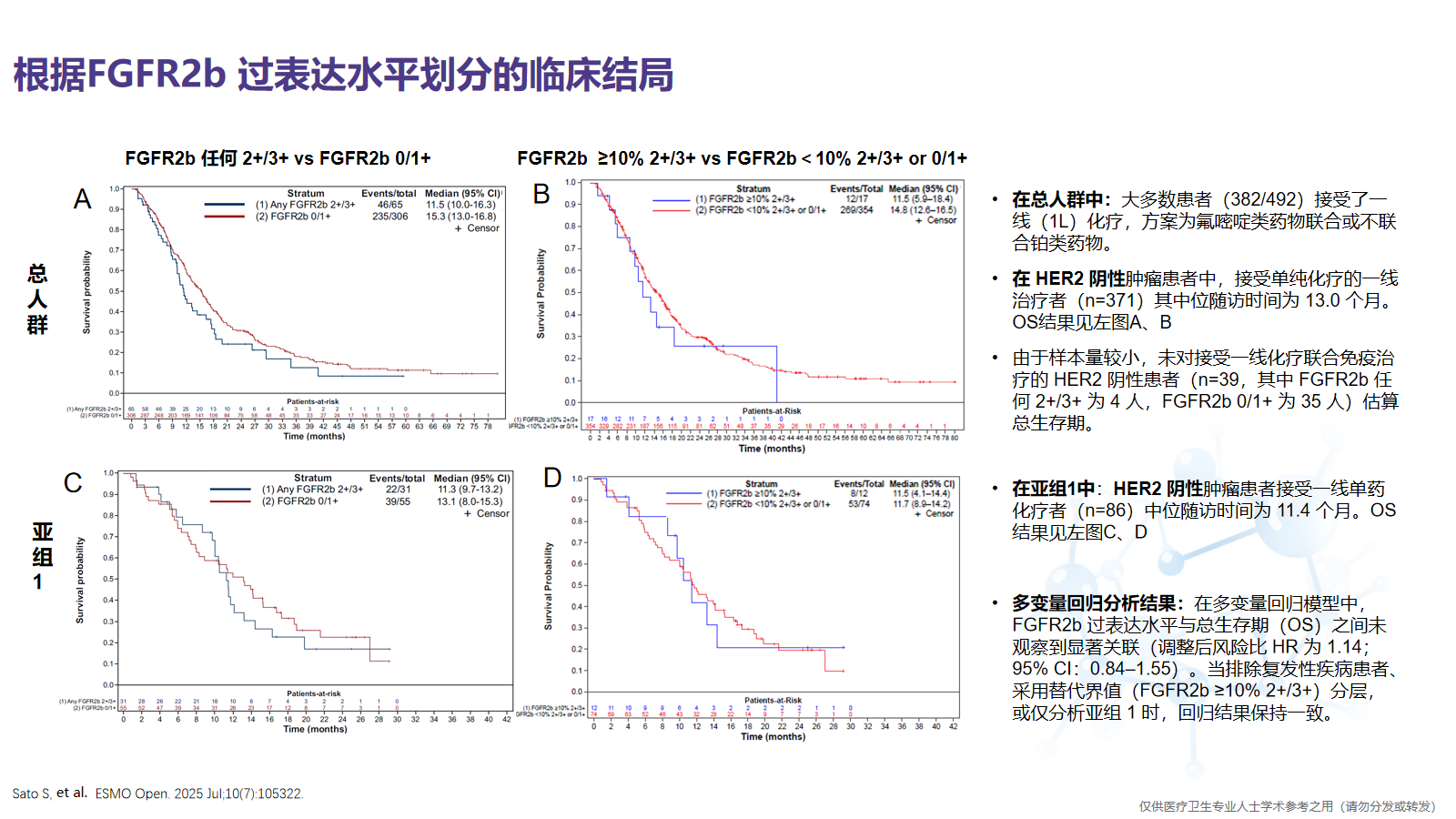
我们也非常关注FGFR2b 过表达和预后是否相关。既往有研究报道,FGFR2b 过表达与弥漫型组织学类型及 N 分期相关,但在本研究中FGFR2b表达状态与组织学类型及淋巴结转移之间未观察到显著相关性。既往也有报道,FGFR2b过表达与胃癌预后不良相关,但本研究未观察到 FGFR2b过表达与OS之间的统计学差异。另外,我们也非常关注FGFR2b的过表达与免疫治疗的疗效是否相关,本研究由于接受一线化疗联合免疫治疗的样本量较小,未对这部分人群进行深入的刻画。
本研究作为一个单中心回顾性分析,可能更多的还是对于FGFR2b过表达的一些临床背景特征的刻画,那么这一部分人群的话,还是需要转化研究来观察过表达人群当中肿瘤微环境有哪些特点,是一个热的环境还是冷的环境,不仅要观察淋巴细胞的个数,还要观察它的功能。因此,FGFR2b过表达是否与不良预后相关,尤其是是否影响免疫治疗疗效,后续还有待进一步研究和探索。
精准检测是关键步骤,多学科协作优化胃癌精准治疗策略
在本研究中,样本采集时间与生物标志物的检测结果呈现一定关联。造成该差异的可能原因包括:组织抗原性随时间下降、肿瘤内标志物表达的异质性等,还有一个非常重要的因素就是我们还需要去考虑小标本和手术大标本不同的组织处理流程,这方面可以借鉴HER2的管理流程。日本的这一项单中心的回顾性的分析,还是提供了一些比较重要的信息,第一,采用近期采集的标本还是非常重要的。另外,在治疗过程中,动态采集也是非常重要的,特别是在胃镜可及且患者可接受的情况下。
综上,我们应积极为晚期胃癌及胃食管结合部癌患者开展 FGFR2b 检测。目前,部分临床中心已将其纳入免疫组化检测项目。特别是在相关治疗即将临床可及之际,更呼吁内科、外科、影像科及病理科多学科团队密切合作,将 HER2、MMR、PD-L1、CLDN18.2、FGFR2b 等关键生物标志物纳入检测范围,并探索基于影像学的影像组学分析。通过多组学手段全面刻画患者特征,深入解析多标志物共高表达的模式,从而更精准地进行患者分层,助力制定个体化治疗方案。
1. Wainberg ZA, Kang YK, Lee KW, et al. Bemarituzumab as first-line treatment for locally advanced or metastatic gastric/gastroesophageal junction adenocarcinoma: final analysis of the randomized phase 2 FIGHT trial. Gastric Cancer 2024; 27(3): 558-70.
2. Wainberg ZA, Enzinger PC, Kang YK, et al. Bemarituzumab in patients with FGFR2b-selected gastric or gastro-oesophageal junction adenocarcinoma (FIGHT): a randomised, double-blind, placebo-controlled, phase 2 study. Lancet Oncol 2022; 23(11): 1430-40.
3. Sato S, Rhodes SL, Aoki Y, et al. Clinical characterization of FGFR2b expression in patients with advanced gastric or gastroesophageal junction adenocarcinoma. ESMO Open 2025; 10(7): 105322.
4. Rha SY, Zhang Y, Elme A, et al. Prevalence of FGFR2b Protein Overexpression in Advanced Gastric Cancers During Prescreening for the Phase III FORTITUDE-101 Trial. JCO Precis Oncol 2025; 9: e2400710.
(左右滑动查看)



(点击标题可下载查看)
*以上信息涉及尚未在中国获批的产品/适应症。此信息仅作信息分享用途,不应被理解为这些产品/适应症在中国获批或注册。
相关文章回顾(点击可查看详情):
1.沈琳教授:2025 CSCO胃癌指南框架性更新,指引胃癌精准诊疗新方向
2.GC云讲堂 | 张小田教授:2025 CSCO 胃癌诊疗指南——晚期转移性胃癌的药物治疗和分子诊断更新要点
3.GC云讲堂 | 盛伟琪教授:FGFR2b——胃癌新兴靶点
4.GC云讲堂丨邱红教授:贝玛妥珠单抗解锁胃癌精准治疗新篇章
排版编辑:yu












 苏公网安备32059002004080号
苏公网安备32059002004080号


