在肿瘤治疗领域,三阴性乳腺癌因其独特的生物学特性和治疗挑战而备受关注。近年来,以戈沙妥珠单抗(SG)和T-DXd为代表的抗体偶联药物(ADC)以其精准的靶向作用和强大的治疗效果,已成为晚期及转移性三阴性乳腺癌(mTNBC)二线及后线治疗的重要选项。此外,其他靶向Trop-2的ADC如SKB264和Dato-DXd,目前正在进行临床研究,以探索其在治疗中的潜力。
本期【肿瘤资讯】特邀青海大学附属医院赵久达教授,深入盘点ADC药物在TNBC治疗中的真实世界安全性数据,以期为临床实践中的安全性管理带来启示。
特邀嘉宾
青海大学附属医院乳腺疾病诊疗中心
中国抗癌协会中西医整合肿瘤专业青年委员会副主任委员
中国抗癌协会青年理事会常务理事
中国老年保健协会乳腺癌专业委员会常务委员
中国医师协会肿瘤学分会乳腺癌学组委员
国家抗肿瘤药物临床应用监测的中青年专家委员会委员
国家癌症中心癌症筛查专家委员会乳腺癌筛查专业委员会委员
中华肿瘤健康管理学院副秘书长
北京肿瘤病理精准诊断研究会青委会常务委员
青海省抗癌协会青年理事会副理事长兼秘书长
青海省抗癌协会中西医整合肿瘤专业委员会主任委员
乳腺癌专业委员会副主任委员
治疗精准治疗专业委员会副主任委员
青海省预防医学会乳腺疾病预防与控制专业委员会副主任委员
全球视角,远见明察
TNBC ADC临床实证不断积累
SG作为TNBC治疗的先锋药物,已经在不同国家和患者群体中积累了丰富的真实世界研究(RWS)数据,提供了关于安全性和疗效的宝贵见解1–5。
表1 SG在mTNBC中的主要RWS概览
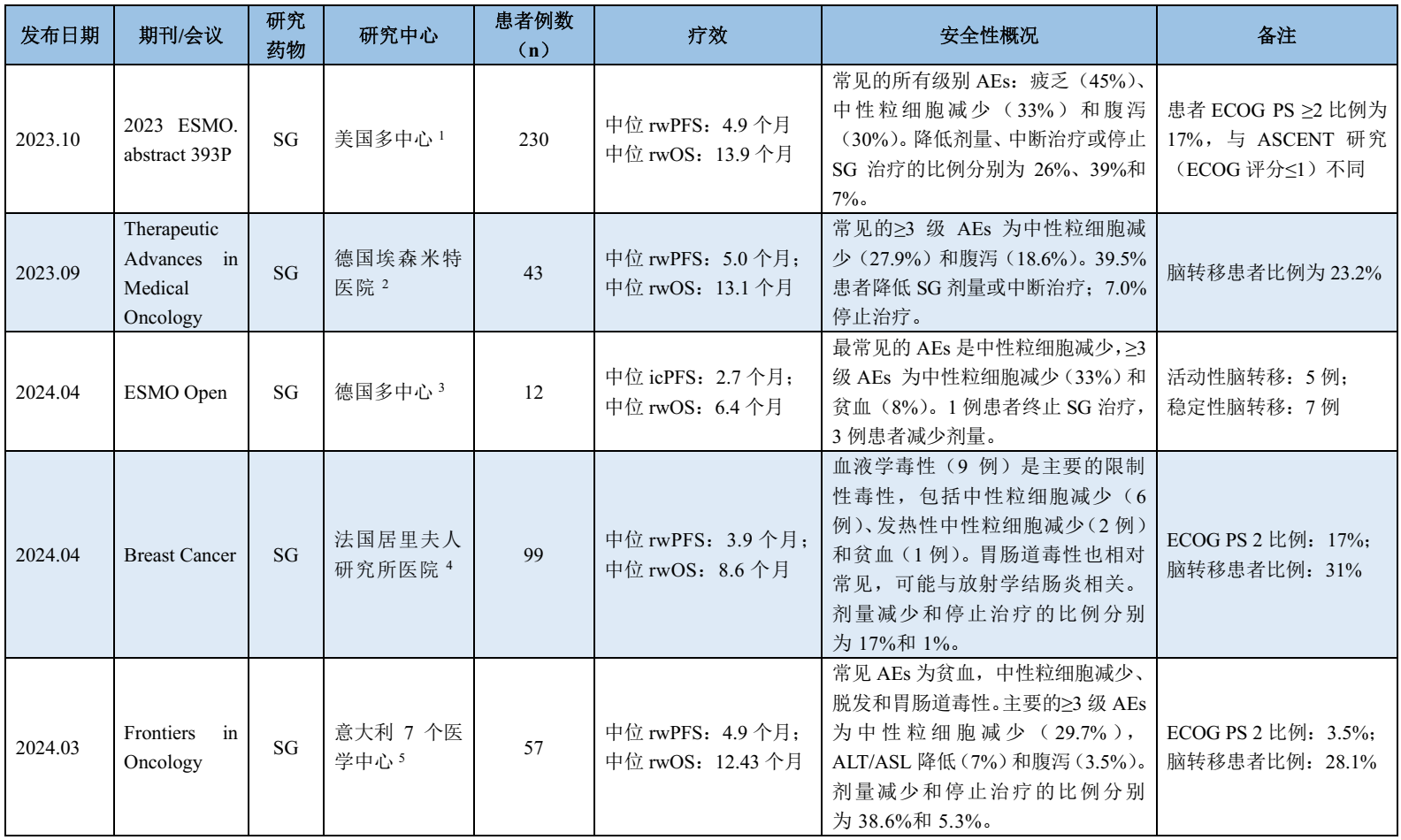
此外,T-DXd在mTNBC患者群体中的RWS也提供了初步的疗效证据6(见后文),而SKB264和Dato-DXd目前正处于积极的临床试验阶段,尚无RWS数据。
拨云见日,欣欣向荣
SG真实世界安全性可控
作为全球首个获批用于mTNBC治疗的Trop-2 ADC药物,SG不仅引领了精准靶向治疗的新潮流,还在实际应用中展现了其安全性和疗效。目前,来自多个国家的RWS为SG在mTNBC治疗和管理中的应用提供了有力证据和经验。
美国RWS证据
在2023年ESMO大会上,公布了一项美国医院中SG治疗mTNBC患者的大样本RWS证据1。该研究纳入230例患者,63%为白种人,26%为黑种人,4%为亚裔人群;中位年龄为60岁;约20%的患者在基线时ECOG体能状态较差。尽管如此,SG作为二线治疗药物,也展现出了中位真实世界无进展生存期(rwPFS)为4.9个月和中位真实世界总生存期(rwOS)为13.9个月的显著疗效。安全性方面,疲乏(45%)、中性粒细胞减少(33%)和腹泻(30%)是报告的常见不良事件(AEs)。因毒性而需要降低剂量、中断治疗或停止SG治疗的患者比例分别为26%、39%和7%,略高于ASCENT的结果(降低剂量:22%;停止治疗:5%)7。此外,58%的患者在接受SG治疗时同时接受了粒细胞集落刺激因子(G-CSF)治疗,这可能有助于管理血液学毒性。该RWS数据与Ⅲ期ASCENT研究的结果一致,证实了SG在种族多样化临床环境中的有效性和耐受性。
表2 SG治疗中断、剂量调整和G-CSF应用的情况
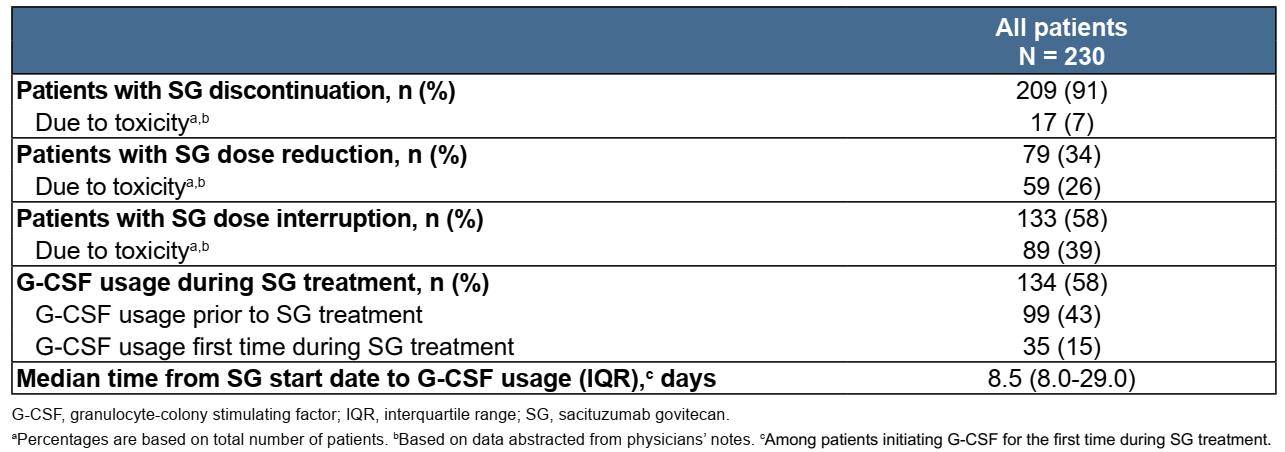
德国RWS证据
2023年9月,Therapeutic Advances in Medical Oncology期刊发表了一项德国埃森米特医院(KEW)中mTNBC患者接受SG治疗的(n=43)小样本RWS结果2。中位随访时间为12.9个月,患者的中位rwPFS和中位rwOS分别为5.0个月和13.1个月。最常报告的任何级别AEs为脱发 (90.7%)、腹泻 (37.2%)、疲乏 (34.9%)、贫血 (34.9%) 和中性粒细胞减少症 (32.6%)。最常见的≥3级 AEs 为中性粒细胞减少 (27.9%) 和腹泻 (18.6%)。39.5%的患者在治疗开始后因药物相关 AE 而降低SG剂量或中断治疗,其中腹泻是主要原因;7.0%的患者停止治疗。本研究未发现新的安全性信号,总体安全特征与IMMU-132研究8和ASCENT研究7的安全性结果相似,但本研究中脱发和腹泻的比例偏高,恶心和呕吐的比例更低。由于本研究的样本量较小且为回顾性分析,因此无法明确脱发的原因。总体而言,来自德国的RWS表明SG在 mTNBC 患者中的安全性和有效性特征与临床试验数据一致。
表3 KEW队列、IMMU-132研究和ASCENT研究中报告的AEs发生率
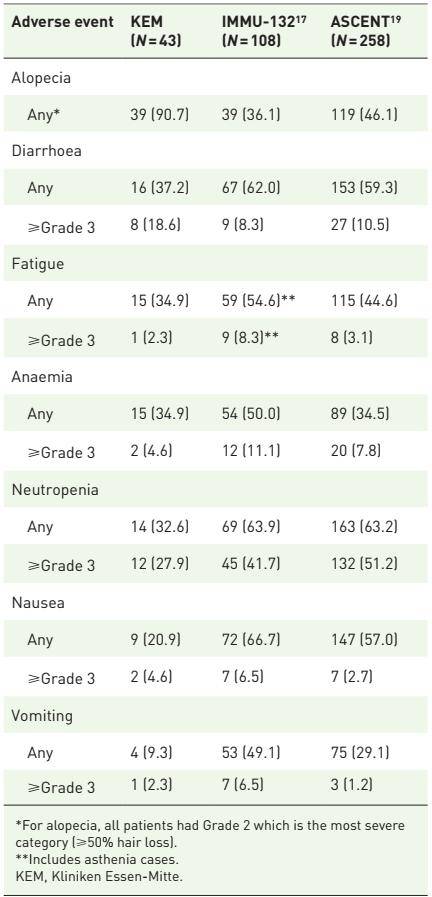
2024年4月,ESMO Open期刊发布了一项德国多中心RWS数据3,分析了SG对伴有稳定和活动性脑转移(BM)mTNBC患者(7例为稳定性,5例为活动性BM)的疗效。患者中位年龄为50.5岁;SG治疗的中位治疗持续时间为71天;中位既往化疗线数为2.5。在 SG 治疗前,11例(92%)患者既往接受过脑部放疗,2例 (17%) 接受过BM手术。在该真实世界分析中,所有患者的中位颅内无进展生存期(icPFS)为2.7个月,中位OS为6.4个月。在ASCENT试验中, SG组脑转移患者的中位PFS为2.8个月,中位OS为6.8个月9。本研究表明 SG在真实世界环境中治疗稳定和活动性 BM 的有效性和安全性与大型Ⅲ期试验相似。在安全性方面,1例患者终止SG治疗,3例患者减少剂量。最常见的AEs是中性粒细胞减少,≥3级AEs 为中性粒细胞减少(33%)和贫血(8%),均可通过预防用药或进行对症处理来缓解。
表4 SG治疗持续时间、疗效和停药原因
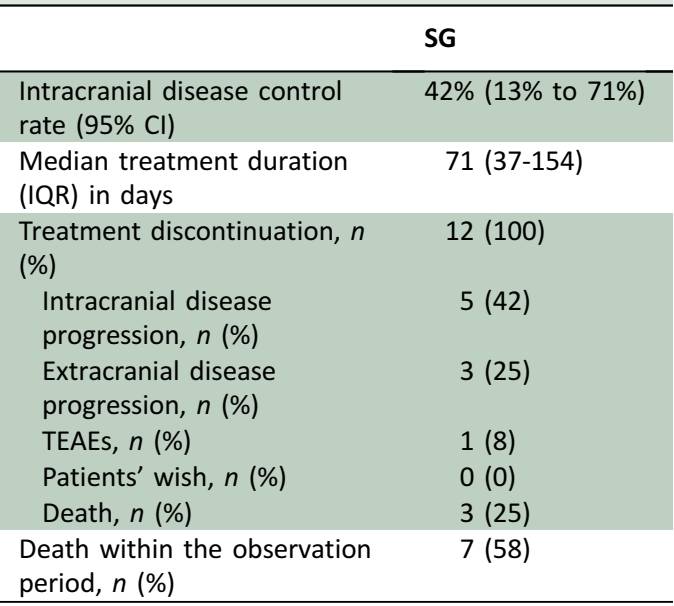
法国RWS证据
2024年4月,Breast Cancer期刊在线发布了法国居里夫人研究所医院99例接受SG治疗的mTNBC患者的前瞻性队列RWS4,其中12%的患者在初次诊断时即为IV期。在中位随访时间9.7个月时,总体人群的中位rwPFS为3.9个月(95%CI:3.4-5.0), 中位rwOS为8.6个月(95%CI:7.1-11.9);在符合ASCENT研究主要分析纳入标准的48例患者中,中位rwPFS为4.4个月(95%CI:3.5-7.0),中位rwOS为10.6个月(95%CI:9.3-NR)。与ASCENT试验中SG组(中位PFS:5.6个月;中位OS:12.1个月)结果相比虽略低,但仍然优于标准化疗组。
本研究中总体人群的生存数据可能受到了一些不良预后因素的影响。首先,17%的患者具有较差的ECOG体能状态(PS≥2),这在ASCENT试验中不符合入选标准。其次,ASCENT研究的主要研究终点为无脑转移人群亚组数据,在脑转移患者的亚组分析中,SG组的中位PFS和OS分别为2.8个月和6.8个月。而法国RWS中31例患者存在脑转移,该人群的中位rwPFS为3.7个月(95%CI:2.6-6.2),中位rwOS为6.7个月(95%CI:6.3-NR),且6例影像学可评估患者的颅内病灶达到部分缓解。这表明,尽管存在不良预后因素,SG治疗在RWS脑转移患者中仍能取得与ASCENT研究相似的抗肿瘤效果。
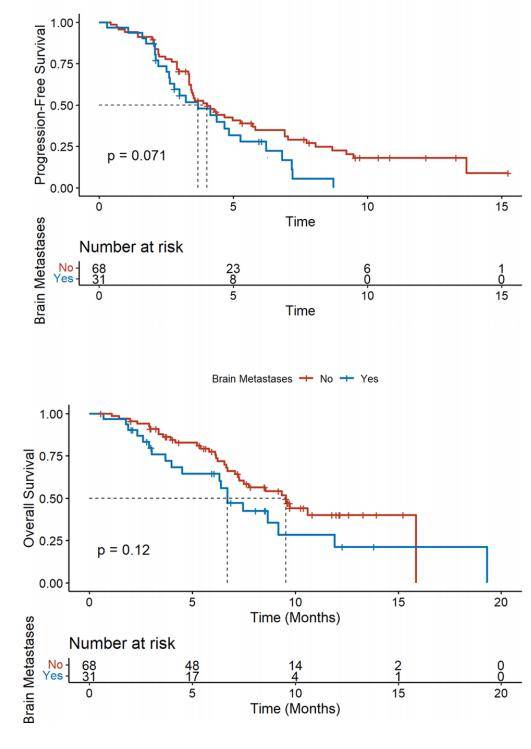
图1 脑转移患者的PFS和OS
在安全性方面,血液学毒性(9例)是主要的限制性毒性,包括中性粒细胞减少(6例)、发热性中性粒细胞减少(2例)和贫血(1例)。胃肠道毒性也相对常见,可能与放射学结肠炎相关。因毒性导致剂量减少和治疗中断的患者比例较低,分别为17%和1%,没有与SG相关的死亡,其安全性特征与ASCENT试验结果相符。此外,研究指出,主要的胃肠道和血液学毒性反应通常可通过预防性或治疗性干预措施以及适时的剂量调整得到有效管理。这一发现为SG在临床应用中的安全性管理提供了进一步的信心。
意大利RWS证据
2024年3月,Frontiers in Oncology期刊上发表了一项意大利的多中心RWS,涉及7个医疗中心的57例mTNBC患者5。与ASCENT研究相比,该研究纳入了更高比例的肺、骨和淋巴结转移患者,且包括了BM人群,这些患者通常预后较差。中位随访10.6个月,患者的中位rwPFS为4.9个月,中位rwOS达12.43个月,与ASCENT研究中包括BM患者群体(n=267)的中位PFS(4.8个月)和OS(11.8个月)的结果相符。
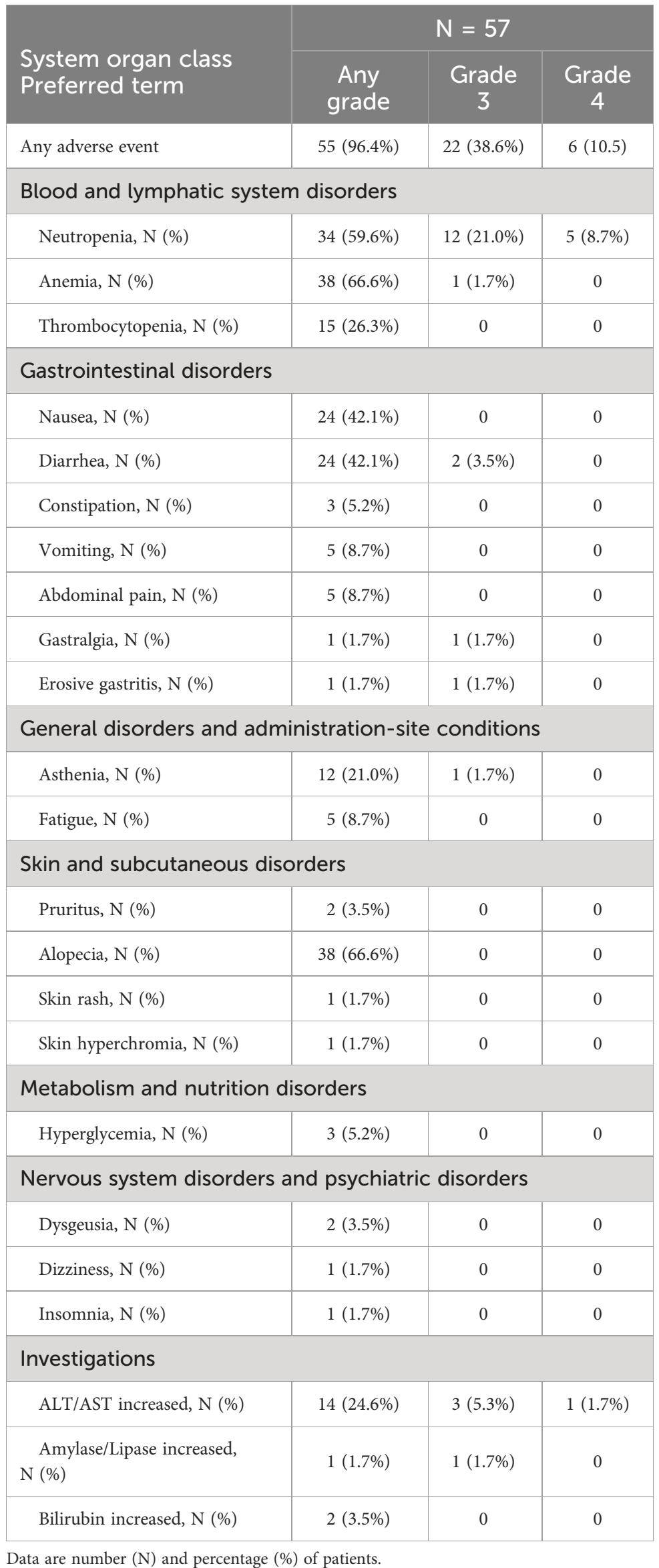
在安全性方面,SG在该意大利研究中表现出了良好的安全性概况,与关键试验的预期一致。报告的最常见的TRAEs包括血液学毒性(贫血67%,中性粒细胞减少60%)、脱发(67%)和胃肠道毒性(恶心42%,腹泻39%)。值得注意的是,胃肠道不良事件的发生率明显低于ASCENT研究,3-4级中性粒细胞减少的发生率也较低(3级:21% vs 34%;4级:9% vs 17%)。这一差异主要归因于预防性用药的广泛使用,这有助于降低SG的血液学毒性和胃肠道毒性的发生率。具体来说,75.4%的患者接受了包括糖皮质激素、5-HT3受体拮抗剂或NK1受体拮抗剂在内的止吐预防措施,26.3%的患者治疗前接受了预防性阿托品治疗,39%的患者治疗过程中接受了减少剂量。这项意大利的RWS结果进一步证实了SG在mTNBC患者中的安全性和疗效,该研究强调了预防用药和支持性措施在管理治疗毒性方面的重要作用。
表5 治疗相关不良事件
备受关注,持续探究
TNBC T-DXd真实世界安全性仍待探索
2024年6月的ASCO年会上,一项T-DXd用于转移性乳腺癌的回顾性研究提供了在mTNBC人群中的RWS证据6。
表6 T-DXd在mTNBC人群中的RWS
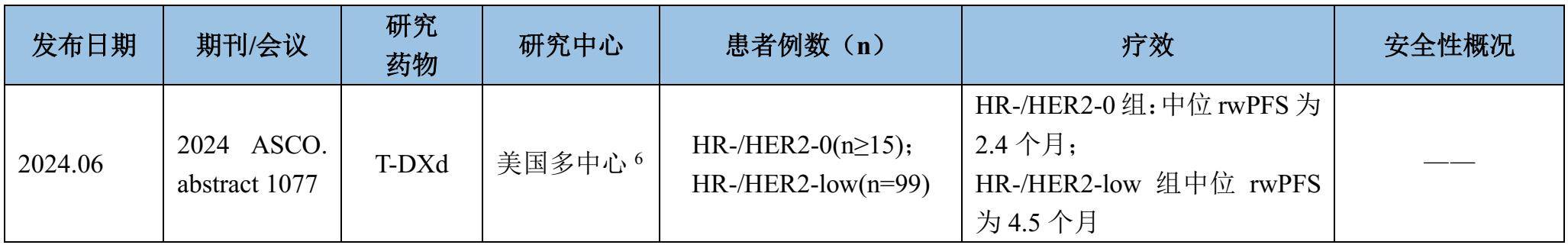
该研究分析了Flatiron Health数据库中美国医疗中心接受T-DXd治疗的患者数据。其中,HR-/HER2-0(IHC 0;n≥15)人群的中位rwPFS 为2.4个月(95%CI:1.8-5.7);HR-/HER2-low(IHC 1+ 或2+未扩增;n=99)人群的中位rwPFS为4.5个月(95%CI:3.8-6.3),低于DESTINY-Breast04研究10中T-DXd治疗HR-/HER2-Low探索性亚组的PFS结果(6.3个月)。
此外,该研究并未报告T-DXd的安全性结果。通过这项研究,我们对T-DXd在特定mTNBC患者群体中的应用有了更深入的了解,同时也凸显了对真实世界安全性数据的需求,以便更全面地评估T-DXd在mTNBC临床治疗中的潜力和价值。
小结
在mTNBC的治疗领域,来自多个国家的真实世界研究一致表明,SG在多样化的患者群体中展现了良好的耐受性和显著的生存益处,其中,SG常见的中性粒细胞减少和腹泻等AEs,临床中处理经验较为丰富,可通过相关预防性用药,明显降低其发生率和严重程度。对于T-DXd及其他新型ADC药物如SKB264和Dato-DXd,我们仍需更多的RWS数据来全面评估其安全性。总之,ADC药物在TNBC治疗中的应用前景广阔,但安全性管理仍需依赖于持续的临床研究和实践积累。随着更多数据的涌现,我们期待为mTNBC患者提供更为精准和安全的治疗策略。
1. Kevin Kalinsky, et al. 2023ESMO. abstract 393P.
2. Reinisch M, et al. Ther Adv Med Oncol. 2023;15:17588359231200454.
3. Dannehl D, et al. ESMO Open. 2024;9(5):102995.
4. Alexandre De Moura, et al. Breast Cancer. 2024 Apr 10.
5. Caputo R, et al. Front Oncol. 2024;14:1362641.
6. Paolo Tarantino, et al. 2024 ASCO. abstract 1077.
7. Bardia A, et al. N Engl J Med. 2021;384(16):1529-1541.
8. Bardia A, et al. N Engl J Med 2019; 380: 741–751.
9. Véronique Diéras, et al. 2021 SABCS. Abstract PD13-07.
10. Shanu Modi, et al. 2023 ESMO. abstract 376O.
排版编辑:肿瘤资讯-老猫











 苏公网安备32059002004080号
苏公网安备32059002004080号


