2024 美国癌症研究协会(AACR)大会日前在美国加州圣地亚哥顺利召开并圆满落幕。在肺癌治疗领域,令人关注的HER2(ERBB2)ADC德曲妥珠单抗(DS-8201,T-DXd)临床研究结果再次惊艳亮相国际舞台,程颖教授首次重磅公布中国人群DESTINY-Lung05研究结果。德曲妥珠单抗(DS-8201,T-DXd)是目前为止肺癌领域首个且唯一获得FDA批准的HER2(ERBB2)ADC,CDE官网显示德曲妥珠单抗(DS-8201,T-DXd)已被纳入优先评审,此次中国研究数据的公布将为中国人群的未来应用提供证据和支持。【肿瘤资讯】特邀哈尔滨医科大学附属肿瘤医院于雁教授解读DESTINY-Lung05研究数据亮点及研究意义。
本期特邀专家—于 雁 教授
哈尔滨医科大学附属肿瘤医院 内科教研室主任 博士生导师
中国临床肿瘤学会 (csco) 理事
黑龙江省抗癌协会常务理事
黑龙江省医学发展基金理事
黑龙江省医学会理事会理事
中国抗癌协会化疗专业委会常委中国临床
中国临床肿瘤学会肿瘤支持与康复治疗委会常委
中国医促进会肿瘤肿瘤舒缓治疗学分会常委
中国医药教育协会肺部肿瘤专业委员会常委
中国抗癌协会癌症康复与姑息治疗委员会常委
中国抗癌协会肺癌专业委员会委员
中国抗癌协会肿瘤异质性与个体化治疗专委会常委
黑龙江省医师协会肺癌专业委员会主任委员
黑龙江省医学会癌症姑息息治疗委员会主任委员
黑龙江省抗癌协会癌症康复与姑息治疗专业委员会主任委员
黑龙江省抗癌协会肿瘤药物临床研究专委会候任主任委员
中华转移性肿瘤杂志编委中国肿瘤临床与康复杂志编委
研发历程坎坷,化疗、免疫疗法、TKI等药物在HER2(ERBB2)突变肺癌患者中疗效不佳
随着精准治疗时代的到来和基因检测技术的普及和广泛应用,HER2(ERBB2)突变晚期非小细胞肺癌(NSCLC)的治疗日益受到临床医生的广泛关注。然而令人遗憾的是,临床常见化疗方案、免疫疗法在HER2(ERBB2)突变晚期NSCLC患者中疗效不佳。研究显示,HER2(ERBB2)突变NSCLC患者从培美曲塞治疗中的获益低于ALK/ROS1融合患者,中位无进展生存期(PFS)分别为5.1 vs 9.2个月(P=0.004)[1]。虽然免疫治疗在经治晚期NSCLC患者总体人群中的疗效优于化疗,但HER2(ERBB2)突变患者并不能从免疫单药中获益,有研究显示,HER2(ERBB2)突变接受免疫单药的ORR为7%,远低于KRAS、BRAF、ROS1和EGFR变异患者[2]。大分子特异性抗体例如曲妥珠单抗在乳腺癌患者中疗效优,但在HER2(ERBB2)突变晚期NSCLC患者中显示出较低的临床疗效,约为10%;曲妥珠单抗+帕妥珠单抗+多西他赛治疗HER2(ERBB2)突变晚期NSCLC的疗效也不理想,有效率约为29%[1]。总体而言,临床上多种治疗方案难以满足治疗需求,亟需开发新型的治疗策略。
研究者一直也在不断探索其他疗法在HER2(ERBB2)突变肺癌治疗领域的价值,例如探索及开发了新型的小分子TKI药物,包括非选择性酪氨酸激酶抑制剂:阿法替尼、达可替尼、奈拉替尼等,以及选择性HER2(ERBB2)酪氨酸激酶抑制剂Poziotinib、吡咯替尼等,以期进一步改善HER2(ERBB2)突变晚期NSCLC患者的疗效。
阿法替尼已被批准治疗EGFR突变转移性NSCLC,但其在HER2(ERBB2)突变患者中的疗效令人失望。临床前研究虽然显示出有希望的疗效,但NICHE临床试验显示,阿法替尼治疗化疗进展后HER2(ERBB2)突变NSCLC患者的客观缓解率(ORR)仅为8%,中位PFS为15.9周 [3] ,目前无有力证据支持阿法替尼单药或联合治疗策略在HER2(ERBB2)突变晚期NSCLC患者中的疗效。达可替尼在EGFR敏感突变晚期NSCLC患者中具有良好疗效,在一项多中心II期临床研究中,达可替尼治疗HER2(ERBB2)突变和HER2(ERBB2)扩增患者的ORR分别为12%和0%[4]。临床前研究显示,奈拉替尼加入mTOR抑制剂在肺腺癌肿瘤细胞中具有协同作用,显示良好的抗肿瘤活性,但临床试验显示,奈拉替尼单药对HER2(ERBB2)突变NSCLC患者几乎无效,PUMA-NER-4201研究中奈拉替尼联合temsirolimus在HER2(ERBB2)突变患者中显示一般的疗效,ORR为19%[5]。吡咯替尼是一种不可逆的EGFR/HER2(ERBB2)/HER4受体小分子抑制剂,在一项II期多中心、前瞻性临床研究中,吡咯替尼治疗HER2(ERBB2)突变晚期NSCLC患者的ORR为30%,中位PFS为6.9个月[6],在另一项吡咯替尼一线或后线治疗HER2(ERBB2)突变晚期NSCLC患者的II期临床研究中,ORR为19.2%,中位PFS为5.6个月。目前有III期研究正在进行中。Poziotinib也是一种不可逆的新型EGFR/HER2(ERBB2)受体抑制剂,在ZENITH20-2试验中,Poziotinib治疗HER2(ERBB2)突变晚期NSCLC患者的ORR为27.8%,中位PFS为5.5个月[7]。安全性方面有78.9%的患者发生3级TRAE,后续开展的ZENITH20-4研究进一步验证了疗效和安全性,结果显示疗效一致,安全性结果显示有近70%的患者发生≥3级TRAE。
总体而言,大部分小分子TKI类药物在HER2(ERBB2)突变晚期NSCLC患者中疗效不佳。吡咯替尼在此类患者中的疗效和安全性值得进一步验证,而Poziotinib的安全性问题可能是限制临床研究继续开展和临床应用的主要原因。
德曲妥珠单抗(DS-8201,T-DXd)成功破局,开启HER2(ERBB2)突变晚期NSCLC治疗新时代
临床常见治疗方案在HER2(ERBB2)突变晚期NSCLC疗效不佳,而相关靶向疗法的探索也历经坎坷。与此同时ADC药物的研发也在不断优化中,截至目前ADC药物的研发已历经了约100年的时间,HER2(ERBB2)ADC一直引领着ADC药物在肺癌治疗领域不断前行、展露锋芒,并取得了后续的重大突破。
早期开展的转化研究显示,HER2(ERBB2)突变 NSCLC会优先内化HER2(ERBB2)抗体的偶联复合物,并可克服其他HER2(ERBB2)靶向药物的耐药性,这支持德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变患者人群中进一步的临床开发和验证。首次人体临床试验结果显示,德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变 NSCLC患者中的ORR达到72.7%,显示出初步良好的抗肿瘤活性[8]。后续进一步开展的DESTINY-Lung01、DESTINY-Lung02再次验证了德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变晚期NSCLC后线治疗的卓越疗效。在JCO杂志在线发表的DESTINY-Lung02最新结果中[9],基线特征显示有近40%的患者接受了两线以上的治疗,德曲妥珠单抗(DS-8201,T-DXd)在5.4mg/kg和6.4mg/kg的总体ORR为49%和56%,疾病控制率(DCR)分别为93.1%和92%(表1)。两剂量组的不良事件在临床上可控,安全性良好,而5.4mg/kg组的安全性更优。
表1 DESTINY-Lung02研究疗效分析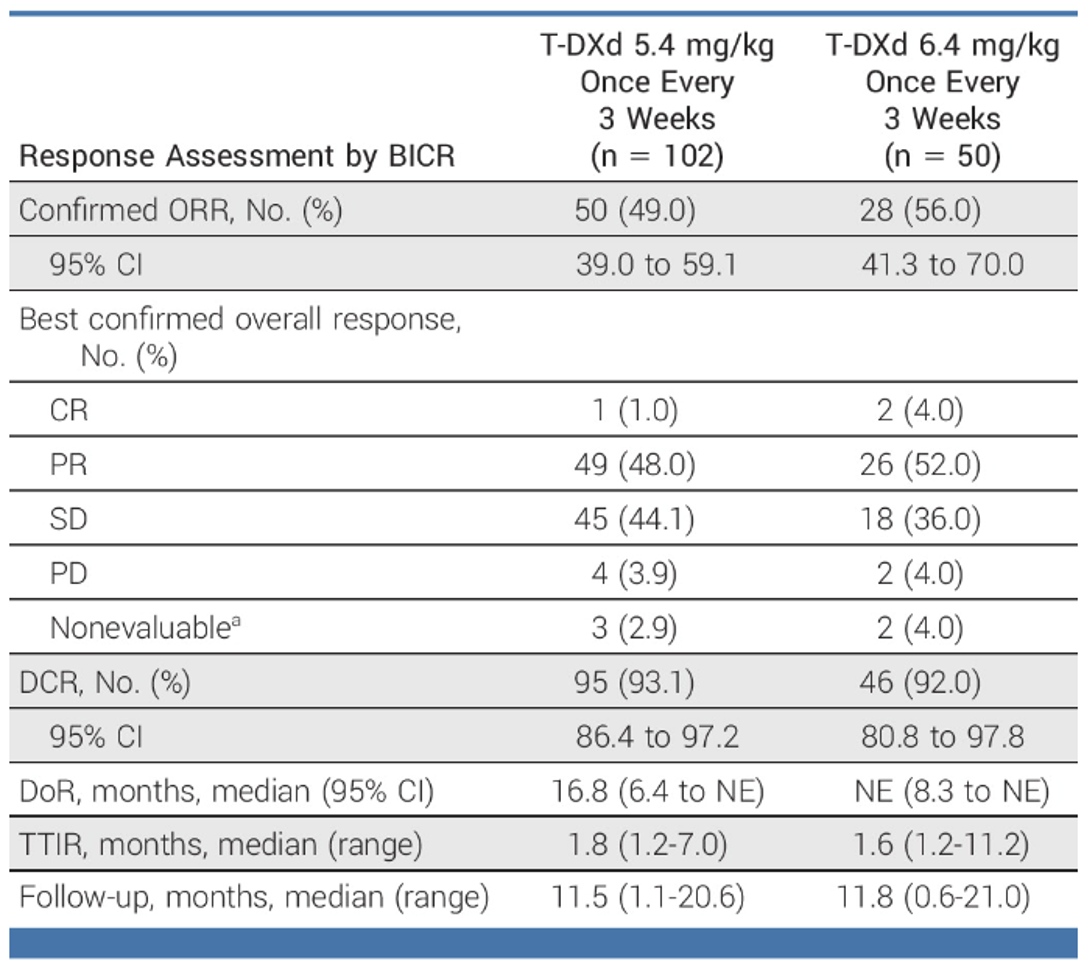
值得指出的是,2023 ESMO大会上公布的DESTINY-Lung01和DESTINY-Lung02汇总分析结果提示[10],5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)颅内疗效更优。结果显示,5.4mg/kg和6.4mg/kg组患者确认的颅内ORR(IC-cORR)分别为50%和30%,颅内疾病控制率(IC-DCR)分别为92.9%和73.3%(表2),中位颅内缓解持续时间(IC-DOR)分别为9.5个月和4.4个月。总体而言,两剂量组德曲妥珠单抗(DS-8201,T-DXd)在伴脑转移HER2(ERBB2)突变转移性NSCLC患者中均具有良好的颅内活性。
表2 DESTINY-Lung01/DESTINY-Lung02汇总分析疗效结果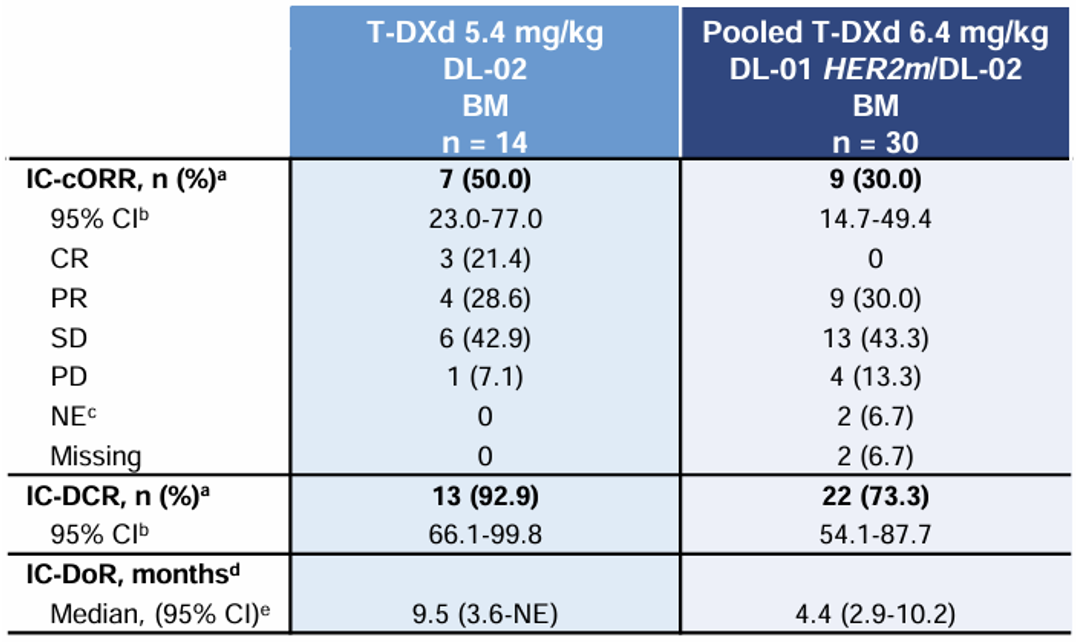
基于HER2(ERBB2)ADC药物研发的成功以及取得的系列研究成果,令人欣喜的是,HER2(ERBB2)突变晚期NSCLC领域于2022年终于迎来FDA批准的首个靶向疗法、首个且目前唯一的ADC药物——德曲妥珠单抗(DS-8201,T-DXd),自此HER2(ERBB2)突变NSCLC正式进入ADC药物治疗的新时代。
德曲妥珠单抗(DS-8201,T-DXd)之所以能在该领域取得重大突破,离不开它结构上将化疗和靶向疗法集于一身,经过结构优化后最大限度的避免了化疗的全身毒性,呈现出高效低毒的特点。作为一种新型ADC药物,德曲妥珠单抗(DS-8201,T-DXd)由基于四肽的可裂解接头将曲妥珠单抗与拓扑异构酶I抑制剂DXd偶联而成。DXd是高活性细胞毒载药,其抗肿瘤活性是化疗的约1000倍。连接子为蛋白酶可切割连接子,内化后被肿瘤细胞中过表达的肽酶选择性裂解而释放高效细胞毒药物,这种连接子可在血浆中可保持稳定,能避免载药过早脱落造成的毒性。德曲妥珠单抗(DS-8201,T-DXd)优化的药物抗体比率(DAR)为8,即每个抗体与约8个细胞毒药物连接,可增强抗肿瘤疗效。另外,德曲妥珠单抗(DS-8201,T-DXd)具有旁观者效应,可渗透细胞膜,杀伤临近肿瘤细胞,进一步增强抗肿瘤活性。
DESTINY-Lung05登陆2024 AACR,为德曲妥珠单抗(DS-8201,T-DXd)未来在中国人群中的应用提供依据
德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突变晚期NSCLC患者中的卓越疗效已在DESTINY-Lung01、DESTINY-Lung02等研究中得到证实,更新结果多次在国际学术舞台上惊艳亮相,且得到国内外肺癌领域专家的广泛认同和共同期待。基于前期取得的成果,为进一步验证德曲妥珠单抗(DS-8201,T-DXd)在中国人群中的疗效,由吉林省肿瘤医院程颖教授牵头在中国30多家中心开展了中国桥接研究——DESTINY-Lung05[11],这是一项开放标签、单臂、II期临床研究,旨在评估德曲妥珠单抗(DS-8201,T-DXd)用于至少一线治疗期间或治疗进展后HER2(ERBB2)突变转移性NSCLC中国患者的疗效和安全性。关键入组标准包括病理学确认的非鳞状转移性NSCLC患者、至少接受过一种抗肿瘤全身治疗、经FFPE肿瘤组织检测为HER2(ERBB2)突变、WHO或ECOG评分为0或1、按RECIST 1.1标准经研究者至少有一个可测量病灶。主要终点经ICR评估确认的ORR,次要终点包括由研究者评估确认的ORR、以及ICR和研究者评估的DOR、DCR、PFS。
2024 AACR大会上公布的结果显示,截至2023年9月23日数据分析时,中位随访时间为9.8个月,72例HER2(ERBB2)突突转移性NSCLC患者至少接受1剂5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)治疗(全分析人群)。基线特征显示,分别有58.3%、41.7%的患者既往接受过2线及以上、1线治疗。分别有93.1%、90.3%、68.1%、68.1%的患者既往接受过细胞毒化疗、含铂化疗、免疫治疗、抗血管生成药物(表3)。
表3 DESTINY-Lung05研究基线特征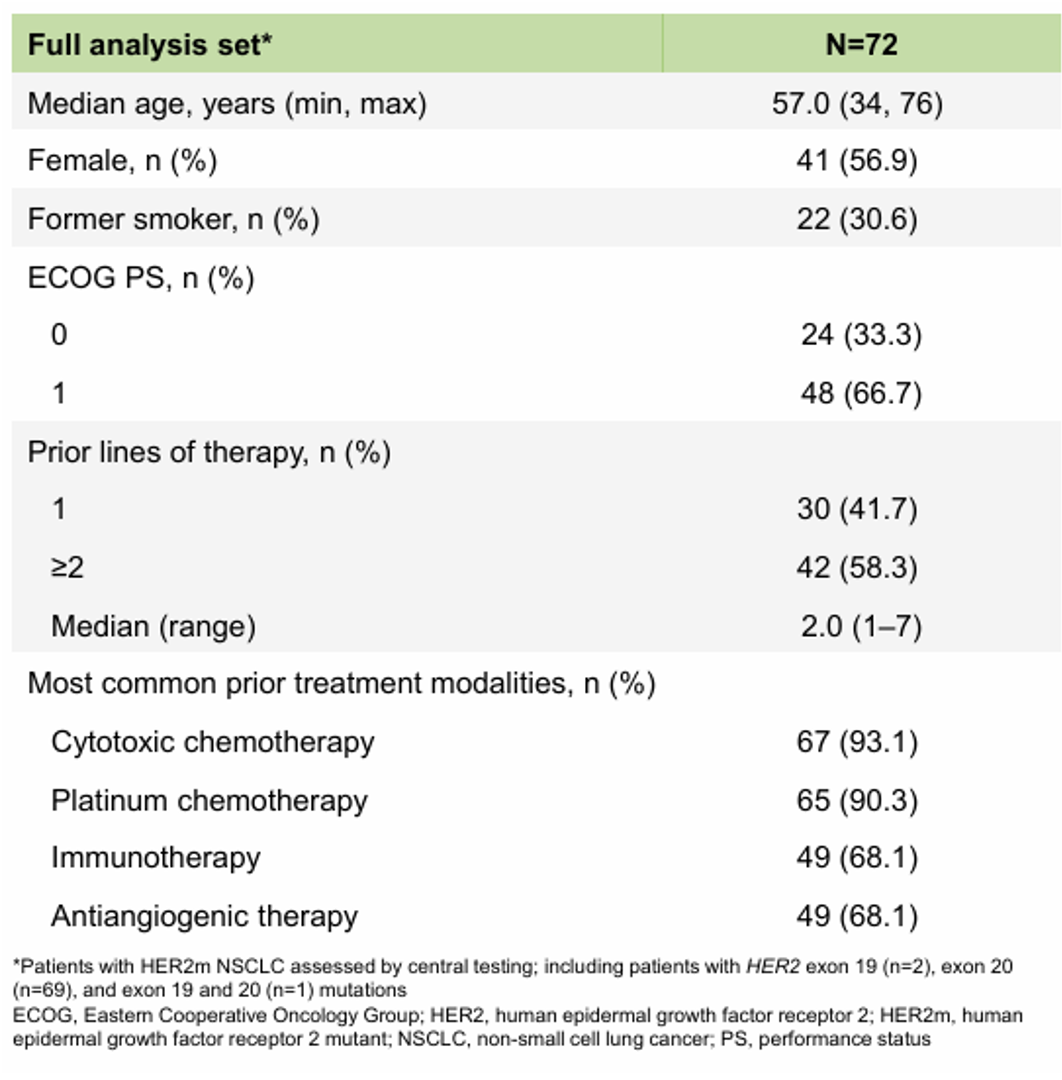
疗效分析显示,中位随访9.8个月时,由ICR评估确认的ORR为58.3%,其中1.4%的患者达到完全缓解,56.9%的患者达到部分缓解,中位DOR未达到,DCR为91.7%(表4,图1),中位PFS未达到,12个月PFS率为55.1%。由研究者评估确认的ORR为58.3%,中位DOR为9个月,DCR为93.1%,中位PFS为10.8个月,12个月PFS率为39.7%。
表4 由ICR评估患者的最佳缓解
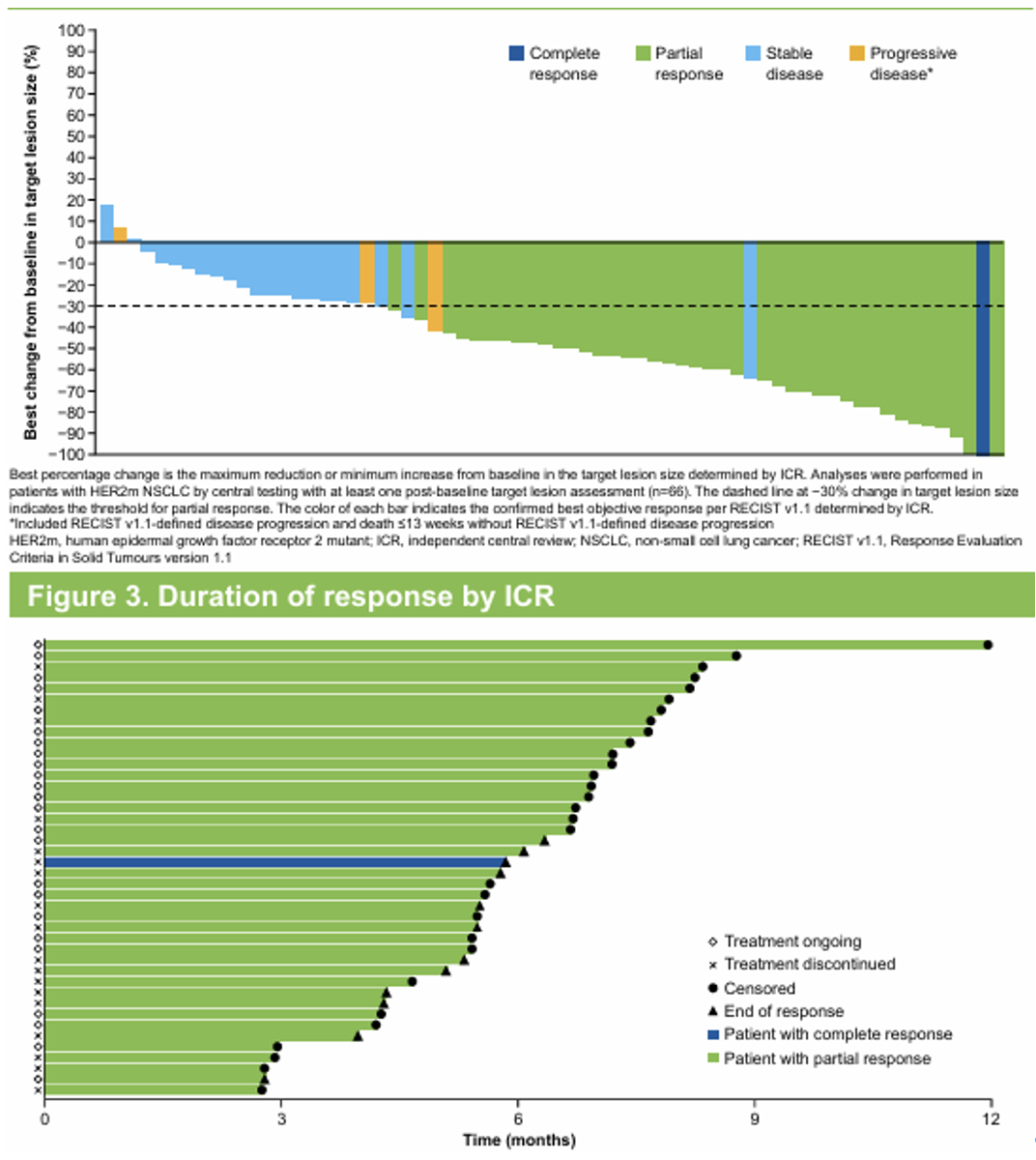 图1 由ICR评估患者的最佳靶病灶变化和DOR
图1 由ICR评估患者的最佳靶病灶变化和DOR
安全性结果显示,德曲妥珠单抗(DS-8201,T-DXd)的中位暴露时间为7.9个月,3级及以上药物相关不良事件(AE)发生率为51.4%,无5级药物相关AE发生。最常见(≥5%)药物相关≥3级AE为中性粒细胞减少症(26.4%)、血小板减少症(18.1%)和白细胞减少症(11.1%)和淋巴细胞减少症(6.9%)。药物相关AE导致2.8%的患者停药,经中心评估任意级别药物相关ILD/肺炎发生率为9.7%,其中大部分为2级事件。
总体而言,5.4mg/kg德曲妥珠单抗(DS-8201,T-DXd)在HER2(ERBB2)突突转移性NSCLC中国人群中显示出有临床意义和持久的缓解,以及可控的安全性特征。疗效结果与DESTINY-Lung02研究一致,安全性特征也与德曲妥珠单抗(DS-8201,T-DXd)已知安全性类似,研究结果支持在中国人群中使用德曲妥珠单抗(DS-8201,T-DXd)。
结语:
随着肺癌精准治疗时代的发展和推进,HER2(ERBB2)突变晚期NSCLC患者的治疗不断被关注,面对临床上多种常用治疗手段疗效不佳的困境,研究者将新型ADC药物引入HER2(ERBB2)突变肺癌的治疗中,经过了早期转化研究和多项临床研究的证实,德曲妥珠单抗(DS-8201,T-DXd)突破疗效困境,成为肺癌领域经FDA批准的目前首个且唯一的HER2(ERBB2)ADC,为此类患者带来了新希望,有望成为新的选择。今年AACR大会上首次公布德曲妥珠单抗(DS-8201,T-DXd)中国研究数据,这为HER2(ERBB2)突变晚期中国人群的治疗和应用提供了循证医学证据和参考数据,期待未来更多临床研究结果的公布。
J[1]Ren S, Wang J, Ying J, et al. Consensus for HER2 alterations testing in non-small-cell lung cancer. ESMO Open. 2022 Feb;7(1):100395. doi: 10.1016/j.esmoop.2022.100395. Epub 2022 Feb 8. Erratum in: ESMO Open. 2022 Jun;7(3):100482. PMID: 35149428; PMCID: PMC8844658.
[2]Mazieres J, Drilon A, Lusque A, et al. Immune checkpoint inhibitors for patients with advanced lung cancer and oncogenic driver alterations: results from the IMMUNOTARGET registry. Ann Oncol. 2019 Aug 1;30(8):1321-1328. doi: 10.1093/annonc/mdz167. PMID: 31125062; PMCID: PMC7389252.
[3]Dziadziuszko, R. Smit, E.F. Dafni, U.et al. Afatinib in NSCLC with HER2Mutations: Results of the Prospective, Open-Label Phase II NICHE Trial of European Thoracic Oncology Platform (ETOP). J. Thorac. Oncol. 2019, 14, 1086–1094.
[4]Kris, M.G. Camidge, D.R. Giaccone, G.et al.Targeting HER2 aberrations as actionable drivers in lung cancers: Phase II trial of the pan-HER tyrosine kinase inhibitor dacomitinib in patients with HER2-mutant or amplified tumors. Ann. Oncol. 2015, 26, 1421–1427.
[5]Gandhi, L.Besse, B.; Mazieres, et al. Neratinib ± Temsirolimus in HER2-Mutant Lung Cancers: An International, Randomized Phase II Study. J. Thorac. Oncol. 2017, 12, S358–S359.
[6]Zhou C, Li X,Wang Q. et al. Pyrotinib in HER2-Mutant Advanced Lung Adenocarcinoma After Platinum-Based Chemotherapy: A Multicenter, Open-Label, Single-Arm.Phase II Study JCO. 2020; 38: 2753-2761
[7]Le X, Cornelissen R,Garassino M, et al.Poziotinib in Non–Small-Cell Lung Cancer Harboring HER2 Exon 20 Insertion Mutations After Prior Therapies: ZENITH20-2 Trial.JCO. 2022; 40: 710-718
[8]Li BT, Michelini F, Misale S, et al. HER2-Mediated Internalization of Cytotoxic Agents in ERBB2 Amplified or Mutant Lung Cancers. Cancer Discov. 2020 May;10(5):674-687. doi: 10.1158/2159-8290.CD-20-0215. Epub 2020 Mar 25. PMID: 32213539; PMCID: PMC7196485.
[9] Goto K, Goto Y, Kubo T, et al. Trastuzumab Deruxtecan in Patients With HER2-Mutant Metastatic Non-Small-Cell Lung Cancer: Primary Results From the Randomized, Phase II DESTINY-Lung02 Trial. J Clin Oncol. 2023 Nov 1;41(31):4852-4863. doi: 10.1200/JCO.23.01361. Epub 2023 Sep 11. Erratum in: J Clin Oncol. 2024 Feb 1;42(4):485. PMID: 37694347; PMCID: PMC10617843.
[10] Li BT, et al. Trastuzumab deruxtecan (T-DXd) in patients (pts) with HER2(ERBB2)-mutant (HER2m) metastatic nonesmall cell lung cancer (NSCLC) with and without brain metastases (BMs):Pooled analyses from DESTINY-Lung01 and DESTINYLung02. 2023 ESMO 1321MO.
[11]Trastuzumab deruxtecan (T-DXd) in Chinese patients (pts) with previously treated HER2 mutant non-small cell lung cancer (NSCLC): primary analysis from the Phase 2 DESTINY-Lung05 (DL-05) trial. Abstract CT248/7,2024 AACR.
排版编辑:肿瘤资讯-Rex











 苏公网安备32059002004080号
苏公网安备32059002004080号


