肝细胞癌(HCC)作为原发性肝癌中最常见的类型,仍在全球范围内带来重大的临床挑战。EZH2作为多梳抑制复合体2(PRC2)的核心组分,通过其SET结构域具有组蛋白甲基转移酶活性,并在多种癌症中频繁过表达。然而,EZH2在HCC中的确切作用及调控机制仍不明确。本研究旨在通过整合TCGA数据库的转录组学、甲基化及临床数据,系统评估EZH2表达及其阶段依赖性甲基化模式在HCC预后预测中的价值,并探索其调控免疫极化和代谢重编程的潜在机制。
研究背景
HCC是全球范围内最常见的原发性肝脏恶性肿瘤,约占所有肝癌病例的90%,其发病率和死亡率均位居全球前列。尽管近年来在手术切除、肝移植、局部消融及系统性治疗(包括多激酶抑制剂和免疫检查点抑制剂)方面取得显著进展,但由于多数患者确诊时已属晚期,总体预后仍然较差。因此,探索HCC发生发展的分子机制并寻找可靠的预后生物标志物,对于改善患者个体化治疗策略具有重要意义。
EZH2作为PRC2的核心催化亚基,通过其SET结构域介导组蛋白H3第27位赖氨酸三甲基化(H3K27me3),从而在基因沉默和染色质重塑中发挥关键作用。近年研究发现,EZH2在多种实体瘤中呈过表达状态,与肿瘤恶性进展、转移及不良预后密切相关。在HCC中,EZH2不仅可通过表观遗传修饰抑制抑癌基因(如p21、p16、KLF2)表达,还能调控非组蛋白(如STAT3、NF-κB)活性,促进肿瘤细胞上皮-间质转化(EMT)和侵袭转移。此外,EZH2在肿瘤微环境(TME)重塑中的作用日益受到关注,其可通过抑制抗原呈递分子表达、增强调节性T细胞(Treg)活性并招募髓源性抑制细胞(MDSC)和肿瘤相关巨噬细胞(TAMs),协助肿瘤细胞实现免疫逃逸。
尽管EZH2在HCC中的致癌作用已初现端倪,但其表达调控的表观遗传机制及其与肿瘤进展阶段相关的动态变化尚不明确。DNA甲基化作为重要的表观遗传修饰,在基因表达调控和肿瘤异质性中扮演关键角色。启动子区CpG岛高甲基化通常导致基因转录沉默,而基因体区甲基化则可能与转录激活相关。然而,EZH2基因在HCC不同阶段的甲基化模式及其临床意义仍有待深入解析。本研究旨在通过整合TCGA数据库的转录组学、甲基化及临床数据,系统评估EZH2表达及其阶段依赖性甲基化模式在HCC预后预测中的价值,并探索其调控免疫极化和代谢重编程的潜在机制。
研究方法
患者队列与数据来源 本研究纳入来自癌症基因组图谱(TCGA)数据库的肝脏肝细胞癌(LIHC)队列,共包含421例具有完整临床信息及mRNA表达谱的HCC患者样本。所有数据均通过GDC数据门户获取。患者平均年龄为59.2岁,男性占68.4%。根据组织学分级,将患者分为早期组(Grade 1-2,n=235)和晚期组(Grade 3-4,n=137),以反映肿瘤分化程度随疾病进展的动态变化。
EZH2表达与生存分析 利用UALCAN在线分析平台评估EZH2在HCC肿瘤组织与正常肝组织中的mRNA表达差异,采用转录本每百万(TPM)值进行定量。通过人类蛋白质图谱(HPA)获取EZH2蛋白水平的免疫组化(IHC)染色数据。根据EZH2表达量上四分位数将患者分为高表达组(TPM>上四分位,n=88)和低/中表达组(TPM≤上四分位,n=333),采用Kaplan-Meier法绘制总生存期(OS)曲线。为进一步验证EZH2的独立预后价值,采用多变量Cox比例风险回归模型校正年龄、性别、肿瘤分级等混杂因素,计算风险比(HR)及95%置信区间(CI)。
肿瘤浸润免疫细胞评估 通过TIMER数据库分析EZH2表达与肿瘤纯度及六种免疫细胞浸润水平的相关性,包括B细胞、CD8+ T细胞、CD4+ T细胞、巨噬细胞、中性粒细胞和树突状细胞(DCs)。采用Pearson相关分析计算相关系数(r)及其统计学意义。
DNA甲基化分析 从UALCAN数据库和UCSC Xena平台获取EZH2基因甲基化数据。分析涵盖启动子区、5'非翻译区(5'UTR)及基因体区的9个CpG位点。甲基化水平以β值表示(0=完全未甲基化,1=完全甲基化)。根据甲基化水平上四分位数将患者分为高甲基化组(β值>上四分位)和低甲基化组(β值≤上四分位)。针对早期和晚期HCC分别进行生存分析,识别具有阶段特异性预后价值的CpG位点。
基因集富集与通路分析 采用基因集富集分析(GSEA)软件(v4.3.2)评估与cg08558971和cg18416251甲基化状态相关的信号通路。设置1,000次基因集置换以获得稳健统计量,错误发现率(FDR)<0.05视为显著。利用R软件clusterProfiler包进行基因本体论(GO)和京都基因与基因组百科全书(KEGG)通路富集分析,筛选两种相反甲基化模式下的共同差异表达基因:模式1为早期高甲基化cg08558971合并晚期低甲基化cg18416251;模式2为早期低甲基化cg08558971合并晚期高甲基化cg18416251。
统计学处理 所有统计分析均在R软件(v4.4.1)中完成,采用survminer、forestplot、ggplot2等包进行可视化。两组间比较采用Student's t检验或Wilcoxon秩和检验,相关性分析采用Pearson法。生存分析采用log-rank检验。双侧P < 0.05为差异有统计学意义。
研究结果
EZH2高表达与HCC不良预后及免疫细胞浸润相关
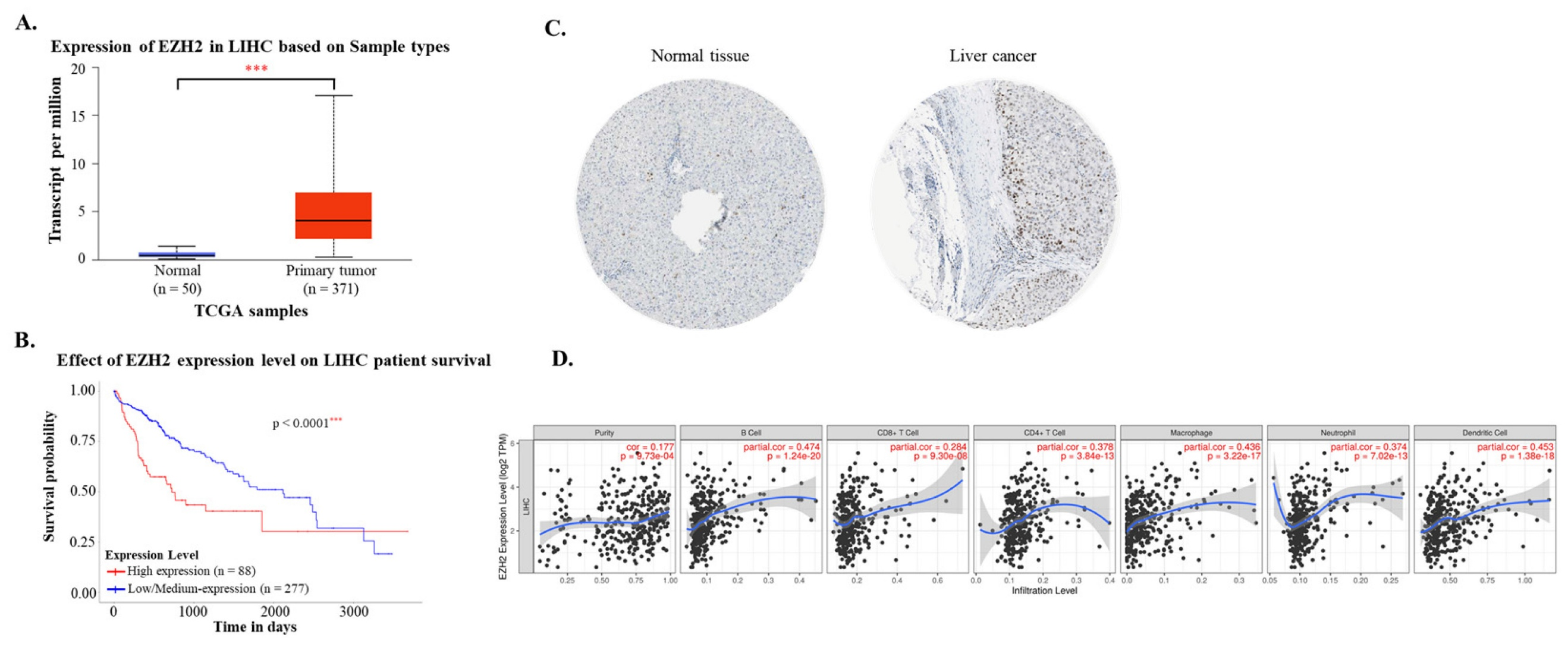
UALCAN数据库分析显示,EZH2 mRNA在HCC肿瘤组织中的表达显著高于正常肝组织(P < 0.001)。HPA的IHC数据进一步证实EZH2蛋白在肿瘤组织中呈强阳性染色。生存分析表明,EZH2高表达组患者的OS显著低于低/中表达组(P < 0.0001)。多变量Cox回归分析校正混杂因素后,EZH2高表达仍为HCC患者不良OS的独立预测因子(HR=1.86,95%CI 1.30~2.67,P = 0.0007)。
TIMER数据库分析揭示EZH2表达与肿瘤纯度(r = 0.177,P = 9.73×10-4)及多种免疫细胞浸润水平呈显著正相关,包括B细胞(r = 0.474,P = 1.24×10-20)、CD8+ T细胞(r = 0.284,P = 9.3×10-8)、CD4+ T细胞(r = 0.378,P = 3.84×10-13)、巨噬细胞(r = 0.436,P = 3.22×10-17)、中性粒细胞(r = 0.374,P = 7.02×10-13)和DCs(r = 0.453,P = 1.38×10-18),提示EZH2可能通过调控肿瘤免疫微环境促进HCC进展。
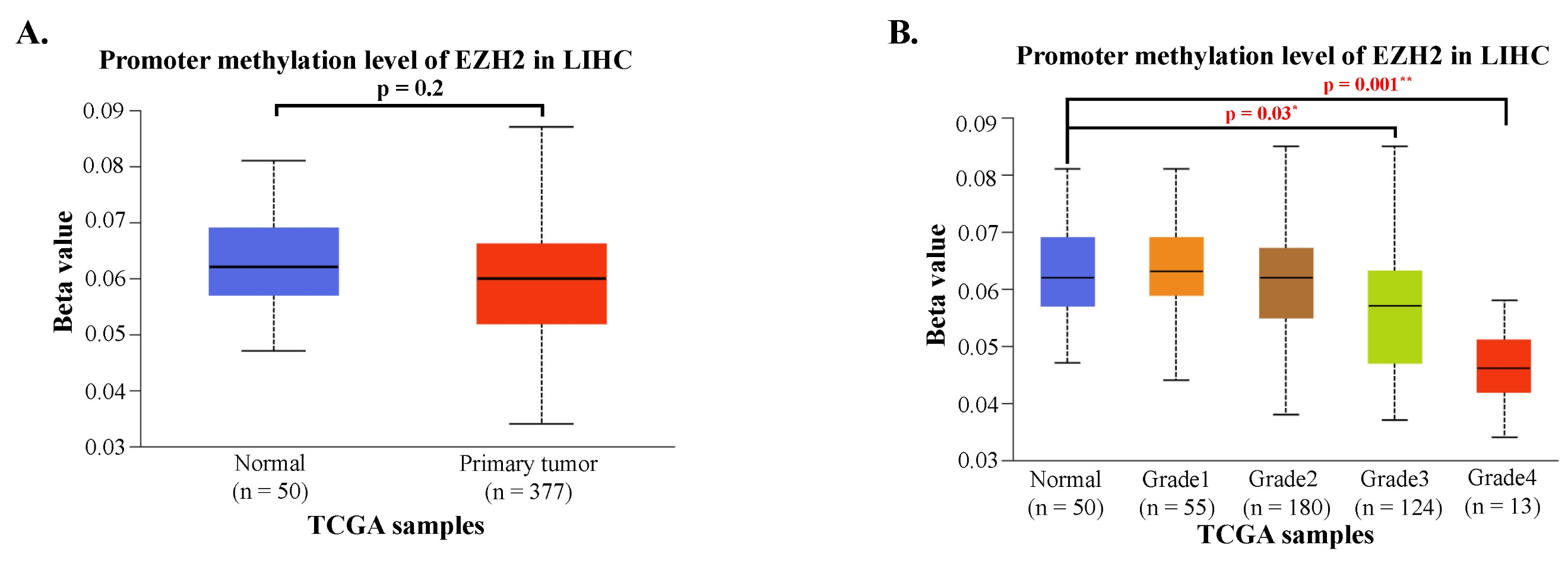
EZH2启动子甲基化在晚期HCC中显著降低
尽管EZH2启动子区总体甲基化水平在肿瘤与正常组织间差异无统计学意义(P = 0.2),但按肿瘤分级分层后,晚期HCC(Grade 3-4)的启动子甲基化水平较正常组织显著下降(P = 0.001),表明启动子去甲基化可能介导了晚期HCC中EZH2的表达上调。
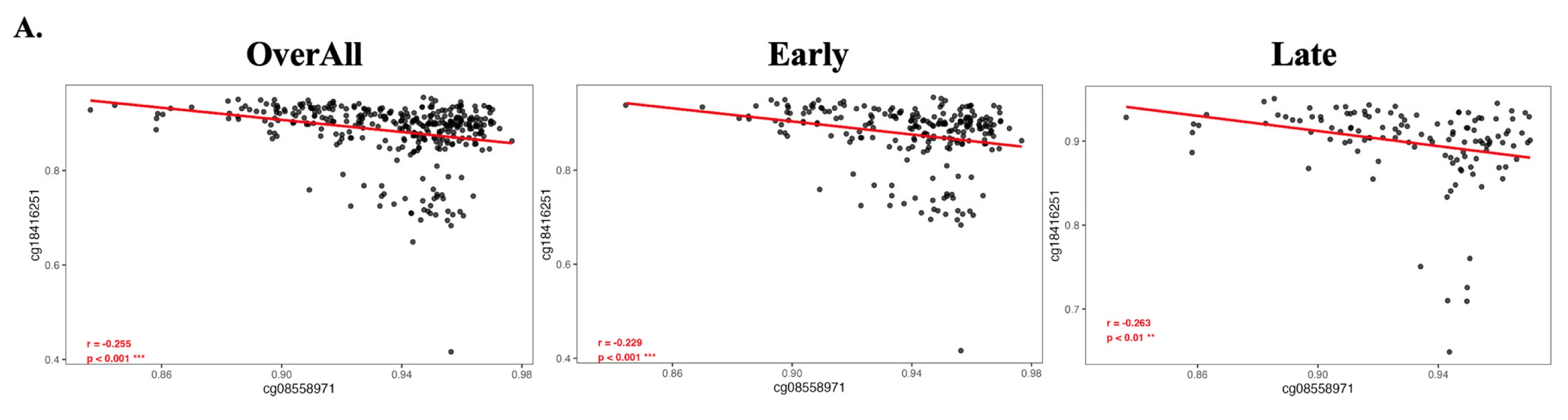
cg08558971与cg18416251呈现阶段依赖性反向甲基化模式
对EZH2基因9个CpG位点的深入分析发现,位于5'UTR的cg08558971与位于第一内含子的cg18416251呈现独特的反向甲基化特征。早期HCC中cg08558971高甲基化(HR=1.78,P = 0.01)及晚期HCC中cg18416251低甲基化(HR=0.31,P = 0.01)均与不良预后显著相关。Pearson相关分析显示,这两个位点在总体队列(r = -0.263,P < 0.001)、早期组(r = -0.255,P < 0.001)及晚期组(r = -0.229,P < 0.001)中均呈稳定负相关,提示其存在反向调控关系。
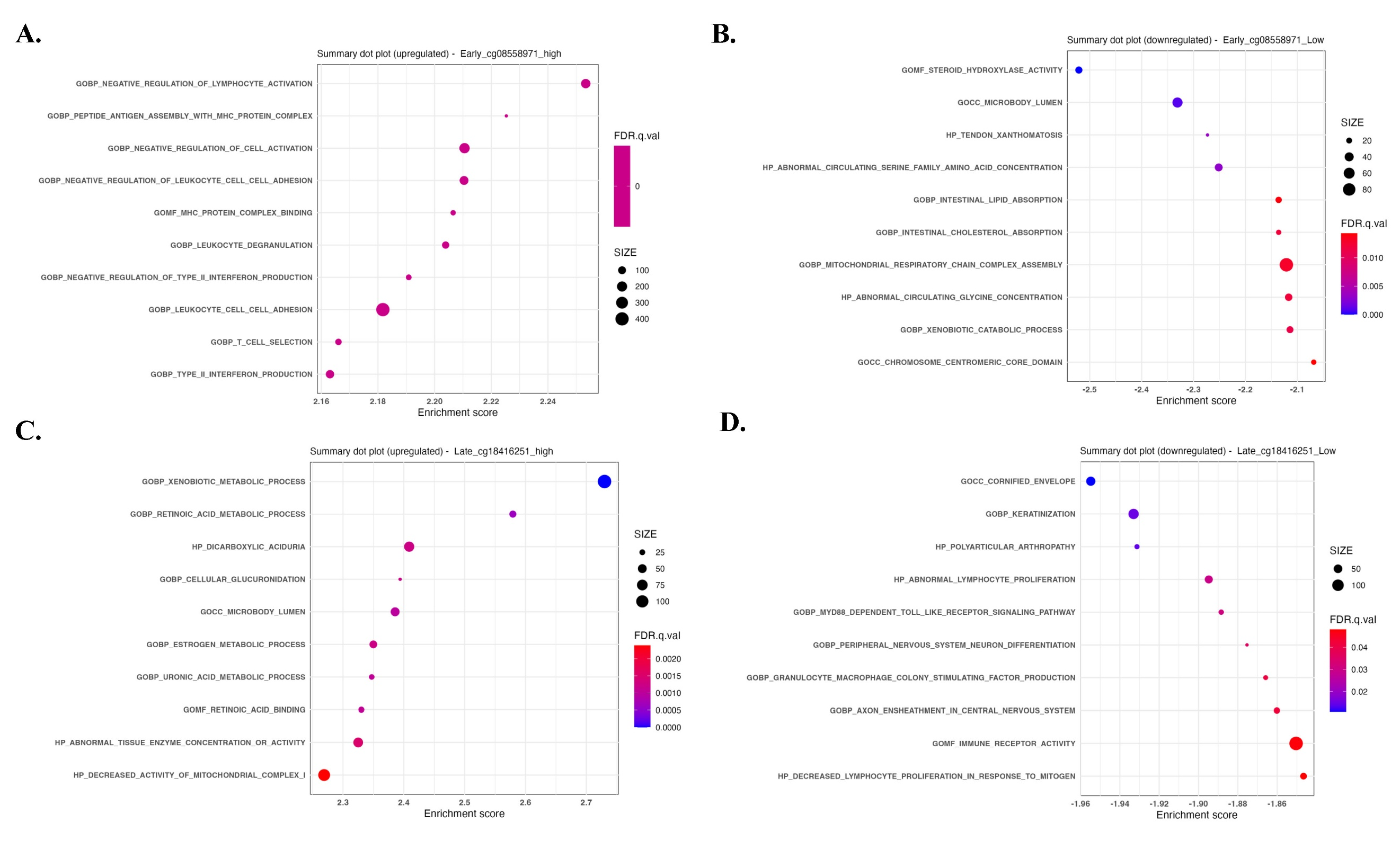
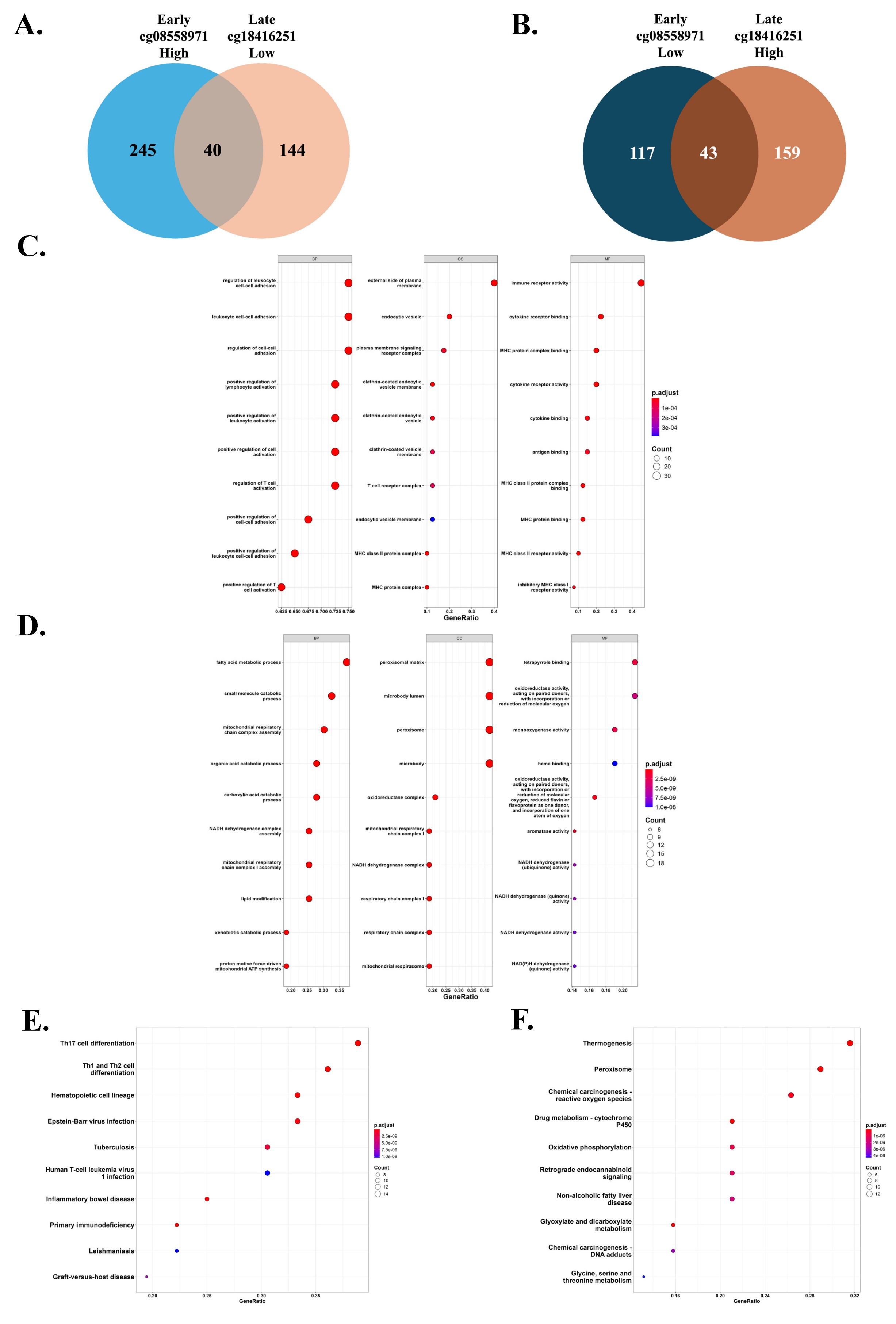
反向甲基化模式分别富集免疫与代谢通路
GSEA分析显示,高cg08558971甲基化合并低cg18416251甲基化的模式显著富集T辅助细胞分化相关通路,包括Th1、Th2和Th17细胞分化(NES > 1.5,FDR < 0.05)。相反,低cg08558971甲基化合并高cg18416251甲基化则主要富集代谢相关通路,如过氧化物酶体功能和产热作用。Venn图分析鉴定出40个基因共享于免疫富集模式,43个基因共享于代谢富集模式。GO和KEGG分析进一步证实,免疫相关基因主要参与T细胞活化与分化,而代谢相关基因集中于脂肪酸氧化和线粒体呼吸链。
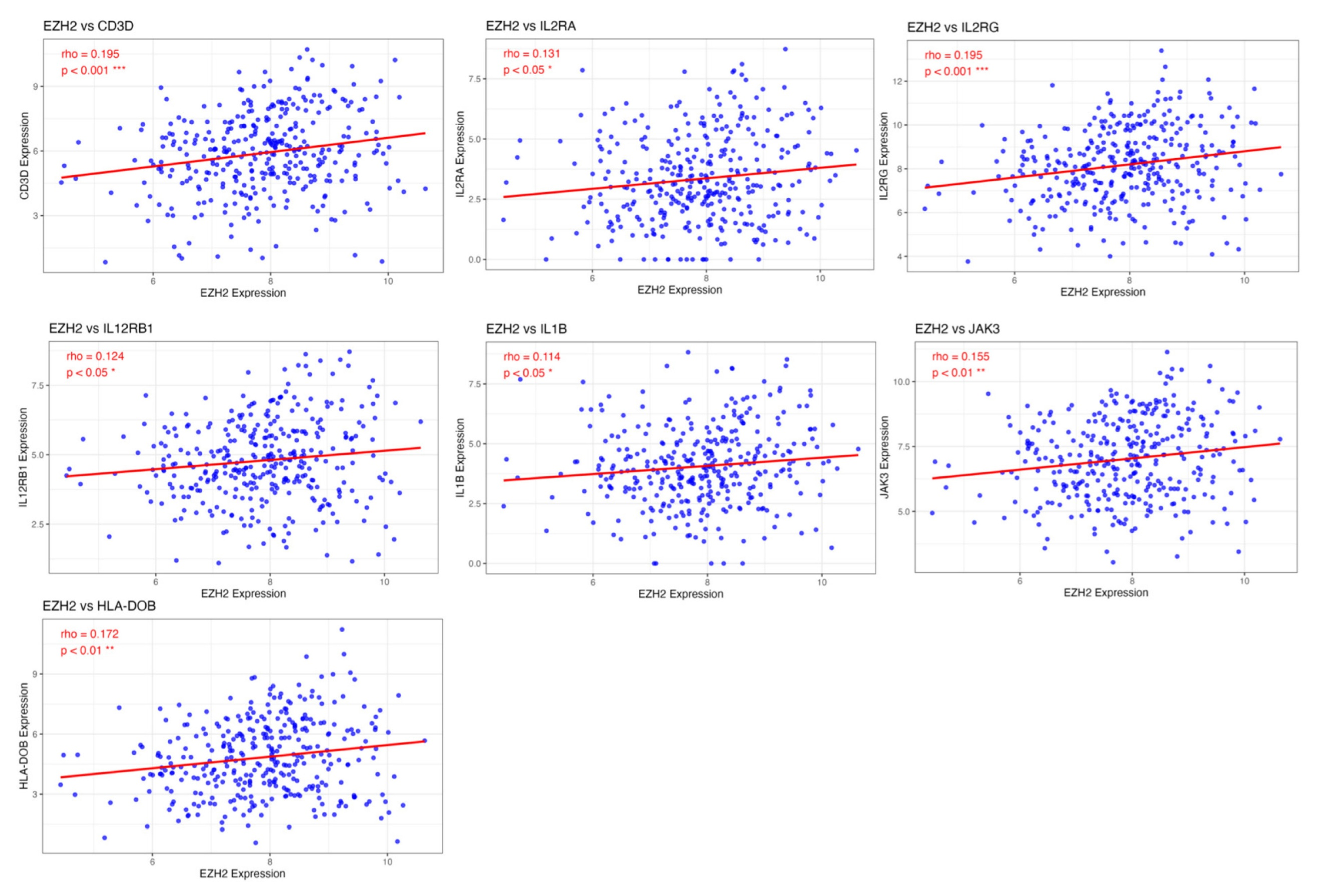
EZH2表达与Th17分化正相关、与过氧化物酶体功能负相关
基因相关性分析表明,EZH2表达与Th17分化关键基因IL1B(r = 0.155,P < 0.01)、IL2RA(r = 0.131,P < 0.05)、JAK3(r = 0.155,P < 0.01)及HLA-DOB(r = 0.172,P < 0.01)呈显著正相关。相反,EZH2与过氧化物酶体功能基因(AGXT、BAAT、CAT、DAO、EHHADH、EPHX2、HAO1、HAO2、PHYH、PIPOX)及产热相关基因(COX16、NDUFA13、NDUFA2、NDUFB8、NDUFC2、NDUFS4)呈显著负相关(r = -0.114至-0.414,P < 0.05至P < 0.001)。这提示EZH2可能通过IL-1β/RORC轴促进病理性Th17反应,同时抑制过氧化物酶体β氧化和适应性产热,驱动肿瘤代谢重编程。
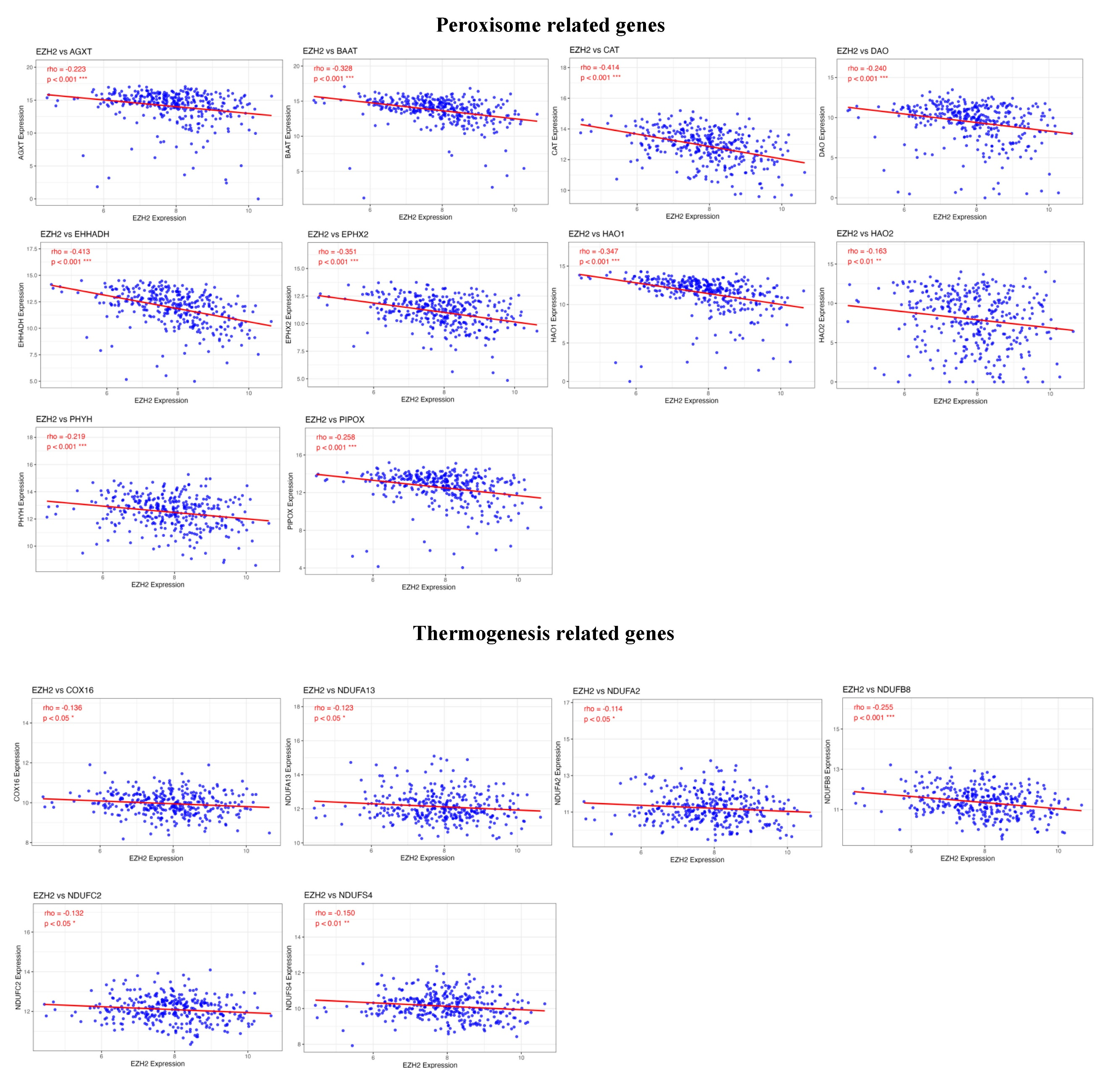
本研究通过大规模生物信息学分析,系统阐明了EZH2在HCC中的阶段依赖性表观遗传调控机制及其免疫代谢调控功能。主要结论如下:(1)EZH2高表达是HCC患者独立的不良预后标志物,且与多种免疫细胞浸润增加相关;(2)鉴定出两个具有阶段特异性预后价值的CpG位点cg08558971和cg18416251,其反向甲基化模式贯穿HCC进展全过程;(3)这些甲基化模式通过差异化调控T细胞分化与过氧化物酶体代谢通路,塑造免疫抑制性微环境;(4)EZH2表达与Th17促癌轴正相关,与代谢抑癌通路负相关,揭示其作为免疫代谢检查点的双重角色。
尽管本研究基于公共数据库分析,需进一步的体外实验和动物模型验证,但上述发现为EZH2作为HCC预后预测生物标志物提供了坚实证据,并为靶向EZH2的表观遗传治疗策略奠定了理论基础。未来研究应聚焦于:(1)通过ChIP-seq和DNA甲基化测序明确cg08558971和cg18416251的功能调控机制;(2)探索EZH2抑制剂与免疫检查点抑制剂或代谢调节剂联合应用的协同效应;(3)在前瞻性队列中验证EZH2甲基化模式对免疫治疗反应的预测价值。综上所述,EZH2的阶段依赖性甲基化调控网络为HCC的精准诊疗开辟了新的研究方向。
Chien YC, Wu GW, Wu JY, Liu LC, Hsieh YH, Yu YL. Stage-dependent EZH2 methylation correlates with immune polarization, metabolic suppression, and unfavorable outcomes in hepatocellular carcinoma. Int J Med Sci. 2025;22(16):4201-4213. Published 2025 Oct 1. doi:10.7150/ijms.119496
审批号:CN-175730
审批时间:2025-12-23
有效期至:2026-12-23
声明:本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考。
排版编辑:肿瘤资讯-李鑫











 苏公网安备32059002004080号
苏公网安备32059002004080号


