浙江省肿瘤医院胸部肿瘤内科主治医师 博士 硕士生导师
兼任浙江省头颈肿瘤重点实验室成员
中国科学院大学附属肿瘤医院课题组长培养对象
院级“30人才”培养对象
国家自然科学基金获得者
浙江省医学会肿瘤营养与治疗学分会青年委员
浙江省医师协会肿瘤MDT专业委员会青年委员
浙江省抗癌协会肺癌专业委员会胸壁(膜)、纵隔肿瘤学组秘书
近年来以第一作者或通讯作者发表SCI论文20余篇
国际会议口头报告2项,全国性会议口头报告1项
目前主要从事胸部肿瘤内科基础和临床研究
曾主持多项国家级课题和省级课题。获得国家专利10余项
副主编专著一部,参与撰写专家共识一篇
获得浙江省科技进步二等奖
ALK融合作为“钻石”突变,是实现肺癌“慢病化”管理的排头兵,是晚期肿瘤精准诊疗的践行者。虽然早在2018年11月2日FDA已批准第三代ALK- TKI洛拉替尼在国外上市,然而直到2022年4月29日洛拉替尼才获得NMPA的全线批准。随着“皇冠”加冕,洛拉替尼作登上了ALK-TKI群雄四起的中国舞台。
洛拉替尼是专门设计的全新三代小分子大环酰胺结构的ALK抑制剂,几乎对目前临床已知的所有获得性ALK单一的二次突变均有效。与一、二代TKIs无法完全进入结合口袋的长链不同的是,洛拉替尼的大环紧凑结构可以更好地结合ATP口袋,有助于发挥其活性1。

尽管在CROWN研究2中,洛拉替尼显示出卓越的疗效(详见下表),然而任何靶向药在治疗过程中均不可避免地发生耐药。且三代ALK-TKI耐药机制更加复杂,尚缺乏大型的耐药机制相关研究,目前多数探索正处于临床前阶段。
ALK-TKI药物关键数据总结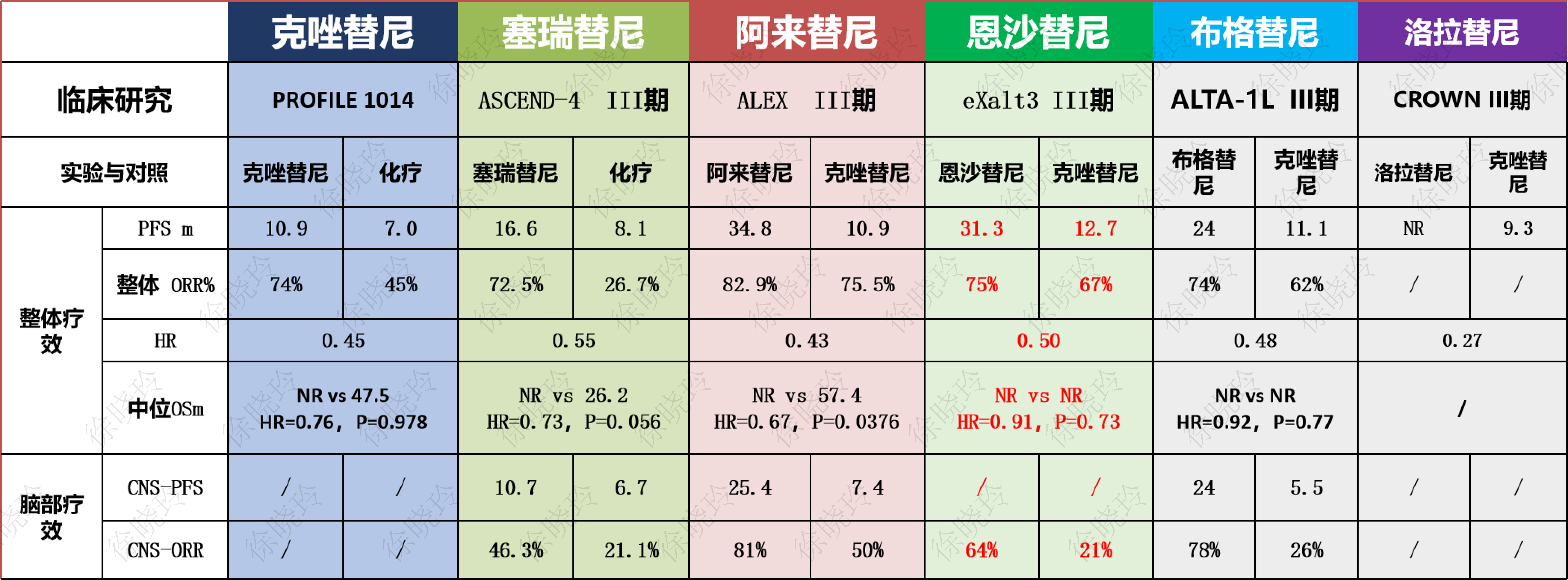
注:数据来源于不同研究,仅供专业人士谨慎解读 参考文献 2-8
一、 第三代ALK-TKI耐药机制复杂,异质性强
洛拉替尼的耐药机制主要分为ALK通路依赖和非依赖两大类。
1.ALK通路依赖的在靶机制(ALK激酶区域的继发突变)
洛拉替尼导致的耐药继发突变多为复合突变9-11。Hua等12分析了116例接受ALK-TKI治疗的疾病进展后患者血浆标本的ALK突变情况。与第一代(12.1%)和第二代(20.8%)ALK-TKI相比,洛拉替尼治疗后进展的患者中复合ALK突变更常见(36.4%)。Dagogo-Jack等13对84例接受不同ALK-TKI治疗的阳性NSCLC患者的血浆标本进行了ALK突变检测。在纳入的46/70例第二代ALK-TKI和22/29例洛拉替尼治疗后进展的患者中,分别有23%和48%的患者检测到≥2种ALK突变(p = 0.017);其中最常见ALK复合突变为L1196M+G1202R12, 14。
目前已发现的复合突变形式和药物敏感性整理如下图。
复合突变耐药图谱
2、 ALK通路非依赖的脱靶耐药机制
主要包括旁路激活(SRC 10、PI3K-AKT 20和Ras-MAPK 20等)、MET-扩增21,17, 18、BRAF V600E 21、共存的TP5322、EGFR或KRAS突变22、NF2缺失10, 20、上皮向间质转化(EMT)10, 17和小细胞转化19等。
二、洛拉替尼耐药后的应对策略
1. ALK通路依赖的复合突变
重回第一、二代ALK-TKI
第一、二代ALK-TKI可逆转部分由于继发复合突变而产生的耐药性。早期发表在新英格兰杂志中的个案报道提示,复合突变(如含有1198F继发突变)导致的耐药可被克唑替尼逆转15, 16。此外,含1171N/S突变导致的耐药可被二代ALK-TKI逆转17-19。既往研究显示ALK复合突变体G1203N+L1196M对洛拉替尼具有高水平耐药性10, 11,而笔者经治的一例该复合突变的患者,服用复瑞替尼的最佳疗效可达SD(详见典型病例1)。

典型病例1:洛拉替尼耐药后出现 D1203N+L1196M复合突变,对复瑞替尼敏感
开发第四代靶向药物
第四代ALK抑制剂TPX-0131是一个紧凑的大环结构,便于插入腺苷结合口袋。细胞实验结果显示,除了对I1171N/S/T和G1269S的敏感性不如塞瑞替尼、阿来替尼和洛拉替尼外,TPX-0131对其它ALK突变类型的敏感性超过既往ALK-TKI,尤其对G1202R/L1196M抑制性强,IC50仅为0.7nmol/L27。NUV-655是一款新型ALK抑制剂,对洛拉替尼耐药的G1202R突变或复合突变(G1202R/L1196M、G1202R/G1269A、G1202R/L1198F)具有良好的抑制能力28。2.联合旁路靶点或多靶点抑制剂
针对相关旁路激活的患者,ALK抑制剂联合靶向药物如MEK、MET、CDK4/6抑制剂等23, 24用于治疗可能具有一定的治疗前景。
目前,已有多项联合MEK抑制剂模式如阿来替尼+Cobimetinib(NCT03202940)、色瑞替尼+Trametinib(NCT03087448)和布格替尼+Binimetinib(NCT04005144)的临床研究正在进行中,结果令人期待。
EMT是ALK-TKI发生耐药的重要机制之一。Recondo G等人10在细胞活性抑制试验中,通过大量的化合物筛选,发现联合Src抑制剂Saracatinib可以逆转EMT 10, 17,从而克服洛拉替尼的耐药性。
在临床前研究中20,对洛拉替尼耐药细胞进行RNA测序提示PI3K/AKT和RAS/MAPK通路有明显改变;功能验证也证实了这些途径参与了细胞对洛拉替尼的耐药性的形成。因此联合相应的PI3K抑制剂等有望克服耐药。
体外试验结果显示,在体外暴露于洛拉替尼的NSCLC细胞发生了获得性EGFR活化20,而活化的EGFR通路可被Erlotinib阻断从而恢复对洛拉替尼的敏感性。这提示联合EGFR-TKI也可能是克服洛拉替尼的耐药机制之一。
FMS样酪氨酸激酶3(FLT3)突变是急性髓系白血病的治疗靶点,也是预后不良的标志。有基础研究显示FLT3抑制剂Gilteritinib可能对洛拉替尼耐药的I1171N+F1174I和I1171N+L1198H复合突变有效25。其他多靶点抑制剂亦可能通过抑制旁路途径恢复洛拉替尼的敏感性。
2.联合化疗或抗血管靶向药物
众所周知,联合化疗方案有助于克服肿瘤异质性,与靶向药具有协同增效的作用。而抗血管靶向药物可以改善肿瘤乏氧状态,重塑血管免疫微环境,亦有靶向增敏作用。对目前暂无特殊耐药机制的患者,可以考虑联合化疗或抗血管靶向药物。
3.病理类型的转化
组织学类型转化是靶向药耐药的重要机制之一。一项个案报道汇报了一例经洛拉替尼治疗后出现肺腺癌向鳞癌转化,同时伴有MET扩增的病例26。小细胞转化是较多见的病理类型转化模式,Coleman N等19报道了一例经治的洛拉替尼治疗后的患者发生小细胞转化同时伴有1196M突变的患者,后续应用长春瑞滨联合卡铂无效。而笔者经治的洛拉替尼治疗后小细胞转化的患者,表现出对小细胞经典方案依托泊苷联合卡铂、伊立替康单药良好的反应性(详见典型病例2)。因此,推荐发生组织学组化的患者根据组织学类型进行方案的选择。

典型病例2:洛拉替尼耐药后出现小细胞转化,对小细胞方案敏感
4.联合免疫治疗
ALK患者中存在一定比例的PD-L1高表达患者。既往回顾性分析IMMUNOTARGET研究29和前瞻性 ATLANTIC研究30的结果均未显示PD-1/PD-L1抑制剂对ALK阳性患者具有明显疗效。此外,在研的几项31-33PD-1/PD-L1抑制剂联合不同代 ALK-TKI的I期临床研究中都因为严重毒性不良反应的高发生率而被迫提前终止。因此,目前PD-1/PD-L1抑制剂暂不常规推荐用于ALK阳性的患者。

洛拉替尼耐药机制和应对策略思维导图
三、困惑和争议:“好药先用”还是“序贯接力”?34, 35
1.正方:好药先用
强效入脑,“冠”绝群雄
洛拉替尼不是P-gp蛋白和BCRP的底物36,不易被泵出,且具有更好的亲脂性,因此具有强大的脑脊液通透率。在I期研究中,三名连续服用100 mg洛拉替尼每天一次患者的平均未结合脑脊液与血浆的比率为 0.79(0.65、0.77、0.94)37。作为比较,阿来替尼的未结合脑脊液与血浆比率在美国I期研究中为0.3 38。在CROWN 研究中,洛拉替尼显着改善了颅内进展时间的HR(cause-specific HR [csHR]),csHR 为 0.07(95% CI:0.03-0.17),即使是阿来替尼在东方人群中数据,也难与之媲美(J-ALEX39中csHR为0.22[95% CI:0.10-0.48], ALESIA 40中csHR为0.14 [95% CI: 0.06-0.30])。值得注意的是,在CROWN研究2中,洛拉替尼的3年无颅内进展生存率为92.3%,颅内进展风险降低92%,数据非常亮眼2。

对V3亚型的独特优势
不同的ALK-TKI在V1和V3亚型中疗效不同。回顾性研究显示V3亚型的患者对克唑替尼获益时间更短41。在 ALEX 研究中,阿来替尼在EML4-ALK V1中的总体反应率为90.9%,但在V3亚型中仅为 68.0%。对于EML4-ALK融合患者,V1型 vs. V3型的中位 PFS分别为未达到和34.9个月42。在ALTA-1L 中,布格替尼对EML4-ALK V1型 (84%)和EML4-ALK V3 型(91%)患者实现了同样高的总体缓解率,但相应的中位 PFS仍有差异(未达到vs. 24个月)。JCO杂志上发表的一项回顾性研究显示,洛拉替尼对经一、二代ALK-TKI治疗后的V3亚型患者疗效更佳43。临床前细胞抑制试验表明,在所有六种 ALK-TKIs 中,洛拉替尼对 Ba/F3 细胞中的野生型EML4-ALK V1和V3型的抑制作用最强,IC50在两种亚型中分别为0.27 nM 和4.46 nM 44。
一线使用可能减少复杂耐药突变的产生
真实世界分析表明9,洛拉替尼在ALK-TKI 难治性的ALK+ NSCLC患者中的中位 PFS随着先前ALK-TKI 线数的增加而降低,这与其在ALK+ NSCLC患者中的2期全球性研究中的数据一致45。有学者指出一代→二代→三代ALK-TKIs序贯治疗策略,可能更易出现ALK复合突变,导致所有可用ALK-TKIs的高度耐药,并降低洛拉替尼后线治疗的疗效11, 17。此外,洛拉替尼具有广泛的活性,可对抗大多数ALK继发性突变,因此可能预防ALK靶点耐药突变的发生。但目前CROWN研究2中一线洛拉替尼的耐药机制相关数据尚未披露,且缺乏其他大型的研究数据,因此ALK-TKI使用顺序是否影响复合突变的发生率尚不明确。
前路虽难, 尤可期许-复合耐药突变破解有道
一方面,部分洛拉替尼耐药的患者可以重新使用一、二代ALK-TKI获得缓解;另一方面,洛拉替尼跨线使用或联合化疗等其他药物,有望使部分患者再度缓解。具体见上述耐药机制部分。
2.反方:序贯接力
第一个PFS只是起点,不能代表终点
对于ALK-TKI的患者来说,我们的目标是长生存,因此第一个PFS赢得漂亮只是一个起点,让最终的OS更长才是我们努力的终点。因此,如何基于分子检测进行最佳的排兵布阵,对于实现慢病化管理的目标极为重要。
目前CROWN研究2中洛拉替尼组的中位PFS尚未到达。已披露的数据显示,基于BIRC评估的克唑替尼中位PFS 为 9.3个月, HR 为0.28 (95% CI:0.19-0.41)。假设随着时间的推移采用等比例风险模型,应用“Back of the envelope(封底)”计算的方法,预计的 BIRC评估的洛拉替尼中位PFS为33.2 a(95% CI:22.7-48.9)个月,是迄今为止在一线 ALK 抑制剂试验中报告的最长中位 PFS(阿来替尼为34.8个月)42。因此先使用二代TKI,耐药后根据再次活检NGS检测的结果,序贯使用能克服多数二代TKI耐药突变的洛拉替尼,也可能是值得选择策略之一。
此外,CROWN研究2不允许对照组的患者进行交叉,这就导致许多对照组的患者在后线没有机会使用洛拉替尼,我们无法也从这项研究中直接观察到不同给药顺序是否影响最终的OS。
a由于是基于等比例风险模型的推算,没有应用一些加权或分段指数分布等优化措施,结果需谨慎参考。
不同ALK-TKI排兵布阵

以上数据来源于临床研究,仅供专业人士谨慎参考。
值得注意的是,因各研究入组条件等均有不同,仅参考已公布临床研究数据并将PFS时间简单叠加进行临床决策,显然是不可取的。而且真实世界的中病例复杂多变,部分患者可能是旁路激活等原因所致的耐药,因此我们需要综合更多的个体化因素才能做出合理地治疗决策。
与众不同的不良反应
莎士比亚有句经典谚语:“Uneasy lies the head that wears a crown”-为王者无安宁。洛拉替尼固然具有诸多优点,但是却让少数患者“寝食难安”。
虽然在CROWN研究2中,仅21%的患者出现认知不良反应,16% 的患者对洛拉替尼产生了与情绪相关的不良反应。但在洛拉替尼的后线研究中,54%的患者46报道了以下至少一种情况:(1)癫痫发作; (2)幻觉; (3)认知功能的改变; (4)情绪改变(包括自杀意念); (5)言语改变;(6)精神状态变化;或 (7)与睡眠有关的不良反应。笔者所在的医疗组也遇到过一例服用洛拉替尼后出现幻视、精神错乱的患者,经减量后上述症状好转。
目前在我国洛拉替尼尚未进医保,患者经济负担重,这也是我们必须考量的现实因素。
三代ALK-TKI耐药机制复杂,对肿瘤进化选择压力更大,复合耐药突变更难克服,后续治疗选择有限。
结语
欲戴“皇冠”,必承其重,在应用三代ALK-TKI靶向治疗的同时,我们必须了解后续的耐药机制及其破解之道;同时我们也需要关注和重视洛拉替尼的特殊不良反应,帮助患者取得躯体和精神的全面获益。
欲达高峰,必忍其痛,对于我们青年肿瘤医师来说,须磨砺以出锋芒,继前圣之绝学;须弘道笃行,厚德精医,为患者身心开太平。











 苏公网安备32059002004080号
苏公网安备32059002004080号


