【 例 】
Helen N. 女,越南人,65 岁,从不吸烟,既往有高胆固醇血症,最近几周出现劳累性呼吸困难、轻微干咳伴左侧后背部肩胛下轻微疼痛。当地医院胸部DR片提示左侧胸水。
患者住院进一步检查,胸穿引流出约 1100 ml 胸水,呼吸困难和咳嗽症状改善。胸水细胞学检查提示腺癌,TTF-1(+),符合原发性肺癌。放胸水后做 CT 发现左肺下叶一个大小约 4.3cm 的肿块,双肺多发的直径小于 1 厘米的小结节,考虑转移。PET-CT显示左肺下叶原发灶、肺部实性结节、左肺门、第 7 站淋巴结、双侧纵隔淋巴结、左侧肾上腺孤立性转移灶均呈高代谢。头颅MRI未见转移灶。
分子标志物检测提示 ALK 重排阳性,EGFR 和 ROS1无突变、PD-L1阴性(0%)。
开始口服克唑替尼靶向治疗,后未再出现胸水;2 月后复查CT疗效评价PR,原发病灶最大径缩减为 2.6cm,纵隔淋巴结和肾上腺转移灶缩小,胸膜结节消失。服用克唑替尼 5 月后复查 CT 提示肺部病灶轻微退缩,但是头颅 MRI(距之前 MRI 检查约 6 个月)发现右侧顶叶及左侧枕叶分别有一个大小约 5mm 和 3mm 的无症状性占位,周围无水肿。
问题一:
以下哪项干预措施最不适合在此时进行?
停用克唑替尼,调整为二代 ALK 抑制剂
继续口服克唑替尼,脑部病灶进行立体定向放疗(SRS)
停用克唑替尼,调整为二代 ALK 抑制剂,脑部病灶进行立体定向放疗(SRS)
全脑放疗(WBRT),停用克唑替尼,调整为二代ALK抑制剂
【答案】 D
【讨论】
脑转移在晚期 NSCLC 中较为常见,但对于 ALK 阳性 NSCLC 患者来说是一个特别的挑战,在整个病程中,60%-90% 患者将出现颅内进展。颅脑是首发转移常见的部位,在口服克唑替尼的患者中高达 40%-50%,这与克唑替尼中枢神经系统渗透差有关。
目前 NCCN 指南指出,无症状脑转移病灶适合进行局部治疗,之后继续克唑替尼治疗或调整为已批准的二代 ALK 抑制剂(色瑞替尼、艾乐替尼)。口服克唑替尼靶向治疗的患者出现颅内进展,考虑是因为药物较难通过血脑屏障,而不是对药物真正的耐药,所以在局部治疗控制中枢神经系统病灶后,可不调整全身治疗方案,患者颅外病灶仍然对治疗反应良好,长期有效。另一方面,脑部放疗后调整为二代 ALK 抑制剂也符合 NCCN 指南推荐。
重要的是,即使不对脑转移灶进行局部治疗,也可观察到颅内病灶对二代ALK抑制剂有反应,包括色瑞替尼、艾乐替尼和其他如FDA尚未批准的brigatinib;然而相关研究中的患者数量太少,无法比较这些药物的疗效。考虑到这些药物对颅内病变的疗效,可以调整克唑替尼为二代ALK抑制剂,根据观察到的颅内反应后续可能会不需要局部治疗,尤其是小的局限的无症状脑转移灶。
如果采用放射治疗,对于脑转移灶数量非常有限的患者,尤其是转移灶小且无症状时,立体定向放射治疗(SRS)优于全脑放疗(WBRT)。立体定向放射治疗至少可达到 80%-90% 的局部控制率,与 WBRT 相比,SRS 无长期认知功能缺陷的风险。对于那些脑转移灶初始治疗后甚至是治疗后几年反应良好的 ALK 阳性患者,如果可以的话,最好还是推迟 WBRT。
Helen N. 脑部小转移灶进行 SRS 且耐受良好。继续服用克唑替尼3 个月,此时再次出现干咳。复查CT提示原发肿瘤多发转移,左侧肾上腺出现新发转移灶约 2.7cm,肺部出现几个新发结节,最大约1.2cm。复查头颅MRI可见之前治疗过的脑部转移灶,未见新发颅内转移灶。
问题二:
如果患者接受二代ALK抑制剂,下列哪项最有可能指导你下一步治疗?
在这种情况下,色瑞替尼疗效卓越
在这种情况下,艾乐替尼疗效卓越
在这种情况下,Brigatinib疗效卓越
没有直接的对比试验明确的指出一种药物优于另一种药物
【答案】 D
虽然不同 ALK 抑制剂的疗效存在一些差异,但是没有直接的对比研究明确地指出一种药物优于另一种药物。
【讨论】
此时,考虑不同治疗方案之间的差异是合理的。如表 3 总结,在接受克唑替尼治疗后进展或毒性不能耐受的患者中进行单臂试验,证明色瑞替尼、艾乐替尼和 brigatinib 均疗效显著。然而色瑞替尼和艾乐替尼已获批,而 brigatinib 没有。
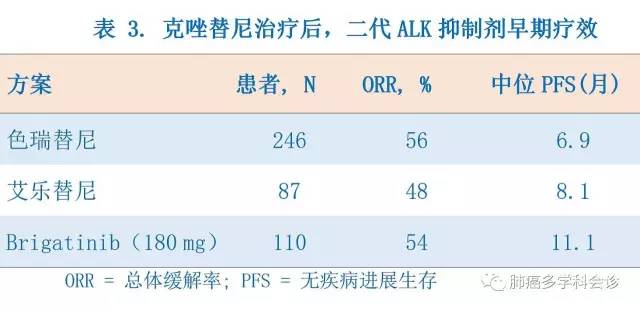
虽然我们可以看到这些药物疗效的差异,推测可能存在显著的临床差异来指导治疗方案的选择,然而对于克唑替尼获得性耐药的 ALK 阳性患者,哪种药物是最佳的二代 ALK 抑制剂,还没有直接的对比试验提供一个明确的结论或建议。
通过颅外疗效评估,没有比较性的证据提出明确的最优选择,你可以根据其他因素选择下一步治疗方案。
问题三:
下列哪项关于二代ALKA抑制剂治疗的陈述是正确的?
色瑞替尼引起的胃肠道毒性是剂量限制性的,通过下调剂量大多可以控制
多数患者不能耐受艾乐替尼标准初始剂量
brigatinib 治疗过程中最令人担心的一个问题是后期出现的肺部毒性
ALK 抑制剂经常引起心动过缓,这需要下调剂量或中断治疗
【答案】 A
初始治疗剂量按照 FDA 推荐,每天 750mg,色瑞替尼治疗相关不良事件如恶心、呕吐、腹泻的发生率较高。当剂量调整至 600mg 或 450mg 时,通常患者耐受更好。色瑞替尼服用期间低脂饮食能够显著减少胃肠道不良反应。
【讨论】
ALK 阳性患者克唑替尼获得性耐药后有多种药物可以选择,可根据医生的判断和一些其他特征(如每种药物的毒性)来选择治疗方案。 初始治疗剂量按照 FDA 推荐,每天 750mg,色瑞替尼治疗相关的恶心、呕吐、腹泻的发生率较高,99% 的患者出现不同程度的胃肠道反应,62%的 患者需要下调剂量。当剂量调整至6 00mg 或 450mg 时,通常患者耐受较好,同时低脂饮食也可显著降低胃肠道毒性,这种做法参照高剂量的药代动力学参数,不过疗效还未被证实。相反,服用艾乐替尼的患者约 16% 需要下调剂量,不良反应包括便秘(36%),疲乏(33%),肌痛(24%),外周水肿(23%),3/4级肌酸激酶升高(8%)。
Brigatinib 也是一种ALK抑制剂,但目前尚未批准用于 NSCLC。多数患者对该药耐受良好,约 20% 的患者需要将剂量从每天 180mg 下调。呼吸困难、咳嗽、组织缺氧、渗出性肺炎等呼吸系统毒性罕见,但是应当十分注意。约 6% 的患者可出现肺毒性,通常在治疗开始第一周内出现,并且常见于第一周以每天 90mg 的剂量开始治疗,后续剂量递增至每天 180mg 的患者。某些患者通过暂时暂停治疗可成功控制不良反应,但是一些患者因为肺部不良事件需终止服用 brigatinib。
心动过缓是一种罕见但偶有报道的 ALK 抑制剂相关不良事件,通常为轻度且无症状,很少需要具体的干预措施,在停用 ALK 抑制剂治疗后可缓解。
Helen N. 停用克唑替尼,开始足量(600mg 口服,每天2次)服用艾乐替尼,耐受良好,仅出现轻微的对称性足部水肿,肌酸激酶水平轻度升高。服药2月后复查提示所有的可测量病灶均缩小,之后定期复查提示疾病稳定,又继续服用艾乐替尼 7 个月。脑部影像学检查未见新发病灶。服药 9 个月后复查胸部 CT 提示肺部有一个结节从 8mm 增大至 13mm,但其他病灶未见变化。
问题四:
下一步你最可能选择?
标准治疗:再活检或切除进行分子检测指导后续治疗
进展病灶局部切除或消融,继续艾乐替尼治疗
改为全身治疗
增加艾乐替尼的剂量
【答案】 B
在这种情况下,对进展病灶进行切除或消融,继续服用艾乐替尼是合理的治疗策略。ALK 阳性 NSCLC 患者在获得性耐药时可考虑进行分子检测,但此时不是一个标准治疗方案。 增加艾乐替尼的剂量可能会提高疗效,但是没有证据支持这一观点,而且可能会增加不良反应的发生率。
【讨论】
ALK 阳性 NSCLC 患者获得性耐药可考虑进行分子检测,但此时不是一个标准的治疗方案。对于特定的ALK二次或三次突变 NSCLC 患者目前尚无明确的后续治疗方案。EGFR 突变阳性 NSCLC,T790M 突变是主要的获得性耐药机制,并且 FDA 已经批准三代 EGFR TKI - 奥希替尼用于治疗该耐药突变。然而,ALK 阳性 NSCLC 的获得性耐药机制非常复杂,未发现主要的耐药机制并且至少有 15 种不同的获得性突变。无论是通过组织活检或使用血浆检测的“液体活检”,再活检和分子检测仍然是一个研究工具而不是一个标准治疗方案;不过这种策略仍不失为一种选择,可能会发现一个新的相关靶点,促进对 ALK 阳性 NSCLC 获得性耐药生物学方面更深入的了解。增加艾乐替尼的剂量可能会提高疗效,但是没有证据支持这一假设。此外,应考虑到这种方法可能会带来更多的不良反应,并且疗效不明确。
在探索获得性耐药机制时,应考虑影像学上的进展是否是弥漫性的或是否有临床意义。在疾病控制良好的基础上, “寡转移”或某一病灶的进展或某些部位非常局限的进展模式越来越被认可。这种情况下,治疗指南倾向于推荐继续原方案治疗或对进展的病灶进行局部切除或放射治疗,而全身治疗不作任何改变。对于多数患者来说,这种方法已被证明是可行的,可潜在延长全身治疗持续反应时间,不伴有后续疾病的进展。
即使多发病灶出现可测量的弥漫性进展,如果患者对该治疗耐受良好且疾病进展相对惰性,此时可不作任何改变继续目前的全身治疗方案。
Helen N.局部进展病灶接受立体定向放射治疗(SART),耐受良好,没有明确不良反应。患者继续服用艾乐替尼,之后 6 个月内感觉良好,此时复查CT提示多数肺部可见结节及肾上腺结节广泛进展,并且肝脏出现 2 个新发病灶。对进展区域可获得病灶进行活检,发现 EML4-ALK I1171N 突变。
问题五:
下列哪项后续治疗是最不恰当的?
A.卡铂/培美曲塞
B.派姆单抗(Keytruda)
C.色瑞替尼
D.临床试验中的劳拉替尼(Lorlatinib)
【答案】 B
FDA批准派姆单抗用于既往治疗过且PD-L1表达 >1% 的患者,对于无PD-L1表达的患者不适合应用。
【讨论】
对于二代 ALK 抑制剂获得性耐药的患者,目前尚无数据直接比较后续治疗方案。其他的 ALK 抑制剂,如色瑞替尼或 brigatinib,或许在艾乐替尼治疗后使用会有显著的疗效,可能是存在特定的ALK耐药突变,但目前后续ALK抑制剂的作用如何尚不确定,未经试验检验。
ALK 抑制剂获得性耐药突变包括一系列 ALK 二次重排,劳拉替尼是一个研究中的三代 ALK 抑制剂,前临床研究证实其对广泛 ALK 抑制剂耐药突变有效;对于接受二代 ALK 抑制剂治疗的患者也有显著活性。由于 FDA 未批准该药物,所以只有通过临床试验获得。
NCCN 指南推荐,对于晚期无驱动基因突变的 ALK 阳性肺腺癌患者,经多线标准治疗后进展时可选择进行全身治疗。对于既无驱动基因变异又无 PD-L1 高表达(>50%)患者,全身治疗指以铂为基础的双药化疗。在这种情况下,卡铂/培美曲塞是最常用的治疗方案。
FDA 批准派姆单抗用于既往治疗过且 PD-L1 表达 >1% 的患者,对于无 PD-L1表达的患者不合适应用。此外,与无驱动基因变异的患者相比,免疫检查点抑制剂对ALK阳性患者的疗效欠佳。
Helen N. 开始接受卡铂联合培美曲塞化疗,2 周期后疗效评价 PR,4 周期后无明显变化。之后应用培美曲塞进行单药维持治疗超过 2 个月,无明显毒性且持续有效,计划继续维持治疗。











 苏公网安备32059002004080号
苏公网安备32059002004080号


