间变性淋巴瘤激酶(ALK)融合是非小细胞肺癌(NSCLC)的关键驱动基因。自2011年克唑替尼开启ALK阳性NSCLC的靶向治疗以来,新一代ALK酪氨酸激酶抑制剂(TKIs)陆续问世,全面革新了ALK阳性NSCLC的治疗策略,改善了患者的生存预后。ALK阳性NSCLC正逐步迈入“慢病管理”时代。在此背景下,【肿瘤资讯】特别邀请汕头大学医学院附属肿瘤医院林英城教授,围绕耐药机制的深入理解与治疗序列的科学规划,系统分享其对ALK阳性NSCLC全程管理策略优化路径的见解。
汕头大学医学院附属肿瘤医院
中华医学会肿瘤学会肿瘤内科专家委员会委员
中国临床肿瘤学会(CSCO)理事
CSCO罕见肿瘤专家委员会常委
CSCO肿瘤支持与康复专家委员会委员
中国抗癌协会癌症康复和姑息治疗专委会委员
广东省医学会肿瘤分会副主任委员
广东省胸部肿瘤防治研究会副会长
广东省研究型医院学会肿瘤内科专委会副主任委员
广东省临床医学会精准医疗专委会副主任委员
广东抗癌协会癌症康复和姑息治疗专委会副主任委员
广东省健康管理学会肿瘤防治专业委员会副主任委员
广东省药学会乳腺癌临床用药指导委员会副主任委员
中国南方肿瘤合作组(CSWOG)常务委员
直面耐药——ALK阳性NSCLC高质量长生存的最大掣肘
林英城教授:ALK阳性NSCLC靶向治疗疗效显著,患者因此获得了长期高质量生存的机会。这一突破不仅使临床治疗面临长期用药与全程管理的新常态,也推动着临床关注焦点从初始治疗疗效,拓展至耐药机制探索、治疗策略优化、长期用药安全性及患者生活质量(QOL)等多方面。
其中,耐药依然是ALK阳性NSCLC治疗中不可避免且最具挑战性的临床困境,严重制约了患者的长期生存获益。那么,如何延缓或避免耐药的发生?耐药出现后临床又该如何抉择?目前,我国已有多种ALK抑制剂陆续获批上市,ALK阳性NSCLC的治疗选择日益丰富。这既为临床医生提供了更多有力的“武器”,也提出了更高的要求:即在初始治疗阶段,如何为患者规划一条最长的“无耐药生存之路”?又如何精准把握耐药机制,实现提前干预?
主动干预——ALK阳性NSCLC从深度缓解到局部巩固的管理新路径
林英城教授:既往临床策略多是在耐药发生后再行处理,而如今我们需要主动干预。首先,在患者初始治疗阶段,选择能够带来更长无进展生存期(PFS)和更深肿瘤缓解的药物至关重要。以布格替尼为例,其疗效已获得临床广泛认可。该药具有快速强效的缩瘤能力,能够显著降低肿瘤负荷、实现深度缓解,从而为延缓耐药构筑起第一道防线。ALTA-1L研究结果显示,布格替尼治疗组中56%的患者达到深度缓解(肿瘤缩小达到76%~100%)[1,2];且数据表明,达到深度缓解的患者较未达到者展现出更优的生存获益[1]。这一良好的系统控制,为患者的长期预后奠定了基础。
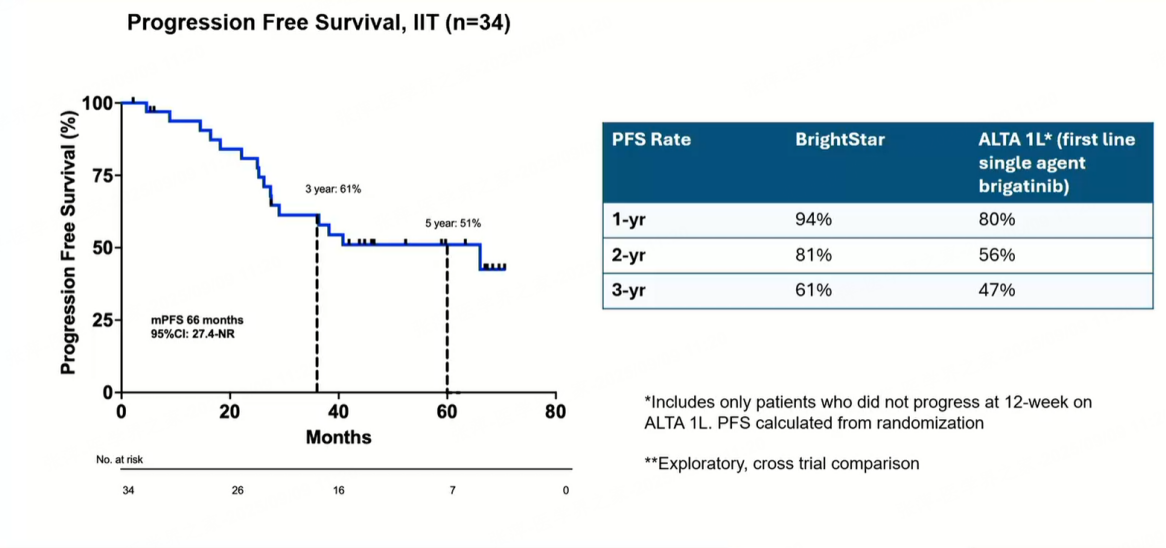
其次,需重视多学科综合治疗的作用。当患者经系统治疗达到一定缓解深度后,需及时进行局部治疗干预。对此,BRIGHTSTAR研究前瞻性地探索了“诱导+巩固”的优化策略,评估了布格替尼诱导后序贯局部巩固治疗(LCT)的临床价值。该研究纳入的34例患者中,82%的患者存在3个以上的肿瘤病灶,41%的患者伴有脑转移[3]。经布格替尼诱导治疗8周后,患者的疾病控制率(DCR)高达100%,客观缓解率(ORR)达79%(n=27)[3]。在此基础上,94%(32/34)的患者接受了LCT,包括放疗(n=27)、手术(n=3)及手术联合放疗(n=2)[3]。这种“药物诱导+局部巩固”的模式显著提升了缓解深度,将影像学部分缓解(PR)转化为更持久的疾病控制,使患者的中位PFS长达66个月(图1)[3]。这一结果为进一步延缓ALK-TKI耐药提供了全新思路,也为局晚期及晚期不可切除患者带来了新的治疗希望。
此外,布格替尼的一线治疗还为后续序贯治疗保留了充足空间。耐药后序贯多种ALK-TKIs,患者的中位PFS2可达74.7个月[4]。在耐药管理中,临床建议积极进行再活检,以明确组织学诊断及基因变异类型,从而精准指导二线药物的选择。同时,面对耐药机制的复杂化和治疗手段的多样化,必须高度重视多学科团队(MDT)协作,涵盖肿瘤内科、呼吸内科、胸外科、放疗科、化疗科、病理科、影像科及心理支持等多个科室,构建全方位的诊疗体系,结合患者具体情况制定个体化综合治疗方案,方能真正实现患者生存获益的最大化。
科学决策——ALK阳性NSCLC耐药后的治疗选择
林英城教授:尽管ALK-TKI耐药在临床上不可避免,但经过数十年的深入研究,临床对耐药机制有了更深刻的认识,并探索出多种克服耐药的策略。目前研究显示,ALK-TKI耐药的产生机制复杂多样,主要分为原发性耐药与继发性耐药[5],临床可根据不同耐药机制采取相应的治疗策略。然而,肿瘤的异质性进一步增加了克服耐药的难度;与此同时,针对ALK或相关耐药途径的新药不断涌现,ALK-TKI适应症也在持续拓展,使得临床决策日趋复杂。对于耐药后局部进展的患者,可采用局部治疗手段;而系统治疗则需依据耐药基因类型等因素制定差异化策略。
在众多ALK-TKIs中,布格替尼展现出了独特的ALK抑制谱,其对17种ALK耐药通路突变显示了抑制活性[6],且对包括 G1202R、L1196M及I1171N在内的常见ALK继发突变均具有良好的抑制作用[7]。在临床实践中,布格替尼的这种广谱抑制活性也得到了充分验证。在已报道的多项临床病例及J-ALTA、ALTA-2等研究中,对于ALK-TKI经治后出现L1196Q、L1196M、G1202R、V1180L、G1269A、I1171S、I1171N等不同ALK耐药突变患者,布格替尼均展现出了有效的疾病控制能力[8-12]。
这也折射出更广泛的临床现状:虽然新一代ALK-TKI已成为全球广泛使用的一线标准方案,但患者在一线TKI治疗失败后,后续治疗策略的选择仍是亟待解决的关键临床问题。2022年ASCO披露了J-ALTA研究的最终分析,该研究难治性扩展队列共纳入了47例经阿来替尼±克唑替尼治疗的患者,其中74%的患者仅接受过阿来替尼治疗,26%的患者接受过克唑替尼+阿来替尼治疗。IRC评估的中位PFS达到7.3个月(95%CI:3.7-12.9), ORR为34%(95%CI:21%~49%),DCR为79%(95%CI:64%~89%),中位OS达28.4个月(95% CI:16.2~NR)[13]。前瞻性观察性WJOG11919L/ABRAID研究中,队列A共纳入102例可评估疗效的患者。阿来替尼治疗后序贯布格替尼的中位PFS为6.51个月;无论是否存在ALK耐药突变(包括G1202R),布格替尼均显示出疗效,且安全性特征与既往报告一致,未增加其毒副作用[14]。对于克唑替尼经治的ALK阳性NSCLC患者,布格替尼同样展现出持久的疗效和可控的安全性。在ALTA 1/2期研究中,中位随访27.7个月,B组(布格替尼180mg/d,7天90mg/d导入)经独立评审委员会(IRC)评估的中位PFS达16.7个月[15]。此外,真实世界数据显示,在先前使用克唑替尼、阿来替尼、塞瑞替尼、洛拉替尼治疗失败的患者,布格替尼的中位治疗持续时间亦可达到7.5个月~10.3个月[16]。
更重要的是,布格替尼不仅具备确切的疗效,更拥有良好的安全性特征。一项评估多种 ALK-TKI一线治疗安全性的 Meta 分析显示,布格替尼1~5级不良事件的累积排名曲线下面积最小,提示其药物毒性较低[17]。优异的安全性确保了患者能够足量、足疗程地坚持治疗,避免了因不耐受而减量或中断治疗带来的耐药风险,从而真正实现了疗效与安全性的双重获益,为ALK阳性NSCLC患者的全程管理提供了坚实保障。
小结
现阶段,晚期NSCLC的诊疗策略正逐步整合精准医学、联合治疗与全程管理三大理念。临床策略也从单纯的“等待耐药后处理”转向“主动延缓耐药发生”与“耐药后精准决策” 并重的双重管理模式。其中,靶向治疗与局部治疗的联合策略,为延缓ALK-TKI耐药、延长有效治疗时间提供了新的可行路径。而在患者全程管理过程中,MDT协作不可或缺。汇聚多学科智慧,制定个体化方案,方能真正实现疗效提升与患者生活质量改善的双重目标。
1. Camidge DR, et al. Association of Depth of Target Lesion Response to Brigatinib With Outcomes in Patients With ALK Inhibitor-Naive ALK+ NSCLC in ALTA-1L. ASCO 2022 9072.
2. Camidge DR, et al. Brigatinib Versus Crizotinib in ALK Inhibitor-Naive Advanced ALK-Positive NSCLC: Final Results of Phase 3 ALTA-1L Trial. J Thorac Oncol. 2021 Dec;16(12)2091-2108.
3.Yasir Y Elamin, et al. BRIGHTSTAR Local Consolidative Therapy with Brigatinib in Tyrosine Kinase Inhibitor-Naïve ALKRearranged Metastatic NSCLC. 2023 WCLC. OA22.04.
4. Delmonte A, et al. Real-world treatment patterns and effectiveness of subsequent treatments following first-line (1L) brigatinib for patients with anaplastic lymphoma kinase positive (ALK+) non-small cell lung cancer (NSCLC) from ALTA-1L. 2024 ELCC. 38P.
5.Poei D, Ali S, Ye S, Hsu R. ALK inhibitors in cancer: mechanisms of resistance and therapeutic management strategies. Cancer Drug Resist. 2024;7:20. Published 2024 May 23. doi:10.20517/cdr.2024.25
6. Zhang S, et al. The Potent ALK Inhibitor Brigatinib (AP26113) Overcomes Mechanisms of Resistance to First- and Second-Generation ALK Inhibitors in Preclinical Models. Clin Cancer Res. 2016;22(22):5527-5538.
7. Horn L, et al. Monitoring Therapeutic Response and Resistance: Analysis of Circulating Tumor DNA in Patients With ALK+ Lung Cancer. J Thorac Oncol. 2019;14(11):1901-1911.
8.Ding M, et al. Clin Lung Cancer. 2019 May;20(3):e229-e232.
9. Latif H. Transl Lung Cancer Res. 2020 Oct;9(5):2145-2148.
10. Ou SI, et al. J Thorac Oncol. 2022 Dec;17(12):1404-1414.
11. Yoshida T, et al. Cancer Sci. 2023;114(9):3698-3707.
12.Lin JJ. J Thorac Oncol. 2018 Oct;13(10):1530-1538.
13. Yoshida T, et al. Cancer Sci. 2023;114(9):3698-3707
14. Prospective observational study of brigatinib after alectinib in ALK-positive, non-small cell lung cancer: Efficacy and biomarker analyses from cohort A of the WJOG11919L/ABRAID trial. 2025 ESMO, 1845MO.
15. Scott N Gettinger, et al. Long-Term Efficacy and Safety of Brigatinib in Crizotinib-Refractory ALK+ NSCLC: Final Results of the Phase 1/2 and Randomized Phase 2 (ALTA) Trials. JTO Clin Res Rep. 2022 Jul 31;3(9):100385.
16. Lin, Huamao M, et al. Real-world treatment duration in ALK-positive non-small-cell lung cancer patients receiving brigatinib through the early access program. Future oncology (London, England) vol. 16,15 (2020): 1031-1041.
17. Luo Y, et al. Comparative safety of anaplastic lymphoma kinase tyrosine kinase inhibitors in advanced anaplastic lymphoma kinase-mutated non-small cell lung cancer: Systematic review and network meta-analysis. Lung Cancer. 2023 Oct:184:107319.11.
排版编辑:肿瘤资讯-momo











 苏公网安备32059002004080号
苏公网安备32059002004080号


