多发性骨髓瘤(MM)是一种由克隆性浆细胞异常增殖所致的血液系统恶性肿瘤。随着蛋白酶体抑制剂、免疫调节剂及CD38单克隆抗体(单抗)等新型药物的临床应用,新诊断MM(NDMM)的诊疗策略已逐步演变为以“诱导治疗序贯持续治疗”为核心的全程管理策略。在此模式下,诱导治疗后如何通过安全、有效的持续治疗方案巩固疗效,已成为影响患者远期预后的关键环节。
伊沙佐米作(I)作为一种口服蛋白酶体抑制剂,因其神经毒性较低、对肾功能影响小以及口服给药便利等优势,已成为MM持续治疗阶段的重要选择之一。在临床实践中,以达雷妥尤单抗(Dara)为代表的CD38单抗诱导治疗后序贯伊沙佐米持续治疗的策略逐步得到应用。该方案借助Dara快速降低肿瘤负荷的优势,再通过伊沙佐米实现长期疾病控制,兼具安全性与便捷性。为此,【肿瘤资讯】特邀中国医科大学附属第一医院张蕊教授与首都医科大学附属北京积水潭医院鲍立教授,基于三例具有代表性的MM病例,系统解析“Dara诱导治疗序贯I-base持续治疗”策略在真实临床环境下的疗效与安全性,以期为该方案在NDMM个体化治疗中的应用提供实践依据与临床参考。
病例一
患者概况
患者男性,58岁,2026年2月因“确诊多发性骨髓瘤3年余,规律治疗后复诊”就诊。患者2022年于外院确诊多发性骨髓瘤,初诊时伴肾功能轻度异常,无明显骨痛、贫血,确诊后规范行诱导治疗及自体造血干细胞移植(ASCT),为评估治疗效果及后续管理复诊。既往无特殊基础疾病,家族史无特殊。
检查结果
生化:肌酐 168μmol/L↑。
血清游离轻链:κ/λ比值12.8↓。
M蛋白:18g/L↑。
血免疫固定电泳:IgA-λ型M蛋白阳性。
骨髓细胞涂片:骨髓浆细胞比例异常升高。
诊断
1. 多发性骨髓瘤(IgA-λ型,DS分期Ⅲ期,ISS分期Ⅱ期);2. 肾功能不全。
治疗经过
2022年11月~2023年3月:予DVD方案(达雷妥尤单抗+硼替佐米+地塞米松)诱导治疗6个周期。
2023年3月:行自体外周血造血干细胞动员与采集。
2023年6月:行ASCT治疗。
2023年6月至今:予IRD方案(伊沙佐米+来那度胺+地塞米松)持续治疗,定期复诊。
疗效与转归
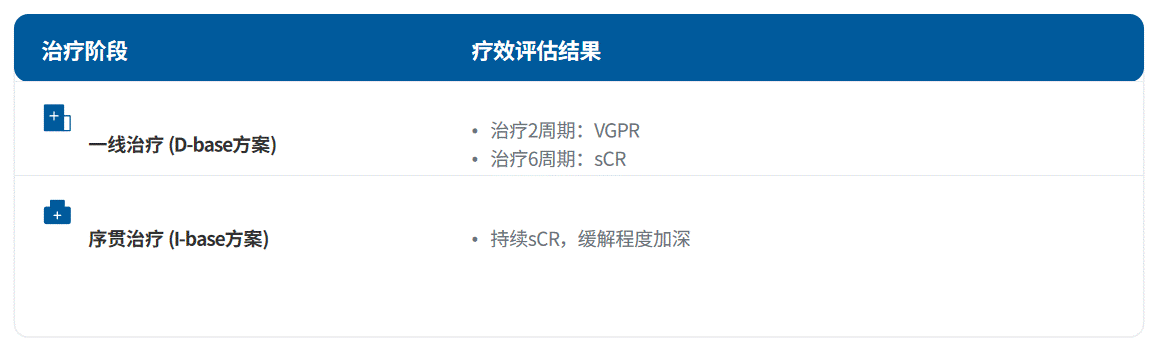
DVD方案诱导治疗2周期后,患者疗效评估达非常好的部分缓解(VGPR),诱导6周期后达严格意义的完全缓解(sCR)。行ASCT后序贯IRD方案持续治疗,多次复查均持续维持sCR(图1)。2026年2月复诊,肾功能较初诊明显改善,无治疗相关不良反应,实现长期深度缓解。
病例小结
该例为中年NDMM患者,初诊伴轻度肾功能不全,无其他基础疾病,适合ASCT治疗。采用DVD方案诱导治疗后快速实现sCR,为移植创造了良好条件,移植后序贯伊沙佐米为基础的IRD方案持续治疗,持续保持深度缓解(sCR)近3年,且肾功能得到改善,无神经毒性、感染等不良事件。该病例证实,对于适合移植的中年MM患者,“Dara诱导序贯I-base持续治疗”是高效的治疗路径,伊沙佐米对肾功能影响小、神经毒性低的优势,使其成为移植后持续治疗的理想选择,可有效延长深度缓解时间,改善患者远期预后。
病例二
患者概况
患者女性,83岁,2025年9月因“血细胞降低3个月”就诊。3个月前无明显诱因出现头晕乏力、皮肤淤青,症状持续不缓解,外院完善骨髓活检后考虑浆细胞骨髓瘤,为求进一步诊治收住入院。既往合并高血压、冠心病、2型糖尿病多年,无特殊个人史及家族史。
检查结果
血常规:白细胞 2.17×10⁹/L↓,红细胞 2.32×10¹²/L↓,血红蛋白 73g/L↓,血小板 116×10⁹/L↓。
生化:葡萄糖 6.48mmol/L↑,丙氨酸氨基转移酶 48U/L↑,天门冬氨酸氨基转移酶 58U/L↑,白蛋白 37.4g/L↓,乳酸脱氢酶 331U/L↑。
免疫检查:IgG 3.93g/L↓,IgM 0.1g/L↓。骨髓组织活检:浆细胞骨髓瘤伴纤维组织增生,符合多发性骨髓瘤病理特征。
骨髓组织活检:浆细胞骨髓瘤伴纤维组织增生,符合多发性骨髓瘤病理特征。
诊断
1. 多发性骨髓瘤(IgD-λ型,DS分期Ⅲ期,ISS分期Ⅲ期);2. 高血压;3. 冠心病;4. 2型糖尿病。
治疗经过
2025年9月~2025年12月:予个体化剂量DRD方案(达雷妥尤单抗+来那度胺+地塞米松)诱导治疗,及时根据不良反应与病情变化调整方案。
2026年1月15日至今:门诊随访病情稳定,转换为伊沙佐米单药维持治疗。
疗效与转归
经DRD方案诱导及剂量调整后,肿瘤负荷得到有效控制。转换伊沙佐米单药口服持续治疗后,病情稳定无进展,末梢神经症状完全缓解,无心脏不适、感染、出血等不良反应,耐受性良好,患者生活质量得到有效保障。
病例小结
该例为高龄NDMM患者,合并高血压、冠心病、2型糖尿病多重基础疾病,体能状态差。采用DRD方案诱导治疗后,序贯伊沙佐米单药口服持续治疗,既实现了肿瘤负荷的有效控制,又最大程度降低了治疗相关风险。该病例证实,“Dara诱导序贯I持续治疗”策略可适配高龄合并基础疾病的MM患者,通过个体化剂量调整与方案转换,能在疗效与安全性之间实现良好平衡,且口服伊沙佐米显著提升了老年患者的治疗依从性。
病例三
患者概况
患者男性,78岁,患者2026年1月因“确诊多发性骨髓瘤7月余”就诊。患者于2025年5月经骨穿、FISH检测后确诊多发性骨髓瘤,予DRD方案初始治疗后,为行系统规范治疗收住入院。既往无重大疾病史,家族史无特殊。
检查结果
血常规:白细胞 0.34×10⁹/L↓,红细胞 3.68×10¹²/L↓,血红蛋白 117g/L↓,血小板 381×10⁹/L↑。
生化:IgA 5.10g/L↑,IgG 3.94g/L↓,IgM 0.13g/L↓。
血清游离轻链:κ 29.1mg/L,λ 41.70mg/dl,κ/λ比值3.00↓。
免疫固定电泳:IgA阳性伴κ型单克隆免疫球蛋白,IgG阳性。
骨髓穿刺活检:浆细胞骨髓瘤。
FISH检测:(1q21)扩增、RB1位点缺失、D13S318位点缺失、P53位点扩增,伴多重高危遗传学异常。
诊断
1. 多发性骨髓瘤(IgA-κ型)。
治疗经过
2025年6月~2025年12月:予DRD方案(达雷妥尤单抗+地塞米松+来那度胺)诱导治疗6个周期。
2026年1月至今:转换为IRD方案(伊沙佐米+来那度胺+地塞米松)持续治疗,28天为1个周期。
疗效与转归
DRD方案诱导治疗期间,患者骨痛症状得到有效缓解,无明显治疗相关不良反应。转换至IRD方案持续治疗后,缓解程度进一步加深,无感染、神经毒性、胃肠道不适等不良反应,耐受性良好。
病例小结
该例为78岁老年NDMM患者,伴多重高危遗传学异常。采用DRD方案诱导治疗时,实现了肿瘤负荷的有效控制;后续序贯伊沙佐米为基础的IRD方案持续治疗,进一步巩固疗效,且治疗期间无不良事件。该病例证实,“Dara诱导序贯I-base持续治疗”策略同样适用于伴高危遗传学异常的老年MM患者,通过个体化剂量调整与全口服的IRD方案,可在保证疗效的同时兼顾安全性,为高危老年MM患者的治疗提供了可行路径。


特邀专家
首都医科大学附属北京积水潭医院血液科主任、主任医师、教授
中华医学会北京分会常务委员
首都医科大学血液病学系副主任
中国医药教育协会转化医学专业委员会主任委员
北京围手术期医学研究会血液专业委员会主任委员
北京慢性病防治与健康教育研究会血液病学专业委员会 主任委员
北京市科委医疗卫生领域专家库成员
《癌症发生与治疗(英文)》编辑委员会编辑
中国医科大学附属第一医院血液科 副主任
教授/主任医师/硕士生导师
医学博士
辽宁省医学会血液学分会委员会委员
辽宁省中西医结合学会血液病专业委员会副主任委员
辽宁省抗癌协会淋巴瘤专业委员会委员
中国抗癌协会淋巴瘤整合康复专业委员会委员
中国康复医学会血液病康复专业委员会委员
中国医药教育协会血液学专业委员会委员
辽宁省医学会医疗鉴定专家库成员
《辽宁医学杂志》、《实用临床医药杂志》编委
获辽宁省科技进步2等奖
承担国家自然科学基金1项
[1] Vassilopoulos S, Vassilopoulos A, Kalligeros M, et al. Cumulative Incidence and Relative Risk of Infection in Patients With Multiple Myeloma Treated With Anti-CD38 Monoclonal Antibody-Based Regimens: A Systematic Review and Meta-analysis [J]. Open Forum Infect Dis, 2022,9(11):ofac574.
[2] Xiang Q, Lu M, Chu B, et al. Transition to IRD maintenance after DRD induction significantly deepens response in transplant-ineligible NDMM: A prospective multicenter study [C]. 2025 EHA, Abs25-13212.
[3] Moreau P, Masszi T, Grzasko N, et al. Oral Ixazomib, Lenalidomide, and Dexamethasone for Multiple Myeloma [J]. N Engl J Med, 2016,374(17):1621-1634.
[4] Richardson PG, Hofmeister CC, Rosenbaum CA, et al. Twice-weekly ixazomib in combination with lenalidomide-dexamethasone in patients with newly diagnosed multiple myeloma [J]. Br J Haematol, 2018,182(4):578-587.
[5] Rifkin RM, Girnius SK, Noga SJ, et al. In-class transition (iCT) of proteasome inhibitor-based therapy: a community approach to multiple myeloma management [J]. Blood Cancer J, 2023,13(1):147.
[6] Joshua Richter, Saulius Girnius, Ruemu Birhiray, et al. In-class Transition from Parenteral Bortezomib to Oral Ixazomib in Newly Diagnosed Multiple Myeloma: Analysis of US MM-6 By Number of Treatment Cycles Received [J]. Blood, 2024,144(Supplement 1):4757.
[7] Chaitanya Acharya, Reyka Jayasinghe, Darwin D'Souza, et al. Daratumumab-based quadruplet therapy in functional high-risk relapse/refractory multiple myeloma patients induces changes associated with CD8 T cell signaling, activation and expansion [J]. Blood, 2025,146(Supplement 1):3955.
[8] 伊沙佐米药品说明书.
排版编辑:肿瘤资讯-李鑫











 苏公网安备32059002004080号
苏公网安备32059002004080号


