多发性骨髓瘤(MM)是一种由浆细胞异常增殖驱动的血液系统恶性肿瘤,其治疗已进入以“深度缓解、长期控制、提升生活质量”为核心的全程慢病管理时代。新诊断多发性骨髓瘤(NDMM)患者临床表现高度异质,涉及不同年龄、疾病亚型及风险分层,特别是伴有高危遗传学异常、造血干细胞移植失败或特定轻链亚型者,其治疗方案的选择更需兼顾疗效、安全性与治疗便捷性。
达雷妥尤单抗(Dara)作为靶向CD38的单克隆抗体,凭借其强效抗肿瘤活性,已成为诱导治疗阶段的核心药物之一;伊沙佐米(I)作为新一代口服蛋白酶体抑制剂,具有神经毒性低、给药便利及对肾功能影响小等优势,为MM长期持续治疗提供了理想选择。为进一步验证“达雷妥尤单抗诱导序贯伊沙佐米持续治疗”策略在真实世界多种临床场景中的应用价值,【肿瘤资讯】特邀深圳市第二人民医院李晓清教授与南方医科大学珠江医院李玉华教授,结合三例不同亚型NDMM患者的诊疗过程,深入剖析该策略的临床获益与实践要点,为个体化治疗提供参考。
病例一
患者概况
患者男性,57岁,因“胸壁疼痛5月余”就诊。2024年2月患者因右胸前壁疼痛就诊,检查提示左第8后肋占位性病变,2024年3月骨髓活检确诊浆细胞骨髓瘤,瘤细胞占比80%,为进一步诊治收住入院。患者自起病以来,精神、食欲、睡眠尚可,二便正常,体重无明显变化。
检查结果
血常规:白细胞 2.61×10⁹/L↓,中性粒细胞绝对值 1.06×10⁹/L↓,血红蛋白 122.0g/L↓,血小板 142.0×10⁹/L。
生化:总蛋白 59.2g/L↓,球蛋白 18.8g/L↓,尿素 8.9mmol/L↑,血β2微球蛋白 1.82mg/L↑,免疫球蛋白A 0.38g/L↓,免疫球蛋白G 6.42g/L↓,免疫球蛋白M 0.09g/L↓,补体C1q 10.60mg/dL↓。
血清/尿免疫固定电泳:IgG-κ型M蛋白、IgG-λ型M蛋白等均为阴性。
尿β2微球蛋白:2.32mg/L↑。
骨髓活检:瘤细胞占80%,Kappa:Lambda=490:10,CD38强阳性(80%)
骨髓涂片:原始及幼稚浆细胞占2.2%,骨髓活检示浆细胞小片状分布,CD38强阳性(30%)。
骨髓流式细胞术:异常浆细胞占有核细胞3.74%,强表达CD138、CD38,表达CD56、cKappa,不表达CD45、CD19等。
FISH检测:RB-1/LAMP1基因缺失、IGH:MAF融合基因等检测结果均为阴性。
颈椎、胸椎、腰椎MR:多发椎体及附件类圆形结节灶异常信号,C4/5-C6/7、L3/4-L5/S1椎间盘不同程度膨、突出,T5-6、T11及L5椎体压缩性骨折,考虑多发性骨髓瘤累及并病理骨折。
诊断
1. 多发性骨髓瘤(IgG-κ型,R-ISS分期Ⅱ期)。
治疗经过
2024年3月~2024年5月:予VRd方案(硼替佐米+来那度胺+地塞米松)治疗5个疗程,疗效评估达部分缓解(PR)。
2024年6月~2024年7月:尝试造血干细胞动员,结果失败。
2024年7月~2025年2月:予DVd(达雷妥尤单抗+硼替佐米+地塞米松)治疗6个疗程,疗效评估达完全缓解(CR)。
2025年3月至今:调整为Id方案(伊沙佐米+地塞米松)持续治疗,已完成11个疗程,维持CR状态。
疗效与转归
VRd方案治疗后患者达到PR,骨髓浆细胞比例从80%降至2.2%;经Dara联合方案治疗后,血清及尿免疫固定电泳均转为阴性,骨髓异常浆细胞比例进一步降低,疗效提升至CR;转换为伊沙佐米单药联合地塞米松持续治疗后,患者维持CR,血常规及生化指标逐步恢复正常,骨痛症状完全缓解,未出现明显药物相关不良反应,耐受性良好,可正常完成门诊随访及治疗。
病例小结
该例为移植动员失败的NDMM患者,经初始VRd方案诱导达PR后,采用Dara联合方案进一步深化缓解至CR,后续序贯伊沙佐米为基础的持续治疗方案,实现了长期深度缓解。伊沙佐米的口服便利性有效规避了移植失败后反复住院治疗的负担,其良好的安全性确保了长期治疗的可持续性,充分体现了“Dara诱导序贯I持续治疗”策略在不适合移植或造血干细胞动员失败患者中的临床价值。
病例二
患者概况
患者男性,38岁,因“双侧肋骨及腰背部疼痛1年余”就诊。1年余前患者睡觉翻身时出现双侧肋骨钝痛,后逐渐累及腰背部,近3月疼痛加重,外院胸部CT提示多发骨质密度减低区,疑似多发性骨髓瘤,血清免疫固定电泳发现单克隆免疫球蛋白,为进一步诊治收住入院。患者自起病以来,精神、饮食、睡眠可,大便正常,小便泡沫多,近2月体重减轻10公斤。
检查结果
血常规:白细胞 9.32×10⁹/L,中性粒细胞计数 4.77×10⁹/L,淋巴细胞计数 3.66×10⁹/L↑,血红蛋白 140.0g/L,血小板 327.0×10⁹/L。
生化:血β2微球蛋白 3.31mg/L↑,尿酸 435.6μmol/L↑,免疫球蛋白D 9992.00mg/L↑,补体C3 4.07g/L↑。
血清蛋白电泳:β2球蛋白 15.9%↑。
血清免疫固定电泳:轻链λ型M蛋白弱阳性(+)
尿免疫固定电泳:游离λ型M蛋白阳性(+),其余类型均为阴性。
游离轻链检测:血清游离κ轻链 12.97mg/L,血清游离λ轻链 1354.83mg/L↑,rFLC 0.0096↓;尿游离κ轻链 48.23mg/L↑,尿游离λ轻链 3478.34mg/L↑,rFLC 0.0139↓。
24h尿总蛋白:1915.90mg/24h↑。
尿β2微球蛋白:0.16mg/L↑。
骨髓涂片:浆细胞占1.5%,胞浆丰富,易见空泡。
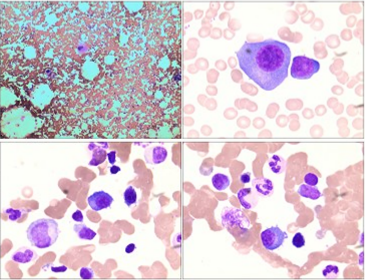
骨髓流式细胞术:异常单克隆浆细胞占有核细胞0.27%,强表达CD138、CD38,表达cLambda,不表达CD45、CD19等。
FISH检测:RB-1/LAMP1基因缺失、IGH:MAF融合基因等检测结果均为阴性。
PET-CT:全身多发溶骨性骨质破坏、局部软组织肿物形成,伴糖代谢增高,SUVmax约7.5,右2前肋病理性骨折。
DR:颅骨、左肱骨头、左锁骨肩峰端、双侧坐骨多发骨质缺损区。
诊断
1. 多发性骨髓瘤(IgD-λ型,DS分期III期A组,ISS分期II期,R2-ISS 1.5分中高危组,伴1q Amp+IGH/CCND1重排);2. 肋骨骨折;3. 感染性发热。
治疗经过
2023年12月~2024年2月:予VRd方案(硼替佐米+来那度胺+地塞米松)治疗2个疗程,复查IgD定量降至192.8mg/L。
2024年2月~2024年12月:调整为Dara+VRd方案(达雷妥尤单抗+硼替佐米+来那度胺+地塞米松)治疗8个疗程,疗效评估达CR。
2025年1月~2025年3月:予Dara+IRd方案(达雷妥尤单抗+伊沙佐米+来那度胺+地塞米松)治疗3个疗程,维持CR。
2025年4月至今:予IRd方案(伊沙佐米+来那度胺+地塞米松)持续治疗,已完成10个疗程,维持CR。
疗效与转归
VRd方案治疗后患者IgD水平显著下降,疼痛症状有所缓解;经Dara联合方案治疗后,血清及尿免疫固定电泳转阴,游离轻链比值恢复正常,骨髓异常浆细胞消失,疗效达到CR;序贯伊沙佐米为基础的持续治疗方案后,患者维持CR状态,骨质破坏相关疼痛完全缓解,免疫球蛋白D水平维持正常,未出现周围神经病变、严重感染等不良反应,生活质量显著提升,可正常回归工作与生活。
病例小结
该例为年轻中高危IgD-λ型NDMM患者,IgD型骨髓瘤临床少见且预后相对较差,经初始VRd方案治疗后疗效不明确,加入Dara后快速达到CR,后续序贯伊沙佐米为基础的持续治疗方案实现长期深度缓解。含伊沙佐米的全口服联合方案,既保证了疗效的持续性,又提升了治疗便利性,适配年轻患者对生活质量的高需求,证实了“Dara诱导序贯I持续治疗”策略在特殊亚型高危NDMM患者中的有效性与安全性。
病例三
患者概况
患者女性,46岁,因“反复胸腰疼4月”就诊。4月前患者弯腰搬重物后出现胸腰部疼痛,弯腰活动受限,2月前疼痛加重并伴腋下放射痛,影响日常生活,2024年1月骨髓细胞学检查示浆细胞占75%,确诊多发性骨髓瘤,接受1疗程VCD方案化疗后,为行后续治疗收住入院。患者自起病以来,精神睡眠一般,食欲食量良好,大便正常,小便正常,体重无明显变化。
检查结果
血常规:白细胞 2.74×10⁹/L↓,中性粒细胞绝对值 1.50×10⁹/L↓,淋巴细胞计数 0.99×10⁹/L↓,血红蛋白 96.0g/L↓,血小板 137.0×10⁹/L。
生化:总蛋白 62.1g/L↓,球蛋白 17.9g/L↓,白/球比例 2.47↑,尿酸 503.4μmol/L↑,血β2微球蛋白 4.50mg/L↑,钙 2.58mmol/L↑,免疫球蛋白A 0.35g/L↓,免疫球蛋白G 4.72g/L↓,免疫球蛋白M 0.11g/L↓,补体C4 0.417g/L↑,补体C1q 11.50mg/dL↓。
血清免疫固定电泳:轻链λ型M蛋白阳性(+)。
尿免疫固定电泳:游离λ型M蛋白阳性(+)。
尿β2微球蛋白:0.31mg/L↑。
骨髓涂片:浆细胞占75.0%,以幼稚浆细胞为主,可见双核浆细胞。
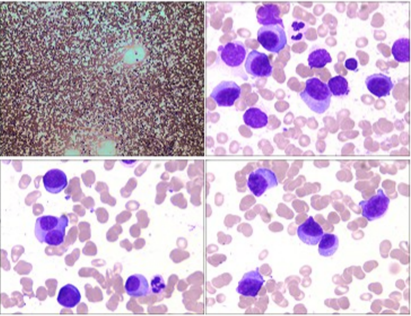
骨髓流式细胞术:异常浆细胞占有核细胞63.14%,强表达CD38,表达CD138、CD56、cLambda,部分表达CD19,不表达CD45、CD27等。
FISH检测:CKS1B基因扩增阳性,CCND1:IGH融合基因阳性。
胸部CT:双侧部分肋骨、颈胸椎及附件多发骨质异常,骨髓瘤改变不除外;右侧第6、7前肋、右侧第8后肋局部骨质欠规整。
诊断
1. 多发性骨髓瘤(λ轻链型,DS分期ⅢA期,ISS分期Ⅱ期,R-ISS分期Ⅱ期);2. 轻度脂肪肝;3. 左肾结石。
治疗经过
2024年1月:予VCD方案(硼替佐米+环磷酰胺+地塞米松)治疗1个疗程,治疗后血象白细胞下降,取消第8天环磷酰胺治疗。
2024年2月~2025年2月:调整为DVd(达雷妥尤单抗+硼替佐米+地塞米松)治疗5个疗程,疗效评估达CR。
2025年3月至今:予伊沙佐米单药维持治疗,已完成11个疗程,维持CR。
疗效与转归
VCD方案治疗后患者出现骨髓抑制,调整为Dara联合方案后,骨髓抑制风险显著降低,治疗后血清及尿免疫固定电泳转阴,骨髓浆细胞比例从75%降至正常,疗效达到CR;转换为伊沙佐米单药持续治疗后,患者维持CR状态,血常规、生化指标恢复正常,胸腰部疼痛症状完全缓解,仅在治疗初期出现轻度胃肠道反应,可自行缓解,无严重不良反应发生,治疗依从性良好。
病例小结
该例为λ轻链型NDMM患者,初始VCD方案治疗后出现骨髓抑制,更换达雷妥尤单抗联合方案后快速达到CR,后续采用伊沙佐米单药实现长期深度缓解。伊沙佐米单药持续治疗方案既保证了疗效,又最大程度降低了用药负担与不良反应风险,其口服给药方式显著提升了患者治疗便利性,为轻链型骨髓瘤患者提供了安全有效的长期管理选择,进一步丰富了“Dara诱导序贯I持续治疗”策略的临床应用场景。


特邀专家
深圳市第二人民医院(深圳大学第一附属医院) 血液内科
中国抗癌协会血液肿瘤整合康复专业委员会 常务委员
中国临床肿瘤学会(CSCO)骨髓瘤专家委员会青年学组 委员
广东省医学会血液病学分会青年委员会 副主任委员
广东省预防医学会血液学分会 常务委员
广东省医学会细胞治疗学会 委员
广东省健康教育协会血液学分会 常务委员
广东省抗癌协会淋巴瘤专业委员会 委员
广东省健康管理学会血液病学专委会 委员
深圳市抗癌协会罕见血液肿瘤专业委员会 副主任委员
深圳市抗癌协会罕见血液肿瘤专业委员会 副主任委员
深圳市抗癌协会白血病专业委员会 副主任委员
深圳市医师协会肿瘤免疫治疗分会 副主任委员
深圳市医师协会血液病学分会 常务委员
深圳市医学会血液病学分会专业委员会 工作秘书
深圳市医师协会淋巴瘤专业委员会 常务委员
南方医科大学珠江医院血液科主任
精准免疫细胞治疗技术广东省工程研究中心 负责人
中国医师协会血液科医师分会 常务委员
中国研究型医院学会血液病精准诊疗专业委员会 副主任委员
中国抗癌协会血液肿瘤整合康复专业委员会 副主任委员
广东省医师协会血液科医师分会 主任委员
广东省医学会血液病学分会 副主任委员
广东省基层医药学会血液学分会主任委员
《血栓与止血学》编委常委
《临床血液学》、《中国肿瘤生物治疗》、《blood(中文版)》《Organ Medicine》编委
研究方向:血液肿瘤免疫治疗
研究成果:承担国家自然科学基金、省市级等科研项目20余项;授权国家发明专利10项,美国发明专利1项;在国内外期刊发表论文100余篇,其中Nature Nanotechnology、Nature Biomedical Engineering、Proc Natl Acad Sci US等重要SCI杂志收录70余篇;先后获军队科技进步二等奖,广东省科技进步三等奖,广东医学科技二等奖,中国女医师五洲女子科技奖等;主编/参编专家共识或指南14部;主编/副主编专著3部
[1] Xiang Q, Lu M, Chu B, et al. Transition to IRD maintenance after DRD induction significantly deepens response in transplant-ineligible NDMM: A prospective multicenter study[J]. Blood, 2025,146(Supplement 1):4059.
[2] Moreau P, Masszi T, Grzasko N, et al. Oral Ixazomib, Lenalidomide, and Dexamethasone for Multiple Myeloma[J]. N Engl J Med, 2016,374(17):1621-1634.
[3] Vassilopoulos S, Vassilopoulos A, Kalligeros M, et al. Cumulative Incidence and Relative Risk of Infection in Patients With Multiple Myeloma Treated With Anti-CD38 Monoclonal Antibody-Based Regimens: A Systematic Review and Meta-analysis[J]. Open Forum Infect Dis, 2022,9(11):ofac574.
[4] Rifkin RM, Girnius SK, Noga SJ, et al. In-class transition (iCT) of proteasome inhibitor-based therapy: a community approach to multiple myeloma management[J]. Blood Cancer J, 2023,13(1):147.
[5] Andrew Yee, Elizabeth O'Donnell, Omar Nadeem, et al. A randomized phase II study of daratumumab, lenalidomide, ixazomib, and dexamethasone in transplant-ineligible or deferred patients with newly diagnosed multiple myeloma: Alliance Foundation Trial 41 (AFT-41)[J]. Blood, 2025,146(Supplement 1):4053.
[6] Chaitanya Acharya, Reyka Jayasinghe, Darwin D'Souza, et al. Daratumumab-based quadruplet therapy in functional high-risk relapse/refractory multiple myeloma patients induces changes associated with CD8 T cell signaling, activation and expansion[J]. Blood, 2025,146(Supplement 1):3955.
[7] Macro M, Hulin C, Vincent L, et al. Real-world effectiveness of ixazomib combined with lenalidomide and dexamethasone in relapsed/refractory multiple myeloma: the REMIX study[J]. Ann Hematol, 2023,102(8):2137-2151.
排版编辑:肿瘤资讯-清雅











 苏公网安备32059002004080号
苏公网安备32059002004080号


