多发性骨髓瘤(MM)是一种以克隆性浆细胞异常增殖为特征的血液系统恶性肿瘤,目前仍无法治愈。随着蛋白酶体抑制剂(PI)、免疫调节剂(IMiDs)及单克隆抗体等新型药物的广泛应用,新诊断 MM(NDMM)的治疗已形成“诱导治疗序贯持续治疗”的全程管理模式,其中长期安全且有效的持续治疗是巩固诱导疗效、维持深度缓解及延缓疾病进展的关键环节。
伊沙佐米作为新一代口服PI,具有生存获益良好、安全性可控以及给药方式便捷等优势,为NDMM的长期持续治疗提供了理想选择。近年来,“达雷妥尤单抗诱导序贯以伊沙佐米为基础持续治疗”这一策略在真实世界中积累了一定证据,展现出疗效与安全性的综合优势,尤其为伴有合并症患者的长期管理提供了可行路径。
为深入探讨该序贯治疗模式在真实世界中的临床价值,【肿瘤资讯】特邀南京医科大学附属无锡人民医院王菱菱教授与南通大学附属医院黄红铭教授,结合两例NDMM病例,对达雷妥尤单抗诱导后序贯以伊沙佐米为基础的持续治疗的诊疗过程、疗效与安全性进行系统剖析与讨论。
病例一
患者概况
患者男性,60岁,因“恶心呕吐伴少尿一月”于2022年3月入院。
检查结果
血常规:WBC 5.43×109/L,HGB 96 g/L↓,PLT 232×109/L。
生化:血钙3mmol/L↑,白蛋白48.9g/L,球蛋白29.7g/L,肌酐841umol/L↑,LDH 356U/L,肾小球滤过率 5.7ml/min/1.73m²↓。
免疫球蛋白:IgA 0.28g/L↓,IgG 5.9g/L↓,IgM 0.25g/L↓;β2微球蛋白:21.34mg/L↑。
血清游离轻链:κ 3.79g/L↑,λ 7.97g/L↑,κ/λ 0.03。
24小时尿蛋白定量:0.54g↑。
免疫固定电泳+轻链:IgD-λ型。
全身低剂量CT:部分腰椎椎体、骨盆骨质密度不均伴骨质破坏。
双肾B超:双肾回声改变(右肾明显),右侧肾动脉血流阻力指数增高。
骨髓涂片:全片瘤细胞异常增生,占43.5%,该类细胞外形不规则,胞浆较丰富,兰色或火焰色,核圆形,偏位,核染色质较细致,可见核仁1~2个,可见双核型瘤细胞。
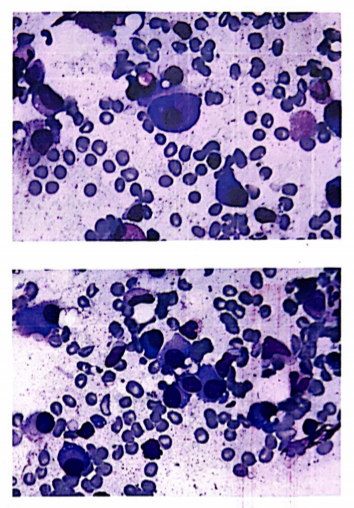
骨髓活检:骨髓增生较活跃(60%),异常浆细胞增多(40%),胞体中等大,胞浆丰富,胞核圆形或略不规则,染色质粗,粒红系各阶段细胞可见,以中幼及以下阶段细胞为主,巨核细胞数量及形态大致正常,分叶核为主:少量淋巴细胞散在分布。网状纤维染色(MF-1级)。
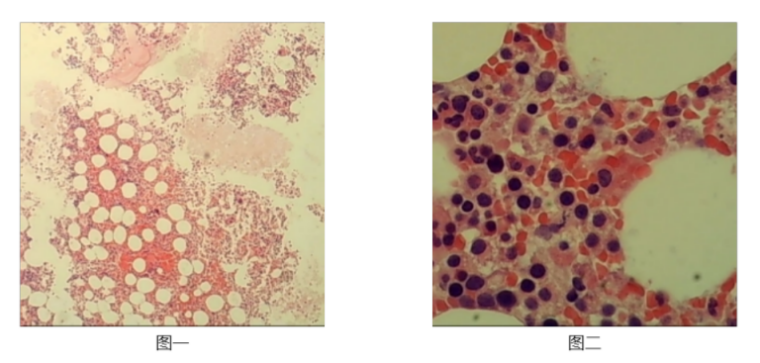
免疫分型:免疫组化示浆细胞:CD38+,CD138+,Kappa-,Lambda+,MUM+,CyclinD1+,CD45-,CD56-,CD20-,Ki67阳性率约10%。标本中可见单克隆浆细胞占有核细胞的10.86%,符合浆细胞肿瘤表型:流式检测中浆细胞易被破环。
FISH:CKS1B基因扩增;IgH基因重排。
染色体:46, XY[20]。
诊断
1.多发性骨髓瘤(IgD-λ型,DS Ⅲ期B组,ISS Ⅲ期);2.肾功能不全;3.多发性骨质破坏。
治疗经过
诱导治疗(2022年3月~6月):予DVD方案(达雷妥尤单抗+硼替佐米+地塞米松)治疗3个周期,同时行血液透析、骨病治疗、抗凝治疗及病毒预防,疗效评估达完全缓解(CR),肾功能部分恢复,尿量正常,脱离血液透析治疗。但出现周围神经病变(PN)。
方案调整(2022年7月~10月):调整为DID方案(达雷妥尤单抗+伊沙佐米+地塞米松)治疗3个周期。
持续治疗(2022年11月起):PN症状较前好转,来那度胺25mg qod口服,予IRD(伊沙佐米+来那度胺+地塞米松)方案持续治疗至今。
疗效与转归
患者接受IRD方案持续治疗后,持续维持CR状态。2023年1月微小残留病(MRD)检测未见单克隆浆细胞;2024年3月复查提示骨髓像仍处缓解状态,2025年6月复查提示仍维持缓解,治疗耐受性良好。
病例小结
该例合并肾功能不全的NDMM患者,经含达雷妥尤单抗的方案诱导治疗达CR后,因出现PN而调整为以达雷妥尤单抗联合伊沙佐米(DID)的治疗方案。后序贯全口服IRD方案持续治疗,不仅长期维持了MRD阴性的深度缓解状态,且安全性表现良好,治疗期间未出现神经毒性加重。此外,口服给药方式显著提升了治疗便利性与患者依从性,契合MM的长期慢病管理理念。
病例二
患者概况
患者男性,52岁,因“腰背部疼痛二年,加重伴活动受限半月”于2024年5月收住骨科,后转入血液科。
检查结果
血常规:WBC 5.21×109/L,HGB 76g/L↓,PLT 188×109/L,CRP 6.9mg/L。
生化:血钙2mmol/L,白蛋白39.3g/L↓,球蛋白21.6g/L,肌酐274.5umol/L↑,LDH 155U/L,肾小球滤过率 21.9ml/min/1.73m²↓。
免疫球蛋白:IgA 0.28g/L↓,IgG 5.61g/L↓,IgM 0.17g/L↓。
24小时尿蛋白定量:6.84g。
血清游离轻链:κ 32.70mg/L↑,λ 30200.00mg/L↑,κ/λ 0.00↓。
尿游离轻链:κ/λ 47.87↑
免疫固定电泳:血清及尿中均检测到单克隆λ轻链。
全身低剂量CT:胸12及腰2椎体变扁;颅骨、两侧肋骨及部分颈胸腰椎椎体、骨盆骨质密度不均伴骨质破坏;颅内CT平扫目前未见明显异常;颈部平扫未见明显异常;两肺少许条索灶;两肺微小结节。
胸腰椎MR:胸腰椎椎体及附件、骨盆多发异常信号;腰2、3、5、胸11、12椎体压缩性骨折,腰3椎体水平椎管变窄;腰椎退变。
骨髓涂片:浆细胞明显增生,考虑多发性骨髓瘤。
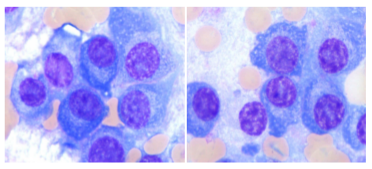
免疫分型:可见单克隆浆细胞占有核细胞的77.23%。表达:CD38,CD138,CD28,部分表达CD20dim,CD200,CD13,不表达CD19,CD56,CD117。
FISH:1q21扩增阳性;RB1、D13S319缺失探针阳性。
染色体:46, XY[3]。
诊断
1.多发性骨髓瘤(λ型,DS Ⅲ期B组,R-ISS Ⅲ期,R2-ISS Ⅲ期;中高危组);2.肾功能不全;3.胸腰椎多发压缩性骨折;4.高钙血症;5.血液透析状态。
治疗经过
诱导治疗(2024年5月~9月):予DVD方案(达雷妥尤单抗+硼替佐米+地塞米松)治疗4个周期,疗效评估达CR。肾功能部分恢复,脱离血液透析治疗,但治疗后出现PN。
方案调整(2024年9月~12月):调整为DID方案(达雷妥尤单抗+伊沙佐米+地塞米松)治疗5个周期。
持续治疗(2025年1月起):PN症状较前好转,来那度胺25mg qod口服,予IRD(伊沙佐米+来那度胺+地塞米松)方案持续治疗至今。
疗效与转归
患者序贯以伊沙佐米为基础的持续治疗方案后,疗效持续为CR,血清免疫固定电泳持续阴性,MRD 检测未见异常浆细胞,肾功能稳定,未出现显著神经毒性或感染事件,整体耐受性良好。
病例小结
该例为中高危NDMM患者,合并肾功能不全、多发骨折,体能状态差。经达雷妥尤单抗联合方案诱导治疗达CR后,序贯以伊沙佐米为基础的持续治疗方案,实现了持续维持CR,且安全性良好,进一步证实了该序贯策略在高危、合并多器官损伤NDMM患者中的临床价值。


特邀专家
南京医科大学附属 无锡市人民医院血液科
南京医科大学讲师
江苏省医学会血液学分会白血病组成员
无锡市医学会血液学分会青委副主任委员
无锡市医学会血液分会移植组秘书
第一作者身份先后在中华血液学杂志、多篇SCI等杂志上发表十余篇科研论文
主持参与省级、市级、南医大科研项目
江苏省医学会血液学会常务委员
江苏省医师协会血液学会委员
中华医学会血液学分会浆细胞组委员
中国女医师协会浆血液专委会浆细胞学组委员
中国少见浆细胞病协作组委员
江苏省医学会血液分会浆细胞学组委员
江苏省研究性医院学会浆细胞病专委常委
江苏省研究性医院学会CART专委委员
南通市抗癌协会血液肿瘤专委会候任主委
在国内外杂志通讯或一作发表论文50余篇,其中SCI论文30余篇,参编著作2部。主持国家级课题两项,省级课题两项,市、院级课题数项。曾获上海市医学科技奖二等奖,中华医学科技奖二等奖,江苏省医学科技奖二等奖,南通市科技进步奖三等奖,南通市青年科技奖。美国Ohio州立Toledo大学访问教授,江苏省“六大”高峰人才,江苏省“333”第三层次人才,南通市“226”第二层次人才。
[1] Qiuqing Xiang, Minqiu Lu, Bin Chu, et al. Transition to IRD maintenance after DRD induction significantly deepens response in transplant-ineligible NDMM: A prospective multicenter study. Blood 2025; 146 (Supplement 1): 4059.
[2] Rifkin RM, Girnius SK, Noga SJ, et al. In-class transition (iCT) of proteasome inhibitor-based therapy: a community approach to multiple myeloma management. Blood Cancer J. 2023 Sep 19;13(1):147.
[3] Chaitanya Acharya, Reyka Jayasinghe, Darwin D'Souza, et al. Daratumumab-based quadruplet therapy in functional high-risk relapse/refractory multiple myeloma patients induces changes associated with CD8 T cell signaling, activation and expansion. Blood 2025; 146 (Supplement 1): 3955.
[4] Andrew Yee, Elizabeth O'Donnell, Omar Nadeem, et al. A randomized phase II study of daratumumab, lenalidomide, ixazomib, and dexamethasone in transplant-ineligible or deferred patients with newly diagnosed multiple myeloma: Alliance Foundation Trial 41 (AFT-41). Blood 2025; 146 (Supplement 1): 4053.
[5] Rifkin RM, Girnius SK, Noga SJ, et al. In-class transition (iCT) of proteasome inhibitor-based therapy: a community approach to multiple myeloma management. Blood Cancer J. 2023 Sep 19;13(1):147.
[6] Joshua Richter, Saulius Girnius, RuemuBirhiray, et al. In-class Transition from Parenteral Bortezomib to Oral Ixazomib in Newly Diagnosed Multiple Myeloma: Analysis of US MM-6 By Number of Treatment Cycles Received. Blood 2024; 144 (Supplement 1): 4757.
[7] Richardson PG, Hofmeister CC, Rosenbaum CA, et al. Twice-weekly ixazomib in combination with lenalidomide-dexamethasone in patients with newly diagnosed multiple myeloma. Br J Haematol. 2018;182(4):578-587.
[8] 伊沙佐米药品说明书.
排版编辑:肿瘤资讯-清雅











 苏公网安备32059002004080号
苏公网安备32059002004080号


