
徐 骁 教授
徐骁,南京医科大学第一附属医院 肝胆 中心,南京
随着肝移植外科技术的进步及围手术期管理体系的完善,受者中远期生存率显著提高,新发恶性肿瘤( DNM )管理的重要性日益凸显。成人肝移植受者 DNM 的发病率约为普通人群的 10 倍,病死率为其 2~3 倍。 DNM 已成为肝移植后生存 >10 年受者最常见的死亡原因。为规范和优化成人肝移植受者 DNM 的诊疗和管理,中华医学会器官移植学分会和中国医师协会器官移植医师分会等组织专家研讨,结合最新循证医学依据和我国临床实践经验,充分借鉴国内外文献,制订《成人肝移植受者新发恶性 肿瘤临床诊疗指南( 2026 版)》(以下简称指南)。该指南系统阐述成人肝移植受者 DNM 的流行病学特征、危险因素、筛查策略及防治原则,提出相关推荐意见,旨在提升肝移植受者术后生命质量及长期生存率。
肝移植; 新发恶性肿瘤; 预防; 诊疗; 管理; 指南
肝移植是治疗终末期肝病的有效手段之一。随着外科技术进步及围手术期管理体系的完善,肝移植受者中远期生存率显著提高,移植后新发恶性肿瘤(de novo malignancy,DNM)的防治重要性日益凸显 [1-3] 。由于长期免疫抑制状态、致癌病毒感染、不良生活习惯等多种因素的综合作用,成人肝移植受者发生DNM的风险显著增高,约为普通人群的10倍 [4‑5] ,且DNM已成为肝移植后生存>10年受者最常见的死亡原因 [6-7] 。为规范和优化成人肝移植受者DNM的诊疗和管理,中华医学会器官移植学分会、中国医师协会器官移植医师分会、中国抗癌协会环境肿瘤学专业委员会组织专家讨论,基于国内外相关文献、循证医学证据并结合我国临床实践经验,制订《成人肝移植受者新发恶性肿瘤临床诊疗指南(2026版)》(以下简称本指南)。本指南采用《牛津大学循证医学中心分级2009版》对推荐意见的支持证据进行评级和推荐强度分级(表1),并在国际实践指南注册与透明化平台(http://www.guidelines-registry.org)进行注册,注册号为PREPARE-2025CN111。

一、指南形成方法
(一)指南专家组建立
本指南由中华医学会器官移植学分会、中国医师协会器官移植医师分会、中国抗癌协会环境肿瘤学专业委员会发起,联合多学科专家共同制订,启动时间为2024年10月13日,定稿时间为2025年12月10日。本指南成立指南专家组,涵盖外科学、内科学、肿瘤学、影像学、流行病学、循证医学等多学科专家。
(二)指南使用者和应用目标人群
本指南适用范围包括但不限于各级医疗机构开展成人肝移植后DNM预防、诊断与治疗。指南的使用者为各级医疗机构的医师及工作人员。指南推荐意见的应用目标人群为接受肝移植的成年受者。
(三)证据检索
本指南对肝移植后DNM相关文献进行系统检索,中英文文献检索关键词包括“肝移植”“新发恶性肿瘤”“流行病学”“危险因素”“筛查”“预防”“免疫抑制剂”“liver transplantation”“de novo malignancy”“epidemiology”“risk factor”“screening”“prevention”“immunosuppressive agent”等;检索数据库包括PubMed、Embase、Cochrane Library、Web of Science、中国知网、万方数据库和维普资讯网络;纳入证据类型包括指南、共识、诊疗规范、系统评价和Meta分析,RCT、非RCT队列研究和病例对照研究等;中英文检索时间为建库至2025年12月,检索语言限定为英文或中文。
(四)推荐意见形成方法
综合考虑临床证据以及我国肝移植受者的偏好价值观、干预措施的利弊等因素,形成证据总结和初拟的推荐意见。为使本指南及推荐意见更加科学且符合临床实践,指南专家组通过邮件邀请成员进行2轮的推荐意见反馈、针对修改意见进行回复和修改,并形成最终推荐意见。
(五)指南发布与更新
本指南发布后,指南专家组将通过以下方式进行传播和推广:(1)在相关学术会议中进行解读。(2)在学术期刊公开发表。(3)通过媒体等进行推广。指南专家组将综合临床实践的需求与证据产生的进展,并参考更新指南报告清单,对本指南进行更新。计划每3年对推荐意见更新一次。
二、DNM的流行病学
(一)发病率
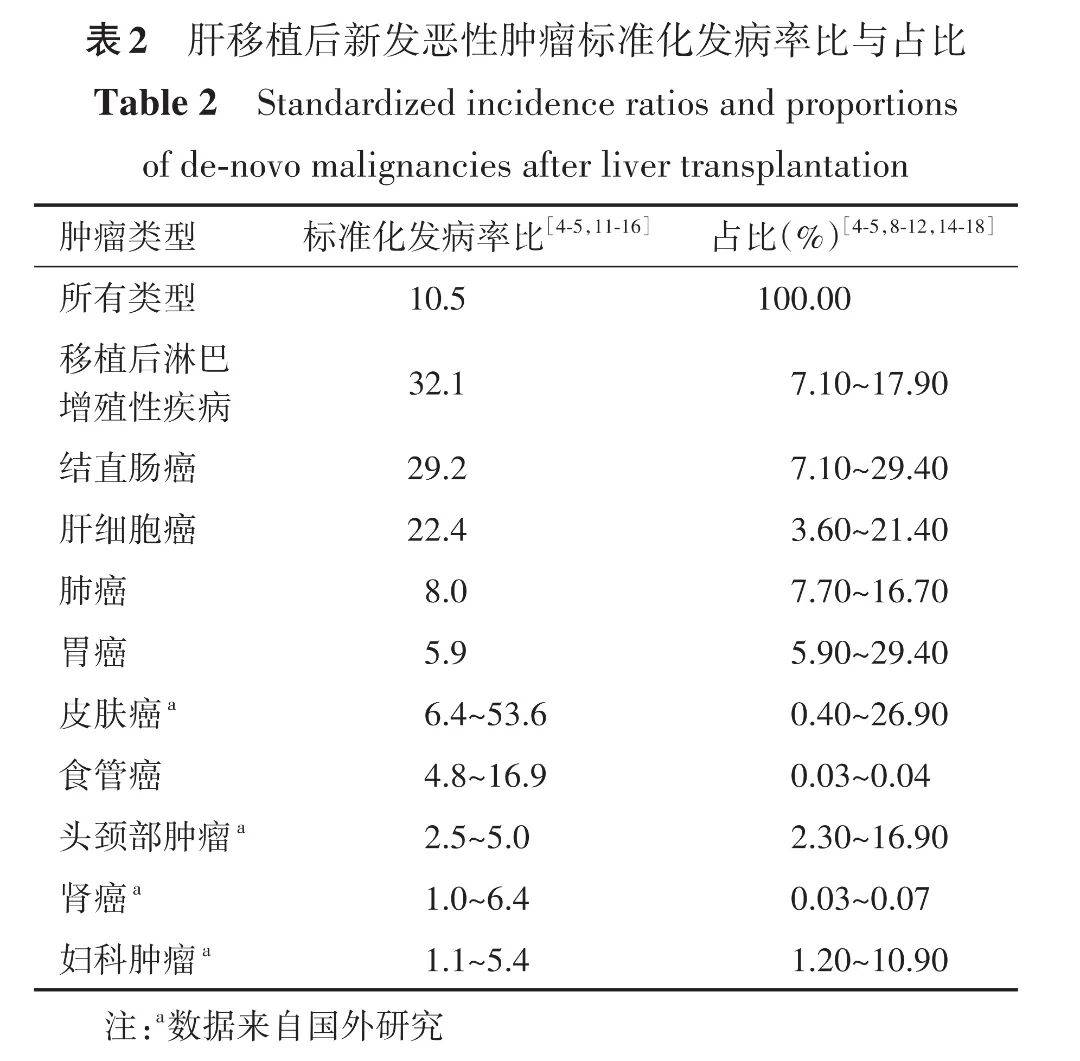
成人肝移植受者DNM的发病率显著高于普通人群,且长期随访数据显示其发病率随时间呈上升趋势 [1,4] 。各类DNM的标准化发病率比(standardized incidence ratio,SIR)及其在肝移植受者恶性肿瘤中的构成比见表2。受免疫抑制方案、地域环境因素及种族差异的影响,DNM的发病率存在显著的地域异质性。已有的研究结果显示:西方国家肝移植受者DNM的总体SIR约为11.6,我国的总体SIR约为10.5 [1,4-6,8-10,19-20] 。
DNM的发病率与多种因素相关,包括长期免疫抑制状态、受者年龄、特殊移植原发病等。长期免疫抑制状态下,肝移植后DNM发病率逐年上升:5、10、20年发病率分别为5.0%~7.7%、10.9%~11.5%、18.8%~22.0% [11,21‑22] 。年龄增长与发病率呈正相关,一项纳入798例肝移植受者的研究结果显示:受者年龄每增加10岁,实体肿瘤DNM发病率提升33% [23] 。原发性硬化性胆管炎(primary sclerosing cholangitis,PSC)或酒精性肝病(alcoholic liver disease,ALD)是发生DNM的高危因素 [12,23] 。
推荐意见1:成人肝移植受者DNM发病率显著高于普通人群,其发病率与长期免疫抑制状态、受者高龄、特殊移植原发病如PSC等因素呈正相关(证据级别:3a,推荐强度:B)。
(二)病死率
DNM是导致成人肝移植受者中远期死亡的重要原因。一项西班牙的多中心临床研究(纳入15998例患者)结果显示:约3.2%的受者在移植后10年内死于DNM [24] 。我国的肝移植数据显示:受者诊断为DNM后的病死率为42.0%~57.1% [5,9,17] 。当罹患相同类型和分期的恶性肿瘤时,肝移植受者的病死率为普通人群的2~3倍 [25] 。其原因可能与长期免疫抑制状态、合并症负担较重等因素有关。
国外研究结果显示:不同类型DNM的标准化死亡率比(standardized mortality ratio,SMR)存在显著差异。按SMR降序排列,部分高SMR的DNM类型包括非黑色素型皮肤癌(SMR为30.9)、食管癌(SMR为8.9)、移植后淋巴增殖性疾病(posttransplant lymphoproliferative disorders,PTLD,SMR为8.6)、肝胆恶性肿瘤(SMR为4.4)、黑色素瘤(SMR为3.2)、口咽部恶性肿瘤(SMR为2.5)、胰腺癌(SMR为2.4)、前列腺癌(SMR为2.3)和结直肠癌(SMR为1.9) [25‑26] 。
肝移植受者常合并多种疾病且存在免疫抑制状态,因此,发生DNM后其对常规抗肿瘤治疗方案不能完全耐受,如免疫检查点抑制剂(immune check-point inhibitor,ICI)治疗。《肝移植术后新发恶性肿瘤的风险评估、预防与管理:国际肝移植协会‑西班牙肝移植学会共识会议指南》提出:肝移植受者常存在多种合并症、面临器官排斥风险并需要联合多种治疗方案,因此,推荐多学科团队(multi-disciplinary team,MDT)诊疗模式 [1] 。MDT模式有助于制订科学、个体化的治疗方案,有效控制肿瘤的同时,最大限度降低移植物丢失风险,从而改善受者的生存预期和生命质量。
推荐意见2:罹患DNM的成人肝移植受者病死率显著高于普通人群,其死亡风险与肿瘤类型相关;应采用MDT诊疗模式,以提高抗肿瘤疗效,降低移植物丢失风险(证据级别:3a,推荐强度:B)。
(三)常见DNM
西方国家常见的DNM类型包括PTLD、皮肤癌(尤其是鳞状细胞癌)、肺癌和胃肠道恶性肿瘤为主。而PTLD和结直肠癌、肝细胞癌等消化系统恶性肿瘤是我国、日本、韩国等东亚国家最常见的DNM类型 [17,27-29] 。
PTLD是实体器官移植后的一类淋巴异常增殖性疾病。肝移植后PTLD的发病率为1.0%~5.5%,SIR为32.1,中位发病时间为术后12个月 [5,30-31] 。PTLD预后较差,1年生存率仅为60.0% [31] 。
新发结直肠癌常发生于肝移植后4年内。一项荟萃分析结果表明:PSC患者肝移植后结直肠癌的年发病率为0.58%,若合并炎症性肠病(inflammatory bowel disease,IBD)则年发病率上升至1.35% [32] 。
新发肝细胞癌的诊断需明确移植时供肝无恶性肿瘤,同时满足以下任一条件:(1)术前受者无肝细胞癌病史,肝移植后于移植肝中发现肝细胞癌。(2)若术前受者罹患肝细胞癌,则需要进行基因型检测证实移植肝的肝细胞癌起源于供肝。然而,基因型检测在临床实践中开展有限,部分新发肝细胞癌被误诊为肝细胞癌复发。一项日本的多中心研究结果表明:在2779例肝移植受者中,术后5例新发肝细胞癌,中位发病时间为9.7年,预后显著优于肝细胞癌复发的患者 [33] 。
三、DNM的危险因素与干预
DNM的主要危险因素包括:长期使用免疫抑制剂、致癌病原体感染、不良生活习惯、代谢性疾病等。此外,不同类型DNM具有其特异性危险因素,见表3。合并多种危险因素会进一步协同促进肿瘤发生和发展 [34] 。

(一)长期使用免疫抑制剂
术后长期使用免疫抑制剂是维持移植物功能的关键,但同时也显著增加DNM的发病率。因此,如何平衡免疫排斥反应与DNM发病率,是肝移植受者长期管理的重要挑战。免疫抑制维持方案相关临床研究证据见表4。
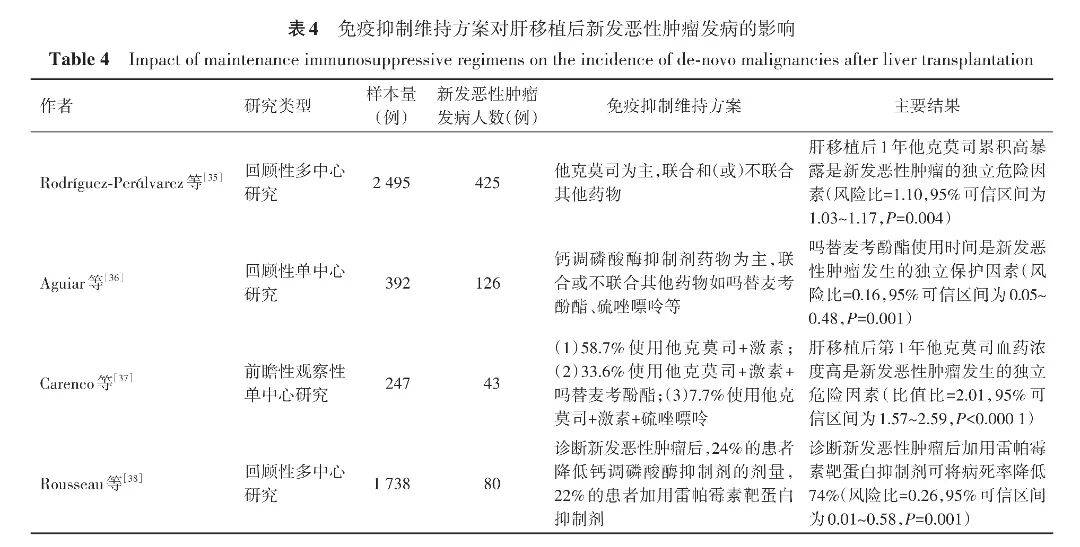
肝移植后免疫抑制诱导治疗常用药物包括抗胸腺细胞球蛋白(antithymocyte globulin,ATG)、抗CD3单克隆抗体和白介素2受体拮抗剂(interleukin-2 receptor antagonists,IL‑2RA)等。ATG和抗CD3单克隆抗体的使用与PTLD和黑色素瘤发病率增加相关。而巴利昔单克隆抗体等IL-2RA的使用尚未被证实会增加DNM发病率 [39-40] 。
免疫抑制维持治疗主要采用以他克莫司、环孢素等钙调磷酸酶抑制剂(calcineurin inhibitor,CNI)为基础的方案。一项法国的前瞻性单中心研究(纳入247例患者)结果显示:肝移植后第1年他克莫司血药浓度高是DNM的独立危险因素( OR =2.01, P <0.0001) [37] 。另一项西班牙的回顾性多中心研究(纳入2495例患者)结果显示:肝移植后1年内平均他克莫司血药浓度高是DNM发生的独立危险因素( HR =1.10, P =0.004) [35] ,提示在维持足够免疫抑制的前提下,应减少他克莫司剂量。同时,一项纳入231例肾移植受者的RCT结果显示:环孢素低剂量组(药物代谢谷水平为75~125ng/mL)术后5年DNM发病率显著低于常规剂量组(药物代谢谷水平为150~250ng/mL)(19%比32%, P =0.03) [41] 。但目前尚缺乏基于RCT的高级别循证医学证据明确CNI药物对肝移植后DNM发病率的影响。
西罗莫司、依维莫司等哺乳动物雷帕霉素靶蛋白抑制剂(mammalian target of rapamycin inhibitor,mTORi)有兼具免疫抑制和抗肿瘤的双重作用 [42-43] 。一项前瞻性RCT(纳入607例患者)结果显示:相较于CNI类药物,肝移植受者使用mTORi可显著降低皮肤癌发病率(6年发病率为4%比9%, P =0.008) [44] 。另外一项纳入21项RCT(合计5876例患者)的荟萃分析结果显示:相较于其他免疫抑制维持方案,肾移植受者使用西罗莫司可显著降低DNM发病率( HR =0.60,95% CI 为0.39~0.93) [45] 。基于《中国肝癌肝移植受者西罗莫司临床应用指南(2024版)》与我国临床实践经验,对于无使用禁忌证且药物耐受良好的受者,可考虑在应用CNI类药物4~6周后,逐步将免疫抑制方案转换为西罗莫司联合低剂量CNI或西罗莫司单药治疗以降低DNM发病率 [46] 。
抗代谢药物主要包括硫唑嘌呤(azathioprine,Aza)和吗替麦考酚酯(mycophenolate mofetil,MMF)。Aza具有光敏性及潜在损害DNA修复机制的作用。已有多项研究表明Aza显著增加实体器官移植术后皮肤鳞状细胞癌发病率 [47-48] 。因此,多数肝移植中心已使用MMF代替Aza。国际心肺移植协会的数据表明:在心肺移植受者中(合计3895例患者),使用MMF的受者DNM发病率显著降低( RR =0.73, P =0.02) [49] 。然而,在肝移植受者中,尚缺乏高质量循证医学证据明确MMF降低DNM风险的作用。MMF的主要价值可能在于其作为CNI减量或撤除方案中的辅助用药,从而间接降低高CNI暴露相关的肿瘤风险。
推荐意见3:在有效预防排斥反应的前提下,减少他克莫司剂量可降低DNM发病率(证据级别:3a,推荐强度:B)。
推荐意见4:肝移植后转换为以西罗莫司为基础的免疫抑制方案可有效降低新发皮肤癌的发病率(证据级别:2b,推荐强度:B)。
(二)致癌病原体感染
有研究证实,EB病毒(Epstein‑Barr virus,EBV)、HBV和(或)HCV以及人乳头瘤病毒(human papillomavirus,HPV)等致癌病原体感染显著增加肝移植受者DNM发病率 [50-52] 。
EBV感染是导致PTLD发生的重要危险因素。EBV基因组可整合至宿主B淋巴细胞内,驱动细胞异常增殖 [53] 。一项美国移植受者科学登记处(纳入40437例患者)的肝移植研究结果显示:EBV抗体阴性受者接受EBV抗体阳性供肝(EBV D + /R ‑ )是发生PTLD的危险因素 [50] 。另一项肾移植领域的研究结果显示:当使用EBV抗体阳性的移植物时,EBV抗体阴性受者发生PTLD的风险显著高于EBV抗体阳性受者 [54] 。为预防PTLD,针对EBV D + /R - 这类高风险人群,需使用阿昔洛韦、更昔洛韦等抗病毒药物、免疫球蛋白等治疗 [31,55] 。
抗HBV和(或)HCV治疗可预防肝细胞癌发生。因HBV肝炎肝硬化接受肝移植治疗的受者,术后应常规接受抗病毒治疗,并且每3~6个月随访1次。针对术后新发HBV感染,若采用普通人群的抗病毒治疗方案,需依据血清HBV-DNA、ALT水平和肝脏疾病严重程度等综合评估抗病毒治疗指征,具体如下:(1)HBV肝炎肝硬化,无论血清HBV-DNA水平。(2)血清HBV-DNA阳性,且符合以下情况之一,①ALT持续异常(>正常值上限),且排除其他原因所致;②无创指标或肝组织学检查,提示肝脏存在明显炎症(Knodell炎症活动度≥2级)或纤维化(Chevallier纤维化分期≥2期);③HBV相关肝外表现,如HBV相关性肾小球肾炎等 [56] 。但在实际临床实践中,若受者血清HBsAg阳性即可考虑积极治疗,并采用高耐药屏障的核苷类似物治疗。而对于HCV‑RNA阳性的受者,均应接受抗病毒治疗 [57] 。
HPV感染是头颈部肿瘤和妇科肿瘤的危险因素。一项纳入664例浸润性宫颈癌患者的多中心研究结果显示:普通人群的子宫颈鳞状细胞癌和子宫颈腺癌中,HPV感染率分别高达97.6%和85.3% [58] 。HPV感染后应采用手术、冷冻、激光等手段破坏可见疣体,联合或不联合干扰素等抗病毒药物治疗。疣体去除后定期随访,最初3个月每2周随访1次,随后可适当延长随访间隔时间,直至末次治疗后6~9个月 [59] 。
(三)不良生活习惯
美国器官共享联合网络数据统计结果显示:肝移植后9%受者重度饮酒,82%受者间歇性饮酒 [60] 。长期大量饮酒是引起DNM的重要危险因素,显著增加食管癌、胃癌等消化道恶性肿瘤的发病率 [61-62] 。此外,ALD也与头颈部肿瘤、皮肤癌、肺癌、结直肠癌、PTLD及肝细胞癌等多种DNM发病率增加相关 [63-64] 。其潜在机制与酒精及其代谢产物乙醛诱导DNA损伤修复能力下降及激活致癌信号通路有关。因此,需积极通过术后宣教,心理支持治疗,给予双硫仑、纳曲酮等药物治疗等方法限制饮酒以预防DNM发生。
吸烟显著增加多种DNM的发病率,包括肺癌、消化道恶性肿瘤、头颈部肿瘤等。一项荷兰的研究结果显示:肝移植后吸烟者(1周≥7支)10年内发生DNM的概率显著高于不吸烟者(12.7%比2.1%, P =0.019) [65] 。值得注意的是,饮酒与吸烟存在显著的协同致癌效应。酒精代谢产生的乙醛以及酒精诱导的细胞色素P450酶活性增强,可促进烟草中的致癌物代谢活化,并降低视黄酸等具有潜在抗癌作用的物质水平,从而协同放大致癌风险。
(四)代谢性疾病
肝移植前存在与术后新发的代谢性疾病不仅显著影响受者的长期生存率和生命质量,同时也增加其发生DNM的风险。
肥胖与乳腺癌、子宫内膜癌、结直肠癌、食管腺癌、胆囊癌及肾癌等多种恶性肿瘤的发生密切相关 [66] 。其潜在机制可能与肥胖相关的慢性低度炎症状态、胰岛素抵抗、脂肪因子分泌失调以及性激素代谢改变等因素有关。肥胖的干预目标为BMI<25kg/m 2 ,首选通过改变生活方式减重,每日能量摄入减至25kcal/kg,但为避免肌肉流失,每日蛋白质摄入量应增至2.0~2.5g/kg [67] 。此外,肥胖可通过药物或外科减重手术进行干预治疗 [68] 。
目前糖尿病每年引发全世界约30万例恶性肿瘤 [69] 。糖尿病的治疗应在改善饮食结构和生活方式的基础上控制血糖,理想目标为空腹血糖<6.7mmol/L(120mg/dL),餐后血糖峰值<8.88mmol/L(160mg/dL)或糖化血红蛋白峰值<7%。同时应调整免疫抑制治疗方案,避免使用糖皮质激素及降低他克莫司剂量 [70] 。
推荐意见5:肝移植后须重视EBV、HBV和(或)HCV等致癌病原体的防治,纠正吸烟、饮酒等不良生活习惯,积极管理肥胖、糖尿病等代谢性疾病,以减少DNM发生(证据级别:3a,推荐强度:B)。
四、DNM术后筛查
规范化的术后筛查是及时发现和早期干预DNM的关键环节。鉴于成人肝移植受者DNM发病率显著高于普通人群,尤其是存在致癌病原体感染、不良生活习惯等危险因素,建议实施更密集的筛查方案,有助于提高DNM的早期检出率,进而改善受者的长期生存率 [71] 。针对不同类型DNM的推荐筛查方案见表5。
推荐意见6:肝移植受者若存在致癌病原体感染、不良生活习惯等危险因素应接受更密集的针对性筛查(证据级别:3b,推荐强度:B)。

(一)PTLD
PTLD筛查首选血清EBV‑DNA定量检测 [72-73] ,通常建议在术后1周内完成基线检测,术后6个月内每个月检测1次,术后第9个月和第12个月各检测1次 [31] 。
对于接受EBV抗体阳性供肝的EBV抗体阴性受者(EBV D + /R ‑ ),若移植后血清EBV‑DNA载量快速升高,应高度警惕PTLD发生的可能,须密切监测发热、腹泻、淋巴结肿大等相关临床症状 [30] ,并考虑适当减少免疫抑制剂用量。当高度怀疑PTLD时,应进行颈、胸、腹及盆腔CT检查扫描,必要时行PET⁃CT检查以评估病变范围和性质。若患者出现头痛、局灶性神经功能缺损或视力改变等神经系统症状,应及时进行头颅MRI检查 [31] 。
推荐意见7:EBV抗体阳性供肝显著增加EBV抗体阴性受者PTLD发病率,术后1年内应定期检测血清EBV-DNA(证据级别:2b,推荐强度B)。
(二)结直肠癌
结直肠癌的筛查推荐采用结肠镜检查并随机活检。IBD患者发生结直肠癌的风险为普通人群的2~3倍 [74-75] 。国际肝移植协会和亚太肝病研究协会建议:患IBD的受者应每年接受1次结肠镜检查 [1,3] 。原发病为PSC的肝移植受者同时合并IBD的风险较高,一项荟萃分析结果显示:北美和欧洲地区PSC患者中IBD的共患率分别约为70%和63% [76] 。因此,对于确诊PSC的肝移植受者,建议行结肠镜检查并随机活检以明确是否合并IBD。即使不伴发IBD,PSC患者相较于普通人群仍具有更高的结直肠癌发病率 [77] ,建议其每3年接受1次结肠镜检查。对于不伴有IBD及PSC的受者,从40岁起应每5~10年接受1次结肠镜检查,并应根据年龄、家族史等个体风险因素调整筛查频率 [78] 。
推荐意见8:患有IBD的肝移植受者应术后每年接受1次结肠镜检查和随机活检,患有PSC但无IBD的受者应术后每3年接受1次结肠镜检查和随机活检(证据级别:2a,推荐强度:B)。
(三)肺癌
低剂量螺旋CT检查(low-dose computed tomography,LDCT)是早期肺癌筛查的重要手段,可显著降低肺癌相关病死率 [79-80] 。虽然X线胸片检查对肺癌有一定诊断价值,但其灵敏度较低,不推荐作为肺癌筛查工具 [81] 。一项欧洲地区多中心临床研究结果显示:肝移植后对吸烟者每年进行LDCT可发现80.0%新发肺癌 [82] 。对于吸烟包年数≥30包年,包括曾经吸烟包年数≥30包年但戒烟不足15年 [83] 的肺癌高风险人群,应每6个月接受1次肺癌筛查,而其余人群每年应至少接受1次肺癌筛查。
(四)皮肤癌
肝移植后新发皮肤癌包括鳞状细胞癌、基底细胞癌和黑色素瘤等,其中鳞状细胞癌和基底细胞癌发病率高,预后较好;而黑色素瘤发病率低,预后较差 [84-85] 。紫外线过度暴露、浅肤色、长期使用免疫抑制剂会增加皮肤癌的发病率 [84,86] 。一项纳入36项研究的荟萃分析发现长期使用免疫抑制剂是发生皮肤癌的危险因素 [87] 。美国肝病研究学会、国际肝移植学会和欧洲肝病学会均建议所有肝移植受者应每年接受1次皮肤检查 [1,3,88] 。
五、DNM治疗
肝移植受者发生DNM后的治疗方案与普通肿瘤患者大致相同,包括手术、放射治疗、化学治疗、分子靶向治疗、ICI治疗等,并且应调整免疫抑制维持方案。应在MDT的科学评估和指导下制订个体化治疗方案、评估疗效与监测不良反应。
(一)调整免疫抑制维持方案
诊断DNM后需及时调整免疫抑制维持方案和用量,减少或停止使用CNI药物,并以mTORi替代 [1,89-90] 。一项纳入38例发生DNM受者的研究结果显示:及时减量或停用CNI药物并转为依维莫司治疗可显著降低受者病死率( HR =0.447, P =0.004) [91] 。但mTORi会导致多种不良反应的发生,如高脂血症、血细胞减少、伤口延迟愈合等,临床上应审慎使用 [92] 。其中血细胞减少可能导致患者无法耐受化疗,而伤口愈合困难增加了手术复杂性。Rousseau等 [38] 的研究结果显示:在180例接受mTORi方案的移植受者中,34%发生了三级不良事件,导致16%的受者暂停化疗。大多数药物不良反应在mTORi减量或停药后可以改善 [93-94] 。目前国外内相关研究较少,缺乏高质量临床循证医学证据,未来有待开展前瞻性多中心临床研究进行验证。
推荐意见9:发生DNM后应及时调整免疫抑制方案,同时警惕药物相关不良反应(证据级别:3b,推荐强度:B)。
(二)手术治疗
早期肿瘤首选手术切除,但肝移植手术史会增加腹部手术的复杂性,需移植科医师术中协助并参与围手术期管理,因此,建议在肝移植中心进行。mTORi不利于手术切口愈合,尤其在高龄、合并糖尿病或营养不良的受者中,需要控制剂量并密切监测术后恢复情况 [95-96] 。Dobrindt等 [97] 的研究纳入14例接受手术治疗的新发上消化道恶性肿瘤患者,结果显示:其中Clavien-Dindo Ⅳ级并发症发生率为21%,1年生存率为50%。早期食管癌、胃癌及结直肠癌可考虑内镜下切除 [96,98] 。Shoji等 [99] 对3例接受肺叶切除术的新发肺癌患者随访8~29个月,结果显示:所有患者生存并且未观察到肿瘤复发。但一项单中心研究发现新发肺癌手术后90d内感染和死亡发生率较高,提示需要优化围手术期管理 [100] 。对于符合移植标准的新发肝细胞癌受者,可考虑再次行肝移植治疗。
推荐意见10:肝移植后DNM的手术治疗应遵循同类肿瘤的常规治疗原则。为保证安全性,建议在移植科医师的协助下开展手术治疗(证据级别:5,推荐强度:D)。
(三)非手术治疗
当病灶难以手术切除时,应个体化选择放射治疗、化学治疗、靶向治疗、ICI治疗等手段延长受者生存时间。
放射治疗可用于根治性或姑息性治疗DNM。研究表明肝移植后放射治疗可安全进行,不会增加病死率 [101] 。一项荟萃分析共纳入103例接受放射治疗的DNM受者,结果显示:中位生存期为8.6~35个月,1年生存率为74%~100%,疗效与普通人群相当 [102] 。此外,常规剂量的放射治疗对移植物具有免疫抑制效应,有利于移植物存活 [2,102] 。
化学治疗和靶向治疗时需要避免药物相互作用产生不良反应。抗代谢免疫抑制剂如Aza和MMF会干扰DNA复制,应避免与其他细胞毒性药物联合使用。紫杉醇和长春花碱应避免与CNI类药物或mTORi联合使用 [103] 。肝功能不全时,在肝脏中代谢的药物需要减少剂量或避免使用,如伊利替康、甲氨蝶呤等。而分子靶向药物如索拉非尼可安全用于肝移植受者 [104-106] 。化学治疗导致的粒细胞减少性发热(febrile neutropenia,FN)指使用化疗药物后引发外周血中性粒细胞<0.5×10 9 /L,或外周血中性粒细胞为(0.5~1.0)×10 9 /L但预计在随后的48h将<0.5×10 9 /L,同时伴有单次口腔温度≥38.3℃或≥38.0℃持续超过1h。FN会增加感染风险,增加治疗费用、延长住院时间,严重者可导致感染性休克、脓毒综合征甚至死亡。肝移植受者的免疫抑制状态是FN发病的危险因素,可参考普通人群的诊治指南进行预防和治疗:例如使用粒细胞集落刺激因子治疗,可降低FN的发病率、持续时间、严重程度及感染率等,有助于完成全剂量强度化疗 [107‑108] 。
ICI治疗肝移植受者仍存在争议,ICI的使用可能诱发移植物排斥反应 [109] 。ICI治疗的相对禁忌证包括:(1)自身免疫性疾病。(2)伴有出血或高出血风险的胃底静脉曲张。(3)特发性肺纤维化、肺炎。(4)有重大心血管疾病、不稳定型心律失常。(5)中度以上腹腔积液或严重感染 [110] 。移植肝组织中PD⁃L1阳性者慎用PD‑1和(或)PD-L1单克隆抗体,可考虑使用细胞毒性T淋巴细胞相关抗原‑4单克隆抗体 [111-113] 。若受者正处于移植物急性排斥反应期,禁用ICI治疗。若经手术、放射治疗、化学治疗等治疗后无法有效控制肿瘤,可考虑使用ICI挽救性治疗 [110] 。ICI治疗可联合贝伐珠单克隆抗体、仑伐替尼、局部治疗等,但不推荐进行双免疫治疗。治疗期间应联合两种及以上免疫抑制剂,降低排斥风险 [114-115] 。
推荐意见11:放射治疗可作为DNM根治性或姑息性治疗手段,不会增加肝移植受者死亡风险(证据级别:4,推荐强度:C)。
推荐意见12:化学治疗或靶向治疗DNM时,应由肿瘤科医师和移植科医师联合评估病情后选择治疗方案并监测疗效(证据级别:5,推荐强度:D)。
推荐意见13:对肝移植后DNM患者,在接受手术、放射治疗、化学治疗等多种治疗手段后肿瘤仍持续进展时,可考虑ICI治疗作为挽救性治疗。建议在ICI治疗前行肝脏穿刺活检,PD-L1表达阳性者应审慎使用PD-1和(或)PD-L1单克隆抗体(证据级别:4,推荐强度:C)。
六、结语
我国器官移植事业已进入历史发展新阶段,越来越多终末期肝病患者因肝移植重获生机。本指南旨在通过系统地回顾和总结肝移植后DNM诊治的最新进展和实践经验,为临床医师提供参考和指导。DNM作为肝移植术后常见并发症之一,严重威胁受者长期生存。术前应对供者和受者危险因素进行充分评估并采取有效的预防措施。术后早期诊断和积极治疗是改善预后的关键。目前DNM的防治仍然充满挑战,但尚未形成统一的规范化策略,未来亟待开展前瞻性、多中心、高质量临床研究,积极探索和建立MDT诊疗新模式,优化术后生活习惯管理、高风险人群筛查、免疫抑制治疗和抗肿瘤治疗方案,以期进一步提升我国肝移植受者长期生存率和生命质量。












 苏公网安备32059002004080号
苏公网安备32059002004080号


