过去二十年,EGFR突变型NSCLC的治疗格局经历从单药到联合的变革。面对第三代TKI单药长期生存率下降、大量高危患者在接受二线治疗前死亡的临床困境,一线联合治疗(如Amivantamab联合lazertinib、奥希替尼联合化疗)强势破局。如今,EGFR突变NSCLC的一线治疗已正式迈入“联合治疗”的新纪元,全面重塑患者的长期生存预期。
EGFR突变NSCLC治疗格局的演变
EGFR突变型NSCLC的治疗在过去二十年间经历翻天覆地的变化。回顾监管获批的时间线,从2003年吉非替尼获批用于三线治疗,到2004年厄洛替尼用于二线,再到后续阿法替尼、奥希替尼等药物的问世,直至2024/2025年Amivantamab联合lazertinib及奥希替尼联合化疗在一线治疗中的获批,整个治疗格局被彻底重塑。随着治疗手段的进步,患者的预后得到显著改善:与过去使用一线吉非替尼时仅约1.5年的中位总生存期(mOS)相比,目前采用一线联合治疗的患者,其预计mOS已超过4年。
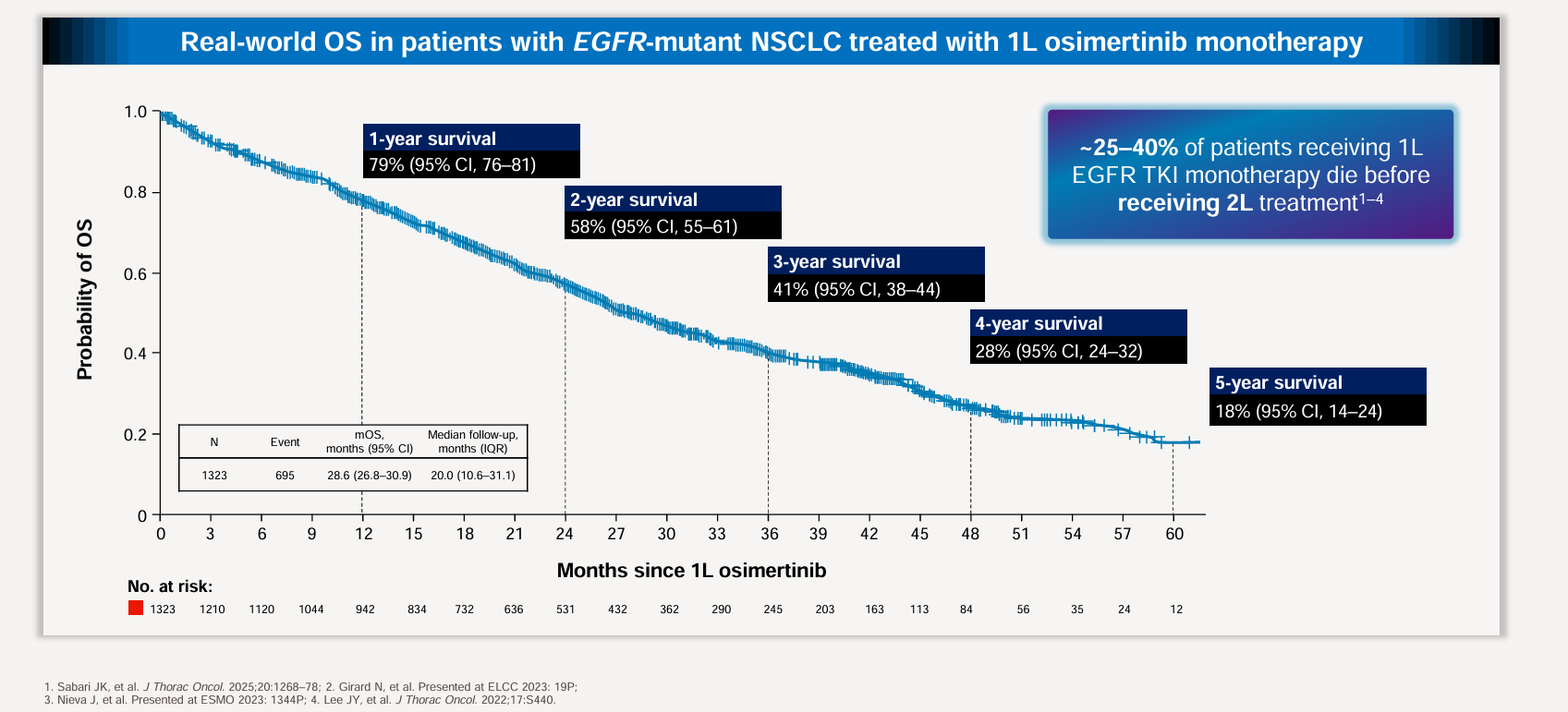
尽管第三代EGFR TKI(如奥希替尼)单药治疗取得重大进展,但患者的长期生存依然面临严峻挑战。在真实世界中接受一线奥希替尼单药治疗的EGFR突变NSCLC患者,其生存概率随着时间推移显著下降:
1年生存率为79%(95% CI, 76-81)
2年生存率为58%(95% CI, 55-61)
3年生存率降至41%(95% CI, 38-44)
4年生存率为28%(95% CI, 24-32)
第5年,生存率仅剩下约18%(95% CI, 14-24)
更为紧迫的是,大约有25%到40%接受一线EGFR TKI单药治疗的患者,在有机会接受二线治疗之前就已经不幸死亡。这也暴露出一线单药治疗目前面临的几大未满足的临床需求:高危患者群体比例大、耐药机制极为复杂,以及长期生存率依然较差。
联合治疗在前线应用的疗效
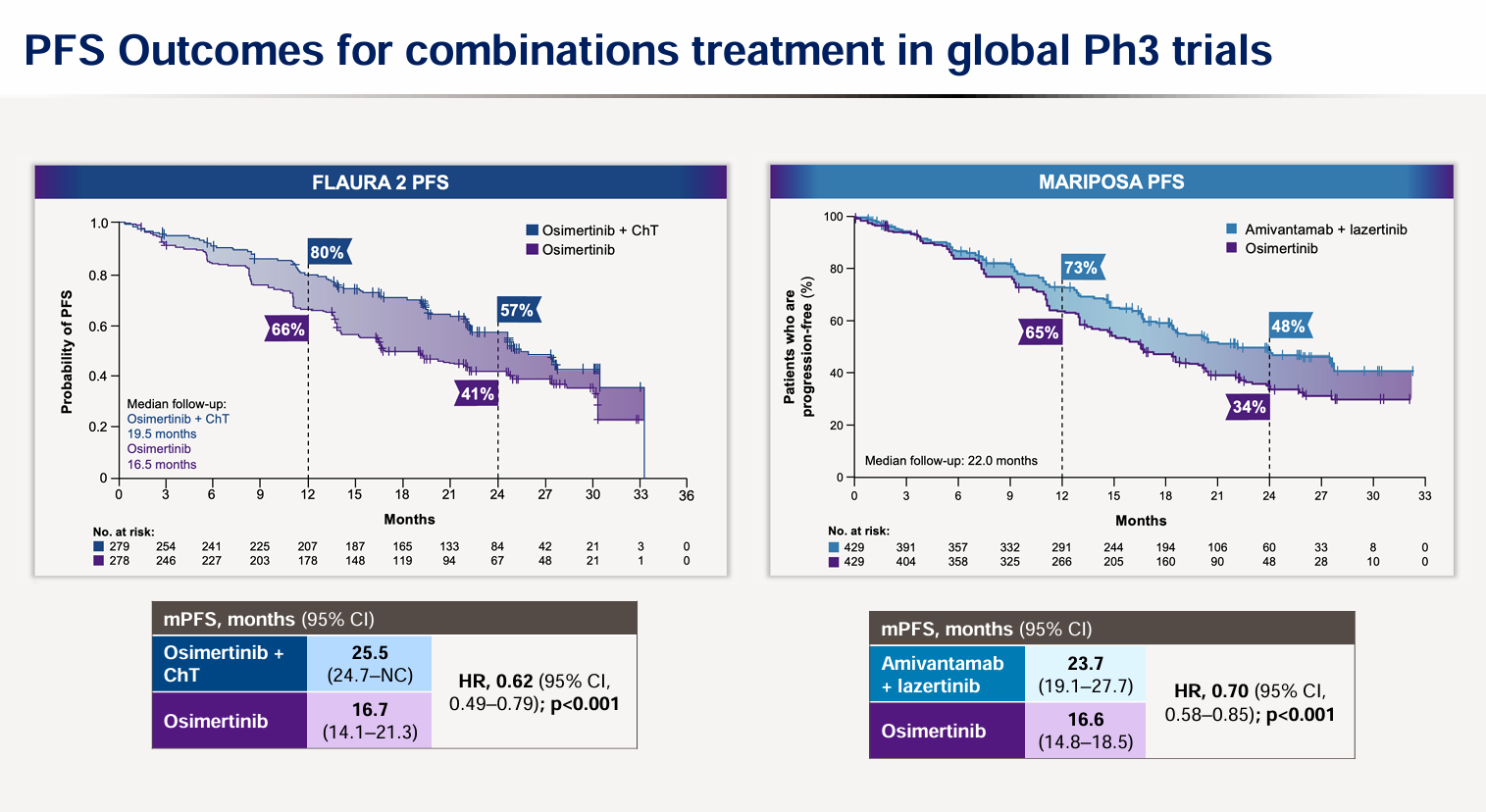
面对单药治疗的局限性,全球性的三期临床试验(如FLAURA2和MARIPOSA)为一线联合治疗提供坚实的数据支持,这些方案在无进展生存期(PFS)和总生存期(OS)上均展现出显著的临床获益。
FLAURA2研究:比较奥希替尼联合化疗与奥希替尼单药的疗效。联合治疗组的中位PFS达到25.5个月,显著优于单药组的16.7个月(HR=0.62;95% CI, 0.49-0.79;P<0.001)。在12个月和24个月时,联合组的无进展生存率分别为80%和57%,而单药组为66%和41%。
MARIPOSA研究:比较Amivantamab联合lazertinib与奥希替尼单药的疗效。联合治疗组的中位PFS为23.7个月,优于奥希替尼组的16.6个月(HR=0.70;95% CI, 0.58-0.85;P<0.001)。在随访的12个月和24个月节点,联合治疗组的无进展生存率分别为73%和48%,同样优于单药组的65%和34%。
不仅是PFS,最终的OS数据进一步巩固联合治疗的优势 。
FLAURA2研究:在中位随访约51.2个月时,奥希替尼联合化疗组的中位OS达到47.5个月,而单药组为37.6个月(HR=0.77;95% CI, 0.61-0.96;P=0.02)。
MARIPOSA研究:在中位随访37.8个月时,Amivantamab联合lazertinib组的中位OS尚未达到(NE),而奥希替尼组为36.7个月(HR=0.75;95% CI, 0.61-0.92;P=0.005) 。联合治疗组在24个月、36个月和42个月的生存率(分别为75%、60%、56%)均持续优于单药组(分别为70%、51%、44%),显示出两条生存曲线随着时间推移呈现持续分离的趋势。
高危亚组患者从联合治疗中深度获益
真实世界中,绝大多数(约89%至95%)的EGFR突变NSCLC患者在基线时就具有至少一项高危特征。这些特征包括高龄(≥65岁,占66%)、伴有脑转移(占36%)、肝转移(占15%)、TP53共突变(占63%)以及基线ctDNA阳性(占85%)等。
面对这些复杂且极易发生早期进展的高危群体,联合治疗展现出强大的底气:
中枢神经系统(CNS)转移:对于基线有脑转移病史的患者,FLAURA2研究中联合治疗带来的PFS HR为0.47(中位PFS 24.9个月 vs 13.8个月)。同时,在MARIPOSA研究中,针对有基线CNS转移的患者,联合治疗组的中位颅内无进展生存期(icPFS)为25.4个月,优于单药组的22.2个月(HR=0.79)。
肝转移:在FLAURA2研究中,伴有肝转移的患者使用联合治疗的HR为0.63;在MARIPOSA中该亚组的HR甚至达到0.58。
TP53共突变:这既是一个预后不良因素,也是联合治疗的预测因子。多项研究数据高度一致:在MARIPOSA中,伴有TP53共突变患者接受联合方案的中位PFS为18.2个月,单药仅为12.9个月(HR=0.65,P=0.003)。FLAURA2中相应亚组的HR为0.57。
ctDNA与微小残留病灶(MRD):研究表明,基线ctDNA状态直接影响患者的预后。基线ctDNA阴性组的3年无病生存(DFS)率可达83.3%,而基线ctDNA阳性且未能被清除(MRD阳性)的患者,其3年DFS率陡降至50.0%。在临床试验中,基线检测到EGFR突变ctDNA的患者,更能从联合治疗中获得显著的PFS提升(如FLAURA2中HR为0.60,MARIPOSA中HR为0.68)。
联合治疗的毒性成本与管理策略
更强效的一线联合治疗方案必然会带来较高的不良反应发生率,这就要求临床在追求疗效的同时,妥善衡量并管理毒性成本。
在不良事件对比方面:
MARIPOSA研究:Amivantamab联合lazertinib组发生3级或以上(G3+)不良事件的比例为75%,严重不良事件(SAE)为49%,因不良事件导致的剂量中断率高达83%,因不良事件停药的比例为35%;而相应的奥希替尼单药组的数据仅为43%(G3+)、33%(SAE)、39%(中断)和14%(停药)。
FLAURA2研究:奥希替尼联合化疗组的G3+发生率为64%,同样大幅高于单药奥希替尼的27%。
然而,针对这些毒性,我们可以通过动态优化策略进行预防和管理:
早期发作特性:在Amivantamab联合lazertinib治疗中,多数关键不良事件(如皮疹、甲沟炎、痤疮样皮炎、口腔炎、静脉血栓栓塞症VTE等)的首发时间均集中在治疗的前4个月(0-4个月)。多数输液相关反应(IRR)发生于首次输注,中位发作时间为1小时,且多数在输注开始后2小时内发生。
预防性用药:通过采用预防性措施可以大幅改善耐受性。例如,实施SKIPPirr方案(使用8mg地塞米松作为预防),可以将输液相关反应(IRR)的发生率从标准的67.4%降低约3倍至22.5%。使用COCOON皮肤管理方案,可将2级或以上皮肤毒性从75%极显著地降低至42%(P<0.0001)。
剂量调整不影响疗效:在MARIPOSA研究中,针对毒性进行的剂量中断并未对最终疗效产生负面影响。数据显示,伴随剂量中断的患者,其中位PFS达到27.5个月,甚至略微优于未中断剂量的25.7个月。
排版编辑:肿瘤资讯-Bear












 苏公网安备32059002004080号
苏公网安备32059002004080号


