胆道肿瘤因其高度异质性,长期以来临床预后不佳。随着分子分型技术和精准治疗策略的迅速发展,胆道肿瘤的治疗范式正经历深刻变革。近年来,针对FGFR2、IDH1、HER2等关键驱动基因的靶向药物相继涌现,显著改善了部分晚期患者的生存结局。与此同时,免疫联合化疗、抗血管生成药物以及其他新型治疗策略也在不断拓展治疗边界。然而,耐药机制复杂、生物标志物筛选体系不完善以及罕见变异人群缺乏高级别证据等问题,仍是当前领域面临的重要挑战。值此契机,特邀浙江大学医学院附属邵逸夫医院梁霄教授,围绕胆道肿瘤分子靶向治疗的最新进展,从耐药机制剖析、二线靶向方案优化,到术后免疫联合策略等多个维度,系统梳理并深度解读关键临床研究证据,以期为临床实践提供理论依据。
浙江大学医学院附属邵逸夫医院
浙江大学医学院副院长
浙江大学医学院附属邵逸夫医院钱塘院区院长助理
浙江大学医学院附属邵逸夫医院普外科副主任
教授、主任医师、博士生导师
浙江省肝脏疾病多组学精准诊治重点实验室主任
浙江省医学会微创外科学分会候任主委
浙江省微创技术质控中心常务副主任
浙江大学微创外科研究所副所长
浙江省医学会加速康复外科分会副主委
国家癌症中心肝癌质控专委会委员
中国医师协会外科医师分会机器人外科专家工作组副组长中国医师协会外科医师分会肝胆青年专家工作组副组长中华医学会外科学分会脾脏及门脉高压症学组委员
美国外科学院委员(FACS)
国际腹腔镜肝切除协会会员(ILLS)
基于分子特征的胆管癌靶向治疗现状与展望
Current status and prospects of targeted therapy for cholangiocarcinoma based on molecular characteristics1
胆管癌(CCA)起病隐匿、预后极差,多数患者确诊时已属晚期,治疗选择有限。近年来,基于分子特征的靶向治疗为晚期CCA患者带来了新希望。本综述系统回顾了当前CCA靶向治疗现状与进展,重点聚焦亚洲人群数据,并深入探讨磷酸酯酶与张力蛋白同源物(PTEN)作为新型生物标志物在指导化疗和靶向治疗中的作用。
通过综合分析多项临床试验,本综述系统评估了针对FGFR、IDH1、HER2、BRAF、KRAS、RET、NTRK、PARP、MDM2-p53等多个靶点的药物疗效。以IDH1为例,IDH1的突变约占iCCA的13%-25%。突变型 IDH1 促进生成致癌代谢物2-HG。2-HG会损害细胞分化,并促进肿瘤发生。IDH1抑制剂艾伏尼布是口服、选择性的、可逆IDH1突变抑制剂。在III期ClarIDHy试验中,艾伏尼布显著延长PFS(2.7 vs 1.4个月)和OS(10.3 vs 5.1 个月,RPSFT校准后)。基于此项研究,美国食品药品监督管理局(FDA)于2021年批准艾伏尼布用于治疗携带 IDH1 突变的既往治疗后进展的、不可切除的局晚期或转移性胆管癌。
针对FGFR2融合/重排的抑制剂如佩米替尼、英菲格拉替尼、福巴替尼等客观缓解率(ORR)可达23%-52%。抗HER2治疗如T-DXd、泽尼达妥单抗等在HER2阳性患者中也表现出良好活性(ORR分别为56.3%和36.4%)。此外,针对BRAF V600E、KRAS G12C、NTRK融合等罕见靶点的药物也显示出潜在疗效。PTEN缺失作为新型生物标志物,与蛋白酶体抑制剂硼替佐米的敏感性相关,I期试验显示其ORR达23.1%。
基于活检与循环肿瘤DNA分析揭示福巴替尼疗效与耐药性的基因组关联因素
Genomic correlates of response and resistance to the irreversible FGFR1-4 inhibitor futibatinib based on biopsy and circulating tumor DNA profiling2
本研究聚焦于不可逆FGFR1-4抑制剂福巴替尼在治疗FGFR变异晚期实体瘤(尤其是CCA)中的基因组学特征及其与疗效和耐药的关系。研究基于FOENIX I/II期试验,纳入226例接受福巴替尼治疗且具有基线或进展期ctDNA样本的患者,通过组织活检和ctDNA测序系统分析了FGFR变异的检测一致性、共存基因组改变与疗效的相关性以及获得性耐药机制。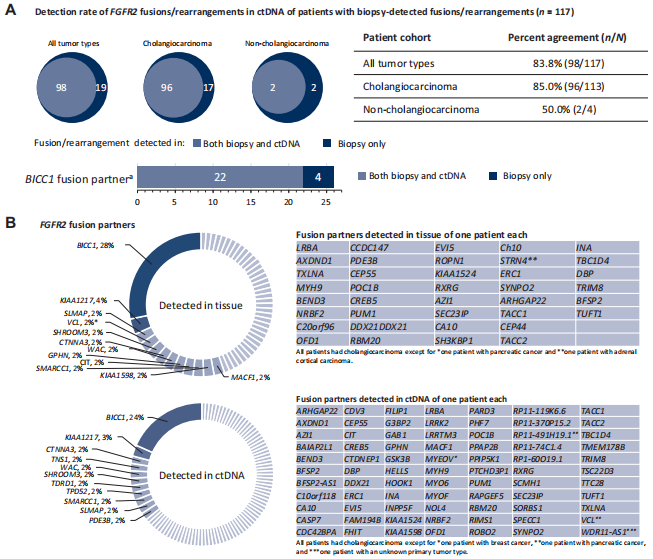
研究结果显示,ctDNA检测FGFR2融合/重排与组织活检的总体一致性为83.8%,在CCA中达85.0%。TP53共突变与疗效无显著相关性,而CDKN2B突变与CCA患者更短的PFS相关(4.8 vs 11.0个月,P=0.03)。获得性耐药分析表明,62% (23/37)的初治CCA患者进展后出现FGFR2激酶域突变,且多为多克隆性,以V565L、V565F和N550K变异最为常见;临床获益者中耐药突变发生率更高(86%)。此外,MAPK通路突变(如RAS、BRAF)也常见于进展后的患者样本中。研究表明,ctDNA是一种可靠的替代性生物标志物检测手段,福巴替尼的耐药机制以多克隆FGFR2激酶域突变为主,未来需联合组织与液体活检以优化患者选择和耐药后治疗策略。
舒尼替尼二线治疗晚期肝内胆管癌:SUN-CK II期试验结果
Sunitinib as Second-Line Treatment in Advanced Intrahepatic Cholangiocarcinoma: Results From the SUN-CK GERCOR Phase II Trial4
舒尼替尼作为一种多靶点酪氨酸激酶抑制剂,具有强效抗血管生成和抗肿瘤活性,前期研究显示其在部分ICC患者中具有疾病控制潜力。本研究旨在评估舒尼替尼作为二线治疗在既往接受过吉西他滨和/或铂类化疗的晚期肝内胆管癌(ICC)患者中的疗效与安全性。该研究为一项多中心、单臂、II期临床试验(SUN-CK,NCT01718327),共纳入53例患者,每日口服舒尼替尼37.5 mg,直至疾病进展或出现不可耐受毒性。主要终点为总生存期(OS),次要终点包括PFS、ORR、疾病控制率(DCR)和安全性。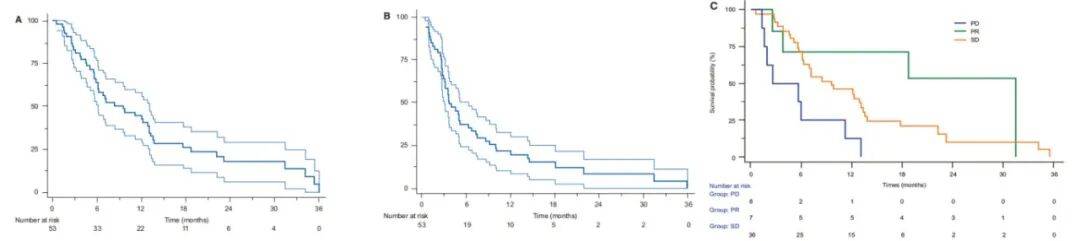
研究结果显示,中位OS为9.6个月(95% CI: 6.1–13.1),中位PFS为3.7个月(95% CI: 3.1–6.4),ORR为14%,DCR为84%。安全性方面,常见3–4级不良事件包括血细胞减少(25%)、高血压(21%)和疲劳(19%)。基线VEGF-A和VEGF-C水平升高与更长OS显著相关。剂量调整后血药浓度仍维持在治疗窗内。Choi标准在24例患者中比RECIST v1.1更能预测缓解持续时间,且基线肿瘤密度与治疗反应存在潜在关联。研究表明,舒尼替尼在经治晚期ICC患者中显示出具有临床意义的抗肿瘤活性和可管理的毒性,VEGF水平及Choi标准可作为潜在预测标志物,值得进一步研究验证。
度伐利尤单抗联合吉西他滨和顺铂治疗晚期胆道癌的免疫介导不良事件
Immune-mediated adverse events in the randomized phase 3 TOPAZ-1 study of durvalumab plus gemcitabine and cisplatin in advanced biliary tract cancer5
本研究基于随机、双盲、全球多中心III期TOPAZ-1试验,评估了在晚期胆道癌(aBTC)患者中,PD-L1抑制剂度伐利尤单抗联合吉西他滨和顺铂(GemCis)方案所引发的免疫介导不良事件(imAEs)的发生情况及其与OS的关联。研究将患者按1∶1随机分配至度伐利尤单抗联合GemCis组或安慰剂联合GemCis组,通过对安全性分析集中680例患者进行事后分析,系统描述imAEs的发生率、发生时间(TTO)、严重程度及转归。
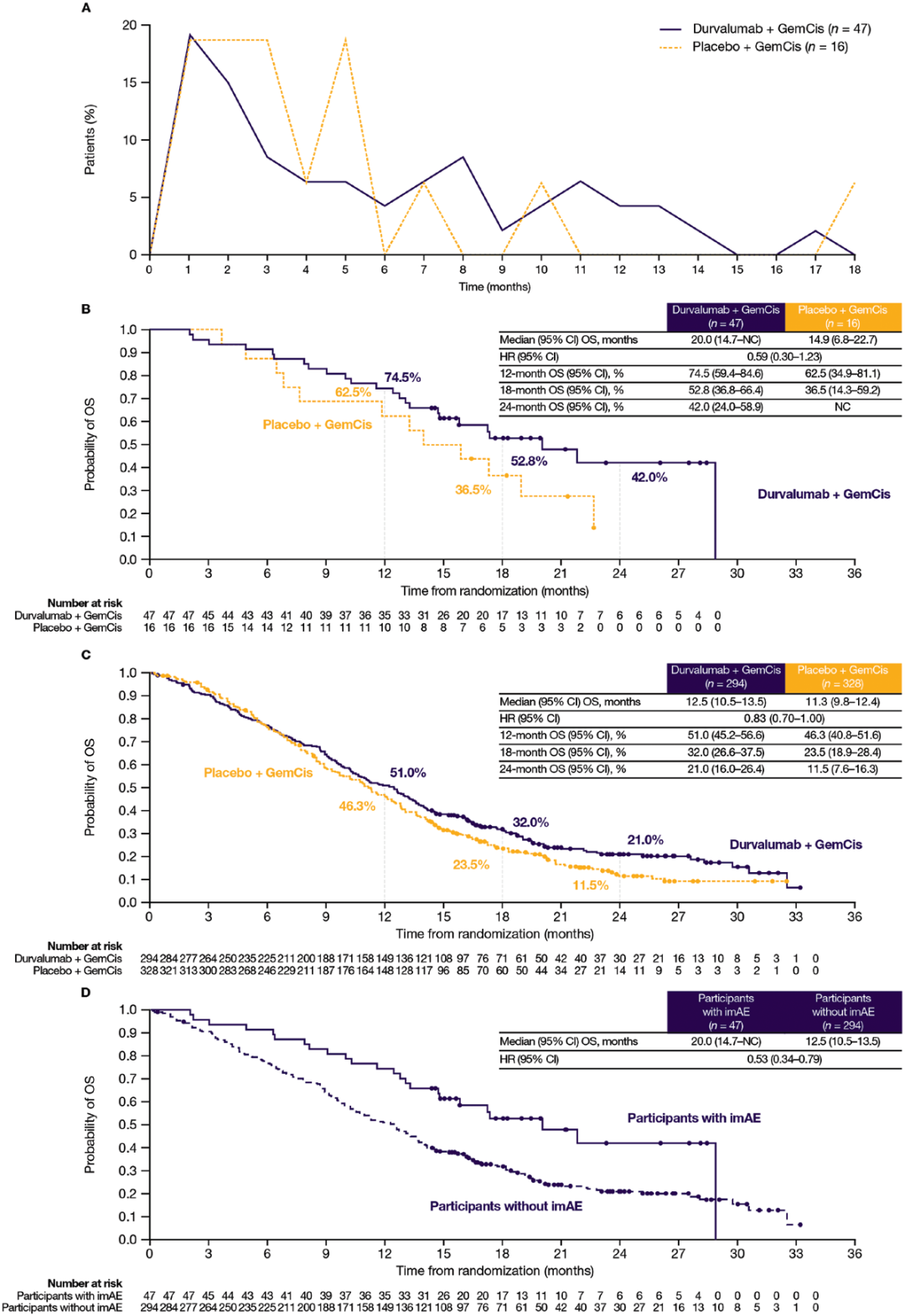
(A)接受度伐利尤单抗+GemCis或安慰剂+GemCis的 imAE 总发生率。(B)接受度伐利尤单抗+GemCis或安慰剂+GemCis且发生 imAE患者 的OS。(C)接受度伐利尤单抗+GemCis或安慰剂+GemCis且未发生 imAE患者的OS。(D)接受度伐利尤单抗+GemCis治疗的参与者按 imAE 状态划分的总生存期。
研究结果显示,度伐利尤单抗+GemCis组imAEs发生率为13.9%,显著高于安慰剂+GemCis组的4.7%,但多数为1–2级,以甲状腺功能减退最为常见。中位TTO在度伐利尤单抗+GemCis组为127天。3-4级imAEs(2.4% vs. 1.5%)和导致停药的比例(0.9% vs. 1.2%)两组相当,度伐利尤单抗+GemCis组无imAE相关死亡,安慰剂组有1例。OS分析显示,无论是否发生imAEs,度伐利尤单抗+GemCis组相对于安慰剂+GemCis组均显示OS获益:在发生imAEs的患者中,HR为0.59(95% CI: 0.30-1.23);未发生imAEs的患者中HR为0.83(95% CI: 0.70-1.00),与主要分析结果一致,但发生imAEs的患者有OS数值上更优的趋势。本研究表明度伐利尤单抗联合GemCis在aBTC中具有显著生存获益,且该获益不依赖于imAEs的发生;研究结果支持该联合方案在临床中的应用,并强调了对imAEs早期识别与处理的重要性。
专家点评
近年来,胆道肿瘤的分子分型和靶向治疗取得了显著进展,尤其在晚期患者中不断涌现出具有临床价值的新策略。本组文献从分子机制、治疗策略到耐药管理,全面反映了当前领域的研究热点及关键探索方向。
基于分子特征的靶向治疗综述系统梳理了CCA中FGFR2、IDH1、HER2等关键靶点的药物疗效,并突出强调PTEN缺失与蛋白酶体抑制剂疗效的关联,为亚洲人群数据积累和生物标志物开发提供了扎实依据。然而,该综述仍局限于已知靶点总结,对新兴机制如肿瘤微环境调控、表观遗传变异等涉及有限,未来需结合多组学数据拓展靶向治疗维度。
FOENIX I/II研究通过组织与ctDNA比对,明确了福巴替尼在FGFR2变异胆管癌中的耐药机制以激酶域多克隆突变为主,且CDKN2B突变提示不良预后。这一发现凸显了液体活检在动态监测中的可靠性,但也揭示出当前FGFR抑制剂的共性困境——耐药复杂性高、缺乏有效后线策略。未来需探索FGFR抑制剂与其他通路(如MAPK)抑制剂的联合应用,以延缓耐药发生。
舒尼替尼II期研究提示其在经治ICC中具有一定活性,且VEGF水平及Choi标准可能成为预测标志物,这与抗血管生成药物在胆道癌中的机制相符。但舒尼替尼作为多靶点TKI,其特异性较低,在当前高选择性药物涌现的背景下,其临床定位逐渐模糊。未来应聚焦于筛选优势人群(如高VEGF表达者),而非泛人群推广。
TOPAZ-1研究的imAEs分析证实了度伐利尤单抗联合化疗的安全性可控,且生存获益与imAEs发生无关,说明疗效不依赖于免疫过度激活带来的毒性风险。这一点区别于某些癌种中irAE(immune-related adverse event, 免疫相关不良事件)与疗效正相关的现象,提示在BTC中应更注重风险平衡与管理,而非刻意追求免疫相关毒性作为疗效替代指标。
总体而言,胆道肿瘤诊疗已进入分子引导下的多维治疗时代,但仍面临耐药机制复杂、生物标志物应用不足、罕见变异治疗证据有限等挑战。未来需围绕动态耐药监测、新型联合策略优化以及真实世界数据积累,推动个体化治疗迈向新高度。
审校:浙江大学医学院附属邵逸夫医院梁霄教授
整理:中国医学论坛报 林颖
审批号:M-TIBSO-CN-202509-00001
本文转自:论坛报
1.Cui X, Huang T, Jiang T, et al. Current status and prospects of targeted therapy for cholangiocarcinoma based on molecular characteristics. Cancer Lett. 2025 Apr 1;614:217540. doi: 10.1016/j.canlet.2025.217540. Epub 2025 Feb 7. PMID: 39924074.
2.Goyal L, DiToro D, Hollebecque A, et al. Genomic correlates of response and resistance to the irreversible FGFR1-4 inhibitor futibatinib based on biopsy and circulating tumor DNA profiling. Ann Oncol. 2025 Apr;36(4):414-425. doi: 10.1016/j.annonc.2024.11.017. Epub 2024 Dec 11. PMID: 39672383.
3.Gros L, Bouattour M, Dumont C, et al. Sunitinib as Second-Line Treatment in Advanced Intrahepatic Cholangiocarcinoma: Results From the SUN-CK GERCOR Phase II Trial. Liver Int. 2025 Aug;45(8):e70196. doi: 10.1111/liv.70196. PMID: 40631456; PMCID: PMC12239060.
4.Antonuzzo L, Takahashi H, Park JO, et al. Immune-mediated adverse events in the randomized phase 3 TOPAZ-1 study of durvalumab plus gemcitabine and cisplatin in advanced biliary tract cancer. Oncologist. 2025 Jul 4;30(7):oyaf148. doi: 10.1093/oncolo/oyaf148. PMID: 40622010; PMCID: PMC12230790.
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关政府部门批准使用的指南或规定。
排版编辑:肿瘤资讯-yu











 苏公网安备32059002004080号
苏公网安备32059002004080号


