十二指肠神经内分泌肿瘤是一类相对少见但又具有高度异质性的肿瘤,其临床个体化管理相对复杂。本次MDT云诊室由复旦大学附属肿瘤医院多学科团队分享3例不同特征的十二指肠神经内分泌瘤病例,并邀请多位专家共同探讨,旨在厘清十二指肠神经内分泌瘤在治疗决策中的关键考量,讨论在观察随访、内镜下治疗、外科手术治疗间如何进行个体化选择。
病例介绍
病例1:
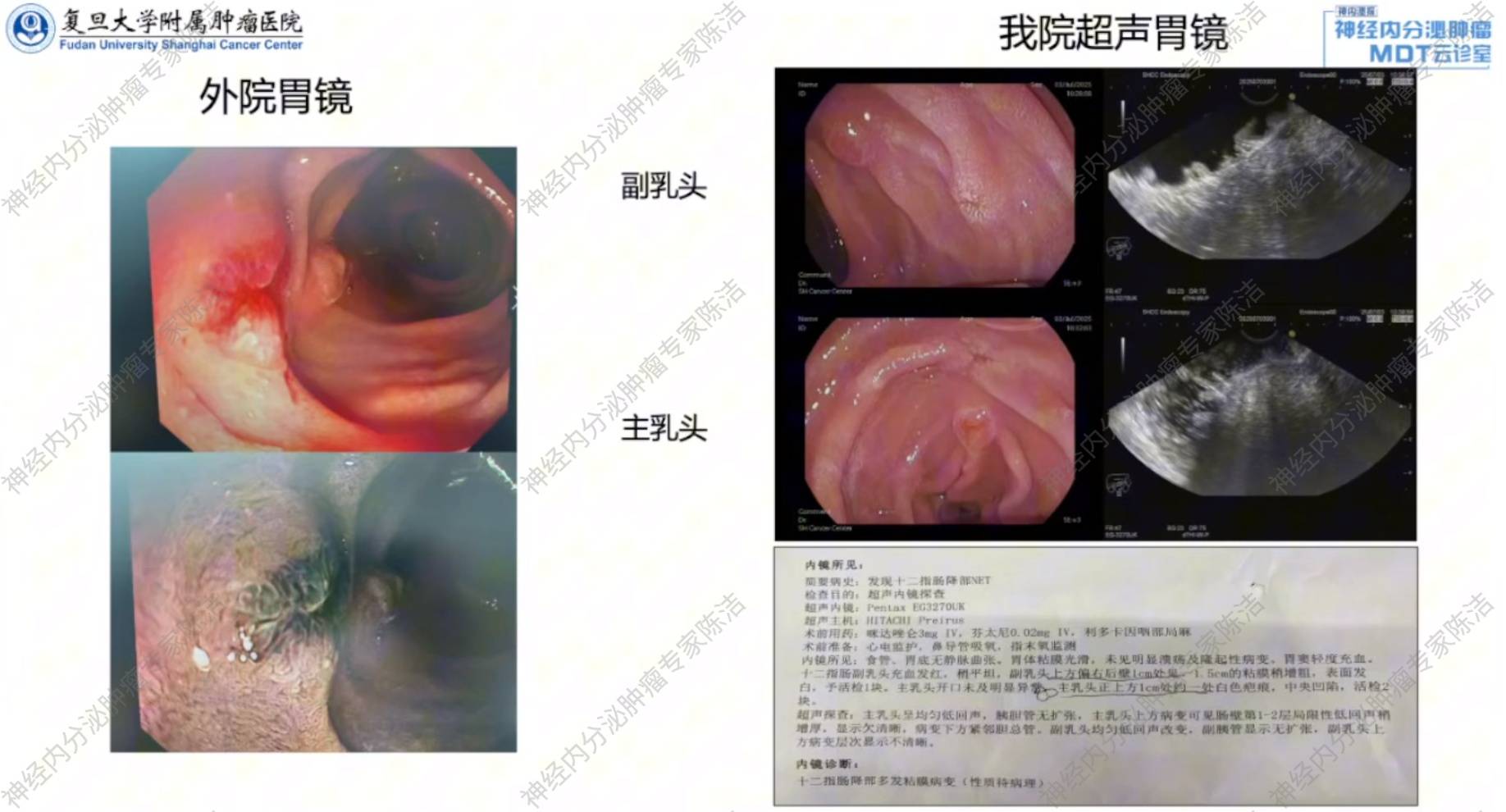
患者为33岁男性,2025年6月为减肥行胃镜下胃转流支架植入术,术中发现十二指肠乳头肿瘤。胃镜:十二指肠副乳头开口处黏膜充血,腺体粗大。活检病理:NET G2,Ki-67为5%,SSTR2 3+。腹部增强CT:脂肪肝,副脾。
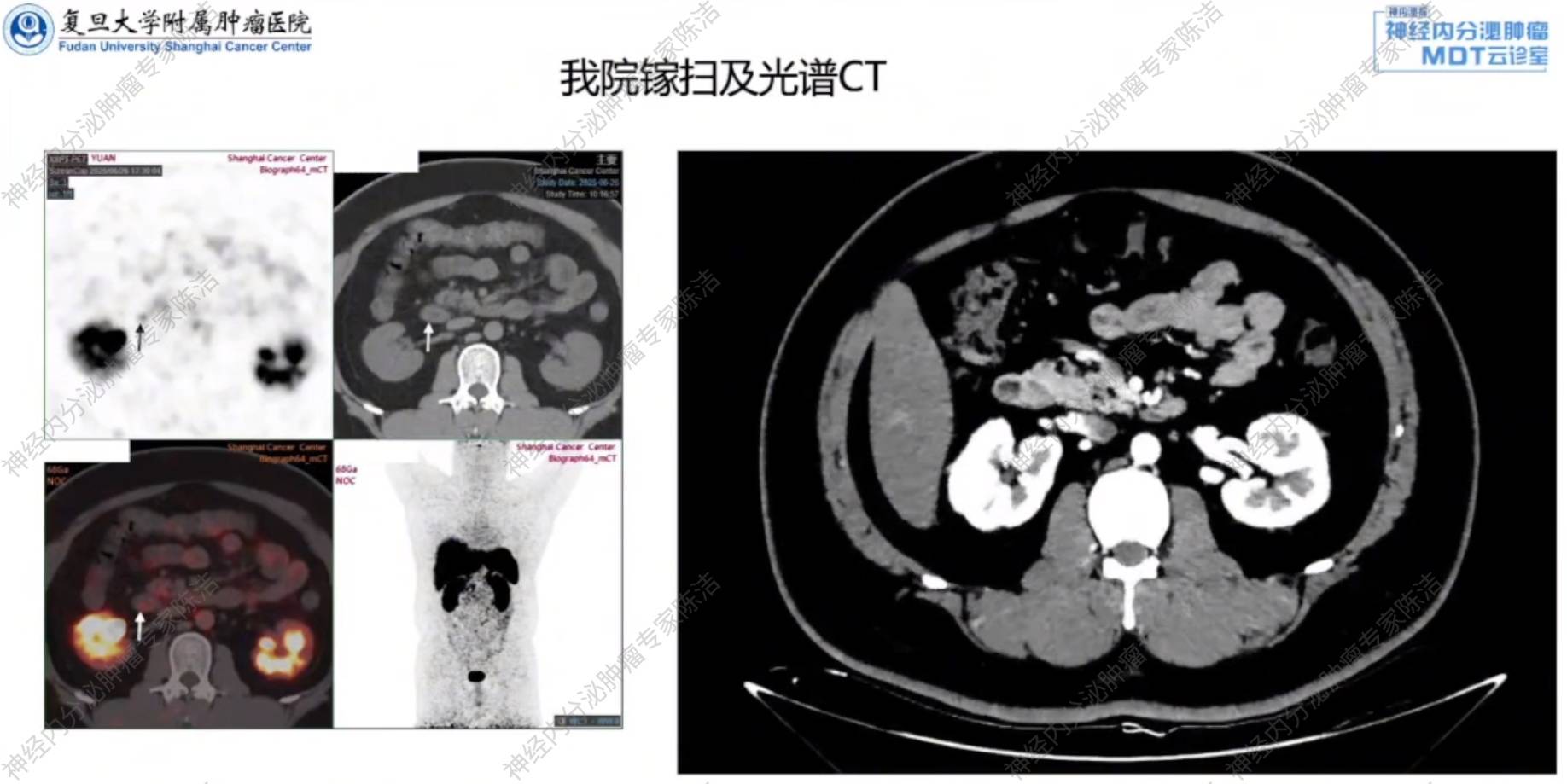
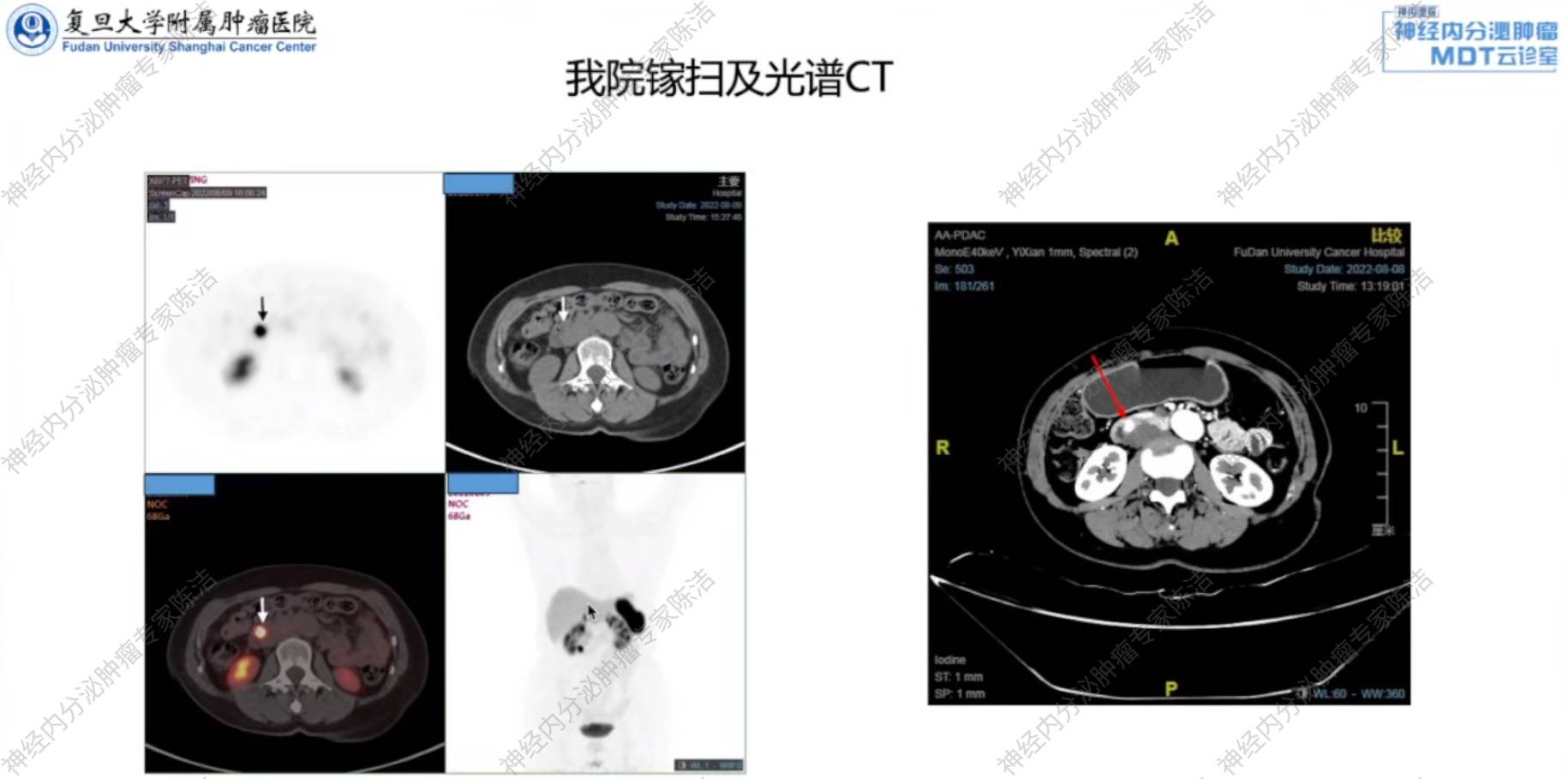
2025年7月,患者于我院就诊,光谱CT示:脂肪肝,未见明确十二指肠病灶。68Ga-SSA-PET/CT示:十二指肠降部可疑结节,NOC摄取轻度增高。超声胃镜:副乳头上方偏右后壁1cm处1.5cm黏膜粗糙,超声下病变层次显示不清,活检1块;主乳头正上方1cm处1白色疤痕,中央凹陷,可见肠壁第1-2层局限性低回声稍增厚,下方紧邻胆总管,活检2块。活检病理:主乳头上方倾向NET G1,副乳头上方黏膜慢性炎。
基于上述全面检查,并与患者沟通后,予采取随访观察策略,每年复查胃镜及光谱CT。


病例2:
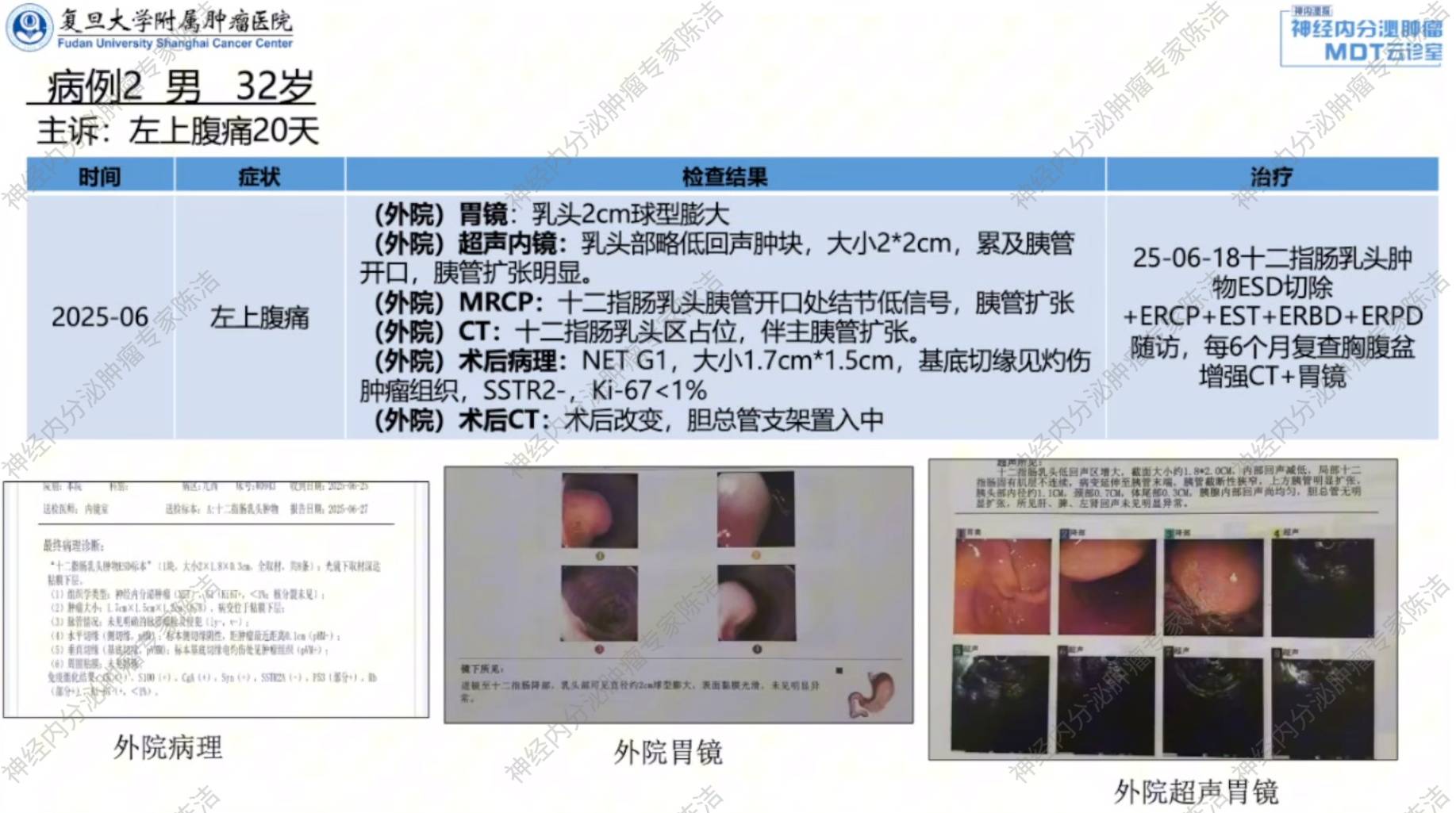
患者为32岁男性,2025年6月因左上腹痛20天,于外院行胃镜检查,于十二指肠乳头见直径约2cm球型膨大,超声内镜:乳头部略低回声肿块,大小2*2cm,累及胰管开口,胰管扩张明显。MRCP:十二指肠乳头胰管开口处结节低信号,胰管扩张。腹部CT:十二指肠乳头区占位,伴主胰管扩张。
2025年6月18日于外院行“十二指肠乳头肿瘤ESD切除+ERCP+EST+ERBD+ERPD”。术后病理:NET G1,大小1.7cm*1.5cm,基底切缘见灼伤肿瘤组织(切缘阳性),SSTR2-,Ki-67<1%。术后CT:术后改变,胆总管支架置入中。后采取定期随访策略,每6个月复查胸腹盆腔增强CT及胃镜。
病例3:
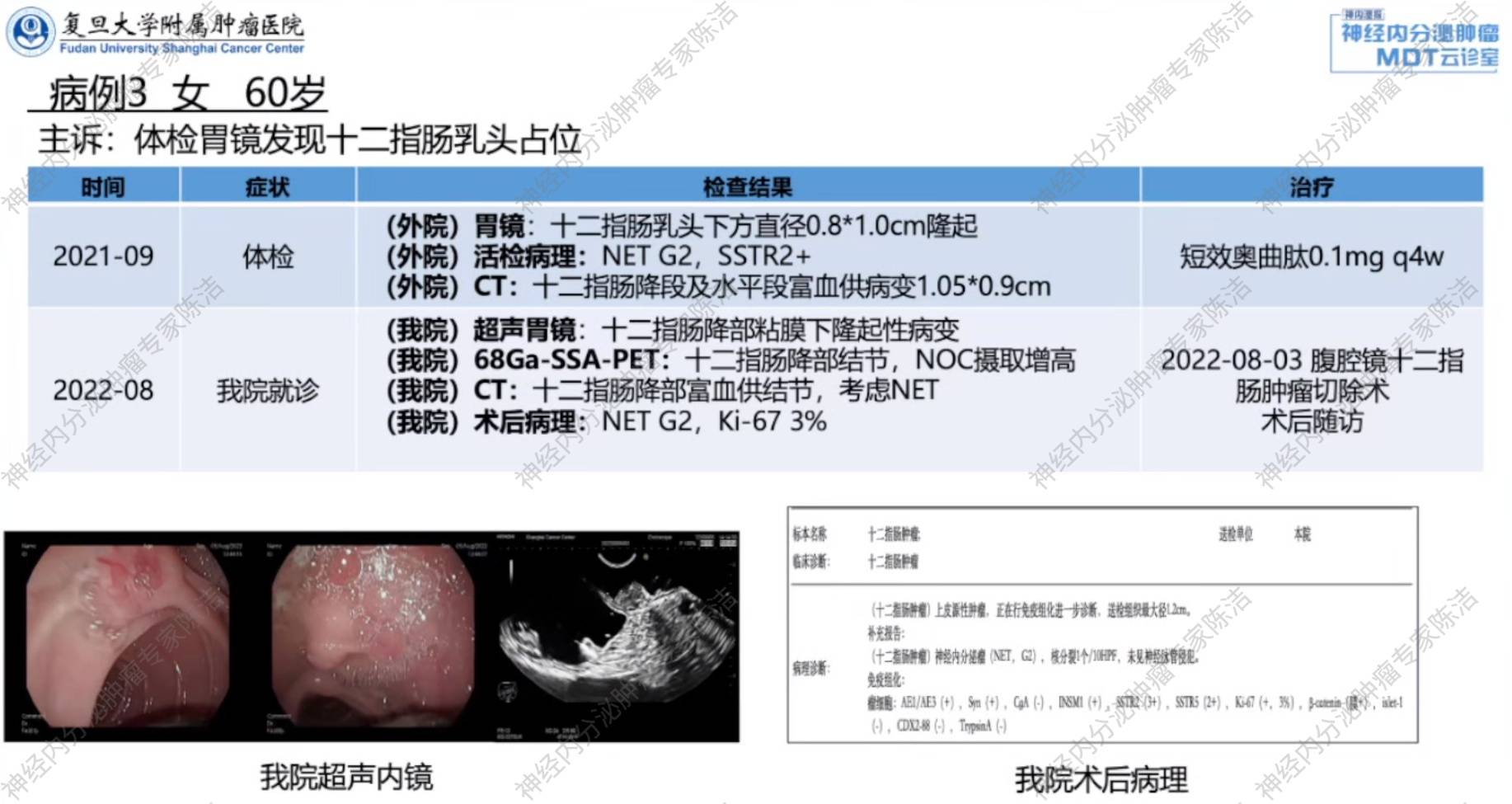
患者为60岁女性,2021年9月外院体检胃镜:十二指肠乳头下方直径0.8cm*1.0cm隆起。活检病理:NET G2,SSTR2+。腹部CT:十二指肠降段及水平段富血供病变,大小1.05cm*0.9cm。外院予以短效奥曲肽0.1mg q4w治疗。
后患者于2022年8月我院就诊,超声胃镜:十二指肠降部黏膜下隆起性病变。68Ga-SSA-PET:十二指肠降部结节,NOC摄取增高。增强CT:十二指肠降部富血供结节,考虑NET。于2022年8月3日我院行腹腔镜十二指肠肿瘤切除术。术后病理:NET G2,Ki-67 3%。
多学科团队(MDT)讨论
病例1:
张宁教授:内镜下可见病灶表面发红,位于乳头上方靠近球部,大小估计在1.5~2.0cm。超声内镜对于明确肿瘤起源层次(黏膜下层)、浸润深度及与周围重要结构(如胆管、胰管)的关系至关重要。此病例病灶紧邻胆总管,无论内镜下治疗还是外科手术,均存在损伤风险。
黄丹教授:结合形态学和免疫组化(Syn、CgA、INSM1强阳性),明确为神经内分泌肿瘤。在我院会诊后,主乳头上方病灶分级修正为G1,而副乳头处为慢性炎症。
徐俊彦教授:68Ga-SSA-PET/CT显示了可疑的轻度摄取,但这种情况特异性不强,考虑是肠道生理性摄取,非明确占位病变。结合免疫组化,若有残留且病灶大,应该可见明显局灶性聚集,目前患者未发现明确病灶。
汤伟教授:这位患者在常规增强CT和光谱CT均未显示明确病灶。
病例2:
黄丹教授:该患者因十二指肠肿块接受了ESD切除,术后病理报告明确了肿块为NET G1,已浸润至黏膜下层,但无脉管或神经侵犯等高危因素。然而,在评估手术切除质量评估时,显微镜下检查发现,其基底切缘(深部切缘)可见肿瘤细胞,这表明肿瘤在垂直方向上并未被完全切除干净。
张宁教授:该病例位于十二指肠乳头,病灶较大(2cm)且引起胰管扩张,内镜下ESD治疗难度极高,风险大,主要并发症为术后胰腺炎和胆管炎。术者在ESD同时行ERCP并放置胰管和胆管支架,是预防并发症的措施。然而,术后病理提示基底切缘阳性,意味着肿瘤未完全切除。
刘晓岗教授:在治疗选择方面,对于2cm大小、位于乳头且已导致胰管梗阻的NET,倾向于首选外科手术。内镜ESD虽然技术上可行,但要达到R0切除并确保足够的切缘深度非常困难,且术后并发症风险高。第二个病例虽然通过放置支架暂时避免了严重并发症,但切缘阳性表明内镜治疗存在局限性。
病例3:
张宁教授:这是一个典型的黏膜下肿瘤表现,表面光滑,超声内镜下呈低回声,起源于黏膜下层(第二/三层),边界清晰,富血供,这些都是神经内分泌肿瘤的典型特征。
徐俊彦教授:68Ga-SSA-PET/CT显示了位于十二指肠降部的高摄取的结节,提示肿瘤SSTR高表达。
汤伟教授:光谱CT清晰显示了位于十二指肠降部的富血供结节,明确了病灶的存在、位置及周围组织结构是否受侵。
徐晓武教授:该病例采用了腹腔镜下十二指肠肿瘤局部切除术,其关键技术点在于:1.术中通过置入导管精确定位并保护十二指肠乳头;2.对肿瘤进行全层楔形切除,确保切缘阴性;3.精细缝合关闭十二指肠壁缺损。相较于ESD,外科手术能更可靠地实现R0切除,尤其对于浸润较深或较大的病灶,是更安全和彻底的选择。
黄丹教授:该病例术后病理确诊为NET G2,对于十二指肠乳头区域的肿瘤,病理诊断需与胰头来源肿瘤相鉴别。通过CDX2(肠源性标志物)和ISL1(胰源性标志物)等免疫组化指标,可以帮助判断肿瘤起源,这对判断预后和指导后续治疗具有重要临床价值。
陈洁教授总结
本次我们分享了3例各具特点的十二指肠神经内分泌肿瘤病例,并听取了多位专家的精辟见解。通过这三个病例的对比,我们可以得出以下几点总结:
十二指肠NET的治疗没有“一刀切”的方案。病例1中,尽管病理提示G2,但病灶微小、影像学隐匿,且患者不愿意接受其它有创操作的风险,最终MDT团队与患者共同选择了密切随访。这体现了在肿瘤整体恶性度低的情况下,尊重患者意愿并进行动态监控的可行性。
病例2警示我们,对于较大(≥2cm)、位置特殊(如十二指肠乳头)、已引起梗阻的十二指肠NET,内镜ESD虽技术上可尝试,但根治性切除的难度和风险极高,易导致切缘阳性。此病例虽短期内避免了大型手术,但留下了肿瘤残留和随访困难(SSTR阴性)的隐患。总体上,内镜治疗更适用于较小的、位置相对安全的、局限于黏膜下层的NET。
病例3展示了理想的治疗路径。对于有手术指征的十二指肠NET,外科手术(尤其是腹腔镜微创手术)能够精准、完整地切除肿瘤,并进行可靠的肠壁修复,是实现根治的首选。特别是对于乳头周围的病灶,外科手术在保护胆胰管功能和保证切缘阴性方面具有不可替代的优势。
这三个病例的诊疗过程充分证明,十二指肠NET的管理必须依赖多学科团队的协作。从影像学的精准定位、内镜的探查评估、病理的精确诊断,到不同治疗方案的权衡利弊,每一个环节都需要跨学科的深入讨论,才能为患者制定出最合理、最安全的个体化治疗策略,最终实现最佳的治疗效果和生活质量。
更多精彩病例,可点击或复制以下链接,粘贴到浏览器查看神经内分泌肿瘤MDT云诊室-胃肠胰神经内分泌肿瘤内镜治疗专场回放:
https://doctor.liangyihui.net/#/doc/152705

本文仅供健康科普使用,不能作为诊断、治疗的依据,请谨慎参阅。











 苏公网安备32059002004080号
苏公网安备32059002004080号


