

肺腺鳞癌是一种罕见且特殊的非小细胞肺癌(NSCLC)亚型,其肿瘤组织中腺癌与鳞状细胞癌两种成分的比例均达到或超过10% [1]。手术切除是该病的主要治疗手段,然而对于晚期无法手术的患者,化疗和分子靶向治疗等替代疗法则成为关键选择。本研究聚焦于一位老年晚期肺腺鳞癌患者。该患者在接受规范的靶向治疗后出现疾病进展,随后采用长春瑞滨软胶囊联合靶向治疗方案,取得了显著的疗效。这一成功案例为晚期肺腺鳞癌的综合治疗提供了新的思路与有益的启示。
特邀嘉宾
病例分享专家
河北医科大学第四医院肿瘤内科
河北省肿瘤内科诊疗中心
河北省抗癌协会肿瘤精准治疗专业委员会青年委员会委员
河北省女医师协会肿瘤内科分会委员
病例点评专家
河北医科大学第四医院肿瘤内科
河北省抗癌协会肿瘤转移委员会委员
北京医学奖励基金会肺癌青委会委员
中国女医师协会乳腺疾病专业青委会委员
河北省女医师协会肿瘤内科专委会委员
河北省抗癌协会肿瘤内科专业委员会青委会委员
中国抗癌协会肿瘤热疗专业委员会河北省分会委员
病例介绍
患者男性,初诊年龄77岁,农民。主诉“左锁上淋巴结肿大半月余,右肺鳞癌8天”。
现病史:患者于半月余前自觉左侧锁上淋巴结肿大,于当地医院就诊,查胸部CT(2023-12-25)示:1、双侧支气管血管束增粗紊乱,2、右肺上叶考虑陈旧结核,3、右肺占位性病变,考虑恶性可能性大,颈部可见肿大淋巴结影,建议进一步检查。遂于当地医院行“淋巴结切除术”,病理(2023-12-28)示:颈部淋巴结转移性鳞状细胞癌。2024年1月5日前往我院就诊,查体示:右颈部可触及一枚约1×1cm大小淋巴结,质硬,固定,无明显压痛,局部皮肤无红肿、破溃;心肺腹部查体未见明显异常。PS:0分。
既往史:既往体健。
个人史及家族史:否认吸烟史,偶有饮酒,无家族遗传病史。
辅助检查:
2024-01-06 胸腹增强CT:右肺上叶软组织肿物影,考虑肺癌;右侧气管旁沟、纵隔、两侧锁上、左侧腋窝、右肺门多发肿大淋巴结,考虑转移;右肺尖部分实行结节影,建议复查;肝S7边缘结节,建议MR增强扫描。
2024-01-06 上腹增强MRI:肝右叶强化结节,异常灌注?建议复查。
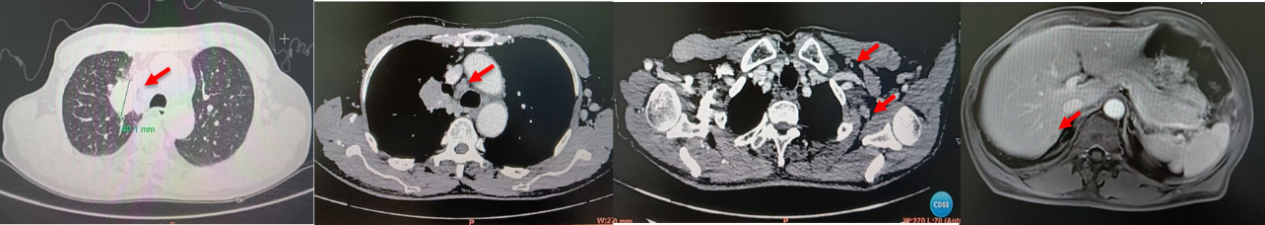
2024-01-06浅表淋巴结彩超:左侧颈血管旁、腋下及双锁上、颈后多发淋巴结结构异常。
2024-01-08 Z-CT:全身骨显像目前未见明确骨转移征象。
2024-01-08 基因检测:EGFR 18号外显子p.L718V错义突变c.2152C>G(p.Leu718Val),丰度71.34%;EGFR 21号外显子p.L858R错义突变c.2573T>G(p.Leu858Arg),丰度69.45%;EGFR 拷贝数扩增,CN=5.9;PIK3CA 21号外显子p.D1045N错义突变c.3133G>A(p.Asp1045Asn),丰度2.01%。
2024-01-08 会诊淋巴结切检病理:转移性低分化癌。加做免疫组化结果(2024-01-12):PD-L1(DAKO 22C3)(TPS:15%),PD-L1(DAKO 22C3)NCR(合格),PD-L1(DAKO 22C3)阳性对照(合格)。加做免疫组化结果(2024-01-16):AE1/AE3(+),P40(部分+),CK5/6(灶性+),TTF-1(+),Ki67(阳性细胞数40%),CEA(+),CK7(+)。癌,结合形态学及病史,考虑肺鳞癌,倾向肺源性。
2024-01-05肺癌五项: 血清胃泌素释放肽前体 79.76↑,癌胚抗原361.40↑,可溶性细胞角蛋白组分 36.47↑,神经元特异性烯醇化酶 24.37↑。
临床诊断:
1. 右肺腺鳞癌(cT2aN3M1 Ⅳ期)
2. 多发淋巴结转移
3. 肝脏结节
治疗过程及疗效评价
一线治疗:2024年1月至2024年8月,行阿美替尼(110mg qd)治疗。疗效评定为PR。
2024年8月5日,复查结果显示:右肺肿物、肝S7段结节增大,建议患者行肝穿刺,并再次行基因检测,家属考虑患者高龄拒绝有创操作。
PFS1:7个月。
表1 肿物、结节大小变化(1)

影像学检查结果(右肺肿物+肝S7段结节)如下图所示:
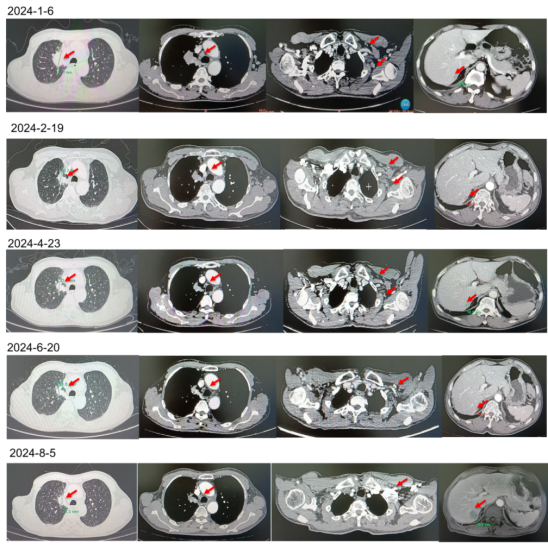
二线治疗:2024年8月至2025年6月,行长春瑞滨软胶囊节拍化疗(周一40mg,周三40mg,周五20mg)+伏美替尼方案治疗。疗效评价结果:PR。
PFS2:10个月。
表2:肿物、结节大小变化(2)
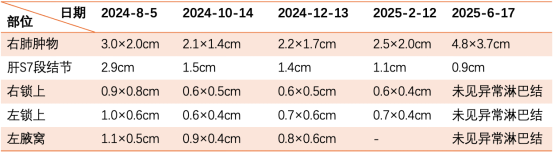
影像学结果(右肺肿物+肝S7段结节)如下图所示:
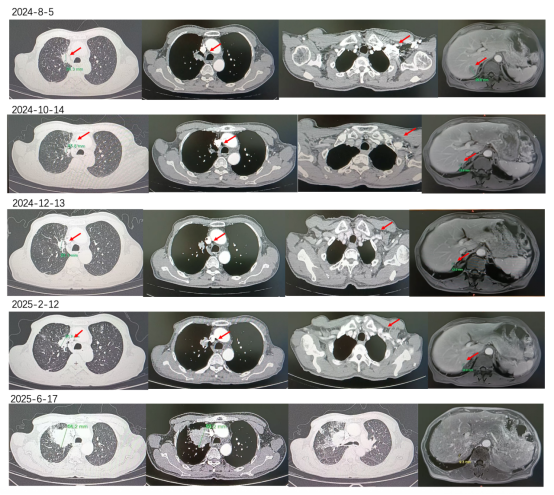
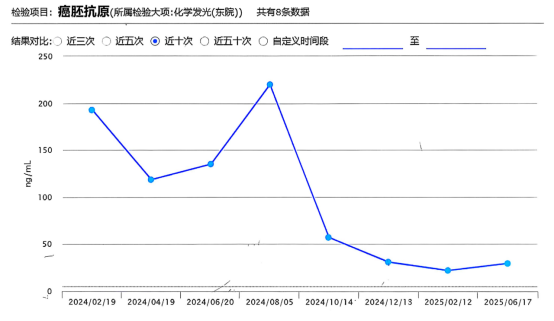
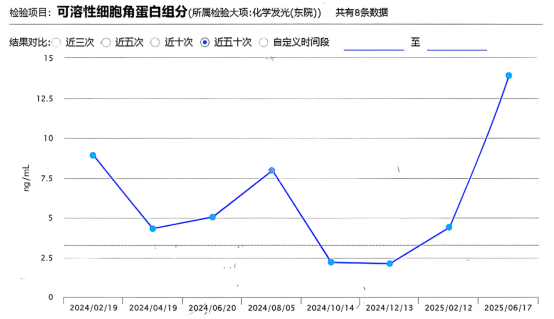
后续治疗:2025年7月12日,患者行(血液标本)基因检测,结果显示仍存在EGFR基因突变。考虑患者淋巴结及肝转移病灶达到临床完全缓解(cCR),建议予肺部原发灶局部放疗,并继续予长春瑞滨软胶囊联合EGFR-TKI全身治疗。
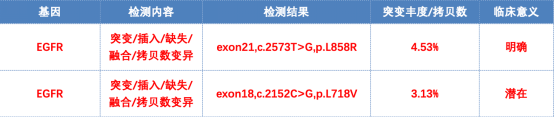
病例小结
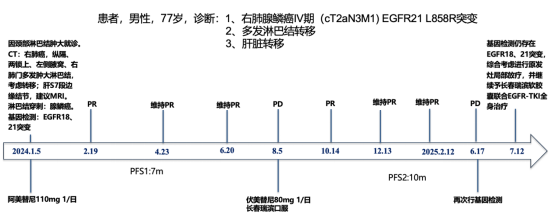
专家点评
本病例为一位初诊77岁男性患者,因“左锁上淋巴结肿大半月余,右肺鳞癌8天”就诊。该患者为临床较为少见的原发性肺癌类型,治疗过程中出现疗效分离的现象,其诊治过程具代表性,值得深入剖析。
在诊断方面,患者于当地医院行胸部 CT检查,明确了右肺占位性病变及其周围情况,提示肺癌可能。随后,患者接受了淋巴结切除术,综合影像学检查及病理会诊和基因检测,最终明确为EGFR驱动基因阳性的晚期肺腺鳞癌患者。
肺腺鳞癌的发病率仅2%-3%[1]。与腺癌和鳞状细胞癌相比,肺腺鳞癌表现出更具侵袭性的生物学行为,往往预示着更复杂的病情和更严峻的预后。为了全面评估肿瘤的全身转移情况,患者还接受了上腹部MRI和PET-CT等检查。检查结果显示,患者已出现多发淋巴结转移以及肝脏结节。综合上述检查结果,临床诊断患者为右肺腺鳞癌,具体分期为cT2aN3M1 Ⅳ期。这一精准的诊断为后续的个体化治疗提供了明确的方向和有力的证据支持。
在治疗方面,既往研究表明,尽管许多肺腺鳞癌患者接受了传统的辅助化疗,但并未观察到其对无复发生存期(RFS)和总生存期(OS)有显著的积极影响[1]。阿美替尼作为中国首个原研的第三代EGFR- TKI,能够通过不可逆地结合EGFR突变蛋白,精准地抑制肿瘤细胞的增殖与存活信号通路。基于患者的基因检测结果以及其高龄等个体特征,一线采用了阿美替尼单药靶向治疗方案。治疗后疗效评定为部分缓解(PR),进一步验证了阿美替尼在晚期EGFR驱动基因阳性NSCLC患者中的显著疗效。旨在对比阿美替尼与吉非替尼一线治疗EGFR突变的局晚期或转移性NSCLC患者的疗效的随机、Ⅲ期临床研究——AENEAS研究结果显示[2]:与吉非替尼相比,阿美替尼一线治疗显著延长了中位PFS近10个月(19.3个月 vs 9.9个月),降低了疾病进展或死亡风险达54%(HR 0.46;95%CI 0.36-0.60;P<0.001)。此外,阿美替尼的中位缓解持续时间为18.1个月(95% CI:15.2个月-不适用),而吉非替尼为 8.3 个月(95% CI:6.9个月-11.1个月)。这些数据充分证明了阿美替尼在延长患者生存时间和改善治疗效果方面的显著优势。
然而,靶向治疗最终不可避免地会出现耐药问题,其中以T790M突变耐药最为常见[3]。本例患者治疗7个月后的复查结果显示疾病进展。鉴于此,临床建议患者进行肝脏穿刺以进行二次基因检测,以进一步明确病情并调整治疗方案,但患者家属拒绝。在二线治疗领域,ALSC003研究评估了伏美替尼在一/二代EGFR-TKI耐药继发T790M突变的晚期NSCLC患者中的疗效与安全性。结果显示,中位随访9.6个月,客观缓解率(ORR)达到74%,在EGFR- TKI耐药后伴T790M突变肺癌患者中展示出了良好的疗效及可接受的安全性[4]。
此外,结合患者既往的治疗经历,考虑到其为肺腺鳞癌患者,EGFR-TKI治疗主要针对腺癌成分,而针对肺鳞癌成分的治疗则主要依赖于化疗。既往研究提示,对于部分肺鳞癌及非鳞癌但缺乏靶向治疗老年NSCLC患者而言,长春瑞滨软胶囊单药治疗是一种临床效果良好且可选择的方案[5]。这主要是因为长春瑞滨软胶囊在保证治疗疗效的同时,具有更低的不良事件发生率。其口服剂型能够减少患者的住院时间及经济负担,避免注射相关并发症,从而显著提高老年患者接受规范有效治疗的依从性,进而延长OS[5-9]。
考虑本例患者高龄,静脉化疗的耐受性通常较差,因此在二线治疗中选择了长春瑞滨软胶囊联合伏美替尼的治疗方案。治疗过程中,患者取得了PR的良好疗效。至2025年6月,患者PFS达10个月,且淋巴结及肝转移病灶达到cCR。这一治疗方案的成功应用,再次证明了个体化治疗策略在晚期肺腺鳞癌患者中的重要性和有效性,为类似病例的治疗提供了有益的参考。
[1] Tomoyuki Hishida, Jiro Okami, Hisao Asamura, et al. Clin Lung Cancer. 2024 Sep;25(6):519-528.e3.
[2] Shun Lu, Xiaorong Dong, Hong Jian, et al. J Clin Oncol. 2022 Sep 20;40(27):3162-3171.
[3]任胜祥,邱天羽. 肺癌精准治疗的发展与展望[J].Cancer Research on Prevention & Treatment, 2023, 50(5).DOI:10.3971/j.issn.1000-8578.2023.22.1208.
[4]Shi YK, Hu XS, Zhang SC, et al. Lancet Respir Med, 2021, 9(8): 829-839. DOI:10.1016/S2213-2600(20)30455-0.
[5] 林金兰, 郭天兴, 潘小杰, 徐振武. 长春瑞滨软胶囊单药节拍化疗一线治疗老年非小细胞肺癌临床疗效观察[J]. 肿瘤防治研究, 2018, 45(11):909-912.
[6] Andrea Camerini , Cheti Puccetti , Sara Donati ,et al.BMC Cancer . 2015 May 6;15:359.
[7]刘花,陈延绅,尤慧柠,等.长春瑞滨药动学及毒副作用研究进展[J].中国药房,2022,33(11):1403-1408.
[8] Yang Y, et al. A randomised, multicentre open-label phase II study to evaluate the efficacy, tolerability and pharmacokinetics of oral vinorelbine plus cisplatin versus intravenous vinorelbine plus cisplatin in Chinese patients with chemotherapy-naive unresectable or metastatic non-small cell lung cancer. J Thorac Dis. 2019;11(8):3347-3359.
[9] Gridelli C, et al. Oral vinorelbine given as monotherapy to advanced, elderly NSCLC patients: a multicentre phase II trial. Eur J Cancer. 2004;40(16):2424-31.
排版编辑:肿瘤资讯-老猫











 苏公网安备32059002004080号
苏公网安备32059002004080号


