晚期鳞状非小细胞肺癌(NSCLC)的治疗选择有限且预后较差,是临床面临的严峻挑战。近年来,以PD-1/PD-L1抑制剂为代表的免疫治疗显著改善了部分患者的生存。III期临床研究GEMSTONE-302证实,舒格利单抗作为一种新型PD-L1抑制剂联合化疗一线治疗IV期NSCLC(包括鳞癌)可带来显著的无进展生存期(PFS)和总生存期(OS)获益,且安全性可控,为晚期肺鳞癌治疗带来了新的突破。本文分享了一例53岁女性IVA期肺鳞癌患者通过接受舒格利单抗联合化疗及后续局部放疗,取得了部分缓解并维持长达23个月以上无进展生存的病例,展现了舒格利单抗在真实世界中的临床价值和良好的应用前景。
本病例由广东医科大学附属医院林燕明医生分享,【肿瘤资讯】特此整理,并邀请广东医科大学附属医院李姝君教授进行点评,与大家共同学习。
广东医科大学附属医院肺部肿瘤病区主治医师、在读博士
湛江市医师协会肿瘤放疗医师分会委员
湛江市医学会肺部肿瘤学分会青年委员会委员
广东省基层医药学会放射肿瘤专业委员会委员
广东省胸部肿瘤防治研究会粤西分会委员
擅长:肺癌的诊断及放化疗治疗。曾参与国家青年基金1项。发表SCI 2篇
患者基本信息与检查诊断
患者信息
女性,53岁,无吸烟史,无饮酒史。
主诉:气促1周,发现左肺占位1天。
现病史:患者于2023年4月27日就诊,主诉一周前无明显诱因出现活动后气促,伴轻微咳嗽及右背部轻微疼痛。当地医院2023年4月26日胸部CT提示左下肺肿块,考虑肺癌伴隆突下淋巴结转移可能。
既往史与家族史:无特殊慢性病史及过敏史。家族史无特殊。
体格检查: PS=1分,双肺呼吸音清,未闻及干湿啰音。心腹检查未见异常。
血液学检查 (2023年4月28日):NSE: 20.00 ng/ml↑, CEA: 5.57 ng/ml↑, CYFRA21-1: 8.930 ng/ml↑, SCC: 0.69 ng/ml。
影像学检查 (CT & PET/CT):
2023年4月30日胸部CT:左下肺近肺门占位,考虑中央型肺癌伴阻塞性肺炎/肺不张,纵隔及左肺门淋巴结转移。左肺下叶局部小叶间隔增厚,不除外淋巴道转移,左下肺静脉受侵可能。左肺上叶舌段、右肺下叶前基底段近斜裂旁亦见结节。
PET/CT(2023年5月9日):
1.左肺下叶中央型肺癌伴阻塞性肺炎、肺不张,请结合病理。
2.纵隔及左肺门区淋巴结转移。左侧胸膜(左侧第7前肋处及第9后肋处)转移瘤。
支气管镜检查 (2023年5月4日):支气管外压狭窄。肺门淋巴结穿刺活检病理提示鳞状细胞癌。纤支镜活检病理提示左肺上叶鳞状细胞癌,可见片状坏死。
病理检查:
2023-05-04行纤支镜活检术:鳞状细胞癌,可见片状坏死。
免疫组化:TTF-1(-), NapsinA(-), Ki67(约40%+), P40(+), CK5/6(+), Syn(-), CgA(-), CD56(个别细胞+), CK(+); 2312261(2): Alk(D5F3)(-)。PD-L1 (SP263):TC约25%;IC约3%。
诊断: 左下肺鳞癌 (cT4N2M1a (胸膜)) IVA期 PD-L1(TC约25%)。
治疗与疗效
2023年5月-7月:接受4个周期的舒格利单抗 (1200mg) + 白蛋白紫杉醇 (380mg) + 卡铂 (490mg) 治疗。
2周期后疗效 (2023年6月20日):病情稳定 (SD),肿瘤缩小。
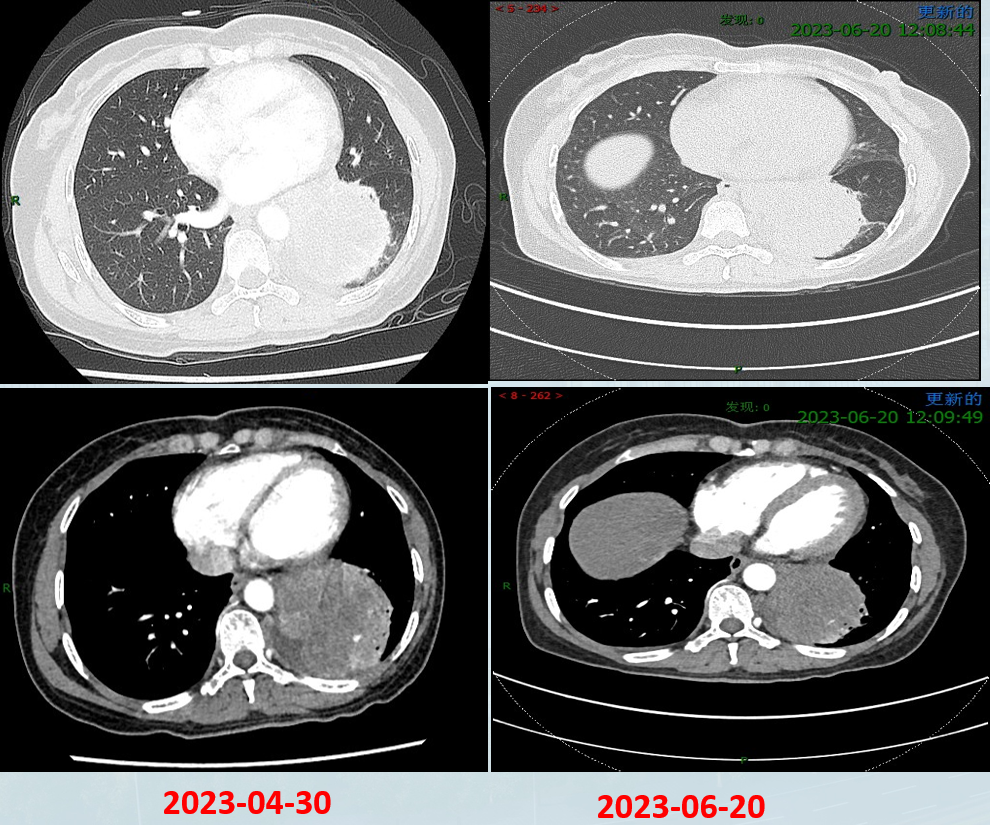
4周期后疗效 (2023年8月2日):部分缓解 (PR)。
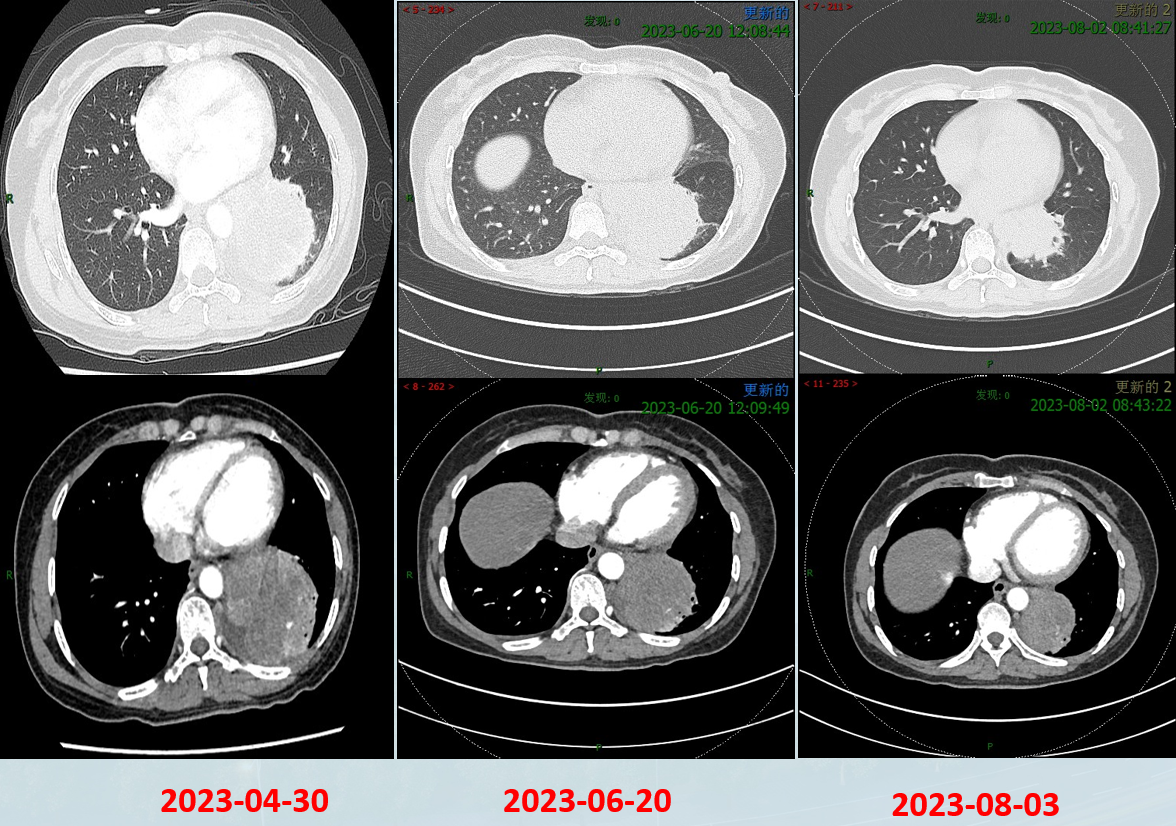
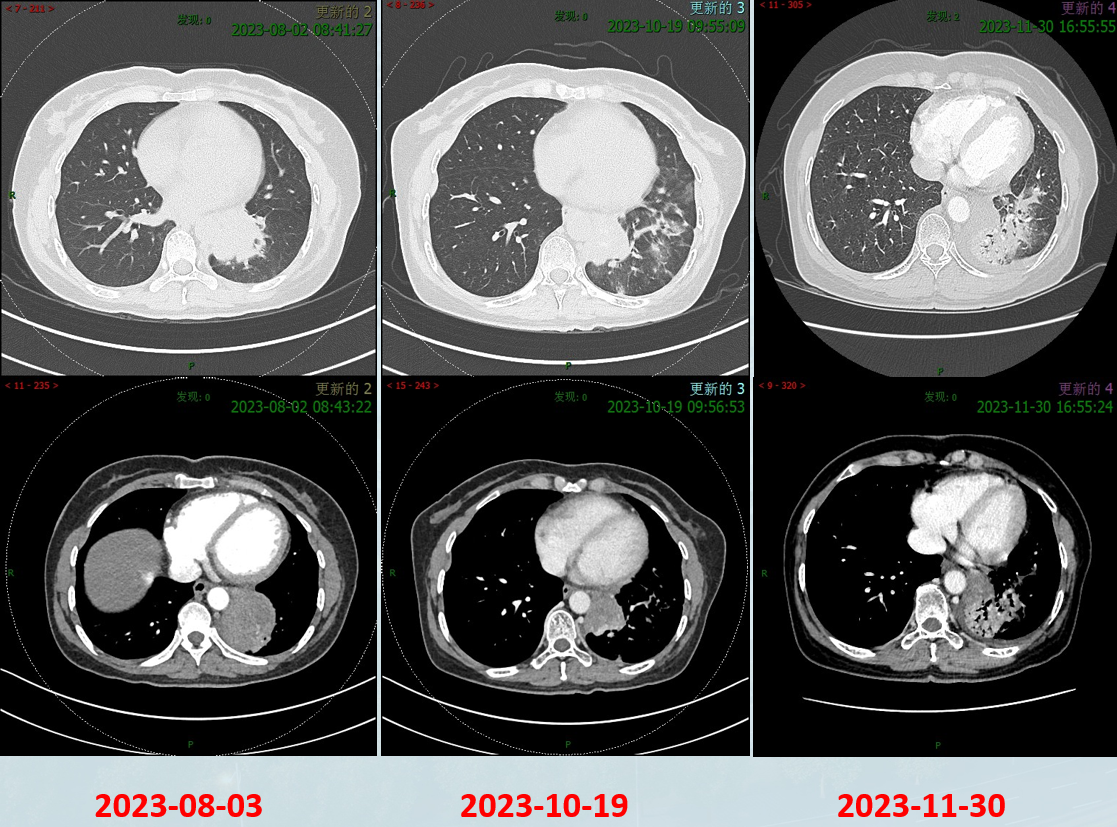
2023年8月-11月:原发灶胸部放疗 (PGTV 60.20Gy/28F)。
2023年10月-11月:放疗后接受2个周期的舒格利单抗维持免疫治疗。
疗效 (2023年10月19日 & 11月30日):持续PR。
肺炎:患者出现肺炎。暂停免疫治疗,并给予激素、抗感染及支气管扩张剂雾化治疗。
随访CT (2024年1月2日, 1月24日, 2月18日):影像显示肺炎相关改变及治疗反应。
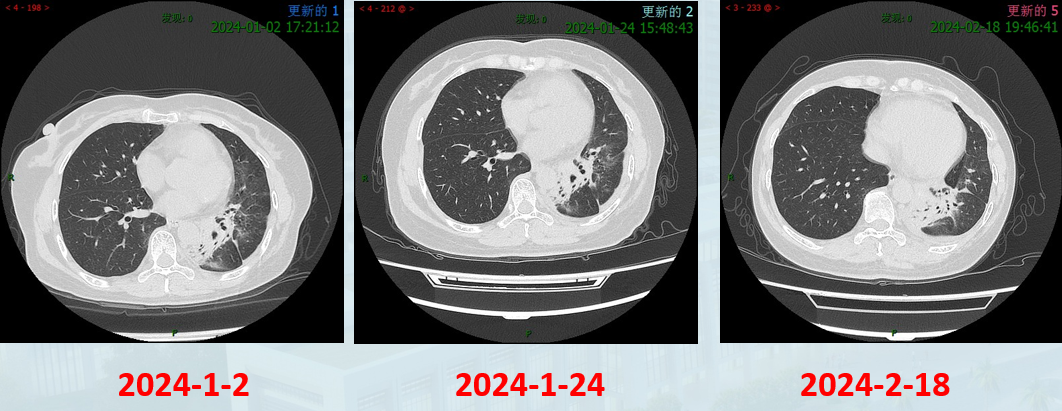
2024年1月25日:重新开始舒格利单抗免疫治疗。末次免疫治疗为2025年3月27日。
后续随访 (2024年3月12日, 4月29日, 6月11日, 7月24日, 9月11日, 10月30日, 12月11日, 及2025年2月13日):持续PR。患者已获得23个月以上的PFS。
复查(2024年10月30日, 12月11日;2025年2月13日,4月16日):
右上纵膈淋巴结:增大SD;T11-T12椎间孔处转移瘤:增大SD。
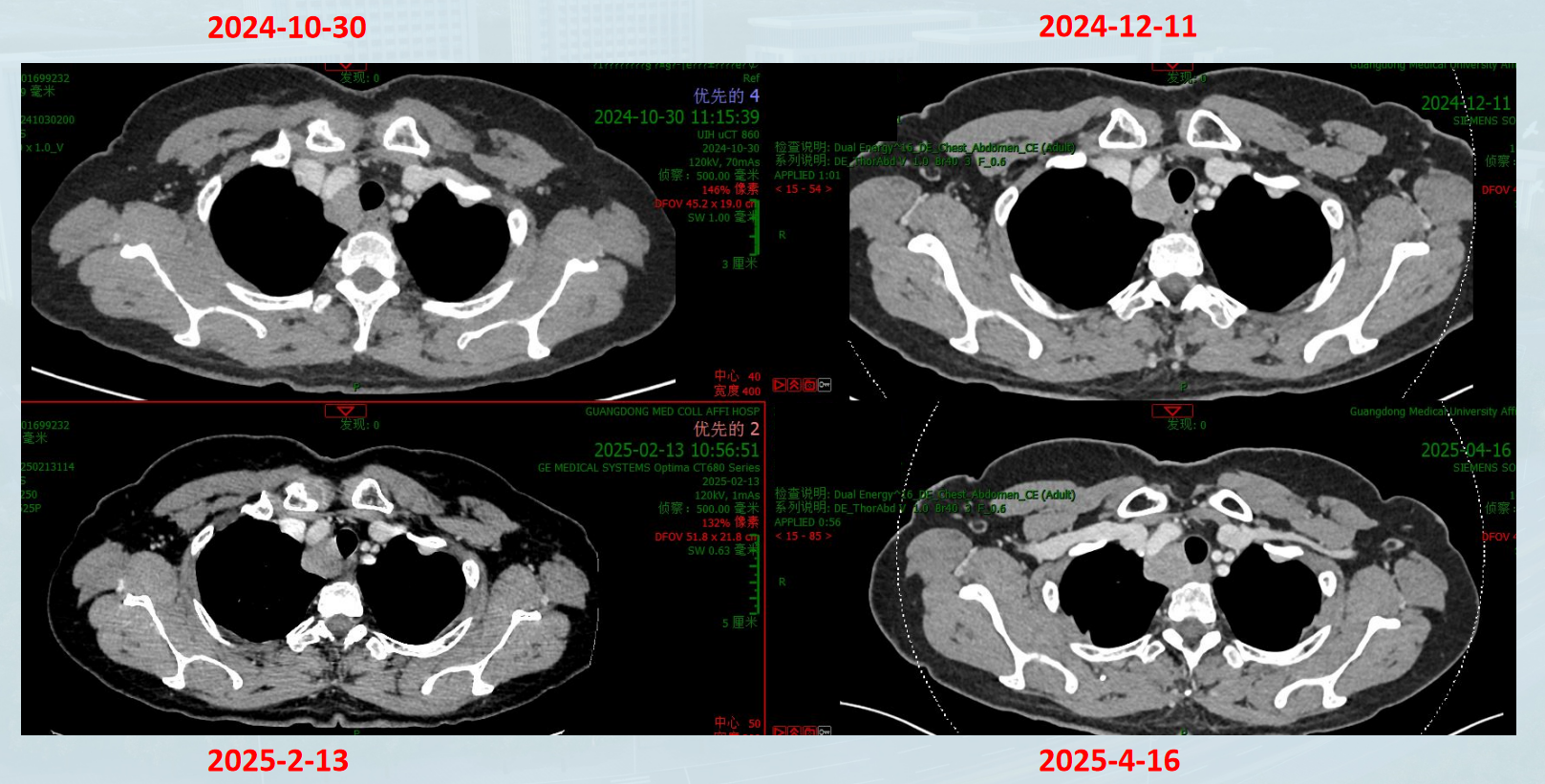
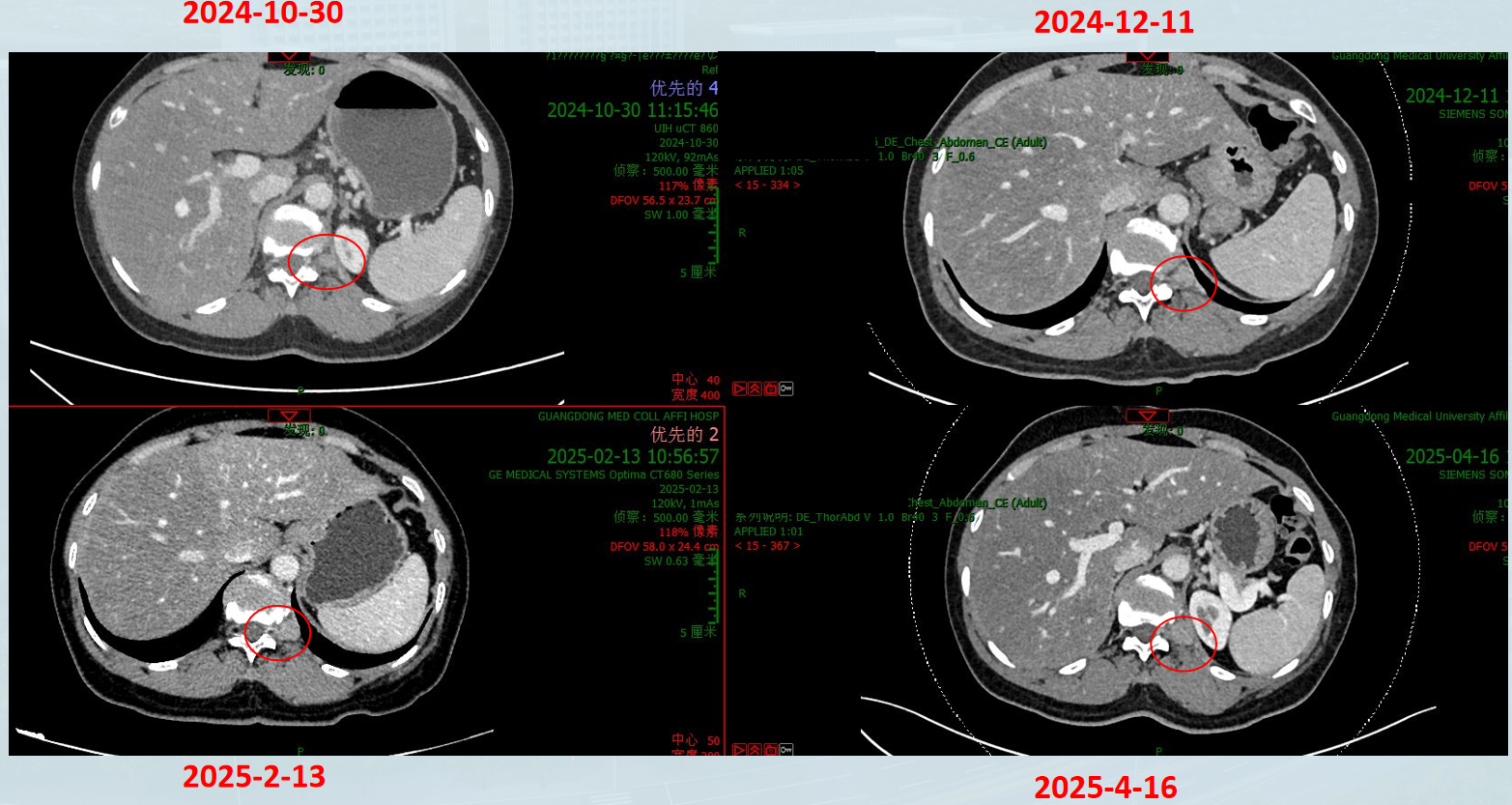
2025年4月疗效评价:增大SD,暂停舒格利单抗免疫治疗。
2025-5-13行姑息性放疗:
右上纵膈淋巴结转移灶:PGTV-nd:61.6GY/28F/2.2GYT11-T12
锥旁转移灶:PGTV:30GY/6F/5GY

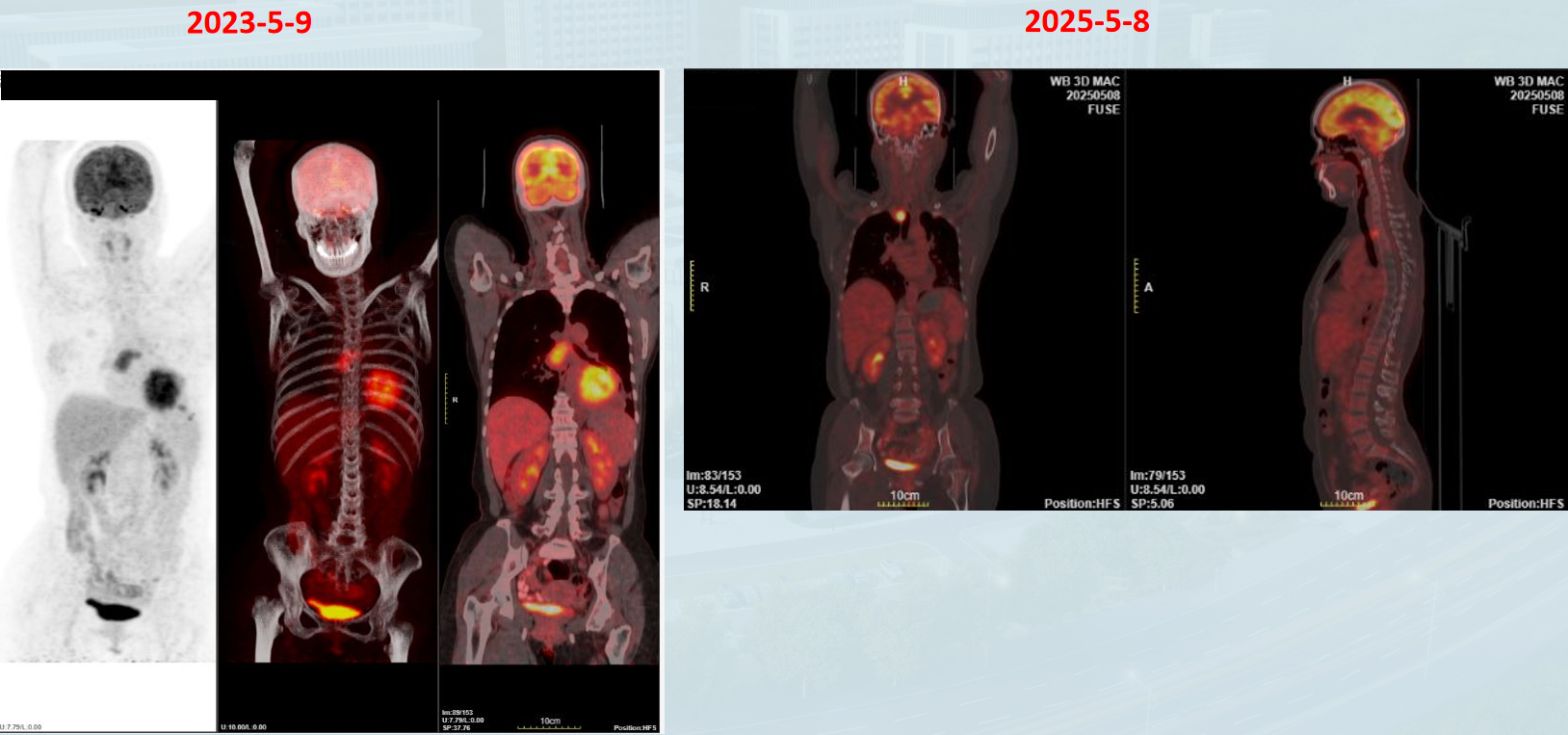
PET-CT前后对比
广东医科大学附属医院肺部肿瘤专区主任医师
湛江市医学会肺部肿瘤学分会副主委
临床医学会真实世界委员会常委
广东省胸部肿瘤防治研究会粤西分会常委
广东省医师协会肿瘤内科医师分会委员
广州市抗癌协会肿瘤复发与转移专业委员会委员
广东省女医师学会肺癌专业委员会委员
广东省抗癌协会肺癌专业委员会委员
广东省抗癌协会肿瘤标志专委会委员
广东省药学会药物临床试验专业委员会委员
广东省胸部疾病学会肿瘤急危重症专业委员会委员
广东省药学会胸外科专业委员会委员
病例点评
李姝君教授:本例患者为一名53岁女性,诊断为左下肺鳞癌伴胸膜转移(cT4N2M1a,IVA期),PD-L1表达TC约25%。该病例的治疗和管理充分体现了一线舒格利单抗联合化疗在晚期肺鳞癌中的良好疗效和耐受性。
舒格利单抗是一款全长全人源PD-L1抑制剂,从结构设计上看,其独特地保留了FcγR结合功能,能够介导抗体依赖性细胞介导的吞噬作用(ADCP),进一步介导巨噬细胞杀伤肿瘤细胞,增强抗肿瘤活性。
III期试验GEMSTONE-302研究数据显示1,舒格利单抗联合化疗一线治疗IV期NSCLC(包括鳞癌和非鳞癌),中位PFS达到9.0个月,中位OS达到25.2个月,均显著优于单纯化疗组。尤其在鳞癌亚组中,舒格利单抗联合化疗的PFS HR值低至0.34,客观缓解率(ORR)超过70%,4年OS率达到27.6%,显示出卓越的疗效。长期随访显示,在多种针对IV期鳞癌的免疫联合治疗方案中,舒格利单抗联合方案在中位OS(23.6个月 vs 12.2个月,延长11.4个月)和4年OS率(27.6% vs 11.7%,提升15.9%)方面的改善幅度最大1–3。
此外,无论PD-L1表达状态如何,舒格利单抗均能带来生存获益。在包括晚期鳞癌与非鳞癌的PD-L1低表达(1%-49%)人群中,舒格利单抗联合化疗一线治疗下中位OS达24.8个月(对照组17.7个月),而PD-L1高表达(≥50%)人群的中位OS更达39.2个月,显著优于对照组(19.8个月),与三代EGFR-TKI单药靶向治疗数据(38.6个月)相近4,为驱动基因阴性患者带来了长期生存的希望。本例患者PD-L1 TC约25%,在接受4程联合治疗后即达到PR,并且持续PR,维持了长达23个月以上的PFS,证实了该方案在真实世界中的有效性。
患者在免疫联合化疗取得PR后,接受了针对胸部原发灶的放疗。对于寡转移或局部病灶控制良好的晚期NSCLC患者,局部巩固治疗如放疗可能带来额外的生存获益,有助于进一步清除肿瘤负荷,延缓疾病进展。
在整个治疗过程中,全面的患者管理对于及时发现和处理肺炎等问题至关重要。本例患者通过暂停免疫治疗、给予激素及对症支持治疗后,肺炎得到有效控制,并成功重启舒格利单抗治疗。GEMSTONE-302研究中,舒格利单抗组发生≥3级免疫相关不良事件 (irAEs) 的比例为3.1%,≥3级免疫相关性肺炎的发生率仅为0.9%,安全性良好5。
舒格利单抗联合化疗方案凭借其在大型临床研究中证实的显著生存获益和良好安全性,已成为晚期鳞状NSCLC的重要一线治疗选择。未来,通过进一步筛选优势人群,探索联合治疗的最佳模式以及克服耐药等问题,舒格利单抗有望为晚期NSCLC患者带来更多获益。
1. Zhou C, Wang Z, Sun M, et al. 1318P Four-year outcomes from GEMSTONE-302 study: First-line sugemalimab plus platinum-based chemotherapy in metastatic non-small cell lung cancer (NSCLC). Ann Oncol. 2024;35:S839. doi:10.1016/j.annonc.2024.08.1374
2. Novello S, Kowalski DM, Luft A, et al. Pembrolizumab Plus Chemotherapy in Squamous Non–Small-Cell Lung Cancer: 5-Year Update of the Phase III KEYNOTE-407 Study. J Clin Oncol. 2023;41(11):1999-2006. doi:10.1200/JCO.22.01990
3. Carbone DP, Ciuleanu TE, Schenker M, et al. Four-year clinical update and treatment switching-adjusted outcomes with first-line nivolumab plus ipilimumab with chemotherapy for metastatic non-small cell lung cancer in the CheckMate 9LA randomized trial. J Immunother Cancer. 2024;12(2):e008189. doi:10.1136/jitc-2023-008189
4. Ramalingam SS, Vansteenkiste J, Planchard D, et al. Overall Survival with Osimertinib in Untreated, EGFR-Mutated Advanced NSCLC. N Engl J Med. 2020;382(1):41-50. doi:10.1056/NEJMoa1913662
5. Zhou C, Wang Z, Sun M, et al. Interim survival analysis of the randomized phase III GEMSTONE-302 trial: sugemalimab or placebo plus chemotherapy as first-line treatment for metastatic NSCLC. Nat Cancer. 2023;4(6):860-871. doi:10.1038/s43018-023-00578-z
排版编辑:肿瘤资讯-高乐乐











 苏公网安备32059002004080号
苏公网安备32059002004080号


