近年来,胃/胃食管结合部(GEJ)腺癌治疗领域取得了显著进展,尤其是在免疫治疗、靶向治疗和联合治疗方面。诸如CheckMate 577和TOPGEAR等研究为GEJ腺癌的围手术期策略提供了宝贵经验;而针对HER2阳性晚期胃癌,新的靶向治疗药物和ADC药物正在改变一线治疗格局;此外,抗血管生成药物在晚期胃癌治疗中的角色也面临新的评估与思考。中国人民解放军总医院苟苗苗教授基于最新的临床研究数据,深入探讨了这些关键领域的研究进展与未来方向,旨在为临床优化胃癌治疗策略提供参考。
日本国立癌研医院 高级访问学者
北京癌症防治学会胃癌防治青年委员会常务委员
CSCO胰腺癌、胆道癌、抗肿瘤药物安全、老年肿瘤防治专委会委员
中国研究型医院学会精准医学与肿瘤MDT专委青年委员、肿瘤外科委员会委员
中国医师协会结直肠肿瘤MDT学组委员、医工融合与智能医学学组委员
中国抗癌协会头颈肿瘤整合康复专委会委员
北京抗癌协会胃癌专业委员会常委
长期以来从事消化道肿瘤的综合治疗,以第一作者发表15余篇SCI论文
多次参与ASCO和ASCO-GI及国内会议交流
CSCO化疗安全管理大赛第一名,个人风采奖
主持一项青年成长课题,参与2项国自然课题和2项重大课题的研究,
撰写中国胆管肿瘤多学科综合治疗专家共识、2023人卫出版社《结肠癌肿瘤学》、中国胃癌肝转移诊断与综合治疗中国专家共识(2024版)
一、胃食管结合部腺癌的治疗策略思考:Checkmate577研究和TOPGEAR研究
CheckMate 577研究:新辅助放化疗联合辅助免疫治疗
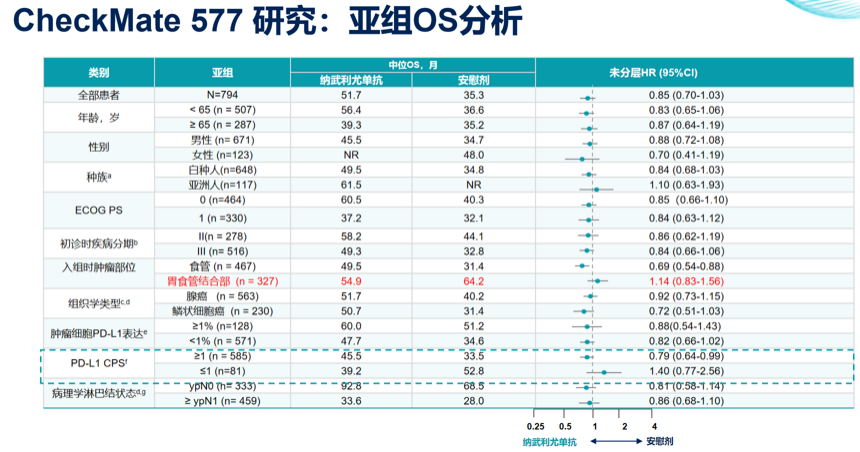
CheckMate 577是一项III期、随机、多中心、双盲临床研究,是首个辅助免疫治疗在接受新辅助放化疗及手术切除后仍存在病理学残留的食管癌或胃食管结合部癌患者中取得阳性结果的研究。该研究旨在评估纳武利尤单抗在接受新辅助放化疗及手术切除后仍存在病理学残留的食管癌或胃食管结合部癌患者中的疗效与安全性。研究共入组794例患者,2∶1随机分配至接受纳武利尤单抗或安慰剂治疗,总计治疗时长为1年。最终结果表明DFS获益显著:纳武利尤单抗组的中位无病生存期(DFS)达到21.8个月,显著优于安慰剂组的10.8个月(HR=0.76;95%CI 0.63~0.91),并且无远处转移生存(DMFS)也显著改善(中位DMFS:27.3个月 vs 14.6个月;HR=0.75)。尽管总生存期(OS)趋势积极(5年OS率提升5%,46% vs 41%;HR=0.85,P=0.1064),但未达到统计学显著差异,这可能与安慰剂组较高的交叉治疗率(60%复发后接受免疫治疗)有关。值得注意的是,研究中54.9%为胃食管结合部患者,51.7%为腺癌患者。亚组分析结果表明,胃食管结合部患者并未能从辅助免疫治疗中获益。
TOPGEAR研究:新辅助放化疗联合围手术期化疗
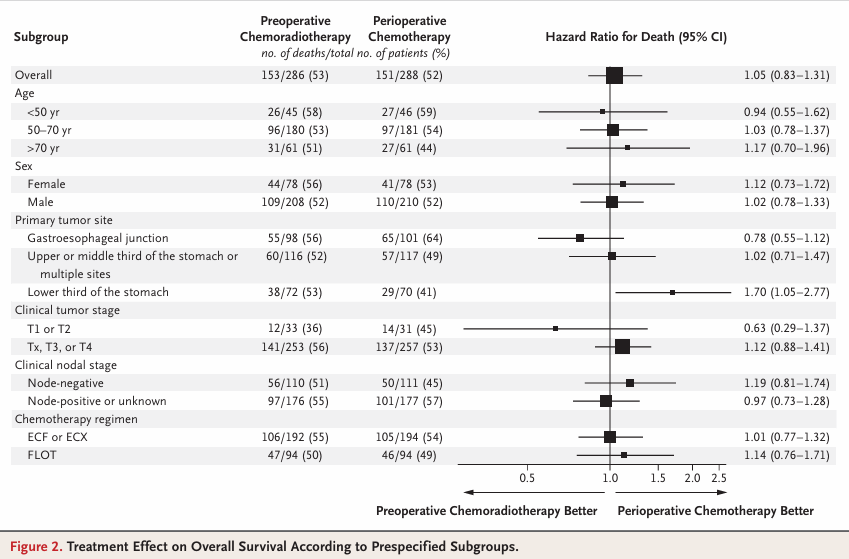
TOPGEAR研究是首个评估术前放化疗(CRT)联合围手术期化疗(CT)在可切除胃/胃食管结合部腺癌患者中临床价值的随机III期试验。研究结果显示,与仅围手术期化疗相比,术前放化疗联合围手术期化疗的病理完全缓解(pCR)率较高(17% vs 8.0%),且未显著增加毒性,然而,研究主要终点总生存期(OS)并无显著差异(46个月 vs 49个月;HR=1.05)。该研究中纳入了56%的胃食管结合部患者,尽管风险比(HR)跨越了1,但似乎腺癌患者在新辅助放化疗中存在获益趋势。如果这些患者在新辅助放化疗术后给予如CheckMate 577研究中的辅助免疫治疗,是否能产生更好的OS数据?
二、HER2高表达晚期胃癌一线治疗:多重选择与策略考量
随着针对HER2靶点的新型药物和联合方案的不断涌现,HER2阳性晚期胃癌的一线治疗选择出现多种组合拳模式,临床选择上将面临更多考量。
KEYNOTE-811:PD-L1 CPS表达水平成为重要考量因素
2024年ESMO年会上,KEYNOTE-811研究的最终OS结果已明确指出,对于PD-L1 CPS≥1的患者,曲妥珠单抗联合帕博利珠单抗和化疗(靶免化)能够带来显著的OS获益,中位OS提升至20.1个月。然而,对于PD-L1 CPS<1的患者,统计学上未能从靶免化模式中获益。因此,在目前的临床实践中,我们是基于KEYNOTE-811研究的循证医学证据去践行,PD-L1 CPS表达水平已成为HER2阳性晚期胃癌一线治疗的重要考量因素。
泽尼达妥单抗(ZW25):HER2靶向双特异性抗体的巨大潜力
HER2靶向双特异性抗体泽尼达妥单抗已获批用于既往接受过全身治疗的HER2阳性不可切除局部晚期或转移性胆道癌的治疗。此外,在2024年ESMO大会上公布了一项II期研究数据,结果表明泽尼达妥单抗联合mFOLFOX6-2化疗或不联合贝伐单抗一线治疗HER2阳性、不可切除、局部晚期、复发或转移性结直肠癌(mCRC)患者显示出抗肿瘤活性和安全性。
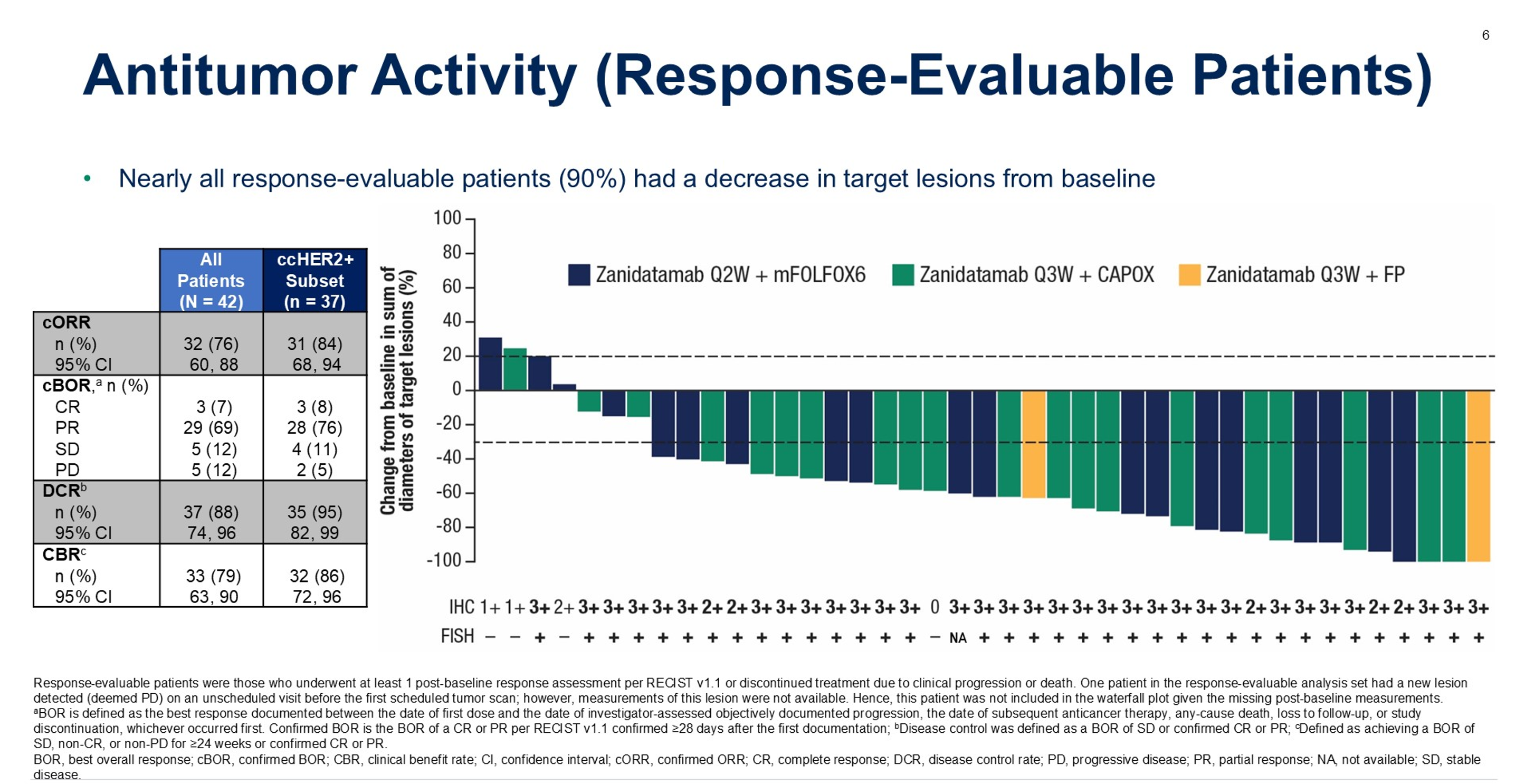
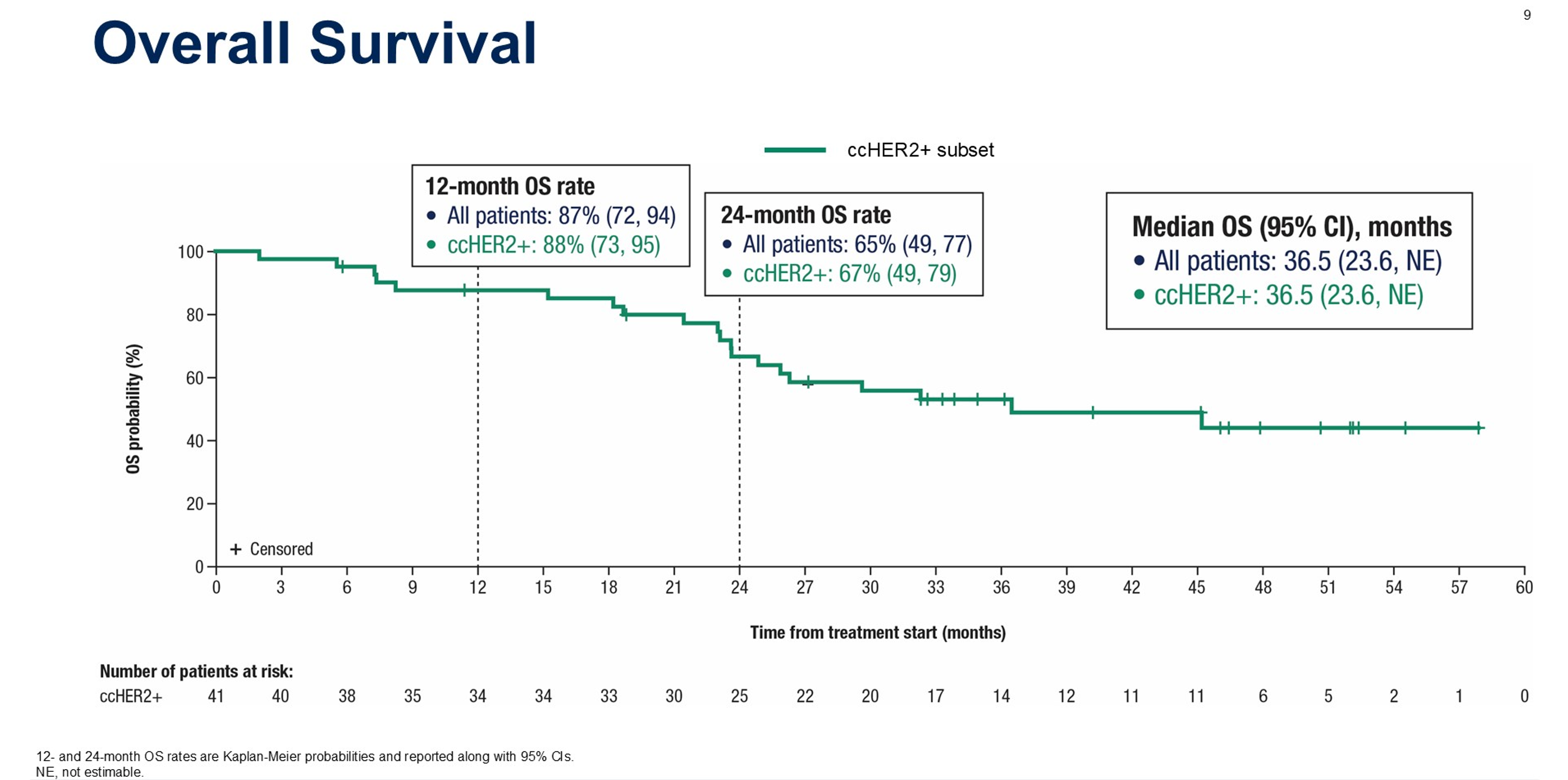
其在胃癌领域同样展现出令人鼓舞的临床应用前景,一项多中心、开放标签的II期临床试验评估了泽尼达妥单抗联合标准化疗作为HER2阳性晚期胃食管腺癌患者一线治疗的疗效和安全性,2024年ESMO公布的数据显示,泽尼达妥单抗+FOLFOX6组经确认的客观缓解率(cORR)达83.3%;今年ASCO公布的4年随访结果进一步显示,所有人群中cORR为76%,HER2高表达亚组中cORR达84%,41例经中心实验室评估为HER2阳性患者的mPFS为15.2个月,中位OS高达36.5个月,这一中位OS提示泽尼达妥单抗具有改变当前一线治疗格局的巨大潜力。安全性方面,腹泻是该方案需要重点关注的治疗相关不良事件,预防性止泻措施实施后,≥3级腹泻发生率从52%降至24%。
此外,一项Ib/II期研究中,泽尼达妥单抗联合替雷利珠单抗及化疗作为一线方案治疗HER2阳性晚期胃癌,2023年ESMO大会更新数据显示,总体ORR为75.8%,中位PFS为16.7个月,中位反应持续时间(DoR)达22.8个月,显示出持久的抗肿瘤活性,其全球III期ZWI-ZW25-301研究正在进行中,其结果有望挑战靶免化的治疗模式。
抗体药物偶联物(ADCs)前移:新一代疗法的竞争
ADC药物的兴起也为HER2阳性胃癌的一线治疗带来了新的可能性,其前移趋势日益明显。
维迪西妥单抗(RC48):2024年ASCO报道的RCT研究结果显示,一线维迪西妥单抗联合替雷利珠单抗和S-1在53例患者中ORR达到94.3%。今年ASCO更新结果显示,意向治疗(ITT)人群中,确认的ORR为89.4%,中位PFS达到13.1个月,OS尚未成熟,但18个月OS率达到67.8%。
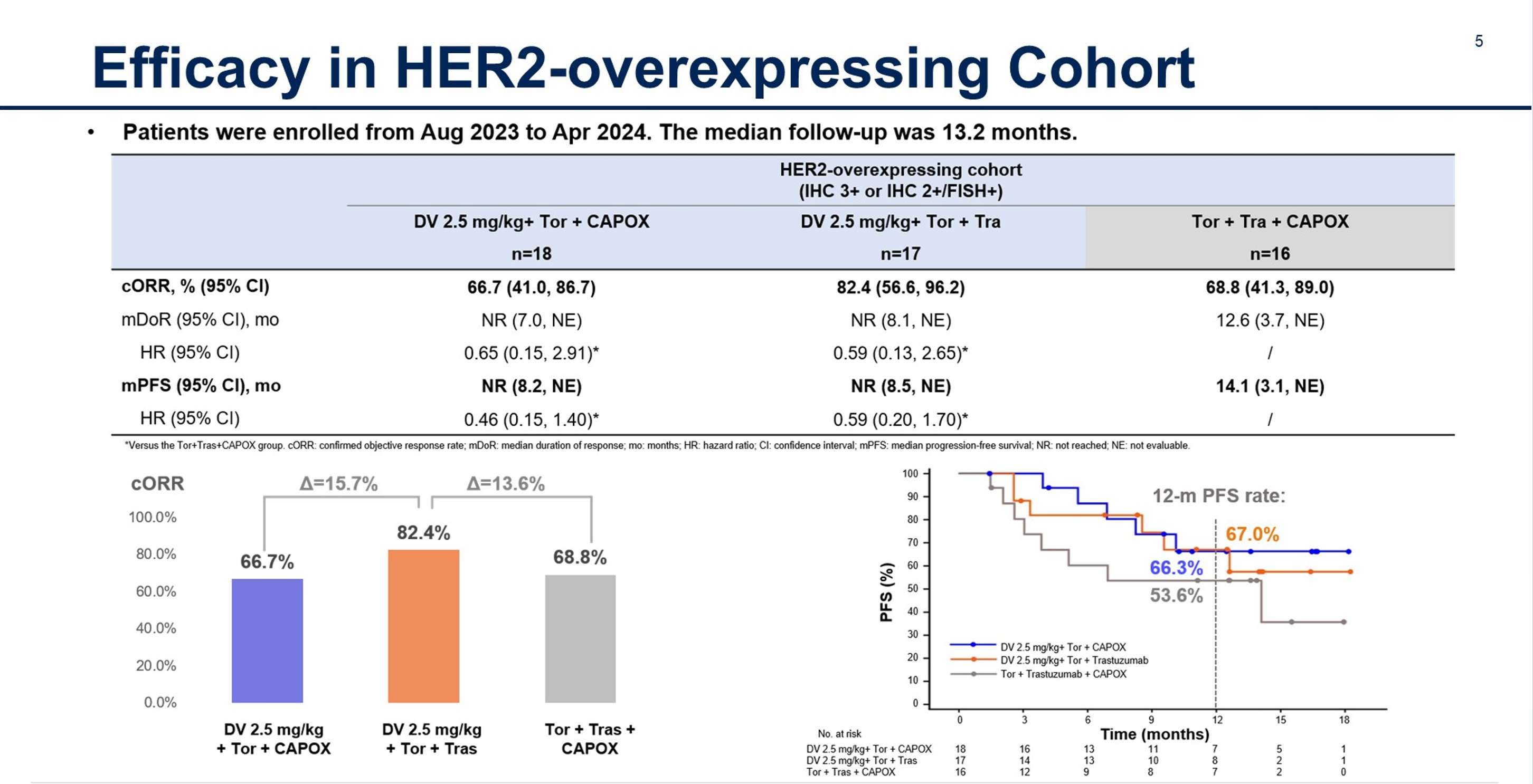
此外,沈琳教授在今年ASCO上口头报告了C027研究结果,强调了根据HER2表达水平采取不同治疗模式的重要性。在HER2高表达或阳性人群中,维迪西妥单抗联合PD-1单抗和曲妥珠单抗,ORR可达82.4%;在HER2中、低表达患者中,维迪西妥单抗+PD-1单抗+化疗的疗效明显优于标准治疗,且通过化疗剂量优化后,安全性也得到明显改善。
德曲妥珠单抗(T-DXd):2024年ESMO大会上,DESTINY-Gastric03研究探索了德曲妥珠单抗单药或联合帕博利珠单抗/卡培他滨的数据,并基于此启动了III期随机对照DESTINY-Gastric05研究。
这些HER2 ADC药物的齐头并进,预示着未来一线治疗领域将出现更多新的选择,最终可能面临多种个性化的治疗选择。但对于胃癌的治疗,全程管理和排兵布阵是一门艺术,未来ADC药物前移后的耐药问题又将成为新的讨论话题。
三、晚期胃癌一线抗血管生成药物:转化治疗的新机遇
在过去,晚期胃癌一线治疗中抗血管生成药物的临床研究屡遭挫折,包括AVAGAST、AVATAR、RAINFALL和RAINSTORM等研究OS均未取得阳性结果,这让研究者们对将抗VEGFR药物联合PD-1抑制剂的策略产生了疑问。
LEAP-015研究的困境
LEAP-015研究是一项随机、开放标签的III期研究,旨在评估帕博利珠单抗联合仑伐替尼和化疗作为晚期/转移性胃食管腺癌一线治疗的疗效。尽管中期分析结果显示,与传统化疗相比,帕博利珠单抗联合仑伐替尼和化疗能够显著提高患者的PFS和ORR,但在最终分析时,对于PD-L1 CPS≥1的患者,OS改善未达到统计学显著性(12.6个月 vs 12.9个月;HR=0.84;95%CI 0.71~1.00;P=0.0244,显著性边界值为0.0204)。
转化治疗:抗血管生成药物的新出路
国内的一些探索性研究为抗血管生成药物在转化治疗中的应用提供了初步的积极证据:
梁寒教授开展的一项前瞻性、单臂、单中心的II期CO-STAR研究评估了信迪利单抗联合阿帕替尼和双药化疗在晚期胃癌患者转化治疗中的疗效。结果显示,经转化治疗的患者中位OS达25.7个月,中位无事件生存期(EFS)达15.3个月。此外,2025年ASCO GI大会上,一项呋喹替尼联合信迪利单抗和SOX转化治疗在不可切除局部晚期或转移性胃/胃食管结合部腺癌的单臂II期临床试验的更新数据显示,在41例可评估疗效的患者中,R0转化率为82.9%,ORR为73.2%,DCR为97.6%。
这些研究结果提示,尽管在晚期胃癌一线治疗中抗血管生成药物面临挑战,但其用于转化治疗可能是一条有前景的出路。
总结与展望
胃/胃食管结合部腺癌的治疗正从传统的单一治疗模式转变为基于分子分型和患者特征的个体化、多模式综合治疗。CheckMate 577和TOPGEAR研究揭示了胃食管结合部腺癌治疗的复杂性,并提示了新辅助放化疗联合术后免疫治疗的应用潜力。对于HER2阳性晚期胃癌的一线治疗,目前面临着靶免化、双特异性抗体和ADC药物等多种治疗选择,需要综合考量。同时,抗血管生成药物在晚期胃癌一线治疗中面临挑战,但在转化治疗领域展现出新的希望。未来的胃癌治疗将更加注重全程管理和排兵布阵,通过不断深入研究肿瘤的生物学特性,开发新的治疗靶点和策略,优化现有药物的组合和应用时机,为胃癌患者带来更长久的生存和更好的生活质量。
排版编辑:肿瘤资讯-Skye











 苏公网安备32059002004080号
苏公网安备32059002004080号


