随着DeepSeek等人工智能(AI)技术的快速发展,医疗领域的智能化探索持续深入。在惰性B细胞淋巴瘤治疗中,布鲁顿酪氨酸激酶抑制剂(BTKi)的临床应用已取得显著进展。而AI的融入正为惰性淋巴瘤的精准化治疗注入新动能。
那么,对于惰性B细胞淋巴瘤
当BTKi遇见AI,会碰撞出怎样的“火花”呢?
DeepSeek将通过智能推演与临床实践案例分析
分析BTKi精准治疗进化的"技术密码"
探讨靶向治疗时代下惰性B细胞淋巴瘤治疗的破局之道
为临床决策提供创新视角
从跟跑到领跑
中国“智”造BTKi
为惰性B细胞淋巴瘤带来治疗新选择
作为一组异质性较强的惰性淋巴系统肿瘤,惰性B细胞淋巴瘤包括滤泡性淋巴瘤(FL)、慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)、华氏巨球蛋白血症(WM)、边缘区淋巴瘤(MZL)及套细胞淋巴瘤(MCL)等主要亚型[1]。
惰性淋巴瘤多见于60岁以上的中老年人,而老年患者常伴随各种基础疾病且体能状态较差。因此,该类患者的治疗需要兼顾安全性和疗效。此外,多个惰性淋巴瘤亚型目前仍不可治愈,因此长期高质量生存是患者的主要治疗目标。随着分子靶向治疗理念的深化,以BTKi为代表的"无化疗"方案为惰性B细胞淋巴瘤的治疗带来了变革,BTKi已成为多个针对惰性淋巴瘤诊疗指南的推荐方案。
此外,新一代BTKi泽布替尼通过分子结构优化,在提升靶点选择性的同时降低脱靶毒性,为惰性B细胞淋巴瘤患者带来更大的生存获益,获得国内外众多指南的一致推荐。另外,泽布替尼还获批用于多种惰性B细胞淋巴瘤亚型,且是目前唯一实现对初治CLL、WM和R/R FL医保覆盖的新一代BTKi,进一步提升了治疗的可及性,改善了患者的生存预后。
在CLL/SLL领域,III期头对头SEQUOIA研究证实泽布替尼单药较免疫化疗方案(苯达莫司汀联合利妥昔单抗)显著延长初治CLL患者的生存。不论患者是否伴有高危因素, 泽布替尼组5年无进展生存(PFS)率相对更高(75.8% vs 40.1%)[2],而III期头对头ALPINE研究则提示其在复发/难治性(R/R)患者中较一代BTKi显现出持续治疗优势,泽布替尼组36个月PFS率更高(64.9% vs54.8%)。对于del(17p)/TP53突变患者,泽布替尼也表现出明显的PFS获益[3]。
泽布替尼是目前唯一获批WM适应症且实现医保覆盖的新一代BTKi
在WM领域,III期头对头ASPEN研究对比泽布替尼与一代BTKi伊布替尼在WM患者中的疗效及安全性。队列1 MYD88MUT患者中,泽布替尼5年PFS率和总生存(OS)率分别为74.8%和82.8%。队列2 MYD88野生型患者中,5年PFS率和OS率分别为39.3%和79.0%。在CXCR4WHIM和TP53MUT患者中亦表现出持久缓解。
在安全性方面,泽布替尼组的房颤/房扑(7.9% vs 23.5%)、高血压(14.9% vs 25.5%)及腹泻(22.8% vs 34.7%)等不良事件(AE)发生率更低(均P<0.01)。动态分析显示,泽布替尼组治疗36个月后感染风险进一步降低(P<0.05),中性粒细胞减少症发生率亦呈下降趋势[4]。基于ASPEN研究的数据,NMPA于2023年5月批准泽布替尼用于WM的一线治疗[5]。
泽布替尼是目前唯一获批R/R FL适应症且实现医保覆盖的BTKi
在R/R FL领域,II期ROSEWOOD研究取得重要进展,泽布替尼联合奥妥珠单抗方案(ZO组)显著提升了总缓解率(ORR;68.3% vs 45.8%),并延长了患者的中位PFS(28.0 vs 10.4个月),且未增加3级以上AE发生率[6]。基于坚实的循证证据,泽布替尼已获国家药品监督管理局(NMPA)批准用于R/R FL的治疗[5]并实现医保覆盖。此外,新一代BTKi还被多项国内外权威指南作为FL的推荐治疗方案[7~8]。
泽布替尼单药及联合方案在MCL治疗中展现卓越潜力
除CLL/SLL、WM及FL适应症外,新一代BTKi泽布替尼在MCL及MZL中亦展现卓越疗效。II期BGB-3111-206研究探索了R/R MCL中国患者接受泽布替尼治疗的疗效。长期随访数据显示,泽布替尼单药治疗ORR达83.7%,其中完全缓解(CR)率高达77.9%。中位PFS达33个月,中位OS未达到[9]。基于BGB-3111-206研究的结果,泽布替尼于2020年6月获得NMPA批准用于成人MCL患者的治疗[5]。
另一项II期研究显示,泽布替尼联合奥妥珠单抗及维奈克拉(BOVen方案)治疗初治伴TP53突变MCL患者,中位随访28.2个月时ORR达96%,CR率高达88%。生存分析揭示2年PFS率达72%、OS率达76%,而疾病特异性生存(DSS)率显著提升至91%,其与OS差异主要源于COVID-19相关非肿瘤死亡事件。
该方案常见AE包括腹泻(多为1-2级)、COVID-19感染等,其中严重不良事件(SAE)发生率较低,未出现非预期安全性信号[9]。
泽布替尼治疗MZL疗效获证,MAGNOLIA研究最终分析揭晓
II期MAGNOLIA研究最终分析显示,经独立评审委员会(IRC)评估,泽布替尼治疗R/R MZL的ORR达68.2%(P<0.001),其中CR率25.8%,与主要分析结果高度一致。值得注意的是,研究中所有MZL亚型均观察到显著疗效,中位至总缓解时间仅2.8个月。
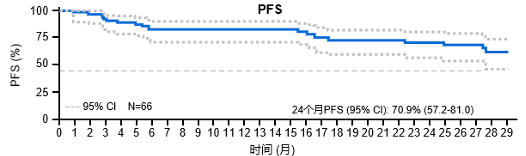
中位随访27.4个月时,中位PFS及DOR均未达到,24个月PFS率达70.9%、DOR率达72.9%。亚型分析显示,淋巴结型与结外粘膜相关淋巴组织型MZL患者24个月PFS率更高。另外,达CR患者24个月PFS率显著优于未达CR患者(87.4% vs 64.7%)。总人群24个月OS率为85.9%,其中脾脏型与结外粘膜相关淋巴组织型患者的24个月OS率达91.7%,淋巴结型患者为80.0%。
该研究的预设亚组分析显示多个难治MZL群体结束泽布替尼治疗后显著获益:≥75岁患者ORR达94.4%;存在≥5cm靶病灶者ORR 达79.2%;末次治疗>2年者ORR达79.3%;值得关注的是,既往接受利妥昔单抗单药治疗及RCVP(利妥昔单抗 +环磷酰胺+长春新碱+泼尼松)方案治疗患者的ORR分别达100%和80%。
EORTC QLQ-C30及EQ-5D-5L评估显示,患者健康状态自第3周期起持续提升,治疗18-24周期达峰值。安全性方面,所有患者均发生≥1项治疗相关不良事件(TEAE),常见TEAE为挫伤(23.5%)、腹泻(22.1%);≥3级TEAE发生率48.5%,以中性粒细胞减少(11.8%)为主,未发现新发安全性信号[10]。根据目前已获得的数据结果,美国食品药品监督管理局(FDA)于2021年9月批准泽布替尼用于接受过至少一次抗CD20治疗的R/R MZL成年患者[5]。
作为我国首个获得FDA批准的原研抗癌新药,泽布替尼自2019年11月在美获批用于治疗MCL实现"出海破冰"后,迄今已在全球超70多个国家及地区获批上市。泽布替尼的适应症“版图”持续扩展,相继斩获初治CLL/SLL、初治WM、R/R FL、R/R MZL等重要适应症,为全球惰性B细胞淋巴瘤患者提供更优治疗选择,同时填补特殊分子亚型患者的临床需求空白。
智能导航精准医疗
AI建模绘制淋巴瘤个体化治疗"全息地图"
新一代BTKi的亮眼数据为惰性B细胞淋巴瘤治疗策略的优化提供了重要支撑。但随着治疗格局的演进,新的命题接踵而至:BTKi在惰性B细胞淋巴瘤中的应用前景是怎样的呢?为此,DeepSeek化身“数据解谜者”,尝试推演BTKi的未来进化方向。让我们跟随算法的推演光束,探向惰性B细胞淋巴瘤精准治疗的下一个坐标。

作为血液肿瘤领域备受瞩目的"明星靶向药物",BTKi正以破冰之势重塑惰性B细胞淋巴瘤的治疗格局。现有临床证据显示,这类小分子药物犹如一把精准的"分子钥匙",在MCL、WM等亚型中诱导深度缓解并维持长期疗效。而新一代BTKi通过优化分子结构,在保持"狙击"B细胞受体信号通路核心作用的同时,进一步提高了安全性,为长期疾病管理提供了可能。基于当前证据,BTKi与CD20单克隆抗体、BCL-2抑制剂等药物的多通路协同治疗方案,可能突破现有治疗局限性,推动惰性B细胞淋巴瘤向功能性治愈目标迈进。
总结
作为B细胞受体信号通路的关键治疗靶点,BTKi持续驱动惰性淋巴瘤治疗策略的优化迭代。循证医学研究证实,以泽布替尼为代表的新一代BTKi通过分子结果优化,在增强靶点选择性的同时显著减少脱靶效应,为长期疾病管理提供药理学基础。ROSEWOOD与ASPEN等前瞻性研究的进展表明,BTKi联合CD20单克隆抗体及BCL-2抑制剂的多通路协同治疗策略,可能突破高危分子亚型的治疗局限性。值得关注的是,AI技术或可重构药物研发范式为克服耐药性挑战提供了新路径。
总体而言,中国原研BTKi的问世和广泛应用不仅为惰性B细胞淋巴瘤患者提供了更优的治疗选择,同时也标志着我国在新药研发领域已具备"定义疗效标准、引领治疗趋势"的创新能力。随着"健康中国2030"战略推进,这种创新势能将持续转化为临床获益,最终实现从"跟跑创新"到"原始创新"的历史性跨越。
1.Elizabeth Smyth, Chan Y Cheah, John F Seymour.Management of indolent B-cell Lymphomas: A review of approved and emerging targeted therapies.Cancer Treat Rev . 2023 Feb;113:102510. doi: 10.1016/j.ctrv.2023.102510.
2.Mazyar Shadman et al., Zanubrutinib Versus Bendamustine and Rituximab in Patients With Treatment-Naïve Chronic Lymphocytic Leukemia/Small Lymphocytic Lymphoma: Median 5-Year Follow-Up of SEQUOIA. JCO 0, JCO-24-02265DOI:10.1200/JCO-24-02265
3.Brown JR, Eichhorst B, Lamanna N, O'Brien SM, Tam CS, Qiu L, Jurczak W, Zhou K, Šimkovič M, Mayer J, Gillespie-Twardy A, Ferrajoli A, Ganly PS, Weinkove R, Grosicki S, Mital A, Robak T, Osterborg A, Yimer HA, Wang M, Salmi T, Wang L, Li J, Wu K, Cohen A, Shadman M. Sustained benefit of zanubrutinib vs ibrutinib in patients with R/R CLL/SLL: final comparative analysis of ALPINE. Blood. 2024 Dec 26;144(26):2706-2717.
4.Dimopoulos MA,et al. Zanubrutinib Versus Ibrutinib in Symptomatic Waldenstr¨om Macroglobulinemia: Final Analysis From the Randomized Phase III ASPEN Study.J Clin Oncol . 2023 Jul 21;JCO2202830. doi: 10.1200/JCO.22.02830.
5.国家药品监督管理局官网https://www.nmpa.gov.cn/zwfw/sdxx/sdxxyp/yppjfb/20240513150859198.html
6.Zinzani P L, Mayer J, Flowers C R, et al. ROSEWOOD: a phase II randomized study of zanubrutinib plus obinutuzumab versus obinutuzumab monotherapy in patients with relapsed or refractory follicular lymphoma[J]. Journal of Clinical Oncology, 2023, 41(33): 5107-5117.
7.中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南2024[M]. 北京: 人民卫生出版社, 2024.
8. NCCN B细胞淋巴瘤(2025. V1)
9. 2021 EHA abstract No. EP789.
10. Opat SS,et al. Safety and efficacy of zanubrutinib in relapsed/refractory marginal zone lymphoma: final analysis of the MAGNOLIA study.Blood Adv . 2023 Sep 8;bloodadvances.2023010668. doi: 10.1182/bloodadvances.2023010668.
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


