多发性骨髓瘤(MM)是一种克隆性浆细胞恶性增殖性疾病,其临床表现多样,预后差异显著。近年来,随着新药的不断涌现和治疗策略的持续优化,MM患者的总体生存有了显著改善。然而,高危MM(HRMM)患者通常对传统治疗反应不佳,且疾病进展迅速,预后较差。目前对于适合移植的MM患者,标准一线治疗方案为硼替佐米、来那度胺和地塞米松(VRd)诱导治疗,随后进行自体造血干细胞移植(ASCT)和来那度胺维持治疗。但对于HRMM患者,VRd方案的治疗效果并不理想。卡非佐米作为新一代的蛋白酶体抑制剂(PI),已有多项研究证明,以卡非佐米为基础的联合方案(K-based方案)有望克服高危患者不良预后,为HRMM带来显著生存改善。本期《MM患者更优预后,更长生存,始于VGPR》系列报道将详细探讨在适合移植HRMM患者中,K-based方案带来的显著疗效获益。
标准一线治疗VRd方案疗效有限,HRMM治疗之路仍充满挑战
目前VRd方案已成为新诊断MM诱导治疗的标准方案,但MM在生物学及临床上都具有高度异质性,患者生存时间存在较大差异[1],其中,HRMM生存期短、易进展、预后极差,已成为骨髓瘤治疗的重点和难点。在VRd方案诱导治疗下,仍有部分HRMM患者缓解深度不够,生存时间不够长。既往一项大样本(977例)美国真实世界研究[2]及Ⅲ期DETERMINATION研究[3]均显示,VRd治疗HRMM,患者获益明显低于标危患者(图1)。这表明对于HRMM患者,仍需更高效的治疗方案来提高患者获益。
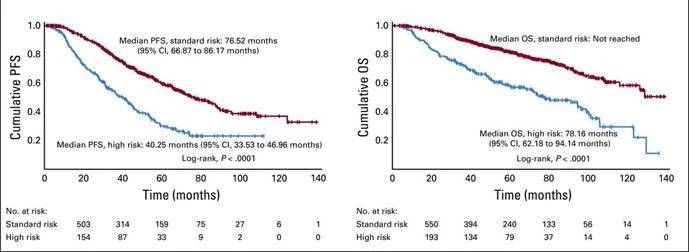
那么,在VRd基础上,又该如何进一步提高HRMM患者的诱导治疗疗效?近年来,随着新药地不断涌现,升级治疗或加入新机制药物有望突破HRMM治疗困境,例如把硼替佐米(V)升级为卡非佐米(K),或联合CD38单抗达雷妥尤单抗(Dara)等。
升级治疗,K-based方案为适合移植高危MM患者开启治疗新格局
新一代PI卡非佐米选择性共抑制β2+β5,具有更强的蛋白酶体抑制和细胞毒性作用[4]。近年来多项临床试验与真实世界研究结果证实K-based方案可为HRMM患者带来更深缓解和更优生存获益。
在开放标签、Ⅱ期SGH-MM1研究[5]中,探索了卡非佐米、环磷酰胺和地塞米松(KCd方案)作为适合移植的HRMM患者一线诱导治疗的疗效和安全性。该研究共纳入了32例≥21岁、适合移植的新诊断HRMM患者,主要研究终点为无进展生存期(PFS),次要终点包括总生存期(OS)和微小残留病灶(MRD)状态。在2014年10月29日至2017年9月11日期间,共有30例患者接受了研究性治疗,中位年龄为61.9岁,其中有23例接受了ASCT,21例完成了巩固治疗。
在诱导治疗、ASCT和巩固治疗后,完全缓解(CR)率分别为33.3%、52.2%和71.4%;分别有63.3%、91.3%和100%的患者达到≥VGPR(图2)。总体MRD阴性率为30%。MRD阳性和MRD阴性患者的中位PFS分别为41.3和40.3个月。在中位随访43.4个月后,中位PFS和中位OS分别为40.3个月和49.5个月。在安全性方面,常见的血液学TEAE包括肺炎、胃肠效应、急性肾损伤和感染并发症。3/4级TEAE的发生率为43.3%。
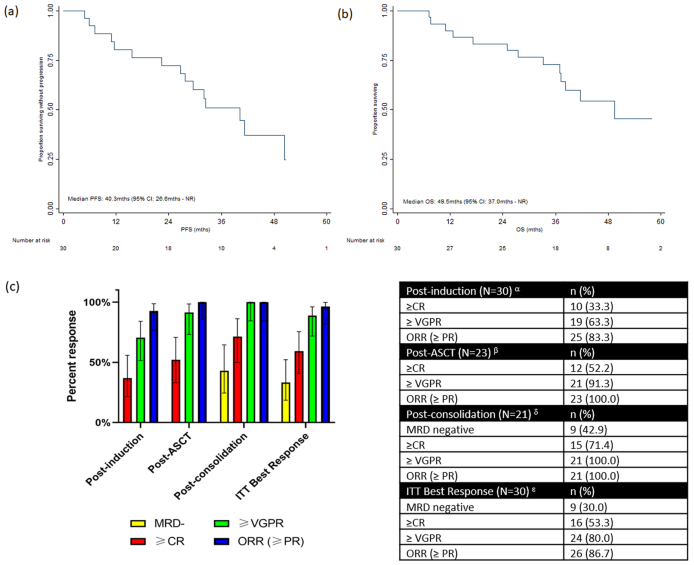
本研究表明,对于适合移植的HRMM患者,KCd方案不仅能够实现较高的深度缓解和持久的疾病控制时间,同时保持了可接受的安全性。因此,K-based方案有望成为适合移植HRMM患者的一种重要治疗选择。
强强联合,K-based+CD38单抗的四联方案在适合移植HRMM患者中疗效显著
目前已有多项研究表明,在三药联合方案的基础上引入CD38单抗,可以显著提升MM患者的临床疗效与MRD阴性率,同时并未增加新的安全性风险。但GRIFFIN研究[6]结果表明,适合移植的新诊断MM患者接受Dara联合VRd(D-VRd方案)治疗,对于伴有≤1个高危细胞遗传学异常(HRCA)的患者,其整体生存状况较为良好;然而,对于含有≥2个HRCA患者,疗效并不尽如人意。
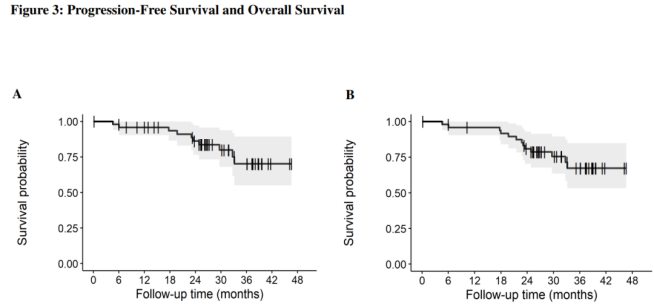
而在Ⅱ期IFM 2018-04研究[7]中,评估了卡非佐米、来那度胺、地塞米松联合Dara(D-KRd方案)诱导和巩固加双移植治疗新诊断HRMM的疗效和安全性。2019年7月至2021年3月期间,研究纳入了50例适合移植的新诊断HRMM患者。36例(72%)患者完成了第二次移植,达到了研究主要终点。按照方案人群(PP数据集),诱导治疗结束后(n=48)客观缓解率(ORR)率为95%,其中VGPR率为60%,CR/sCR率为31%。巩固前(n=42)、早期巩固结束后(n=41)和维持治疗前(n=36)的CR/sCR 率分别为48%,70%和81%(图3A)。诱导治疗结束后MRD阴性率为53%(10-5)和43%(10-6)。维持治疗前,MRD阴性率分别为97%(10-5)和94%(10-6)(图3B)。
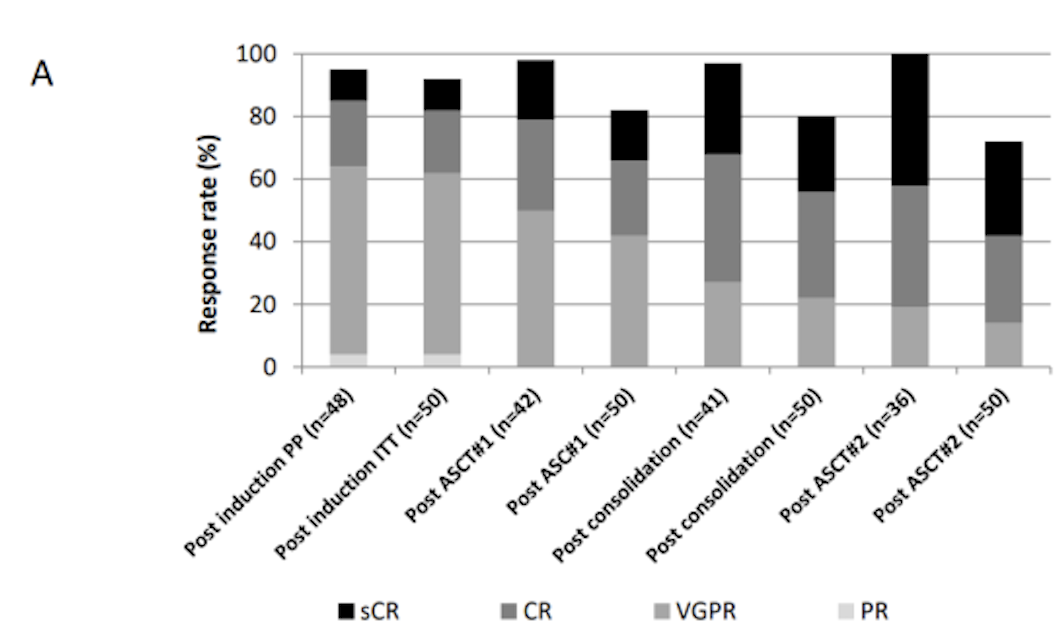
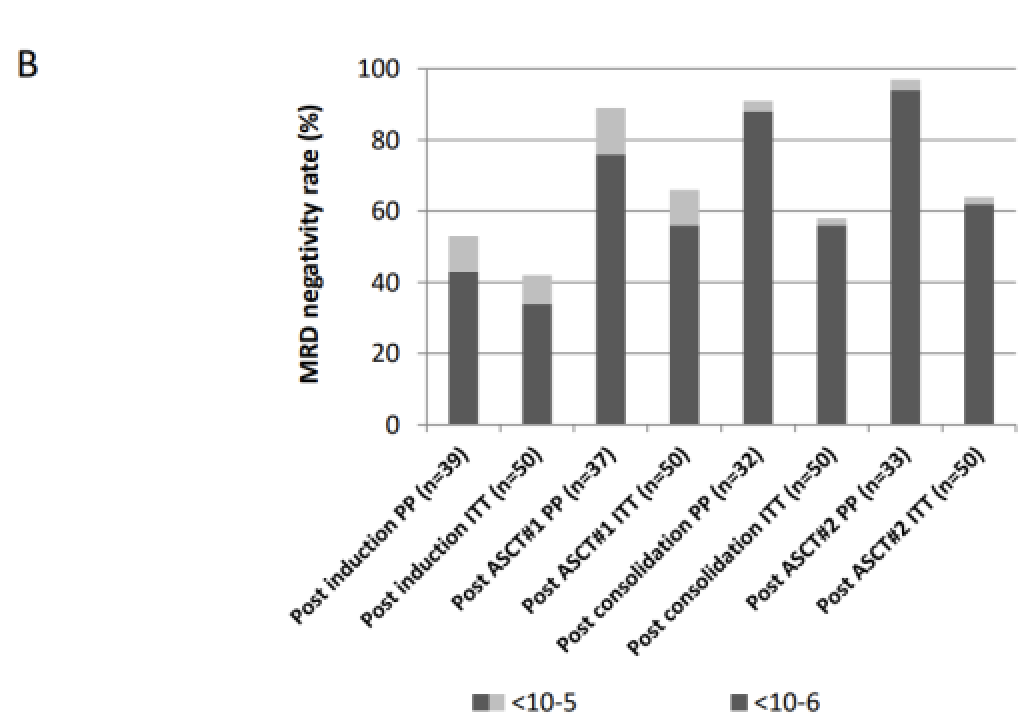
截至2023年7月,从治疗开始的中位随访时间为33个月。中位PFS和OS均未达到。30个月的PFS率和OS率分别为80%和91%(图4)。对基线参数包括细胞遗传学亚组,髓外疾病,R-ISS的预后影响进行了分析。这些参数均与较差的PFS或缓解评估(诱导后反应,诱导后MRD)无关。
在安全性方面,诱导和巩固治疗期间,最常见的血液学AE是中性粒细胞减少,发生率分别为36%和21%,主要为3~4级;非血液学毒性,最常见的不良事件是感染,胃肠道症状,疲劳和精神相关AE。
总体而言,D-KRd串联移植在新诊断HRMM患者中是可行的,并且可获得高MRD阴性率和PFS率。K-based方案诱导+移植+巩固治疗的方式可使适合移植的HRMM患者获得持久的深度缓解。
往期回顾:
【2】MM患者更优预后,更长生存,始于VGPR | KRD用于老年初治高危MM的病例分享
【3】MM患者更优预后,更长生存,始于VGPR|VGPR 或更好的缓解率作为较好的预后因素可用于预测中位PFS
【4】MM患者更优预后,更长生存,始于VGPR|卡非佐米联合治疗1q21+高危初治MM患者中可快速实现≥VGPR
【5】MM患者更优预后,更长生存,始于VGPR | KPD方案治疗一例首次复发MM患者,2疗程即达sCR
【6】MM患者更优预后,更长生存,始于VGPR|ASCT前达到≥VGPR有望提高NDMM患者ASCT后疗效和缓解深度
【7】MM患者更优预后,更长生存,始于VGPR|卡非佐米联合方案治疗一线标准治疗中疾病进展的高危MM患者,4疗程便达VGPR
【8】MM患者更优预后,更长生存,始于VGPR|K-based方案开启适合移植NDMM治疗新篇章:提高≥VGPR率,克服高危,延长生存
【9】MM患者更优预后,更长生存,始于VGPR|一例合并中枢神经髓外病变MM患者接受含卡非佐米方案治疗后达≥VGPR,四肢肌力显著恢复
【10】MM患者更优预后,更长生存,始于VGPR|KDd方案治疗R/R MM可获得近70%的VGPR率
【11】MM患者更优预后,更长生存,始于深度缓解|不适合移植NDMM接受K-based方案治疗可获得较高≥VGPR率,有望改善预后和生存
【12】MM患者更优预后,更长生存,始于VGPR|“因材施药”,PI升级为一例高危NDMM患者带来显著获益,2疗程即达VGPR
【13】MM患者更优预后,更长生存,始于VGPR|聚焦高危,优化治疗,卡非佐米助力一例新诊断HRMM患者实现VGPR
【14】MM患者更优预后,更长生存,始于VGPR|卡非佐米联合方案治疗合并del(17p)的R/R MM患者,4疗程即达CR
【15】MM患者更优预后,更长生存,始于VGPR|卡非佐米联合方案治疗一例伴PN的MM患者,不仅降低PN风险,并能快速实现≥VGPR
【16】MM患者更优预后,更长生存,始于VGPR | 一例首次复发MM患者经KPd方案治疗后快速获得CR,并维持至今
【17】MM患者更优预后,更长生存,始于VGPR|适合/不适合移植NDMM,K-based方案可带来90%~95%左右的VGPR率
【18】MM患者更优预后,更长生存,始于VGPR|K-based方案作为NDMM移植后维持治疗,可带来较高的≥VGPR率,提示更好的预后
【19】MM患者更优预后,更长生存,始于VGPR | K-based方案治疗一例三打击的超高危NDMM,4疗程便达MRD阴性的CR
【20】复发MM患者更优预后,更长生存,始于VGPR|首次复发患者的治疗选择至关重要,KPd方案可带来75%的≥VGPR率
[1] 多发性骨髓瘤预后评估:现状、挑战与思考.中华内科杂志, 2020,59(07):493-495.
[2] Joseph NS, et al.J Clin Oncol 2020 Apr 16;:JCO1902515.
[3] Richardson PG, et al. N Engl J Med. 2022 Jul 14;387(2):132-147.
[4] Besse A, et al. Cell Chem Biol. 2019 Mar 21;26(3):340-351.e3.
[5] Chen YX, et al. A phase 2 study of carfilzomib, cyclophosphamide and dexamethasone as frontline treatment for transplant-eligible MM with high-risk features (SGH-MM1)[J]. Blood Cancer Journal, 2021, 11(9): 150.
[6] Peter Voorhees et al,blood, Tracking no: BLD-2020-005288R1.
[7] Touzeau C, Perrot A, Hulin C, et al. Daratumumab carfilzomib lenalidomide and dexamethasone as induction therapy in high-risk, transplant-eligible patients with newly diagnosed myeloma: Results of the phase 2 study IFM 2018-04[J]. 2022.
[8] 高危多发性骨髓瘤诊断与治疗中国专家共识(2024年版)[J]. 中华血液学杂志,2024,45(05):430-435.DOI:10.3760/cma.j.cn121090-20240312-00090.
[9] Tan C, Nemirovsky D, Derkach A, et al.. Blood, 2022, 140(Supplement 1): 1817-1819.
[10] Leypoldt LB, Tichy D, Besemer B, et al. Isatuximab, Carfilzomib, Lenalidomide, and Dexamethasone for the Treatment of High-Risk Newly Diagnosed Multiple Myeloma. J Clin Oncol. 2024;42(1):26-37. doi:10.1200/JCO.23.01696.
排版编辑:肿瘤资讯-kk











 苏公网安备32059002004080号
苏公网安备32059002004080号


