本期精选4篇在2024年4~6月发表的头颈部肿瘤治疗领域文章。邀请中国中医科学院西苑医院张彤教授进行深入解读。
主要从事消化道肿瘤、头颈部肿瘤等实体瘤的中西医结合治疗
北京癌症防治研究会结直肠癌专委会副主任委员
世界中医药联合会整合肿瘤专业委员会常务委员兼副秘书长
中国老年学和老年医学学会肿瘤分会中医专委会副秘书长
中国老年学和老年医学学会肿瘤康复分会秘书
北京肿瘤防治研究会中医分会委员
北京中西医结合学会肿瘤专业委员会青年委员
北京中西医结合学会甲状腺病专业委员会青年委员


1.ELAN-FIT研究显示改良的EXTREME方案(西妥昔单抗+氟尿嘧啶+卡铂)一线治疗老年复发/转移性头颈鳞状细胞癌(R/M HNSCC)患者获得良好疗效及安全性
2.卡博替尼联合西妥昔单抗治疗R/M HNSCC患者毒性可控,且显示了初步疗效
3.肿瘤负荷与R/M HNSCC患者的生存显著相关,患者一线治疗方案选择应综合考虑 PD-L1 表达及TBS
4.紫杉醇联合卡铂和西妥昔单抗新辅助治疗LA-HNSCC的安全性及有效性
ELAN-FIT研究显示改良的EXTREME方案(西妥昔单抗+氟尿嘧啶+卡铂)一线治疗老年R/M HNSCC患者中获得良好疗效及安全性1
老年R/M HNSCC患者的标准治疗方法尚未确定,既往EXTREME研究已证实EXTREME方案的疗效,但仅纳入较少的老年患者,提示需要在更大的老年患者人群中评估EXTREME方案的疗效和安全性。本研究(ELAN-FIT研究)旨在评估改良的EXTREME方案治疗老年R/M HNSCC患者的疗效和安全性。
ELAN-FIT研究是一项多中心、单臂、II期研究,主要纳入标准包括:年龄≥70岁、ECOG PS评分为0~1、ELAN老年评估(EGE)为非体弱(健康)、不适合进行局部治疗(手术或放疗)、R/M HNSCC患者,入组后患者接受改良的EXTREME方案,即氟尿嘧啶(5-FU)(4000mg/m2,d1-4)+卡铂(AUC 5,d1)+西妥昔单抗(400mg/m2 C1d1,随后使用250mg/m2,d8、15)。在2-6个周期后实现疾病控制的患者中,继续接受西妥昔单抗(500mg/m2,q2w)作为维持治疗,直至疾病进展或出现不可耐受的毒性反应。该研究基于Bryant和Day两阶段设计,结合了疗效和毒性终点。主要疗效终点是中心审查评估的第12周的客观缓解率(ORR),主要毒性终点为不良事件发生率,定义为化疗阶段4-5级不良事件(AE)的发生率、需要停用西妥昔单抗的皮疹(≥3级)、化疗结束后1个月(不可接受的发病率>40%)功能自主性下降(ADL评分较基线水平下降≥2分)。
2013年9月27日至2018年6月20日期间共有22家法国医疗中心的85例患者被纳入了研究,最终纳入分析的符合方案患者78例(至少接受一周期改良EXTREME方案治疗)其中66例(85%)患者为男性,12例(15%)患者为女性。患者接受化疗中位周期数为5个周期,30例(38%)患者完成了6个周期的化疗。研究结果显示12周ORR为40%,疾病进展(SD)为32%,疾病稳定(PD)为 9%。
表1 患者基线数据
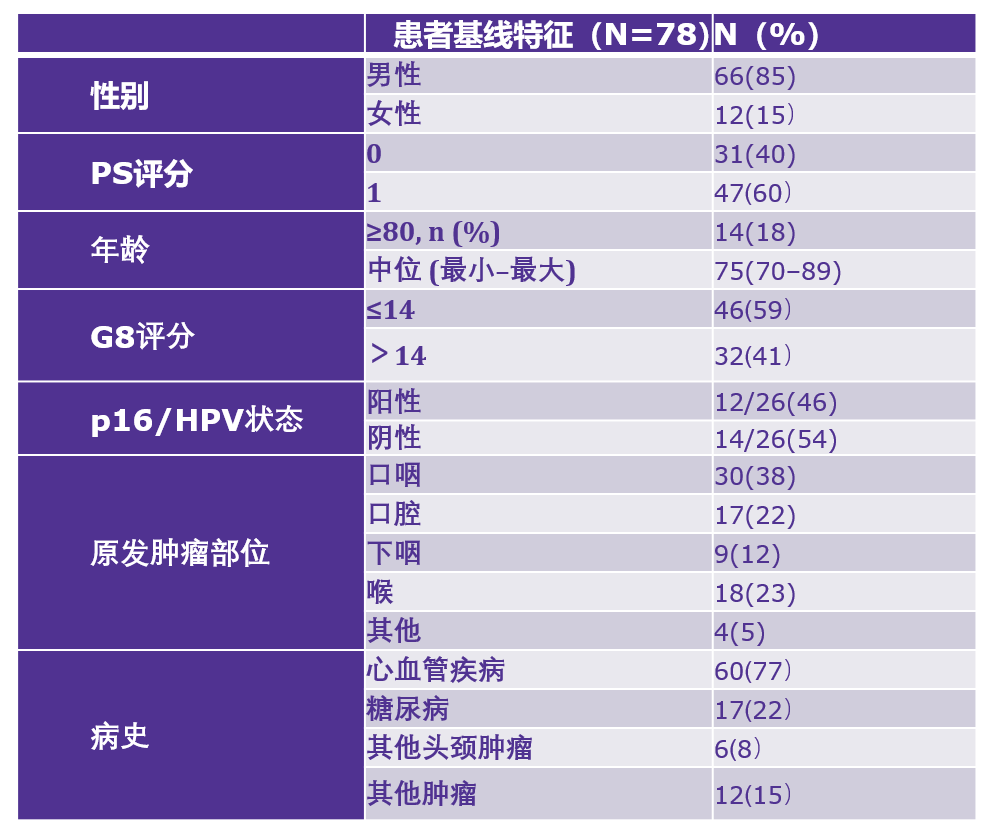
表2 治疗第12周时的肿瘤反应情况

中位随访时间为71.8个月,中位总生存期(mOS)为15.8个月(95%CI:11.0-18.9),3年、5年OS率分别为10.3%、4.3%;中位无进展生存期(mPFS)为6.0个月(95%CI:4.9-7.3),3年PFS率为5.1%。
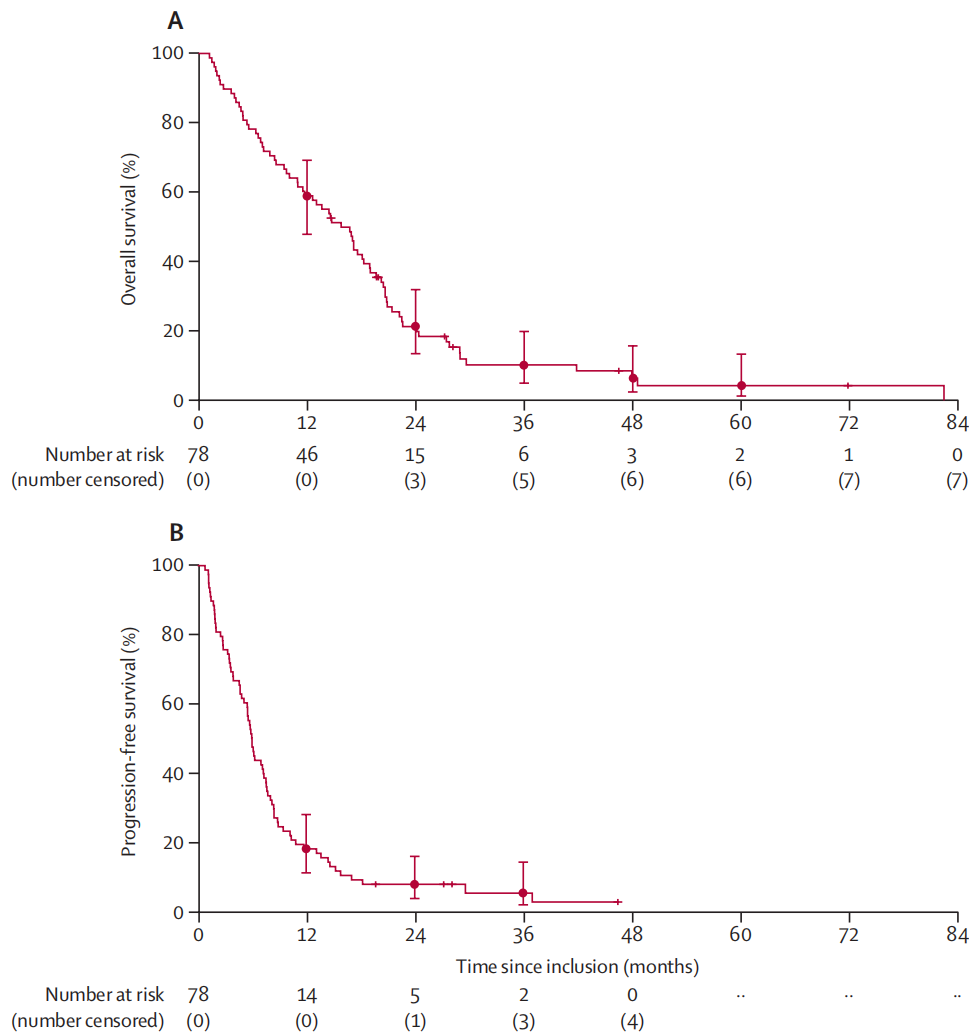
图1 患者OS(A)和PFS(B)结果
安全性方面,主要毒性终点发生率为31%,未出现致死性不良事件。化疗期间,最常见的3-4级AE是血液学事件[白细胞减少(28%)、中性粒细胞减少(26%)、血小板减少(19%)和贫血(15%)]、口腔黏膜炎(18%)、疲劳(14%)、痤疮样皮疹(13%)和低镁血症(12%)。在维持治疗阶段接受西妥昔单抗治疗的44例患者中,最常见的3-4级不良反应是低镁血症(14%)和痤疮样皮疹(14%)。
本研究达到了客观缓解和发病率的主要终点,并显示总生存期与接受标准方案治疗的年轻患者获益一致,表明改良的EXTREME方案可用于经ELAN老年评估(EGE)为健康的老年R/M HNSCC患者。
卡博替尼联合西妥昔单抗治疗R/M HNSCC患者毒性可控,且显示了初步疗效2
目前头颈鳞状细胞癌(HNSCC)一线治疗探索较多,但对于经一线治疗后疾病进展的患者,二线治疗方案的选择十分有限。表皮生长因子受体(EGFR)抑制药物西妥昔单抗是HNSCC的标准治疗方法,AXL、MET和VEGFR受体的激活可以介导对西妥昔单抗的耐药性。卡博替尼是一种小分子多激酶抑制剂(MKI),可抑制与HNSCC相关的多条信号通路,包括VEGFR、AXL和MET信号通路。临床前研究表明,卡博替尼与西妥昔单抗联合用于R/M HNSCC患者的治疗,可能具有协同作用。因此,本研究旨在探索卡博替尼联合西妥昔单抗治疗R/M HNSCC的安全性和耐受性。
本研究是一项I期研究,分为两个阶段:剂量递增阶段和剂量扩展阶段。剂量递增阶段,患者先接受西妥昔单抗的负荷剂量(400 mg/m2,随后每周250 mg/m2)。西妥昔单抗的维持剂量后续改为每两周剂量500 mg/m2;采用“3+3”设计来确定卡博替尼的最大耐受剂量。研究的主要终点是确定卡博替尼与西妥昔单抗联合使用时的Ⅱ期推荐剂量(RP2D)。次要终点包括:ORR、疾病控制率(DCR)、PFS、OS。
本研究共纳入了20例患者进行分析,大部分患者既往接受过免疫检查点抑制剂(95%)、铂类化疗(95%)和西妥昔单抗(80%)治疗。未观察到剂量限制性毒性(DLT),卡博替尼的最大耐受剂量(MTD)为60 mg。在接受治疗的20例患者中,有13例出现了≥3级不良反应(AEs)。未见治疗相关死亡报告。
疗效方面,患者整体ORR为20%,其中4例患者达部分缓解(PR),11例患者SD,DCR为75%。在既往未接受过西妥昔单抗治疗的患者中,采用卡博替尼联合西妥昔单抗的治疗方案,ORR高达50%。总人群患者的PFS为3.4个月,OS为8.1个月。
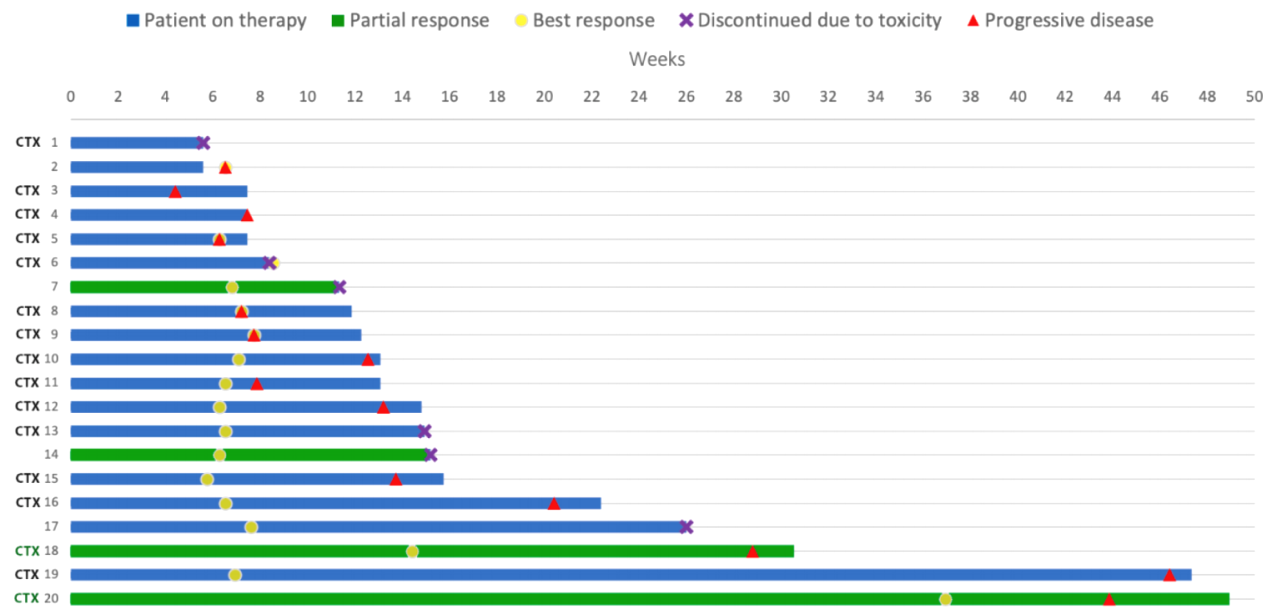
图2 治疗过程中,患者疗效评价图
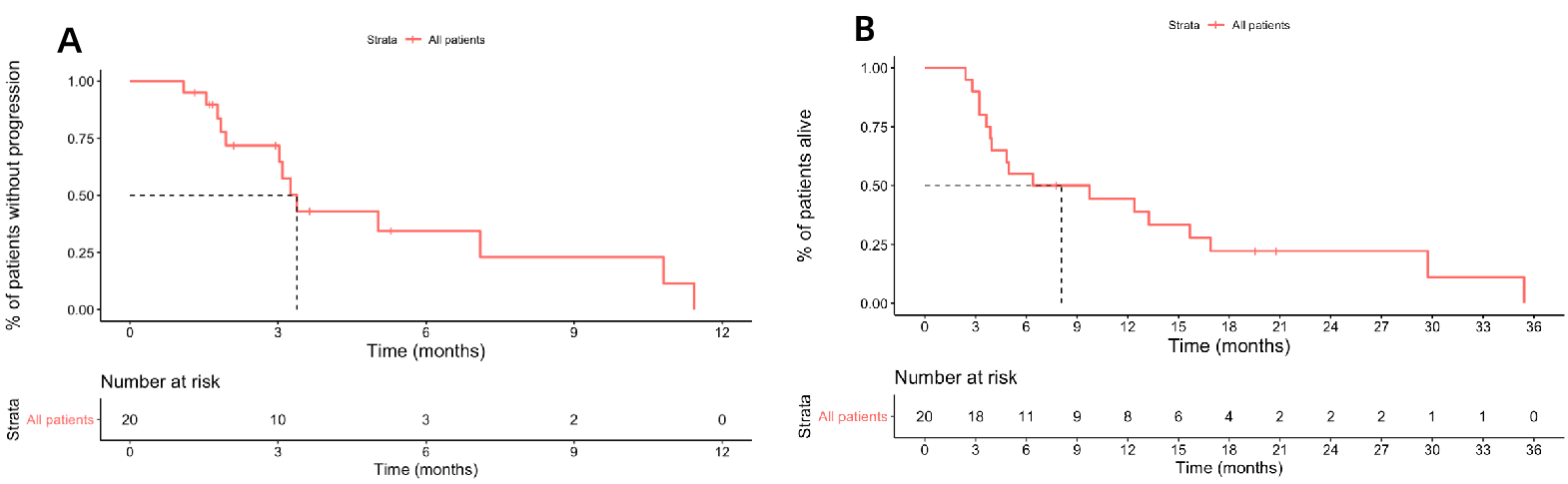
图3 PFS、OS结果
在对肿瘤原发部位和人乳头瘤病毒(HPV)状态进行分层分析时,研究发现约83%的口咽癌患者呈HPV阳性。HPV阳性患者的mPFS相对HPV阴性患者显著改善(mPFS:7.1个月vs 3.1个月)。在调整了年龄、ECOG表现状态和卡博替替尼剂量后,HPV阳性肿瘤患者的进展风险降低了83%。此外,初次使用西妥昔单抗治疗的患者,12个月的OS率为75%。既往使用西妥昔单抗治疗的患者,12个月的OS率为44%。
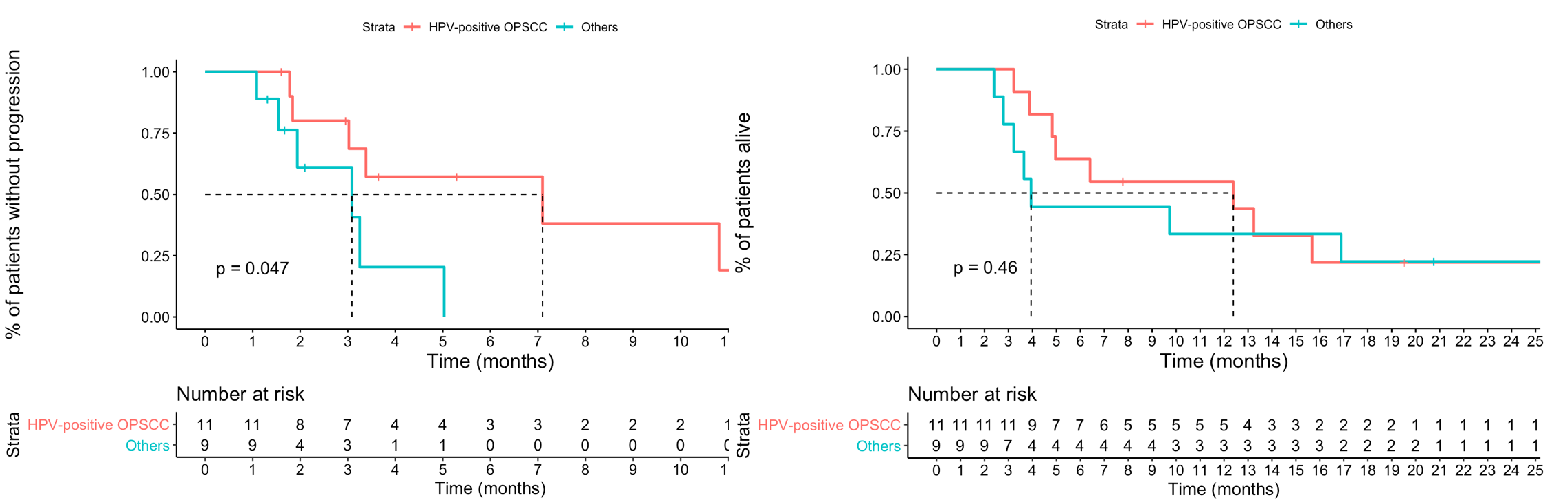
图4 按 HPV状态和肿瘤原发部位分层患者的PFS、OS结果
卡博替尼联合西妥昔单抗治疗R/M HNSCC患者,毒性可控,且显示了初步疗效。西妥昔单抗与靶向AXL/MET/VEGFR的MKIs联合使用值得进一步研究,包括既往经过西妥昔单抗治疗后进展的患者。
肿瘤负荷与R/M HNSCC患者的生存显著相关,患者一线治疗方案选择应综合考虑 PD-L1 表达及TBS3
在R/M HNSCC患者中,肿瘤负荷对生存的意义尚未明确。本研究旨在评估肿瘤负荷评分(TBS)及程序性死亡配体 1(PD-L1)对 R/M HNSCC患者的预后影响。
本研究是一项回顾性研究,研究纳入了2017至2020年间3家医院接受治疗的R/M HNSCC患者共252例,TBS按以下公式计算TBS = (最大肿瘤直径)² + (肿瘤病灶数量)²,TBS cutoff值为5.66, 据此将患者分为高肿瘤负荷组(HTB,TBS大于cutoff值)和低肿瘤负荷组(LTB,TBS小于cutoff值)各126例,患者接受顺铂、5-氟尿嘧啶联合西妥昔单抗(EPF)或帕博利珠单抗(PPF)的一线治疗。采用Kaplan-Meier 曲线,评估PD-L1和TBS与治疗反应的相关性。
结果显示,LTB组患者的PFS、OS均优于HTB组,且与PD-L1状态无关。两组PFS分别为7.1个月 vs 3.9个月(p<0.001);两组OS分别为14.2个月 vs 9.2个月(p=0.001)。
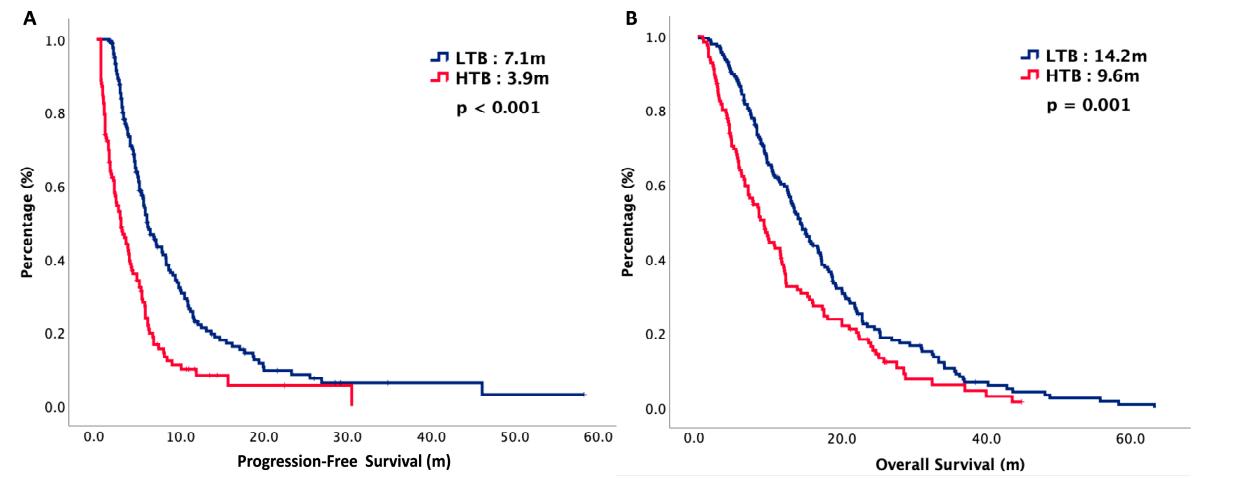
图5 研究的PFS与OS结果
亚组分析显示,无论PD-L1表达如何,HTB患者接受含西妥昔单抗方案(EPF)比接受含帕博利珠单抗方案(PPF)治疗具有更好的生存期;而对于PD-L1阴性LTB患者,接受PPF和EPF的生存结果相似(20.5m vs 18.8m,p=0.585);仅在PD-L1阳性LTB患者,接受PPF治疗的生存期比接受EPF治疗的患者生存期更长(22.8m vs 12.9m,p=0.018)。
另外,多变量分析显示,肿瘤负荷与 OS 显著相关。
表3 多变量分析结果
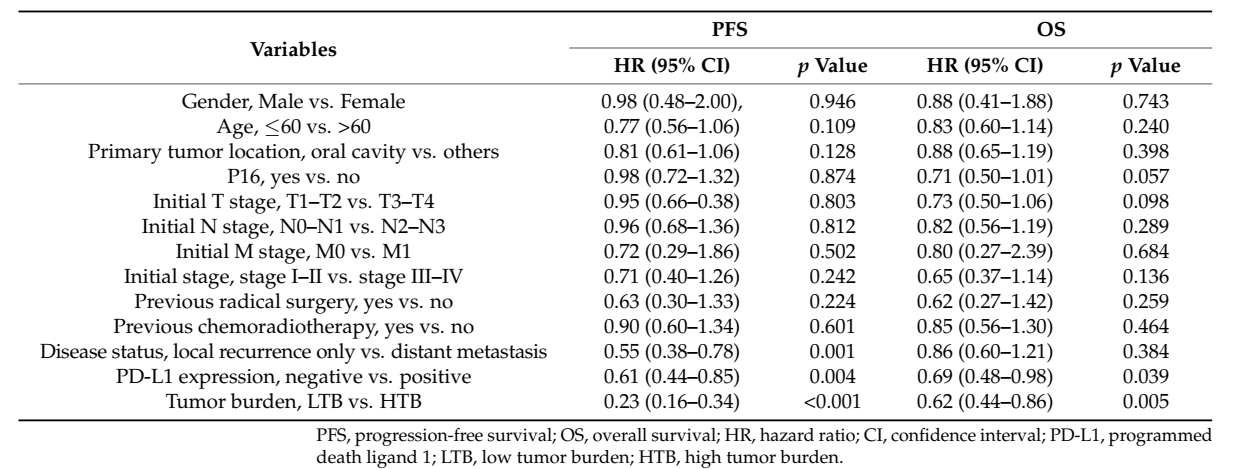
总体而言,肿瘤负荷与 R/M HNSCC患者的生存显著相关,R/M HNSCC综合治疗中应根据PD-L1表达和TBS制定方案。
紫杉醇联合卡铂和西妥昔单抗新辅助治疗LA-HNSCC的安全性和有效性6
局部晚期HNSCC(LA-HNSCC)的标准治疗方案包括根治性手术和同步放化疗(CCRT)。但由于根治性手术通常需要较长时间的等待,患者可能会在此期间出现疾病进展、症状恶化,甚至面临生命危险。术前新辅助化疗(NAC)已在多种癌症中被证实可以缩小肿瘤体积和降低肿瘤分期。多项研究提示使用紫杉醇、卡铂和西妥昔单抗(PCE)治疗R/M HNSCC,具有良好的疗效和可控的安全性。然而,目前尚缺乏关于PCE方案新辅助治疗安全性和有效性的研究。
本研究是一项回顾性研究,旨在评估PCE方案新辅助治疗LA-HNSCC患者的安全性和有效性。具体治疗方案为:紫杉醇100mg/m2第1天、第8天;卡铂AUC=2,第1天、第8天,每3周一次;西妥昔单抗第一天初始剂量为400mg/m2,随后每周250 mg/m2,直至化疗结束。此外,本研究也探索了PCE方案在顺铂不耐受患者中的疗效。
研究共回顾性评估了26例接受PCE方案治疗的患者的基线特征,ORR、不良事件发生率、组织学反应、无复发生存期(RFS)和OS等数据。根据化疗周期数将患者分为两组:1个周期、≥2个周期,对比两组的疗效及不良反应发生率。同时,定义年龄≥75岁的患者或eGFR<60mL/min的患者为顺铂不耐受患者。中位年龄为70岁(27-81岁),治疗开始时的中位eGFR中位数为63.2(41.1-89.7)mL/min。接受PCE方案治疗的患者中有14例(53.8%)不耐受顺铂治疗。
研究结果显示PCE新辅助治疗可获得较好疗效,ORR为65.4%,2年RFS率和OS率分别为61.5%和76.7%(图6)。
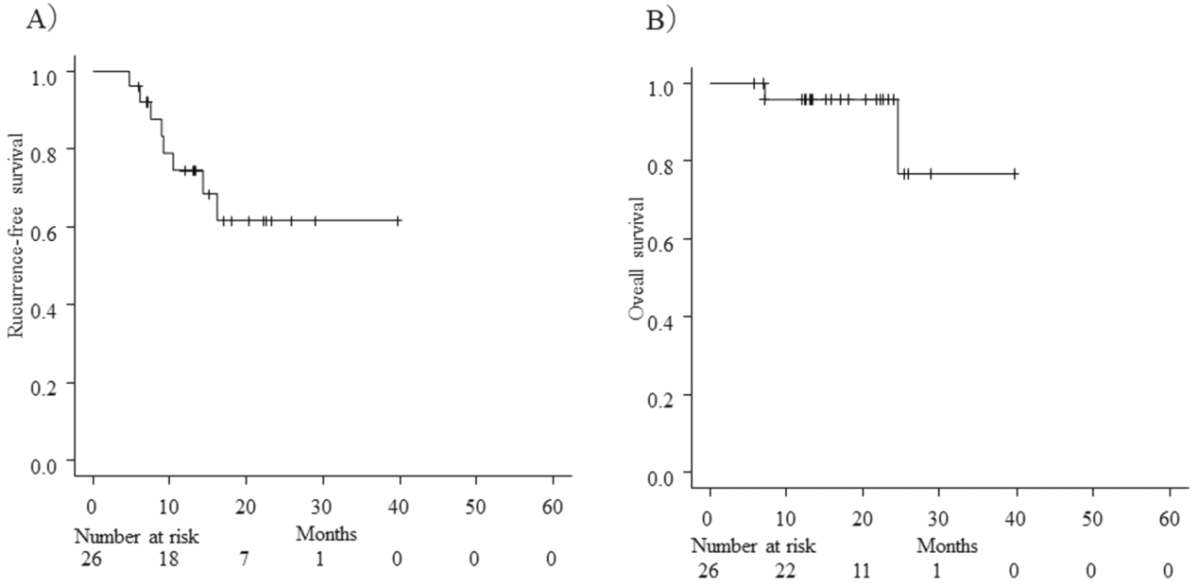
图6 2年RFS率(A)和2年OS率(B)
安全性数据方面,42.3%的患者出现了≥3级的中性粒细胞减少。非血液学毒性方面,厌食、脱发和皮疹的发生率分别为46.2%、46.2%、50%。未发生治疗相关的死亡事件。
亚组分析显示,接受1周期PCE方案治疗(n=11)及≥2个周期治疗(n=14)的患者的ORR为54.5% vs 45.5%(p=0.426),1年RFS率为80% vs 70.5%(p=0.557),2年OS率为100% vs 87.5%(p=0.055)接受1个周期的PCE方案患者中(n=11),不良反应发生率相似。1周期组和≥2周期组,患者在安全性和疗效方面没有明显的差异。此外,顺铂耐受患者和顺铂不耐受的患者在疗效和安全性数据方面也没有明显的差异。
综上,本研究提示,PCE方案新辅助治疗LA-HNSCC患者,包括铂不耐受的患者,可获得较好的疗效及可接受的安全性。
1. Guigay J, Le Caer H, Ferrand FR, et al. Adapted EXTREME regimen in the first-line treatment of fit, older patients with recurrent or metastatic head and neck squamous cell carcinoma (ELAN-FIT): a multicentre, single-arm, phase 2 trial. Lancet Healthy Longev. 2024 Jun;5(6):e392-e405.
2. Desilets A, Pfister DG, Stein S, et al. A phase 1 study of concurrent cabozantinib and cetuximab in recurrent or metastatic head and neck squamous cell cancer. Oral Oncol. 2024 Jul;154:106861.
3. Lien MY, Wang CC, Hwang TZ, et al. Programmed Death Ligand-1 and Tumor Burden Score Dictate Treatment Responses in Patients with Recurrent or Metastatic Head and Neck Squamous Cell Carcinoma. Cancers (Basel) . 2024 Apr 30;16(9):1748.
4. 郭晔, 张陈平. 复发/转移性头颈部鳞癌免疫检查点抑制剂治疗专家共识(2024年版). 中国癌症杂志.2024;34(4):425-438.
5. Dall'Olio FG, Marabelle A, Caramella C, et al. Tumour burden and efficacy of immune-checkpoint inhibitors. Nat Rev Clin Oncol. 2022 Feb;19(2):75-90.
6. Tanaka R, Ueki Y, Ohshima S, et al. Safety and efficacy of neoadjuvant chemotherapy with paclitaxel, carboplatin, and cetuximab for locally advanced head and neck squamous cell carcinoma. Int J Clin Oncol. 2024 May 10.
排版编辑:肿瘤资讯-Bryce
版权归肿瘤资讯所有。欢迎个人转发分享,其他任何媒体、网站如需转载或引用本网版权所有内容,须获得授权,且在醒目位置处注明“转自:良医汇-肿瘤医生APP”。











 苏公网安备32059002004080号
苏公网安备32059002004080号


