我国为胃癌大国,胃癌发病人数占据全球40%以上[1],其中局部晚期及晚期胃癌占比高达70%[2]以上。由于我国胃癌早诊率较低,因而胃癌患者的整体预后较差,其中局部晚期胃癌的5年生存率不到30%[3]。而HER2阳性胃癌,虽然占比不高,仅为10%~20%,但因其生物学行为极差,侵袭性强、转移率高,往往单纯手术无法完全清除病灶,因此提高围术期治疗至关重要[4]。随着免疫时代的带来,免疫治疗在进展期胃癌中的应用现已成为目前的研究热点之一,对于HER2阳性胃癌的围术期治疗,在化疗及抗HER2治疗基础上再联合免疫治疗,可以有效控制肿瘤残留和远处转移,提高手术切除率和最终的治疗效果。由我们和郑州大学第一附属医院王峰教授牵头开展的一项关于“探索HER2阳性可切除胃/胃食管结合部腺癌围术期接受替雷利珠单抗联合曲妥珠单抗及化疗的疗效和安全性的研究“的初步结果惊艳,病理完全缓解(pCR)高达50%以上,并在2023年ASCO(e16084)[5]和ESMO(1539P) [6]大会上展示。基于该研究,本期分享一例HER2阳性胃癌围术期患者全程应用免疫联合化疗及靶向方案进行围术期治疗,并获得pCR及长生存的病例。
患者一般情况
张某,男,68岁,因“上腹部胀痛不适1月余”于2022年5月16日就诊我院,查胃镜病理诊断为(贲门)中分化腺癌,免疫组化dMMR,HER-2(3+)。胃+盆腔增强CT提示食管下段-贲门-胃底病变,考虑胃癌,侵犯脏层腹膜;贲门及胃小弯侧可见多发肿大淋巴结,部分淋巴结融合成团;影像学分期考虑:cT4aN3aM0。Borrmann分型:III型-溃疡浸润型。
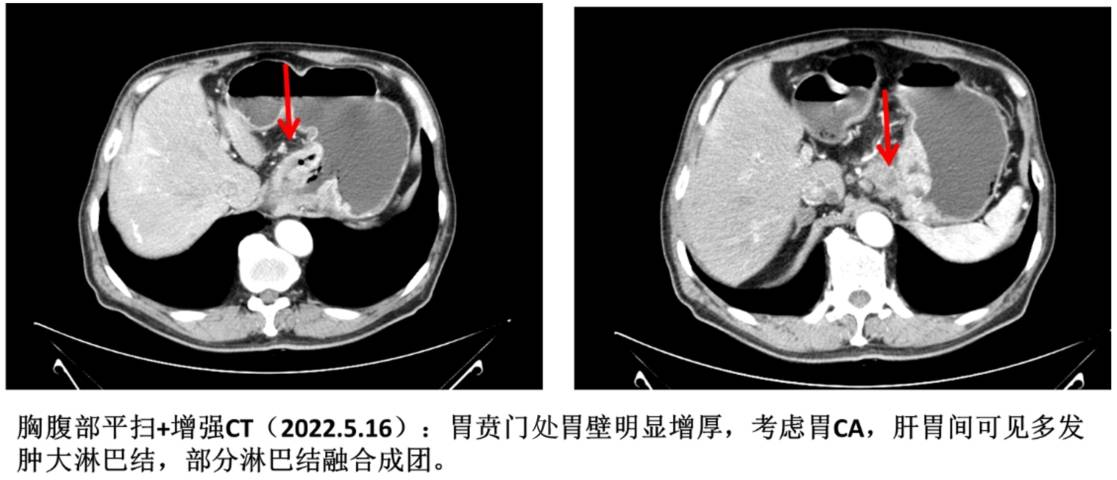
新辅助治疗
患者于2022年5月22日开始给予替雷利珠单抗联合曲妥珠单抗1周期诱导治疗,序贯替雷利珠单抗联合曲妥珠单抗及DOS方案(多西他赛+奥沙利铂+替吉奥)3周期(Q3W)。术前行CT及胃镜检查,均较入院时明显改善。
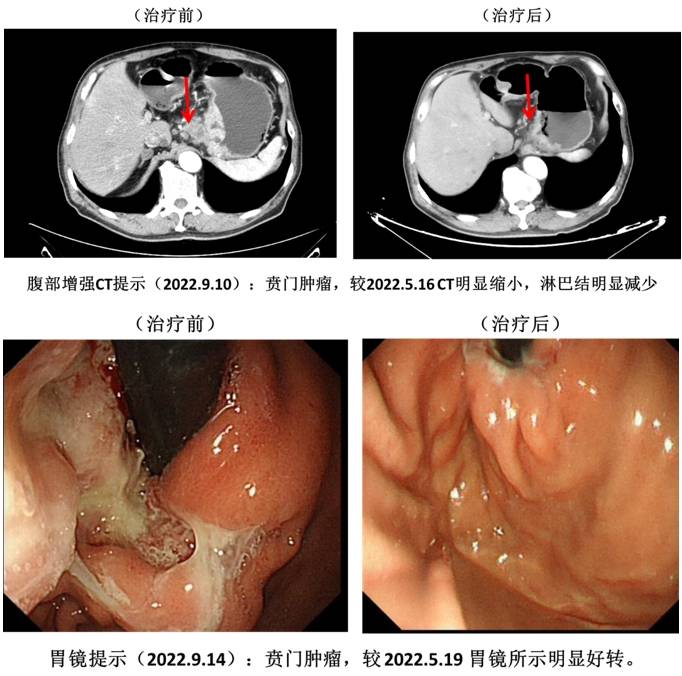
手术切除术及辅助治疗
手术切除:外科评估患者经新辅助治疗后,病灶明显缩小,并于2022.9.15全麻下行腹腔镜近端胃切除术(食管残胃吻合术)。见肿瘤位于贲门胃底小弯侧,大小约4cm×6cm×2cm,浸润浆膜下,呈化疗后改变;胃周见明显数枚肿大淋巴结。病理学检查显示:(近端)黏膜慢性炎佯溃疡形成,局灶纤维化伴黏液变性,符合治疗后改变,TRG分级1级,完全退缩(Mandard标准);经充分取材未见明显肿瘤残存。上下切缘及网膜未见癌;周围淋巴结未见转移癌。

辅助治疗:术后第6周分别给予替雷利珠单抗联合曲妥珠单抗及DOS方案2周期治疗,序贯替雷利珠单抗联合曲妥珠单抗9周期治疗。术后每3个月复查胸腹部平扫及增强CT,至今术后22个月未见复发转移迹象。
本期病例点评专家
赵春临教授、梁卫杰教授
主任医师、医学博士、硕士生导师
中华医学会河南分会肠外肠内营养学专业委员会名誉主任委员
中国医师协会外科医师分会胃肠道间质瘤诊疗专业委员会委员
中国医师协会结直肠肿瘤专业外科专业委员会委员
中国医师协会外科医师分会加速康复外科专家委员会委员
中国医师协会外科医师分会临床营养医师专业委员会委员
河南省医学会普外专业委员会胃肠学组委员
中国抗癌协会河南分会大肠癌专业委员会常务副主任委员
中国抗癌协会河南分会大肠癌专业青年委员会主任委员
中国抗癌协会河南分会胃癌专业委员会常委
河南省食管癌—胃癌综合诊疗中心副主任
河南省中西医结合学会微创外科分会副主任委员
《肠外与肠内营养》杂志编委、《河南外科学杂志》编委
中国抗癌协会第二届胃肠间质瘤专业委员会委员
中国抗癌协会神经内分泌肿瘤专业委员会委员
河南省抗癌协会老年肿瘤青年委员会委员
2019年”达医生——例达巅峰“全国赛三等奖
2020年第三届结直肠外科精英团队临床技能邀请赛总决赛第三名
主持河南省省部共建项目1项,发表SCI文章2篇,最高影响因子5.4,核心期刊发表文章数篇
专家点评
对于局部进展期胃癌的治疗,目前已从过去单一的手术模式转变为手术为主的多学科综合治疗模式。其标准治疗策略包括手术联合术后辅助治疗,或者术前新辅助+手术联合术后辅助治疗。相关研究表明,术前新辅助治疗有助于初始肿瘤临床或病理降期,减少术后复发率,较之单纯手术或辅以术后化疗的治疗方法,在一定程度上能改善患者的预后。本病例为Borrmann Ⅲ型HER2阳性胃癌患者,既往研究显示,与Borrmann 1/2 型相比,Borrmann Ⅲ和Ⅳ型术前新辅助化疗后达到pCR[7]率更低(33%、9%和0),非根治性切除率高(5.8%、14.6% 和 36.3%),术后5年生存率更低(57.2%、48.5%和28.9%[8])。抗HER2靶向药联合化疗方案pCR率多在9.6%~23%[9-10],这种疗效仍然不能满足临床需求,并且进入了瓶颈期,存在巨大的提升空间。而免疫治疗的出现,为胃癌围术期治疗燃起了一线希望。
本病例治疗结果显示给予替雷利珠单抗联合曲妥珠单抗及化疗治疗后,病理完全缓解及术后将近2年未复发,充分彰显了抗HER2治疗与免疫治疗联合具有协同增效的作用。首先是由于免疫治疗的加入,进一步提升了HER2阳性胃癌患者的应答率。临床前研究显示,曲妥珠单抗可以通过树突状细胞增加HER2内化和交叉呈递,从而增加HER2特异性T细胞的反应。此外,曲妥珠单抗还可上调PD-1/PD-L1的表达,诱导肿瘤浸润性淋巴细胞的表达,改善免疫微环境,同时调节主要组织相容性复合体II(MHC II)的表达[11]。而化疗在整体治疗方案亦不可或缺。此外,由于化疗方案选择较为恰当,且剂量适当,患者的整体耐受较好。在该治疗方案中,化疗的作用在于可导致免疫原性细胞死亡,而死亡的肿瘤细胞会刺激树突状细胞,从而增加抗原的加工和呈递,促进CD8+肿瘤特异性T细胞的启动。这些机制均可促使肿瘤内微环境转向利于免疫治疗的环境,进而使得免疫联合抗HER2方案具有协同增效的抗肿瘤作用。
另一原因是替雷利珠单抗在结构上进行了充分的优化,这是一个极具创新性的PD-1抗体,能够更彻底地阻断PD-1/PD-L1的结合,并且经过基因工程改造后,避免了与巨噬细胞上的FcγR相结合,从而消除了抗体依赖的细胞介导的吞噬作用(ADCP效应),避免了因T细胞数量减少而影响抗肿瘤疗效。
综上所述,相信未来以替雷利珠单抗为代表的免疫治疗和抗HER2方案的联合治疗,将给HER2阳性肿瘤患者带来更多治疗惊喜。
[1]. Sung H, Ferlay J, Siegel RL, et al. Global Cancer Statistics 2020: GLOBOCAN Estimates of Incidence and Mortality Worldwide for 36 Cancers in 185 Countries. CA Cancer J Clin. 2021 May;71(3):209-249.
[2]. 周梦龙,章真.局部进展期胃癌术前放疗的优势与思考[J].外科理论与实践,2019,24(01):23-27.
[3]. Allemani C, Matsuda T, Di Carlo V, et al. Global surveillance of trends in cancer survival 2000-14 (CONCORD-3): analysis of individual records for 37 513 025 patients diagnosed with one of 18 cancers from 322 population-based registries in 71 countries. Lancet. 2018 Mar 17;391(10125):1023-1075.
[4]. Huang D, Lu N, Fan Q, et al. HER2 status in gastric and gastroesophageal junction cancer assessed by local and central laboratories: Chinese results of the HER-EAGLE study. PLoS One. 2013 Nov 14;8(11):e80290. Huang D, et al. PLoS One. 2013 Nov 14;8(11):e80290.
[5]. C. Zhao, F. Wang, J. Xia, et al. Efficacy and safety of perioperative chemotherapy combined with tislelizumab and trastuzumab for HER2-positive resectable gastric/gastroesophageal junction cancer (GC/EGJC): Preliminary results of a phase 2, single-arm trial. Journal of Clinical Oncology. Volume 41;Number 16_suppl: e16084
[6]. F. Wang, C. Zhao, J. Xia, et al. Efficacy and safety of perioperative chemotherapy combined with tislelizumab and trastuzumab for HER2- positive resectable gastric/gastroesophageal junction cancer (GC/EGJC): Preliminary results of a phase II, single-arm trial. 2023 ESMO, 1539P.
[7]. Hirata Y, Agnes A, Prakash LR, et al. Borrmann Type Predicts Response to Preoperative Therapy in Advanced Gastric Cancer. J Gastrointest Cancer. 2023 Sep;54(3):882-889.
[8]. Song XH, Zhang WH, Kai-Liu, et al. Prognostic impact of Borrmann classification on advanced gastric cancer: a retrospective cohort from a single institution in western China. World J Surg Oncol. 2020 Aug 13;18(1):204.
[9]. Ralf H, Susanna H-B, Peter C, et al. HER-FLOT: Trastuzumab in combination with FLOT as perioperative treatment for patients with HER2-positive locally advanced esophagogastric adenocarcinoma: A phase II trial of the AIO Gastric Cancer Study Group. Journal of Clinical Oncology 2014 32:15_suppl, 4073-4073.
[10]. Rivera F, Izquierdo-M M, García-A P, et al. Perioperative trastuzumab, capecitabine and oxaliplatin in patients with HER2-positive resectable gastric or gastro-oesophageal junction adenocarcinoma: NEOHX phase II trial. Eur J Cancer. 2021 Jan 20;145:158-167.
[11]. Janjigian YY, Kawazoe A, Yañez P, et al. The KEYNOTE-811 trial of dual PD-1 and HER2 blockade in HER2-positive gastric cancer. Nature. 2021 Dec;600(7890):727-730.
排版编辑:肿瘤资讯-高惠
下期预告
免疫治疗帮助胃癌晚期患者实现持久获益
往期回顾:
【胃癌】转“胃”为安——一例转移性胃癌患者经替雷利珠单抗联合SOX治疗后成功转化达到病理完全缓解
【胃癌】救难“介胃”,白鱼“入”舟——一例转移性胃癌患者经替雷利珠单抗联合介入后达到完全缓解并长期获益











 苏公网安备32059002004080号
苏公网安备32059002004080号


