2024年美国临床肿瘤学会(ASCO)年会于美国时间5月31日在芝加哥盛大启幕,众多国际知名专家学者莅临现场,共同探讨当前国际最前沿的研究发现及临床试验成果。在此,软组织肉瘤研究领域涌现出多项突破性前沿进展。其中,复旦大学附属肿瘤医院严望军教授、王春萌教授领衔开展的一项安罗替尼对比安慰剂术后辅助治疗完全切除高级别软组织肉瘤的双盲、随机、对照试验(摘要号:11562)受到业界大量关注。值此盛会之际,【肿瘤资讯】特邀复旦大学附属肿瘤医院严望军教授、王春萌教授分享了此项研究的主要结果、临床价值,并对未来软组织肉瘤辅助治疗模式进行了探讨。
点击观看严望军教授完整采访视频
复旦大学附属肿瘤医院骨软组织外科科主任
复旦大学附属肿瘤医院脊柱肿瘤诊治中心主任
骨软组织肿瘤多学科综合治疗协作组(MDT) 首席专家
主要学术任职:
上海市抗癌协会第三届肉瘤专委会主委
中国抗癌协会第九届肉瘤专委会副主委
中国医药教育协会骨与软组织肿瘤专业青年委员会副主委
中国初级卫生保健基金会骨与软组织肿瘤专业委员会副主委
上海市中西医结合学会第三届脊柱医学专委会副主委
发明专利 7 项;主持国家自然科学基金 5 项,省部级基金 4 项;
获国家科技进步二等奖 1 项,省部级二等奖以上奖项 11 项。
副主编编写专著 17 部,发表SCI论文 100+ 篇,其中以第一作者和通讯作者发表SCI60+ 篇。
点击观看王春萌教授完整采访视频
复旦大学附属肿瘤医院骨软组织外科副主任医师,医学博士,硕士生导师
中国抗癌协会肉瘤专业委员会软组织肉瘤学组委员
中国抗癌协会原发不明转移肿瘤专委会委员
中国抗癌协会中西医整合骨与软组织肿瘤专委会常委
中国医药卫生文化协会医工融合分会委员
中国医药教育协会骨软肿瘤专委会委员
中华医学会肿瘤学分会腹膜后肿瘤学组委员
上海市医学会/医师协会骨肿瘤学组委员
上海市抗癌协会恶性黑色素瘤专业委员会常委
上海市抗癌协会肉瘤专业委员会常委
安罗替尼显著降低高级别软组织肉瘤(STS)术后复发风险,安全性可控
王春萌教授:高级别STS即使完全切除也有很高的复发风险,这给治疗带来了挑战。安罗替尼是一种多靶点酪氨酸激酶抑制剂,可阻断VEGFR、FGFR和PDGFR等,具有抗肿瘤血管生成和抑制肿瘤生长的作用。鉴于在既往试验中,安罗替尼对不可切除的晚期STS患者有很好的疗效,我们评估了安罗替尼作为完全切除的高级别STS辅助治疗的作用。

这是一项单中心、双盲、随机、对照试验,纳入完全切除后未接受辅助化疗的成年高级别STS患者,并以1:1的比例随机分配接受安罗替尼(12mg,PO,QD,d1-d14,Q3W)或安慰剂治疗,最多6个周期,直到疾病复发,无法控制的毒性或死亡。主要终点包括1年和2年无病生存(DFS)率。
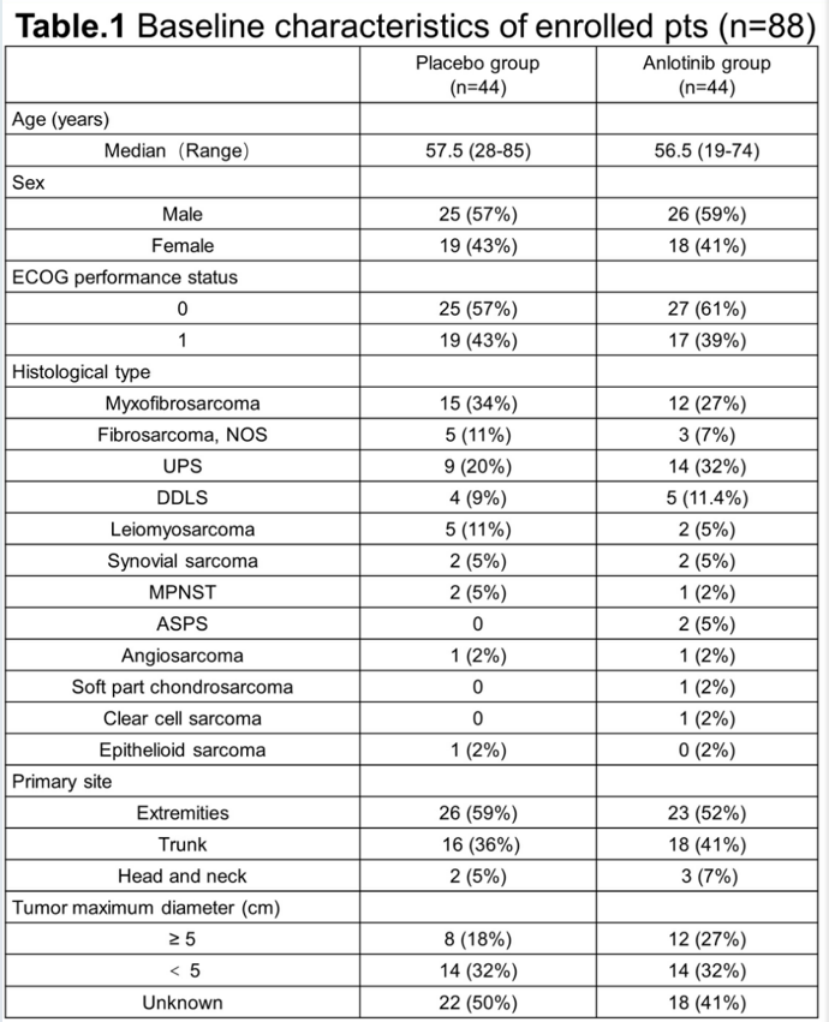
2019年6月至2023年11月,88名患者被随机分配至安罗替尼组(n=44)或安慰剂组(n=44)。截至2024年1月15日,中位随访时长25.99个月,安罗替尼组1年和2年的DFS率分别为88%和77%,而安慰剂组为64%和58%。与安慰剂组相比,安罗替尼组患者疾病复发风险显著降低(HR 0.47,95%CI:0.22~1.00,P=0.0445)。中位DFS尚未达到。基于肿瘤组织学,在黏液纤维肉瘤(1年DFS率:82% vs 61%;2年DFS率:64% vs 43%,HR 0.54,95%CI:0.17~1.65,P=0.2698)和未分化多形性肉瘤(1年DFS率:86% vs 67%;2年DFS率:78% vs 67%,HR 0.58(95%CI 0.12~2.87, P=0.4971)患者中观察到安罗替尼相比安慰剂对DFS有显著改善。
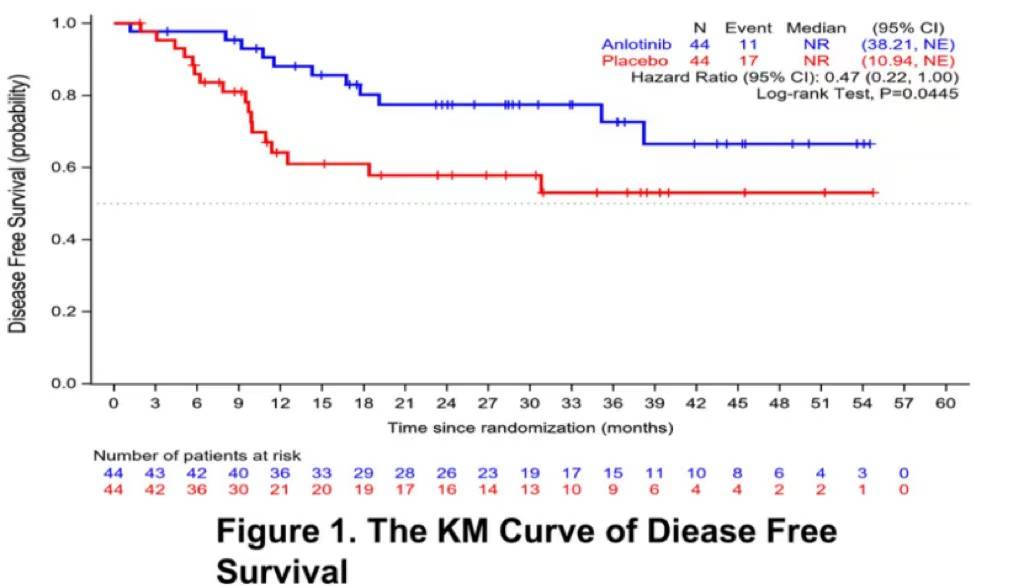
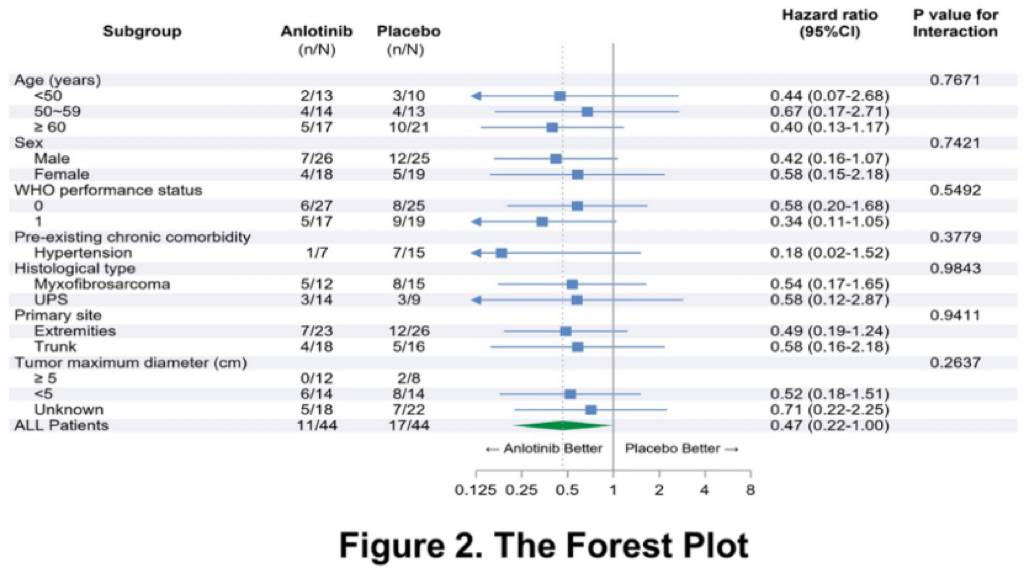
40例患者出现不良事件(87.5%为1~2级,12.5%为3级),其中安罗替尼组30例(68%),安慰剂组10例(23%)。4例患者停用安罗替尼,其中2例因蛋白尿/血尿(2/44,5%),2例因继发手术伤口愈合不良(2/44,5%)。目前的结果表明,安罗替尼可以降低完全切除后高级别STS患者的疾病复发风险,并且具有可接受的安全性。
安罗替尼或将成高级别STS辅助治疗全新选择
王春萌教授:我们这项研究提示,以安罗替尼为代表的靶向治疗可能在STS的辅助治疗中显著改善患者预后,改变当前临床上以化疗为主的STS术后辅助治疗格局。此项研究中,安罗替尼组1年和2年的DFS率分别为88%和77%,而安慰剂组为64%和58%。与安慰剂组相比,安罗替尼组患者疾病复发风险显著降低(HR 0.47,95%CI:0.22~1.00,P=0.0445),且安全性良好,12.5%的患者出现3级不良事件,无≥4级不良事件发生。
既往一项探索多柔比星联合异环磷酰胺对比吉西他滨联合多西他赛围术期治疗高级别STS的随机II/III期JCOG1306研究[1]显示,多柔比星联合异环磷酰胺组的2年无进展生存率为81.9% (95%CI: 69.5-89.7),吉西他滨联合多西他赛组的2年无进展生存率为64.0%(95%CI:51.1-74.4)(HR 2.32,95%CI:1.22-4.39)。两组均无治疗相关死亡。多柔比星联合异环磷酰胺组中88.4%的患者出现3级及以上中性粒细胞减少,而吉西他滨联合多西他赛组中79.5%的患者出现3级及以上中性粒细胞减少。此外,2008年的一项荟萃分析[2]显示,辅助化疗对比术后观察的局部复发风险比为0.73(P=0.02),远处转移及总体复发风险比为0.67(P=0.0001)。
虽未就安罗替尼与化疗术后辅助治疗STS进行头对头比较,但是上述研究在数值上可以看出安罗替尼是疗效和安全性兼具的术后辅助治疗新选择。相较于安慰剂,我们这项研究显示安罗替尼显著降低了高级别STS患者术后复发风险,并且安全性良好。安罗替尼可能为STS的辅助治疗提供新的思路,期待后续进一步随访数据的公布,可以持续显示安罗替尼的临床益处,为高级别STS患者的辅助治疗提供全新选择。
王春萌教授分享了一例其印象深刻的病例。患者70岁,大腿上患有紧贴血管的、高级别粘液纤维肉瘤。入组前曾接受过四次手术,并因恐惧化疗和放疗一直拒绝接受术后辅助治疗,导致术后几乎每年复发一次。第四次复发后参加了本项临床试验,接受第五次手术(R0切除),并保留了肢体。后续揭盲显示,患者属于安罗替尼组,接受了安罗替尼术后辅助治疗。目前其DFS达到24个月,未出现复发,尚在随访中。
安罗替尼相比化疗术后辅助治疗更安全、更便捷
严望军教授:术后辅助治疗旨在消灭亚临床病灶,减少远处转移和复发的风险,提高患者的无复发生存率。但非特指的STS的药物辅助治疗一直存在争议。一项纳入351例患者,大多数为G2/G3高级别肉瘤,年龄16~70岁,探索术后辅助多柔比星联合异环磷酰胺化疗对比单纯手术的随机、对照、III期EORTC62931研究[3]显示,术后辅助化疗并未改善患者的总生存期(OS)和无复发生存期(RFS)。但是,法国肉瘤组的随访数据显示FNCLCC3级STS患者可以从辅助化疗中获益,5年无转移生存率由49%提高到58%(P=0.01),5年OS率由45%提高到58%(P=0.0002)[4]。
自EORTC62931试验在2012年发表以后,已有十多年没有随机对照试验进一步探讨局部高级别STS手术切除后的辅助系统药物治疗方案。目前,CSCO诊疗指南[5]推荐,对于Ⅲ期化疗敏感的STS患者推荐术后化疗,Ⅱ期患者具备以下高危因素时也可考虑术后化疗:肿瘤位置深,肿瘤累及周围血管,包膜不完整或突破间室,FNCLCC 3级,局部复发二次切除术等。术后化疗在伤口愈合后尽早开始,共完成4~6周期。是否选择联合治疗以及治疗疗程,还需要根据患者的具体情况及意愿,综合制订治疗方案。
分子靶向治疗在晚期STS治疗中显示出一定的效果,此项研究使用的安罗替尼具有抑制肿瘤血管新生及抑制肿瘤生长的双重靶向作用。在安罗替尼治疗转移性STS的随机、双盲、安慰剂对照、多中心ALTER 0203研究[6]中,与安慰剂相比,安罗替尼可以显著延长患者无进展生存期,降低疾病进展风险(6.27个月 vs 1.47个月, HR 0.33, P<0.0001)。我们想知道安罗替尼作为高级别STS术后辅助治疗的疗效和安全性,因此开展了此项研究。本项研究也是首个公布软组织肉瘤术后辅助靶向治疗结果的临床试验。
我们这项单中心、双盲、随机、对照试验中,安罗替尼组1年和2年的DFS率分别为88%和77%,而安慰剂组为64%和58%。与安慰剂组相比,安罗替尼组患者疾病复发风险显著降低。40例患者出现不良事件(87.5%为1~2级,12.5%为3级),其中安罗替尼组30例(68%),安慰剂组10例(23%)。目前的结果表明,安罗替尼可以降低完全切除后高级别STS患者的疾病复发风险,并且具有可接受的安全性。但需要注意的是,我们有4例患者因为安罗替尼的不良反应而停药,其中2例为血尿、蛋白尿,另外2例为安罗替尼引起的手术切口愈合不良。再次需要强调,使用安罗替尼务必在患者手术切口充分愈合的情况下进行,以免引起不必要的伤口并发症。
这项研究最主要的临床启示就是,安罗替尼可能在高级别STS的辅助治疗中显著改善患者DFS,为术后辅助治疗提供了更多的药物选择。虽然这项研究在设计上,没有直接比较安罗替尼与当前的标准化疗方案,而是选择安慰剂作为对照组,但是也能从一定程度看到安罗替尼辅助治疗的优势。探索多柔比星联合异环磷酰胺围术期治疗高级别STS的JCOG0304研究[7]显示,围术期化疗的2年无进展生存率为75.7% (95% CI, 63.9-84.1%),约80%的患者出现4级白细胞或中性粒细胞减少。本研究中,安罗替尼组2年的DFS率为77%,12.5%的患者出现3级不良事件,无≥4级不良事件发生。由此可见,术后辅助口服安罗替尼的安全性和便捷性要远远优于术后辅助静脉化疗。
安罗替尼可能为STS的辅助靶向治疗填补空白,改善患者的预后,为STS的辅助治疗提供了新的思路,期待后续进一步随访数据的公布。
展望未来,更多辅助治疗方案的探索将为STS患者带来更好预后
严望军教授:高风险STS患者单纯手术治疗后的复发率较高,术后辅助治疗有望降低复发率,改善患者预后。关于STS术后治疗方案的选择,目前指南推荐的方案包括放疗及化疗,但是辅助放疗可能影响伤口愈合,辅助化疗对部分亚型效果不佳,辅助化疗后仍有较多患者出现局部复发或远处脏器转移,严重影响手术治疗效果和患者的预后。探索更优的辅助治疗策略是临床上较为迫切的需求。
对于STS术后辅助治疗,未来值得探索的研究方向主要有探索不同治疗手段(如化疗、放疗、靶向治疗、免疫治疗等)在STS术后辅助治疗中单独或联合应用,以寻找最佳的治疗方案。例如,今年ASCO会议公布的数据显示,安罗替尼联合PD-L1(贝莫苏拜单抗)抑制剂在腺泡状STS治疗中取得了良好效果[8],这为辅助治疗情境中,靶免联合治疗方案的探索提供了新思路。
未来STS的临床研究应针对一种或几种特定的组织学亚型开展或分析,即体现组织学特异性。本研究对高级别粘液纤维肉瘤和未分化多形性肉瘤均进行了亚组分析,并观察到了安罗替尼组人群获益的趋势。
STS的术后辅助治疗是一个复杂而重要的领域,应积极探索靶向免疫联合或靶向放疗联合等多种治疗模式。但也要牢记,根治性手术切除始终是早中期STS治疗的基石和重中之重, 在此基础上,相信未来会有更有效的辅助治疗策略,为STS患者带来更多的希望和福音。
1. Kazuhiro Tanaka, et al. Results of a randomized phase II/III study comparing perioperative adriamycin plus ifosfamide and gemcitabine plus docetaxel for high-grade soft tissue sarcomas: Japan Clinical Oncology Group study JCOG1306.. JCO 38, 11504-11504(2020).
2. Pervaiz N, Colterjohn N, Farrokhyar F, et al. A systematic meta-analysis of randomized controlled trials of adjuvant chemotherapy for localized resectable soft-tissue sarcoma. Cancer 2008; 113(3):573-581.
3. Woll PJ, Reichardt P, Le Cesne A, et al. Adjuvant chemotherapy with doxorubicin, ifosfamide, and lenograstim for resected soft-tissue sarcoma (EORTC 62931): a multicentre randomised controlled trial. Lancet Oncol 2012; 13(10):1045-1054.
4. Italiano A, Delva F, Mathoulin-Pelissier S, et al. Effect of adjuvant chemotherapy on survival in FNCLCC grade 3 soft tissue sarcomas: a multivariate analysis of the French Sarcoma Group Database. Ann Oncol 2010; 21(12):2436-2441.
5. 《中国临床肿瘤学会(CSCO)骨与软组织肿瘤诊疗指南2023》
6. Chi Y, Yao Y, Wang S, et al. Anlotinib for metastasis soft tissue sarcoma: A randomized, double-blind, placebo-controlled and multi-centered clinical trial. Journal of Clinical Oncology 2018; 36(15_suppl):11503-11503.
7. Tanaka K, Mizusawa J, Fukuda H, et al. Perioperative chemotherapy with ifosfamide and doxorubicin for high-grade soft tissue sarcomas in the extremities (JCOG0304). Jpn J Clin Oncol. 2015 Jun;45(6):555-61. doi: 10.1093/jjco/hyv042.
8. Zhichao Tan, et al. A phase II study of anlotinib and an anti-PDL1 antibody in patients with alveolar soft part sarcoma: Results of expansion cohorts.. JCO 42, 11515-11515(2024).
排版编辑:肿瘤资讯-陈湘钰











 苏公网安备32059002004080号
苏公网安备32059002004080号


