我国是胃癌高发国家,且以中晚期患者为主。腹膜是晚期胃癌最常见的复发转移部位,约有20%的患者在术前或术中诊断有腹膜转移,约50%的III期胃癌患者根治术后发生腹膜转移,既往伴有腹膜转移的晚期患者的中位总生存期(OS)只有3~6个月,5年OS率低于2%[1]。近年来,随着新型药物和治疗技术的革新,部分晚期胃癌伴腹膜转移患者的预后得到了显著改善[1]。南方医科大学南方医院赵丽瑛教授分享1例人类表皮生长因子受体2(HER-2)阳性晚期胃癌病例:患者男性,67岁,胃癌伴腹膜及淋巴结转移(IV期)。该患者胃镜取原发病灶HER-2(1+),经腹腔镜探查发现腹膜转移,腹膜转移灶取病理后再次病理检测发现HER-2(3+)。经多学科讨论后给予:化疗+曲妥珠单抗+PD-1单抗转化治疗,5周期后评价肿瘤缓解后行胃癌根治性手术及术后治疗,一线联合治疗13个月后出现肿瘤进展,进展时以腹膜转移病灶为主,并且出现大量癌性腹水,且患者高龄、一般状况较差(PS评分3分)。二线治疗采用我国自主研发的抗HER-2抗体偶联药物(ADC)药物联合PD-1单抗治疗2周期达到部分缓解(PR),无进展生存期(PFS)已经达到7个月,患者OS已经突破24个月。
病例介绍
病例分享专家
南方医科大学南方医院 普通外科
主要从事胃肠恶性肿瘤围手术期综合治疗
CSCO青年专家委员会 委员
CACA胃部肿瘤整合康复专业委员会 委员
广东省医学会消化肿瘤学分会消化道肿瘤MDT学组 副组长
广东省医学会外科学分会 委员
广东省医学会胃肠外科学分会 委员
广州市抗癌协会胃癌专委会 常委
广州市医学会肿瘤学分会 委员
主持国家自然基金2项,广东省自然科学基金2项
获中华医学会颁发“中华外科青年学者奖”一等奖
参获广东省科学技术进步奖一等奖2项、广东医学科技奖一等奖1项
基本情况
患者,男性,67岁。
主诉:因“进食哽噎感伴呕吐半年余”于2021年10月22日入院。
家族史:无特殊。
ECOG评分:1分
本次诊疗经过
2021年10月13日 门诊胃镜示:环贲门见巨大溃疡,病变侵及贲门口约10cm 范围(图1)。活检病理:胃底贲门低分化腺癌,部分为印戒细胞癌。病理分子及组化:Her-2(1+),PD-L1(22C3)CPS≈2;MLH1(+)、MSH2(+)、MSH6(+)、PMS2(+);原位杂交: EBER(-)。肿瘤标志物: CEA:5.46ug/L,CA-199:199.86U/mL(图2)。
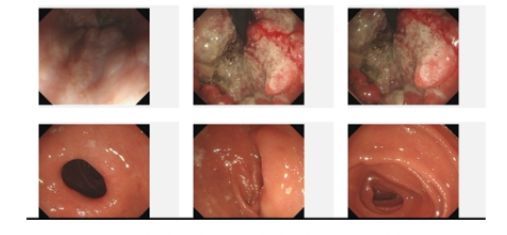 图1 2021年10月胃镜
图1 2021年10月胃镜
 图2 2021年10月病理
图2 2021年10月病理
2021年10月22日 全腹增强CT示:胃底部胃壁不规则增厚,最厚1.9cm, 以贲门为中心向周围生长,侵犯食管下段;胃底贲门周围多发淋巴结转移,最大1.5x2.3cm(图3)。
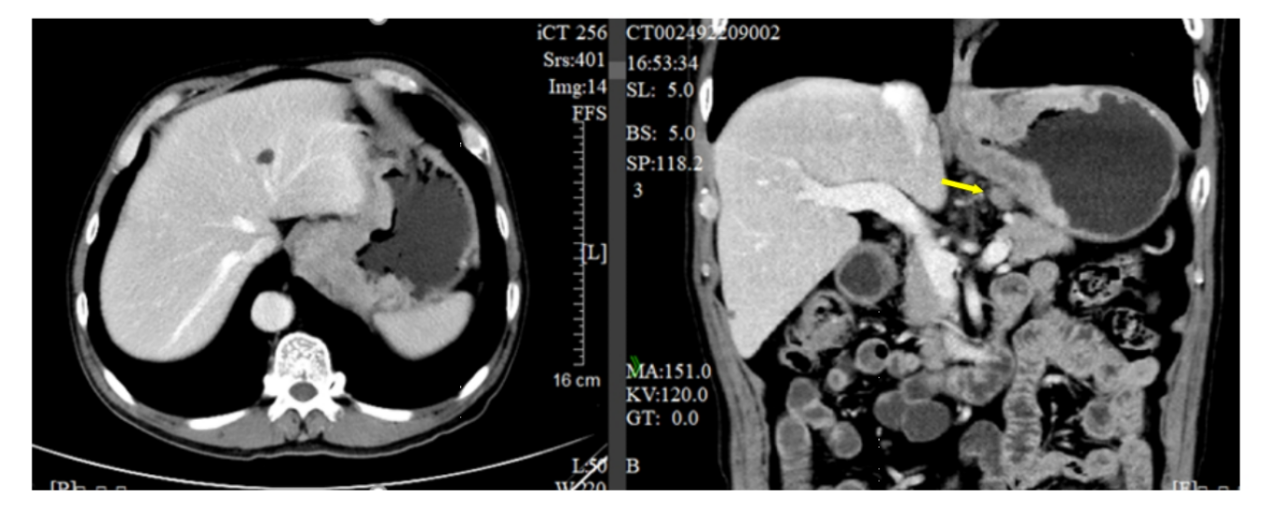 图3 2021年10月全腹增强CT
图3 2021年10月全腹增强CT
2021年10月25日 腹腔镜探查示:腹膜见可以癌结节,PCl评分2分;肿瘤位于贲门胃底,侵出浆膜面,侵犯膈肌脚;胃周淋巴结明显肿大;腹主动脉旁、肠系膜根部等未见明显肿大淋巴结;探查分期:sT4bN2M1。手术:腹腔镜探查+腹膜结节活检+胃周淋巴结活检。术后病理:脱落细胞学阳性(图4)。腹膜结节:见低分化腺癌浸润,符合胃腺癌种植转移;胃周淋巴结1、胃周淋巴结2:淋巴结见癌转移。免疫组化:Her-2(3+)、PD-L1(22C3)CPS≈5、pMMR、原位杂交:EBER(-)(图5)。
 图4 2021年10月术后病理
图4 2021年10月术后病理
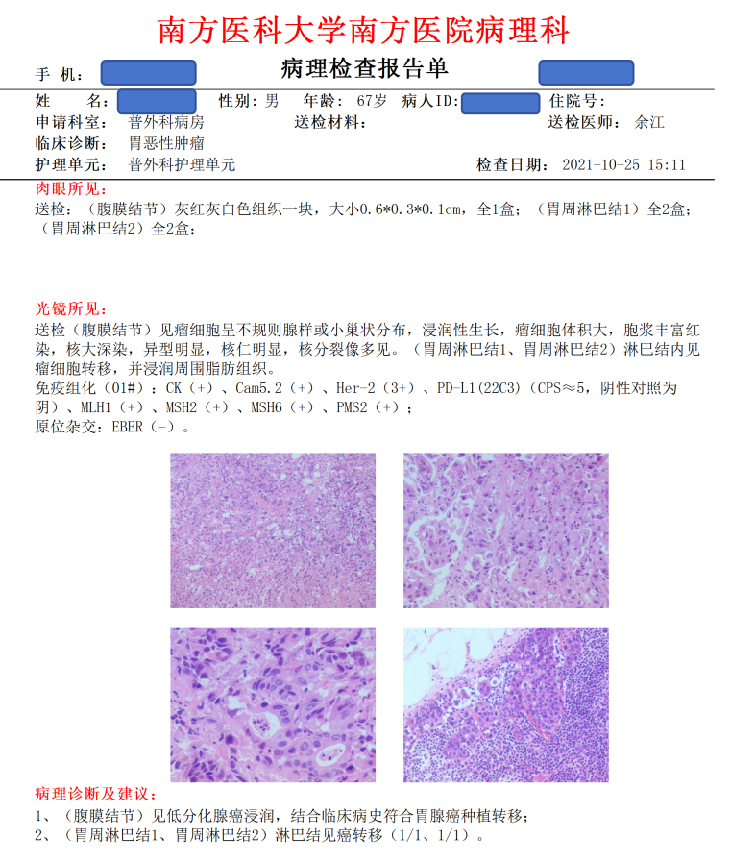 图5 2021年10月术后病理
图5 2021年10月术后病理
临床诊断:1.贲门胃底腺癌(sT4bN2M1,腹膜转移,CY1&P1);2.慢性浅表性胃炎;3.三尖瓣轻度返流;4.双下肢动脉多发斑块;5.双侧颈动脉斑块。
转化治疗
2021年10月28日至2022年1月26日 给予奥沙利铂+卡培他滨+曲妥珠单抗+PD-1单抗5周期转化治疗。
2022年1月26日 增强CT(胸+全腹)示:胃底部胃壁不规则增厚,较前减轻,现最厚1.5cm ( 原1.9cm ), 并侵犯食管下段;胃底贲门周围多发淋巴结转移,较前减少、缩小,现最大0.6X1.4cm (原1.5x2.3cm )(图6)。肺部未见可疑转移性病灶。疗效评价:PR。
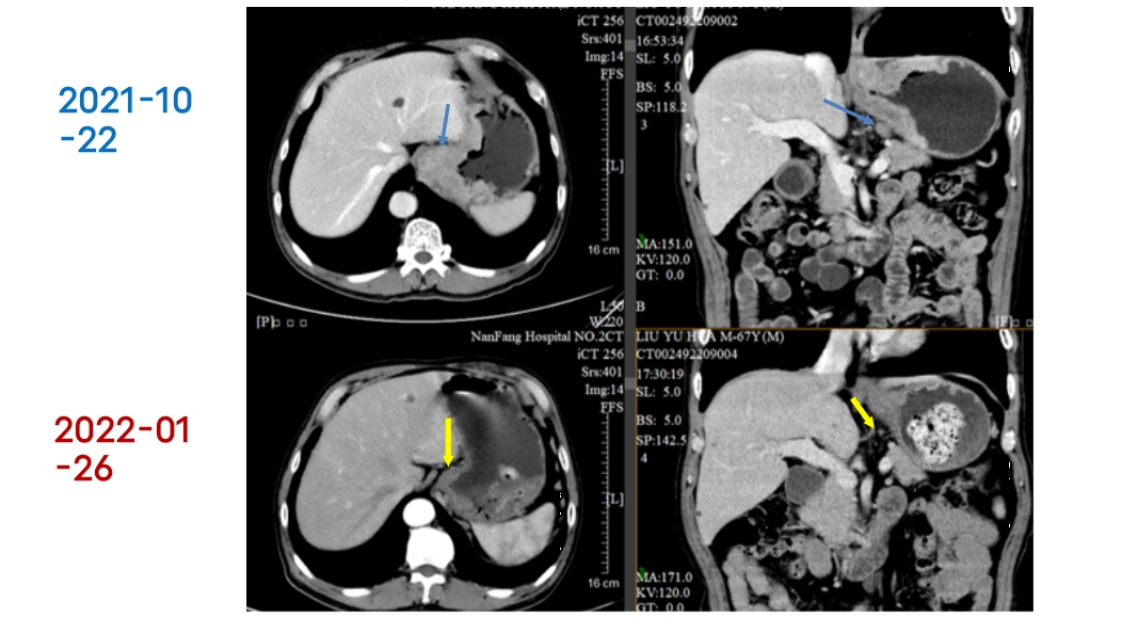
图6 2022年1月全腹增强CT
2022年2月22日 复查胃镜示:1.胃底贲门癌;2.慢性浅表性胃炎(图7)。
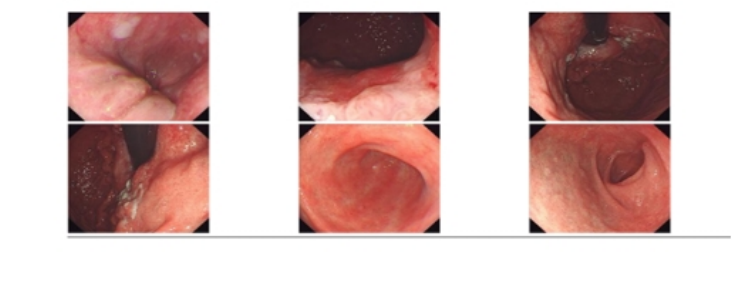 图7 2022年2月胃镜
图7 2022年2月胃镜
22年2月24日 腹腔镜探查示:腹腔内无腹水,左侧膈肌附近腹膜可见单个结节;肿瘤位于贲门胃底大弯侧,环周型生长,局部侵透浆膜侵犯左侧膈肌脚;胃周可见散在肿大淋巴结。术中诊断:贲门胃底癌(sT4bN2Mx)。手术:腹腔镜探查+全胃切除+D2淋巴结清扫+Roux-en-Y吻合术。术后病理:中至低分化腺癌,浸润至浆膜下层,局部累及食管壁全层,TRG评级:2级;(近切缘)及双侧自检切缘未见癌;(腹膜结节)为纤维组织,未见癌;送检淋巴结未见癌转移(0/69);脱落细胞学阴性(图8)。免疫组化: HER-2(1+),PD-L1(22C3)CPS=5,pMMR,EBV(-)。术后病理分期:ypT3N0M0,TRG 2级 。手术后恢复:顺利,术后7天出院。
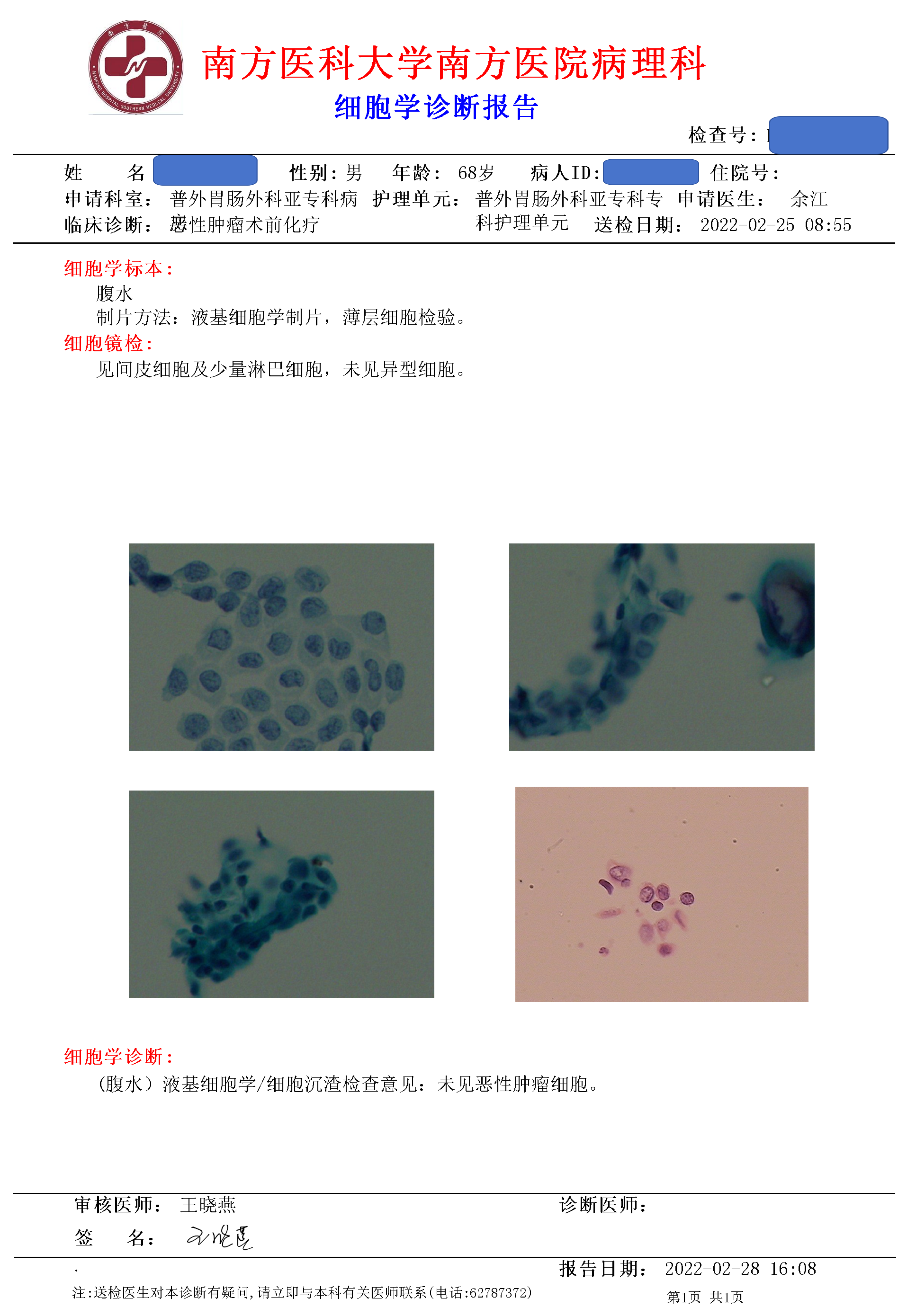 图8 2022年2月术后病理
图8 2022年2月术后病理
术后治疗
2022年4月8日 给予奥沙利铂+卡培他滨+曲妥珠单抗+PD-1单抗第6周期治疗。
2022年5月5日至2022年5月27日,给予卡培他滨+曲妥珠单抗+PD-1单抗第7-8周期治疗(第7程治疗时出现奥沙利铂过敏)。
2022-06-21 复查CT示:全胃切除食管空肠吻合术后,食管空肠吻合口及空肠-空肠吻合口肠壁稍增厚,未见明确肿瘤复发征象;腹腔内及腹膜后见多发小淋巴结,最大径6mm(图9)。
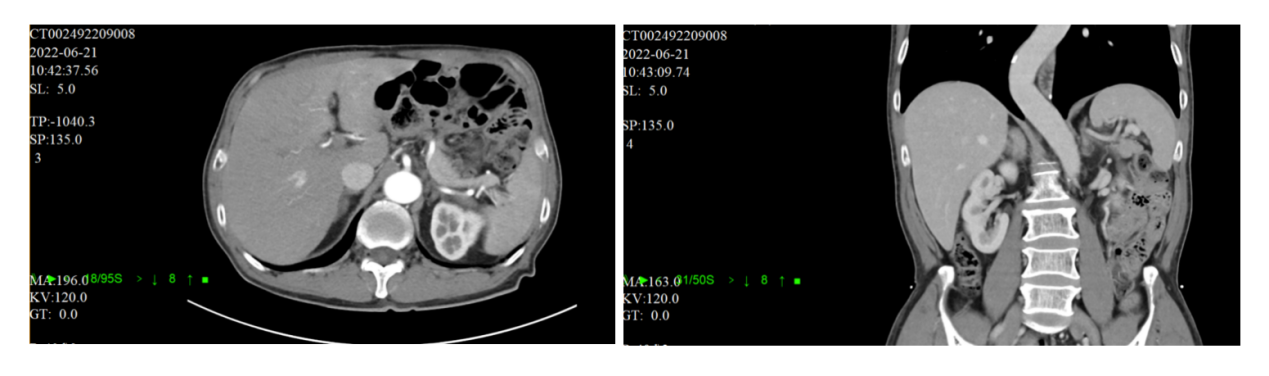 图9 2022年6月腹部CT
图9 2022年6月腹部CT
2022年6月20日至2022年9月27日 给予卡培他滨+曲妥珠单抗+PD-1单抗第9-12周期治疗。2022年9月27日最后一次治疗后患者自行停药。
2022年9月26日 复查CT示:全胃切除、食管空肠吻合术后,食管空肠吻合口及空肠-空肠吻合口肠壁稍增厚,大致同前,未见明确肿瘤复发征象;腹腔内及腹膜后多发小淋巴结,同前(图10)。
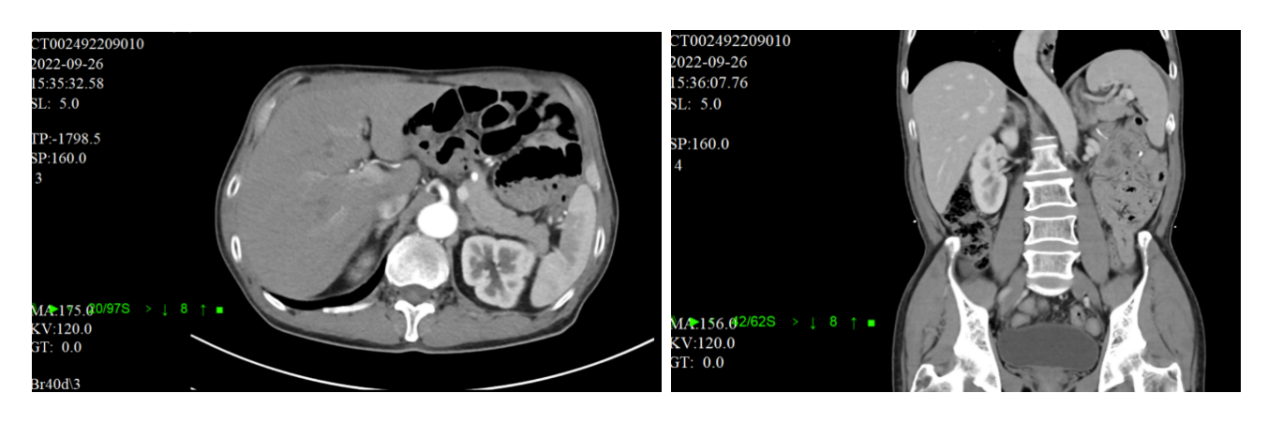 图10 2022年9月腹部CT
图10 2022年9月腹部CT
2023年1月16日 患者因“腹痛伴腹痛2天”急诊就诊。血清指标提示CEA、CA-199 显著上升(图11)。 查体+B超示:腹胀,大量腹腔积液。腹水细胞学送检:见大量腺癌细胞(图12)。
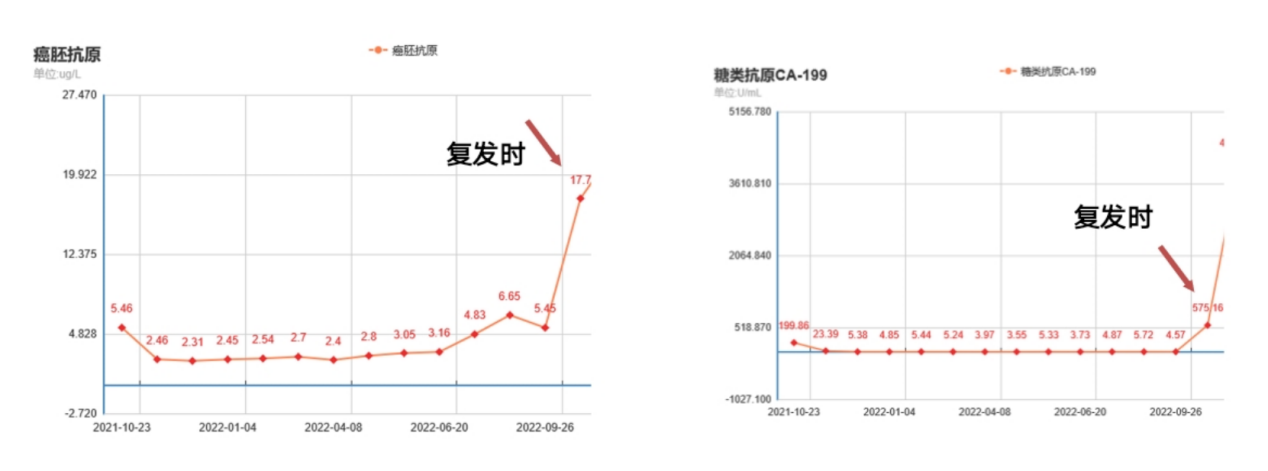 图11 2023年1月血清指标
图11 2023年1月血清指标
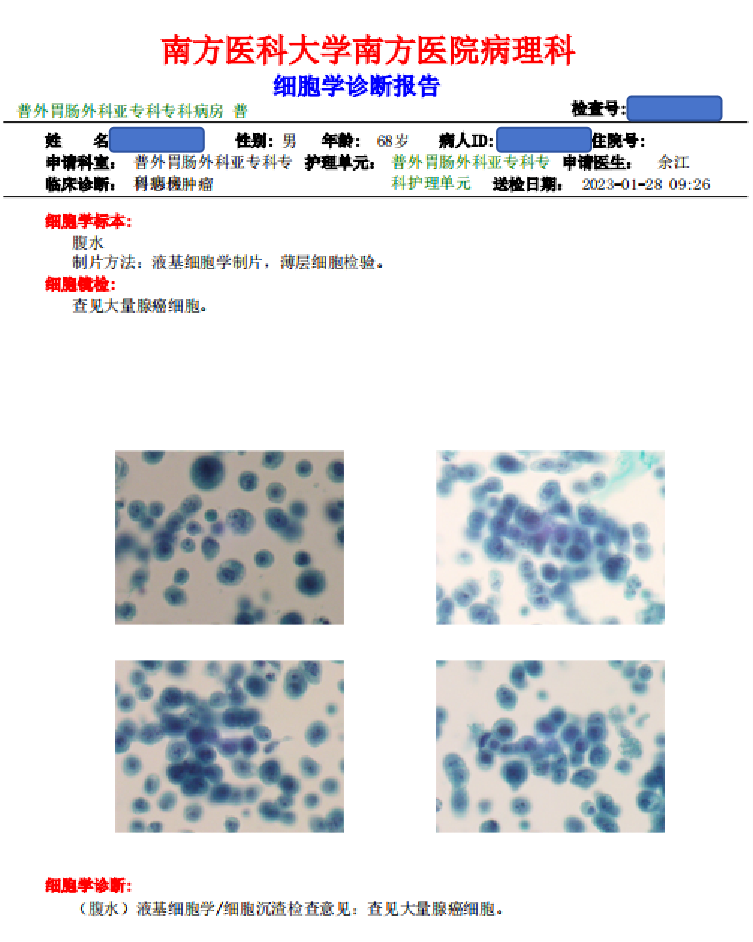 图12 2023年1月病理检查
图12 2023年1月病理检查
2023年1月19日 全腹CT示:全胃切除、食管空肠吻合术后,食管空肠吻合口较前增厚;右侧心膈角区、右侧胸骨旁、肝门区及腹膜后多发肿大淋巴结转移,较大2.1x1.6cm;腹盆腔大量积液,较前进展;腹膜稍增厚,局部见结节影,考虑腹膜转移可能(图13、图14)。
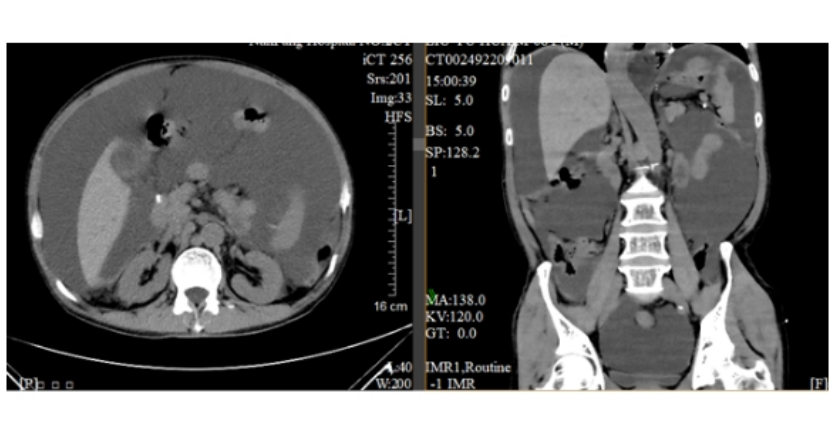 图13 2023年1月全腹CT
图13 2023年1月全腹CT
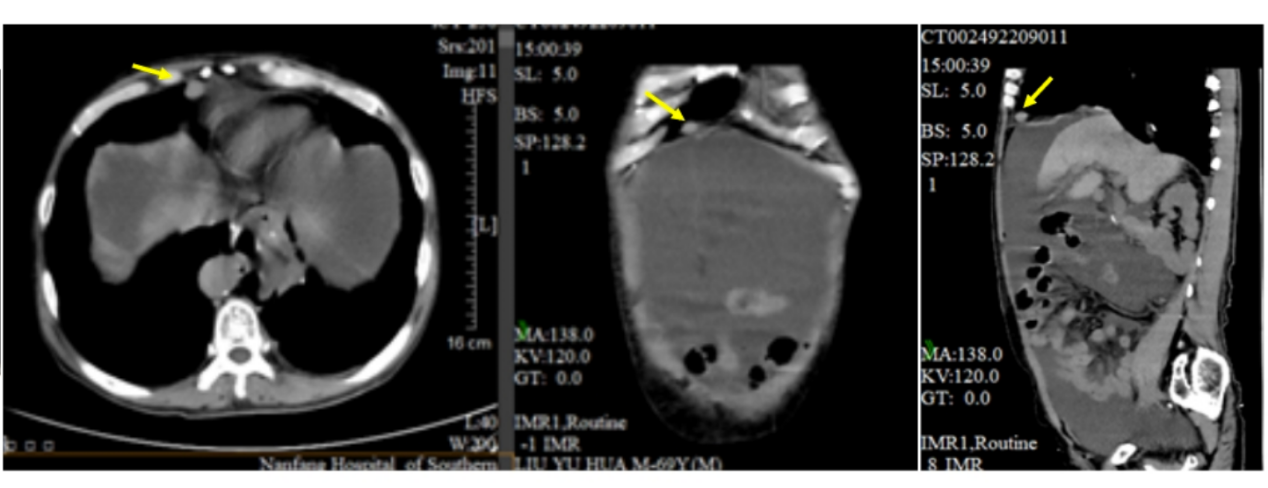 图14 2023年1月全腹CT
图14 2023年1月全腹CT
2023年1月28日腹腔镜探查示:全腹壁、肝脏表面、肝圆韧带、横结肠表面、小肠、盆腔等广泛转移灶,肿物表面呈多发结节状、胶冻样。术后病理:(腹膜结节)低分化腺癌,免疫表型结合临床病史符合胃腺癌转移,局部见脉管内癌栓。术后予多西他赛160mg 腹腔灌注3次。新发腹膜转移病灶再次活检后免疫组化: Her-2(1+)、PD-L1CPS≈1,pMMR、 原位杂交: EBER(-)(图15)。评价:疾病进展(PD)。
 图15 2023年1月病理检查
图15 2023年1月病理检查
临床诊断:1.胃癌(术后复发,rIV);2.腹膜继发恶性肿瘤;3.腹腔淋巴结转移;4.纵膈淋巴结转移;5. 腹腔积液;6.手术后状态(全胃切除术后)。
二线治疗
考虑到患者既往HER-2阳性,PD-L1表达阳性,二线治疗采用抗HER-2 ADC药物联合PD-1单抗治疗。
2023年3月8日、2023年3月30日 给予维迪西妥单抗+PD-1抗体 1-2周期治疗。
2023年3月30日 血清指标示:CEA、CA-199 显著下降(图16)。
 图16 2023年3月血清指标
图16 2023年3月血清指标
2023年4月24日 二线治疗2周期后复查全腹CT示:肝门区及腹膜后多发小淋巴结,较前明显缩小,现较大0.6x0.4cm ;右侧心膈脚区,右侧胸骨旁淋巴结已消失;原腹盆腔大量积液,较前基本吸收;腹膜稍增厚,较前减轻,局部见结节影,考虑腹膜转移(图17)。疗效评价:PR。
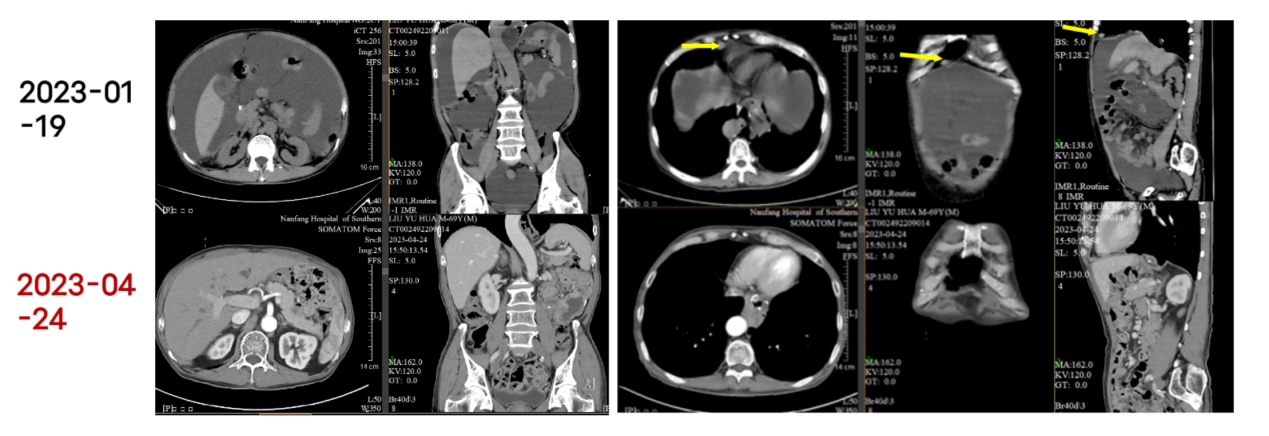 图17 2023年4月全腹CT
图17 2023年4月全腹CT
诊疗经过见图18。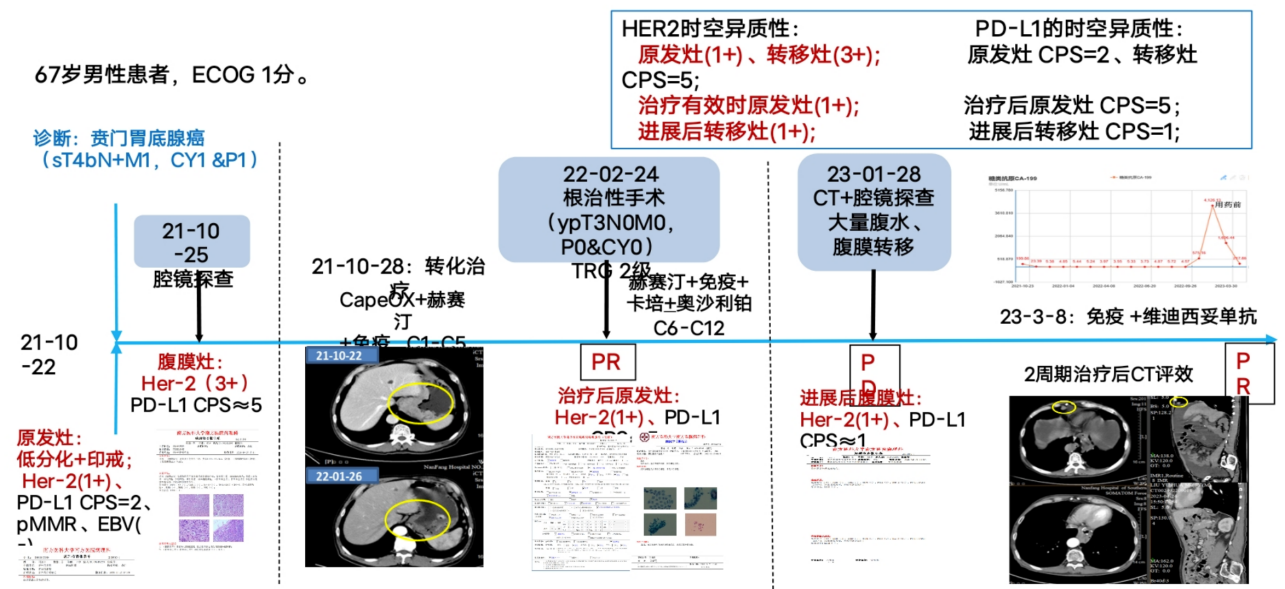
图18 诊疗经过
病例总结
该患者老年男性,晚期贲门胃底腺癌伴腹膜转移,sT4bN2M1,原发灶HER-2(1+),腹膜转移灶HER-2(3+)。奥沙利铂+卡培他滨+曲妥珠单抗+PD-1单抗治疗5周期达到PR,行胃癌根治性手术,术后病理分期ypT3N0M0。术后采用卡培他滨±奥沙利铂+曲妥珠单抗+PD-1单抗治疗7个周期后,患者自行停药。停药三个月后肿瘤复发,出现广泛腹膜转移、淋巴结转移、大量恶性腹水,PS评分3分。二线治疗采用抗HER-2 ADC+PD-1单抗治疗2周期评效PR,PFS达 7个月,OS突破24个月。
病例点评
点评专家介绍
中国腹腔镜胃肠外科研究组(CLASS)创始人
英格兰皇家外科学院院士(FRCS)
国家卫健委能力建设与继续教育外科专家指导委员会上消化道专委会主任委员
国家癌症中心胃癌质量控制专家委员会副主任
中华医学会外科学分会全国委员兼腔镜外科学组胃癌专业负责人
中国医师协会外科医师分会常委兼微创外科医师委员会副主任委员
《中国消化外科杂志》副总编辑
《中华胃肠外科杂志》副总编辑
国之名医-卓越建树奖(2023)
国务院政府特殊津贴专家(2021年)
国家卫生健康突出贡献中青年专家(2020年)
全国卫生计生系统先进工作者(2017年)
中国好医生月度人物(2018年)
美国腹腔镜内镜外科医师协会(SLS)荣誉勋章(2014年)
广东省特支计划杰出人才“南粤百杰”(2020年)
“南粤工匠”(2017年)
首届广东医师奖(2018年)
首届广东优秀临床科主任(2018年)
广东省丁颖科技奖(2016年)
HER-2是胃癌靶向治疗的经典靶点,我国胃癌患者HER-2阳性率约为12%~13%[2,3]。2010年,ToGA研究[4]首次证实抗HER-2靶向药物曲妥珠单抗联合化疗较单纯化疗明显延长HER-2阳性晚期胃癌患者的中位OS,确立了抗HER-2药物的标准一线治疗地位。2021年,KEYNOTE-811研究[5]证实,在曲妥珠单抗联合化疗基础上联合PD-1单抗可以显著提高客观缓解率(ORR)和中位未进展生存期(mPFS)。同时,靶向HER-2的ADC药物也在晚期胃癌中取得突破,进一步延长了HER-2阳性晚期胃癌患者的生存时间。
在我国自主研发的新型抗HER-2 ADC药物关键研究C008[6]中,针对≥2线标准治疗失败的HER-2 阳性晚期胃癌患者,客观缓解率(ORR)达到24.8%,疾病控制率(DCR)为42.4%,中位无进展生存期(PFS)为4.1个月,中位总生存期(OS)达到7.9个月。安全性方面,主要不良反应为血液学毒性,未发现间质性肺炎、心脏毒性等严重不良反应,无治疗相关死亡。基于C008研究结果,该ADC药物在国内获批HER-2阳性晚期胃癌治疗适应证,2023版中国临床肿瘤学会(CSCO)胃癌诊疗指南进一步提升了其推荐等级[7]。另外新版CSCO指南在转移性胃癌二线靶向治疗注释中标注,ADC药物用于胃癌二线治疗可取得良好的效果[7]。
由于胃癌具有高度异质性,《胃癌胃镜活检标本HER-2检测中国专家共识(2023版)》[8]推荐多点活检以提高检测准确性。另外曲妥珠单抗治疗会影响胃癌HER-2状态,因此指南推荐一线使用曲妥珠单抗治疗进展后再次进行胃镜活检病理学检查确认HER-2状态[8]。本例患者初始原发灶HER-2(1+),初始腹腔转移灶HER-2(3+),采用化疗联合曲妥珠单抗和免疫治疗方案转化治疗+根治性手术+维持治疗,停药复发后腹膜转移灶HER-2(1+),体现了胃癌患者HER-2表达的时空异质性,也提示了多点多部位活检对于检测HER-2状态的必要性。本例患者一线进展后瘤负荷量大,出现伴有广泛腹膜转移的大量恶性腹水,既往该类型患者单纯化疗的有效率低,中位OS为3~6个月,且该患者高龄,体力状态差,化疗耐受性差。针对患者初始HER-2(3+)的病理结果,及患者个体情况,二线治疗采用抗HER-2 ADC药物+PD-1单抗治疗,2周期治疗后即达到PR,且患者体力状态快速好转,PFS达到7个月,远超过C008研究中的4.1个月。北京大学肿瘤医院沈琳教授团队新近发表在柳叶刀子刊《EClinicalMedicine》上的探索性I期临床研究结果提示,维迪西妥单抗联合特瑞普利单抗治疗二线及以上胃癌患者的ORR达43%,持续缓解时间(DOR)为5.1个月,DCR为75%,中位PFS 为6.2个月,中位总生存期(OS)为 16.8个月,且安全性良好[9]。以上真实世界病例及临床研究均看到维迪西妥单抗联合PD-1单抗用于二线及以后患者治疗有效性和安全性,期待更大样本量的III期临床研究进一步证实该联合治疗方案的确切疗效。
[1] 中国抗癌协会胃癌专业委员会. 胃癌腹膜转移诊治中国专家共识(2023版)[J]. 中华胃肠外科杂志, 2023, 26(8): 717-728.
[2] Sheng WQ, Huang D, Ying JM, et al. HER-2 status in gastric cancers: a retrospective analysis from four Chinese representative clinical centers and assessment of its prognostic significance[J]. Annals of oncology: official journal of the European Society for Medical Oncology, 2013,24(9):2360-2364.
[3] Huang D, Lu N, Fan Q, et al. HER-2 status in gastric and gastroesophageal junction cancer assessed by local and central laboratories: Chinese results of the HER-EAGLE study. PLoS One. 2013;8(11):e80290.
[4] Bang YJ, Van Cutsem E, Feyereislova A, et al. Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER-2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. Lancet. 2010;376(9742):687-97.
[5] Janjigian YY, Kawazoe A, Yañez P, et al. The KEYNOTE-811 trial of dual PD-1 and HER-2 blockade in HER-2-positive gastric cancer. Nature. 2021 ;600(7890):727-730.
[6] Peng Z, Liu T, Wei J, et al. Efficacy and safety of a novel anti-HER-2 therapeutic antibody RC48 in patients with HER-2-overexpressing, locally advanced or metastatic gastric or gastroesophageal junction cancer: a single-arm phase II study. Cancer Commun (Lond). 2021;41(11):1173-1182.
[7] 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)胃癌诊疗指南[M]. 北京:人民卫生出版社,2023.
[8] 中国抗癌协会胃癌专业委员会, 中国抗癌协会肿瘤内镜学专业委员会. 胃癌胃镜活检标本HER-2检测中国专家共识(2023版)[J]. 中国肿瘤临床, 2023, 50(19): 973-982.
[9] Yakun Wang, Jifang Gong, Airong Wang, et al. Disitamab vedotin (RC48) plus toripalimab for HER2-expressing advanced gastric or gastroesophageal junction and other solid tumours: a multicentre, open label, dose escalation and expansion phase 1 trial. EClinicalMedicine. 2024;68:102415.
排版编辑:盐盐











 苏公网安备32059002004080号
苏公网安备32059002004080号


