IMpower133研究的成功,推开了广泛期小细胞肺癌(ES-SCLC)尘封仅30年的总生存(OS)大门,显示了免疫治疗为患者带来的生存获益的同时,也建立了全新的免疫联合化疗一线模式。如今,ASTRUM-005、CASPIAN、CAPSTONE-1、EXTENTORCH、RATIONALE-312、ETER-701等研究相继取得成功,原本由依托泊苷和铂类化疗占据的“小肺之巅”也逐渐成为了PD-1/PD-L1抑制剂的练兵场。在2023年即将结束之际,【肿瘤资讯】特邀天津医科大学肿瘤医院蒋日成教授回顾ES-SCLC一线免疫治疗的最新进展,剖析不同治疗方案为患者带来的生存获益。
天津医科大学肿瘤医院肿瘤精准检测与转化中心副主任
天津市肿瘤医院空港医院肿瘤精准转化诊疗科科主任
中国抗癌协会肺癌专委会委员
中国抗癌协会靶向治疗专委会委员
中国研究型医院学会肿瘤学专委会常务委员
中国医药教育协会肿瘤化疗专业青年委员会常务委员
中国老年保健协会肿瘤罕见靶点精准诊疗专委会副主任委员
天津市抗癌协会肺癌专委会常务委员
天津市抗癌协会靶向药物治疗专委会常务委员
天津市抗癌协会肺癌专委会青年委员会副主任委员、秘书长
北京慢性病防治与健康教育研究会分子靶向治疗专委会副主任委员
北京肿瘤学会肺癌专委会常务委员
北京癌症防治学会免疫治疗不良反应管理专委会常务委员
中国研究型医院学会精准医学与肿瘤MDT专委会肺癌学组委员
2023 ES-SCLC免疫治疗进展回顾
本年度的世界肺癌大会(WCLC)及欧洲肿瘤内科学会(ESMO)年会中,ES-SCLC的免疫治疗又有多项研究公布了最新结果。
ETER701[1]
这是一项随机、双盲、平行对照、多中心III期临床研究,旨在探索依托泊苷+卡铂的基础上联合安罗替尼±贝莫苏拜单抗一线治疗ES-SCLC患者的疗效和安全性。2023年WCLC中公布了研究中四药组(化疗+安罗替尼+贝莫苏拜单抗)对比单纯化疗组的疗效数据,四药组的中位无进展生存期(PFS)显著改善(6.93个月vs. 4.21个月,HR 0.32,95%CI 0.26-0.41; P<0.0001),两组6个月PFS率分别为59.11%和16.55%,12个月PFS率分别为27.91%和2.29%. 总生存期(OS)方面,四药组也同样取得显著改善(19.32个月 vs. 11.89个月,HR 0.61,95%CI 0.46-0.79;P=0.0002),两组12个月OS率分别为64.12%和49.00%,24个月OS率分别为41.83%和24.24%。
EXTENTORCH[2]
今年ESMO大会中,EXTENTORCH研究报告了结果。这是一项随机、双盲、安慰剂对照、多中心、III期临床研究,探索特瑞普利单抗或安慰剂联合依托泊苷及铂类方案治疗广泛期小细胞肺癌的疗效和安全性。本次报告结果显示,特瑞普利单抗组对比安慰剂组显著改善了PFS(5.8个月vs. 5.6个月,HR 0.667;P=0.0002)与OS(14.6个月 vs. 13.3个月,HR 0.798;P= 0.0327),特瑞普利单抗组具有更高的1年OS率(63.1% vs. 54.9%)。安全性方面特瑞普利单抗联合化疗治疗的安全性与既往研究报道一致,未观察到新的安全性信号。
RATIONALE-312[3]
这是一项随机、双盲、安慰剂对照、多中心的III期研究,旨在比较替雷利珠单抗+化疗与安慰剂+化疗用于ES-SCLC一线治疗的疗效和安全性。2023年WCLC公布的数据显示,替雷利珠单抗联合化疗组对比单纯化疗组显著改善了OS(15.5个月 vs. 13.5个月,HR 0.75,95%CI:0.61-0.92,P=0.0035),两组的1年OS率分别为62.7% vs. 58.4%,2年OS率分别为 33.2% vs. 22.4%,3年OS率分别为25.0% vs. 9.3%. 此外,替雷利珠单抗联合化疗组同样显著改善了PFS(4.8个月 vs. 4.3个月,HR 0.63,95%CI:0.51-0.78;P<0.0001),并具有更好的缓解表现(ORR:68.3%vs. 61.7%)。两组发生≥3级TRAEs发生率为85.5% vs 86.0%,其中最常见的(≥10%的患者)为血液学毒性。
ES-SCLC一线免疫治疗模式已全面建立
此前数十年间,ES-SCLC除化疗外缺少有效的治疗策略,但一线化疗为患者带来的生存获益也极为有限,IMpower133研究的成功改变了这一局面,开辟了ES-SCLC的一线免疫治疗模式。随后,CASPIAN、Capstone-1及ASTRUM-005研究的成功则相继为ES-SCLC的一线治疗带来了新的用药选择。
今年WCLC大会中,IMpower133研究公布了其与IV期、开放标签、非随机、多中心的单臂延伸和长期观察研究IMbrella A 的5年生存数据。IMpower133 研究中接受免疫联合化疗治疗的患者如果在 IMpower133 研究结束时继续接受阿替利珠单抗治疗,或在 IMpower133 研究中停用阿替利珠单抗且处于生存期随访中,将转入 IMbrella A 扩展研究中。结果显示,经过中位59.4个月的随访,接受免疫联合化疗治疗的患者的 3 年、4 年、5 年 OS 率分别为 16%、13% 和 12%[4]。
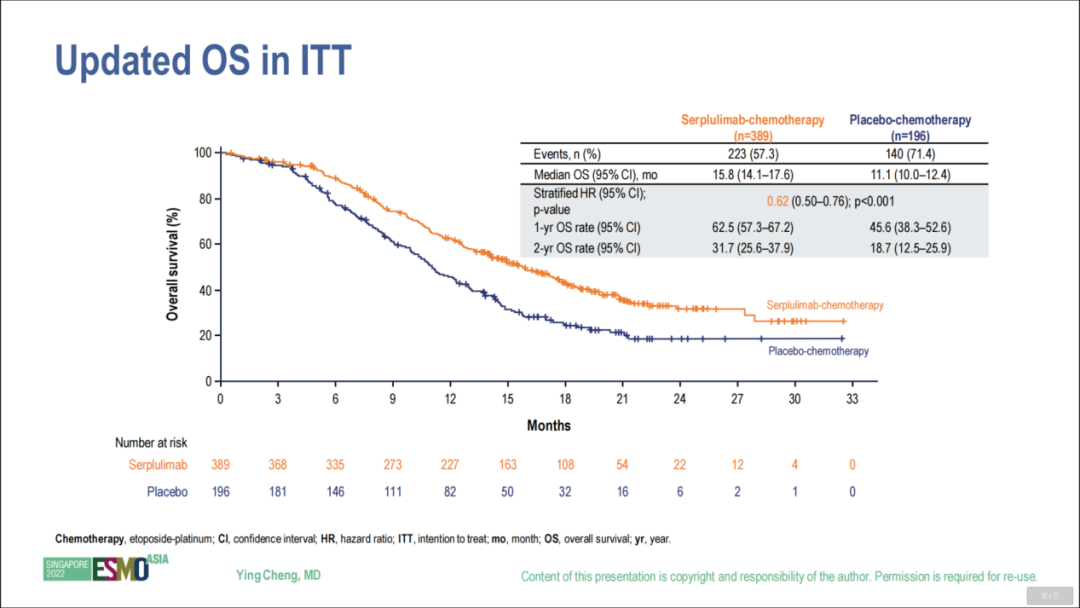
ASTRUM-005研究是首个取得阳性结果的针对PD-1单抗一线治疗ES-SCLC的III期临床研究。这是一项随机、双盲、安慰剂对照的III期临床试验,由来自6个国家的114家中心共同参与,旨在探索斯鲁利单抗联合化疗一线治疗ES-SCLC的疗效和安全性。该研究于2022年ASCO大会中首度亮相并全文发表于顶尖学术期刊JAMA,2022年ESMO ASIA中则公布了19.8个月随访后的生存数据[5,6]。结果显示,在意向治疗人群(ITT)中,斯鲁利单抗联合化疗组对比单纯化疗显著改善了中位OS(15.8个月 vs. 11.1个月,HR 0.62,95%CI 0.50~0.76;P<0.001),斯鲁利单抗联合化疗的1年OS率达到62.5%(vs. 45.6%),2年OS率达到31.7%(vs. 18.7%)。
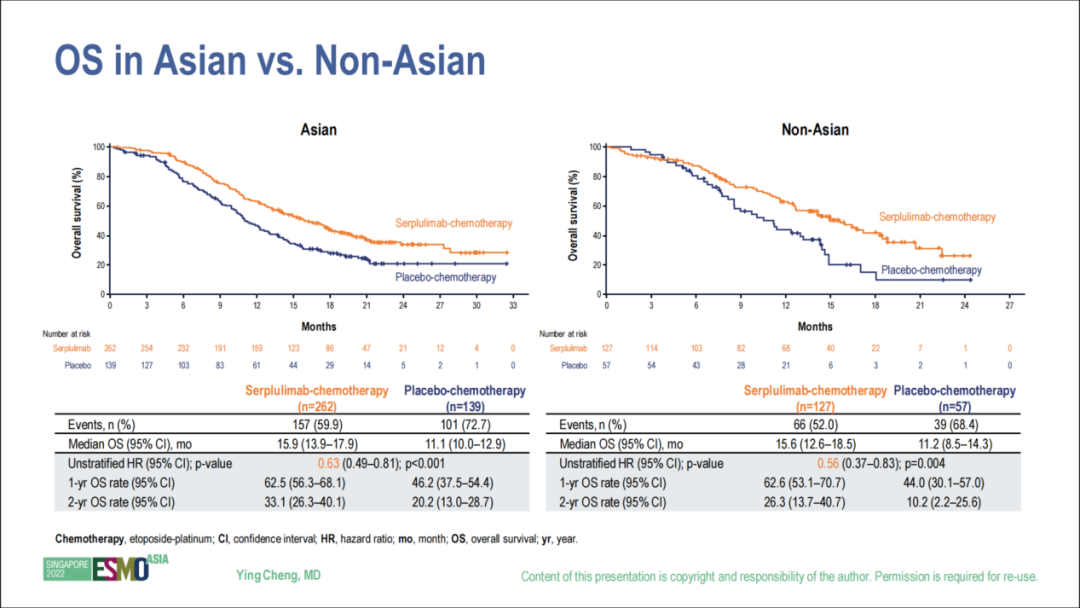
值得关注的是,在亚裔人群中,斯鲁利单抗联合化疗对比单纯化疗组的生存获益更为明显(中位OS:15.9个月 vs. 11.1个月,HR 0.63,95%CI 0.49~0.81;P<0.001),对比化疗组OS延长可达到4.8个月,略多于总体人群的4.7个月与非亚裔人群的4.4个月(15.6个月 vs. 11.2个月,HR 0.56,95%CI 0.37~0.83;P=0.004)。
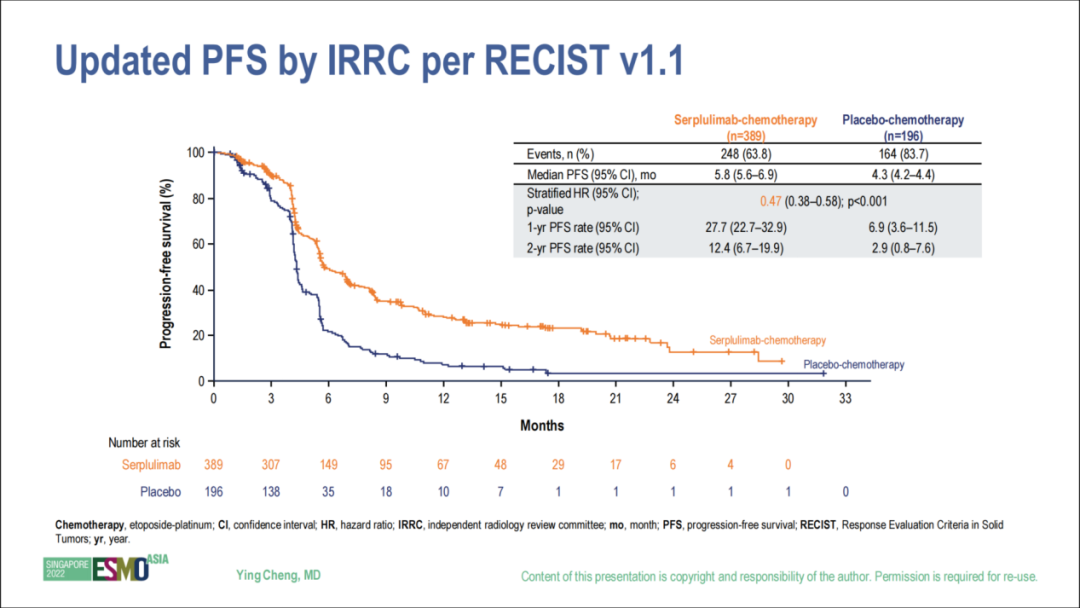
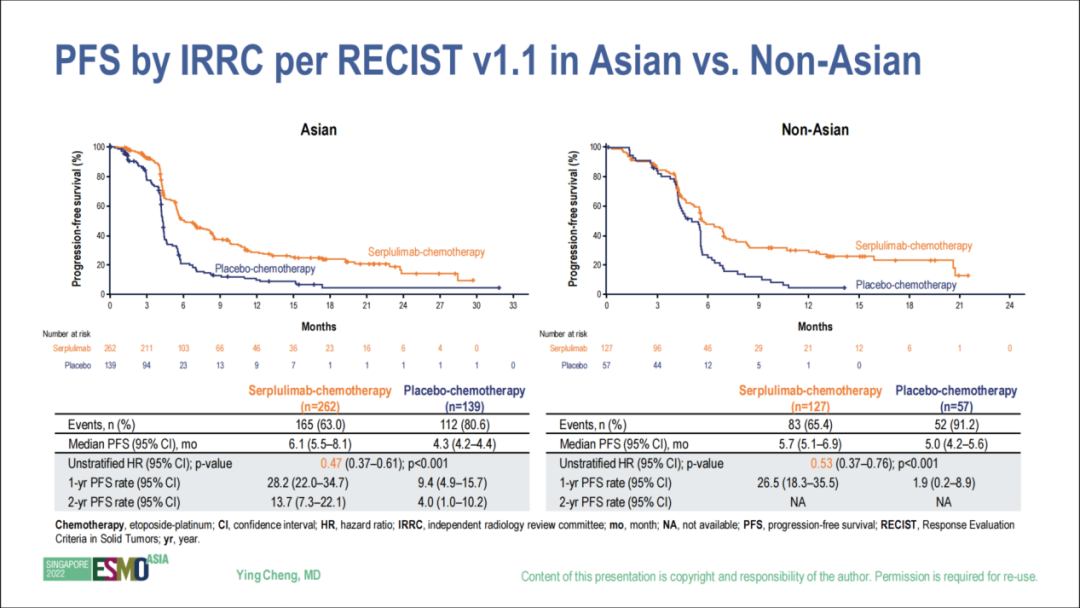
而在PFS方面,斯鲁利单抗联合化疗组对比单纯化疗组的1年PFS率分别为27.7% vs. 6.9%,12.4% vs. 2.9%,提高约4倍。两组中位PFS分别为5.8个月和4.3个月(HR 0.47,95%CI 0.38~0.58;P<0.001),显著降低了53%的疾病进展或死亡风险。亚裔人群中,中位PFS则分别为6.1个月和4.3个月(HR 0.43,95%CI 0.37~0.61;P<0.001)。
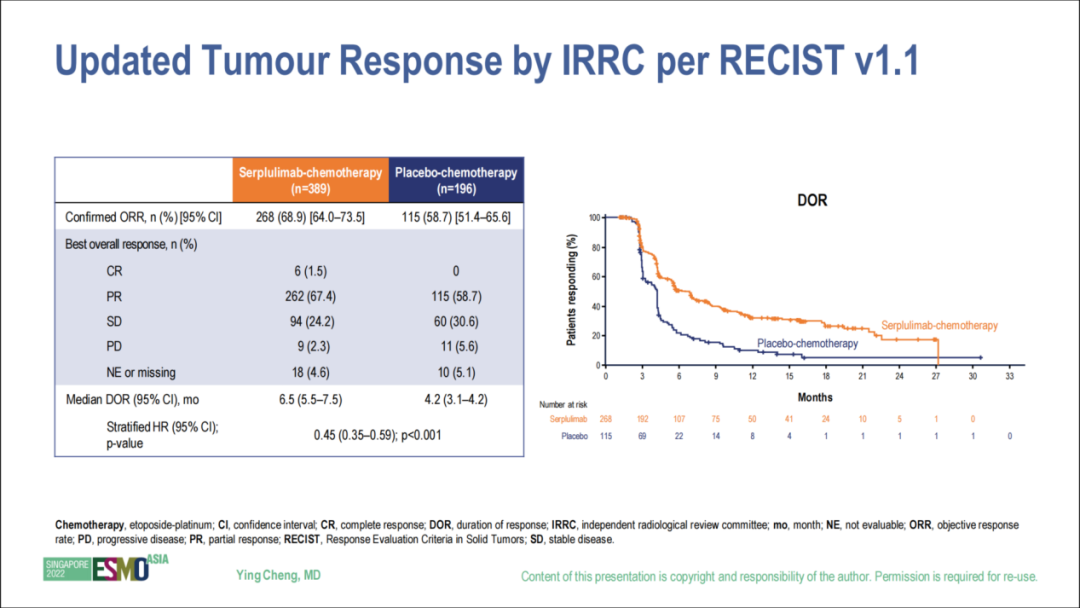
缓解方面,斯鲁利单抗联合化疗组确认的ORR达到68.9%,包括1.5%的患者达到完全缓解(CR),中位持续缓解时间更长(DoR:6.5个月 vs. 4.2个月),显示了高效而持久的缓解能力。安全性方面则整体可控,耐受性良好。
PD-L1单抗地位稳固,斯鲁利单抗为PD-1单抗正名
蒋日成教授:SCLC是一种高度侵袭性的恶性肿瘤,进展较快,易发生转移,很多患者初次就诊时已经处于广泛期,失去手术机会。此前,治疗手段主要依靠依托泊苷+卡铂/顺铂方案,患者中位OS约为10个月,亟需更为有效的治疗手段。
IMpower133和ASTRUM-005研究相继为PD-L1单抗和PD-1单抗在ES-SCLC中的一线免疫治疗模式打开了新局面。虽然PD-1单抗与PD-L1单抗都是靶向PD-1/PD-L1的免疫检查点抑制剂,作用机制为激活肿瘤抗原特异性T细胞,以人体自身细胞免疫过程杀伤肿瘤,但其具体作用靶点也存在差别。在ES-SCLC的治疗中,PD-1单抗的探索也并未如同PD-L1单抗一般顺利。
PD-L1单抗中,自IMpower133、CASPIAN研究成功以后,CAPSTONE-1研究及ETER701相继取得成功,持续佐证了基于PD-L1单抗的联合方案在ES-SCLC一线治疗中的疗效,为患者带来的生存获益也不断延长,至采用了PD-L1单抗+化疗+抗血管生成药物的四药模式的ETER701研究中,患者中位已达到19.32个月,逼近20个月。
而在PD-1单抗中,此前的探索却频频折戟。两大PD-1单抗纳武利尤单抗与帕博利珠单抗在ES-SCLC的探索都并不顺利,其在ES-SCLC领域的多项III期临床研究均未能显著改善ES-SCLC患者生存,并先后撤回FDA获批的SCLC适应症。
PD-1单抗一度被认为无法适用于ES-SCLC的治疗,直至ASTRUM-005扫清质疑,助力斯鲁利单抗成为首个在ES-SCLC一线治疗中为患者带来OS获益的PD-1单抗,并刷新了当时的一线OS记录(15.4个月),该研究全文发表于JAMA也体现了国际学界对其的认可,在后来者迎头赶上之后,截止2023年11月,ASTRUM-005更新的生存数据依然是PD-1单抗在III期临床研究中取得的最好数据(中位OS:15.8个月)。后续同样采取PD-1单抗的EXTENTORCH研究与RATIONALE-312研究相继取得成功,也丰富了PD-1单抗的用药选择。EXTENTORCH研究还首度设置了OS与PFS双终点并成功到达(中位PFS:5.8个月vs. 5.6个月,HR 0.667;P=0.0002)。
截止2023年11月,在PD-1单抗中,ASTRUM-005研究依然保持领先优势:
1. 首个取得阳性结果的PD-1单抗治疗ES-SCLC III期临床研究;
2. 迄今为止最长的总人群OS记录;
3. 降低53%的疾病进展或死亡风险,从数值角度优于同类,亚裔人群中更可降低57%的疾病进展或死亡风险;
4. 目前国内唯一获批适用于ES-SCLC一线治疗的PD-1单抗。
总结
在PD-1单抗中,首个成功的斯鲁利单抗依然保有竞争力优势,国内自主创新研制的PD-1的成功也同样值得欣喜,期待国内创新药持续走出国门,走向世界,以国际品质扬帆出海,为全球患者带来获益。
而另一方面,PD-L1单抗中的相关研究也为ES-SCLC的治疗带来了新的思考。ETER701采取四药联合模式取得了巨大的成功,不过该研究尚未公布化疗+抗血管生成药物的三药队列数据,随着后续数据的更新,或将提示抗血管生成药物在ES-SCLC一线治疗中的应用前景,也将为ES-SCLC的一线临床探索提供更多参考价值。
我们期待看到“小肺之巅”上更多创新药物同堂竞技,为临床医师提供更丰富的用药选择,为患者带来更多临床获益。
[1] Cheng Y, et al. Benmelstobart with Anlotinib plus Chemotherapy as First-line Therapy for ES-SCLC: A Randomized, Double-blind, Phase III Trial. 2023 WCLC. OA01.03.
[2] Cheng Y, et al. EXTENTORCH: A randomized, phase III trial of toripalimab versus placebo, in combination with chemotherapy as a first-line therapy for patients with extensive stage small cell lung cancer (ES-SCLC). 2023 ESMO. LBA93.
[3] Cheng Y, et al. First-line Chemotherapy with or without Tislelizumab for Extensive-stage Small Cell Lung Cancer: RATIONALE-312 Phase 3 Study. 2023 WCLC. OA01.06.
[4] Liu S V, Dziadziuszko R, Sugawara S, et al. OA01. 04 Five-Year Survival in Patients with ES-SCLC Treated with Atezolizumab in IMpower133: Imbrella a Extension Study Results[J]. Journal of Thoracic Oncology, 2023, 18(11): S44-S45.
[5] Cheng Y, Han L, Wu L, et al. Effect of first-line serplulimab vs placebo added to chemotherapy on survival in patients with extensive-stage small cell lung cancer: the ASTRUM-005 randomized clinical trial[J]. Jama, 2022, 328(12): 1223-1232.
[6] Cheng Y, Han L, Wu L, et al. LBA9 Updated results of first-line serplulimab versus placebo combined with chemotherapy in extensive-stage small cell lung cancer: An international multicentre phase III study (ASTRUM-005)[J]. Annals of Oncology, 2022, 33: S1562.
排版编辑:肿瘤资讯- CYY











 苏公网安备 32059002004080号
苏公网安备 32059002004080号


