非小细胞肺癌(NSCLC)包括除小细胞肺癌以外的所有肺上皮癌,占所有肺癌的80%-85%[1]。局晚期NSCLC(Ⅲ期)约占NSCLC患者的30%,局晚期NSCLC患者病情复杂多样,治疗方案的选择存在争议。《2023CSCO非小细胞肺癌诊疗指南》指出,对于可切除的ⅢA、ⅢB期NSCLC患者,新辅助联合手术治疗可作为选择方案之一, CheckMate-816研究显示,纳武利尤单抗联合化疗对比单独化疗显著提高病理完全缓解(pCR)(24.0% vs 2.2%,OR=13.94),延长无事件生存期(EFS)(31.6个月vs 20.8个月,HR=0.63,P=0.005),亚组分析表明,nsqNSCLC患者可从纳武利尤单抗联合化疗中获益 [2];对于不可切除Ⅲ期NSCLC患者,经新辅助治疗或许能增加可手术的机会,指南中推荐(Ⅱ级):经MDT讨论评价诱导治疗后降期手术的可行性,如能完全性切除,诱导治疗后手术治疗[3]。一项针对ⅢB期不可切除NSCLC患者新型治疗模式的探索性研究揭示:在新辅助免疫联合化疗诱导治疗降期后行肺癌根治术,完成手术组患者相较于未手术组患者,具有更长无进展生存期(PFS)(27.5个月 vs 16.7个月),此研究提示新辅助免疫治疗联合手术切除可以成为ⅢB期肺癌患者治疗的新模式 [4]。PD-1抑制剂斯鲁利单抗已获批多项适应症,涵盖小细胞肺癌、肺鳞癌、食管癌及MSI-H实体瘤,本文通过分享一例斯鲁利单抗联合化疗新辅助治疗ⅢB期肺腺癌达到pCR的病例,为临床实践提供参考。
病史简介
基本情况:男,59岁
首诊日期:2023-05-06
主诉:体检发现右肺阴影7月余。
既往病史:有高血压病史2年,口服药物控制血压,有糖尿病病史2年,口服药物控制。
个人史:有吸烟史30年,平均20支/日(2023年4月22日戒烟);否认饮酒史。
家族史:否认家族遗传性病史。
查体:ECOG PS 0分。发育正常,营养良好,神志清楚,正常面容,表情自然,自主体位,言语清晰,查体合作。无全身浅表淋巴结肿大,气管居中,胸廓正常,无肋间隙增宽,叩诊双肺呈清音,呼吸音清音,未闻及啰音,未闻及哮鸣音。
肿瘤标志物:均在正常范围内。
影像学检查:
2023-04-27 PET-CT(见图1):右肺上叶前段MT(最大径约32mm)可能性大;右侧锁骨区、纵隔及右肺门淋巴结转移可能。
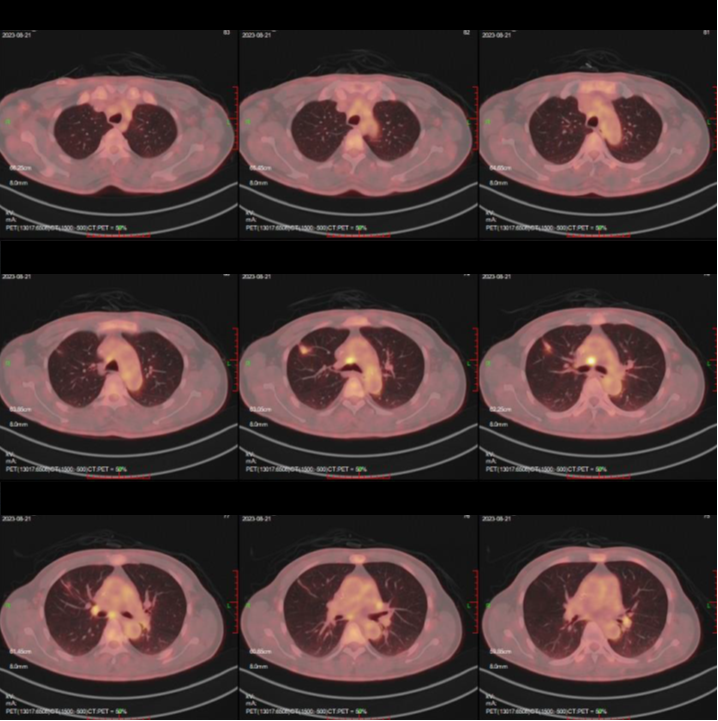
2023-04-28 胸部增强CT(见图2):右肺上叶肺癌可能,建议进一步检查。
2023-04-28 头颅增强MR:脑内少许缺血灶。
肺功能检查:
2023-04-28肺功能:肺通气功能正常。FEV1:3.36;FEV1实测值/预计值:111.8%。
支气管镜检查:
2023-04-28 EBUS:支气管镜经喉罩进入顺利,声门闭合可,气管环清晰,隆突锐利,双侧各叶段管腔通畅,黏膜光整,见少许粘痰,予以吸除,未见新生物,未见出血。超声下见4R淋巴结肿大,边界清,弹性成像提示质硬,内不均匀,血流少,予以穿刺。
病理结果:
2023-05-09右锁骨上淋巴结穿超声刺活检病理结果:转移性肺腺癌。免疫组化:CK(+),P40(-),TTF-1(SPT24)(+)。
2023-05-09右肺超声穿刺活检病理结果:腺癌。免疫组化:PD-L1(22C3)(80%+),PD-L1(E1L3N)(90%+),P40(-),CK5/6(-),TTF-1(+),NapsinA(+),CK(+)。
基因检测(2023-05-06):EGFR、KRAS、BRAF、ALK、ROS1、RET、NRAS、PIK3CA、HER-2、C-MAT(14EXON跳跃突变),均为野生型。
临床诊断:
1.右肺上叶恶性肿瘤:腺癌cT2aN3M0 IIIB期
2.高血压
3.糖尿病
治疗经过:
新辅助治疗:
2023-05-10、06-05、06-26、07-25行4周期免疫联合化疗方案治疗,具体方案为:斯鲁利单抗243mg(4.5mg/kg) d1+培美曲塞0.8g(500mg/m2) d1+卡铂536mg(AUC=5) d1 Q3W。
影像学评估:
2023-08-21 PET-CT(见图1):右肺上叶前段见糖代谢增高的结节影,大小约20×11mm,右肺上叶病灶体积减小,糖代谢减低;右侧锁骨区、纵隔(4R、7组)及右肺门淋巴结多处体积减小糖代谢减低,未见新增淋巴结。
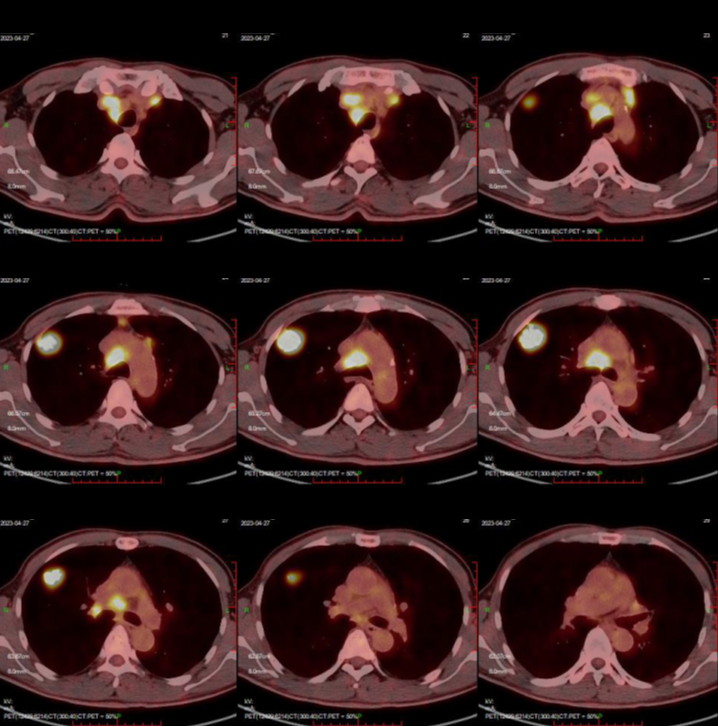 治疗前
治疗前
 4周期治疗后
4周期治疗后
图1 基线及治疗4周期后PET-CT
2023-08-21胸部增强CT(见图2):气管居中,气管-支气管通畅。右肺上叶见软组织密度肿块,长径约1.2cm,边缘毛糙,见分叶、毛刺、小棘状突起、胸膜凹陷征,病灶内密度不均。纵隔右肺门及右侧锁骨上区淋巴结肿大。右肺上叶肺癌可能,较前病灶缩小,请结合临床,建议复查。
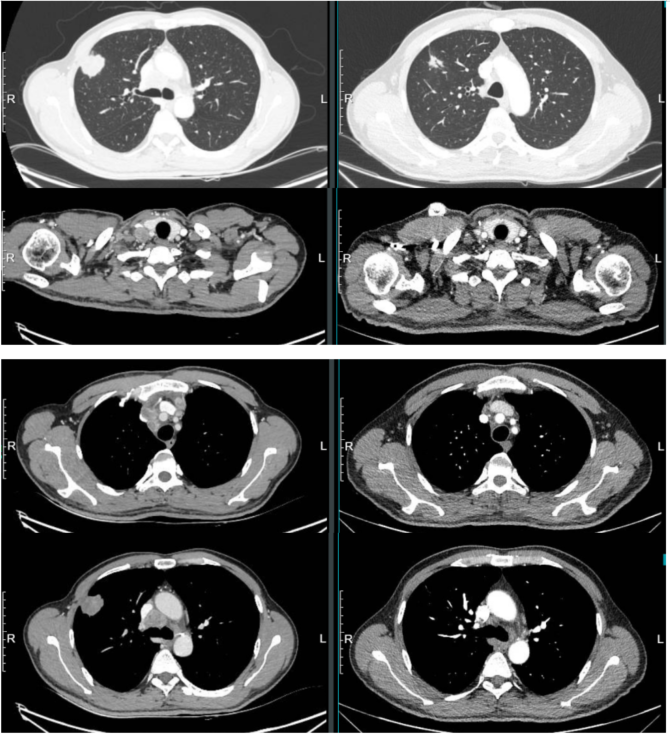 治疗前 4周期治疗后
治疗前 4周期治疗后
图2 基线及治疗4周期后胸部增强CT
2023-08-21头颅增强MR:脑内少许缺血灶。
不良反应:
2023-08-13出现≥3级血小板计数降低的不良反应(28×10^9/L),对症治疗后恢复正常。
术前检查:
2023-08-21肺功能:肺通气功能正常。FEV1:3.23; FEV1实测值/预计值:102.6%。
2023-08-21锁骨上淋巴结超声:未见肿大淋巴结。
手术治疗:
2023-08-25行单孔VATS右肺上叶切除术。
术后病理:
2023-08-25病理结果:存活肿瘤百分比:0%,坏死百分比:10% ,间质百分比(包括纤维化和炎症):90%。(右上叶)瘤床内较多纤维组织增生伴炎症细胞浸润,组织细胞反应,多核巨细胞形成,另见少量坏死,未见明确肿瘤组织,考虑新辅助治疗后反应。淋巴结未见癌转移:第2组(0/1);第3A组(0/1);第4组(0/1);第7组(0/7);第10组(0/3);第11组(0/3)。
疗效评价:病理完全缓解(pCR)。
辅助治疗:
2023-10-09至今给予斯鲁利单抗256mg d1 Q3W辅助治疗。
病例小结:
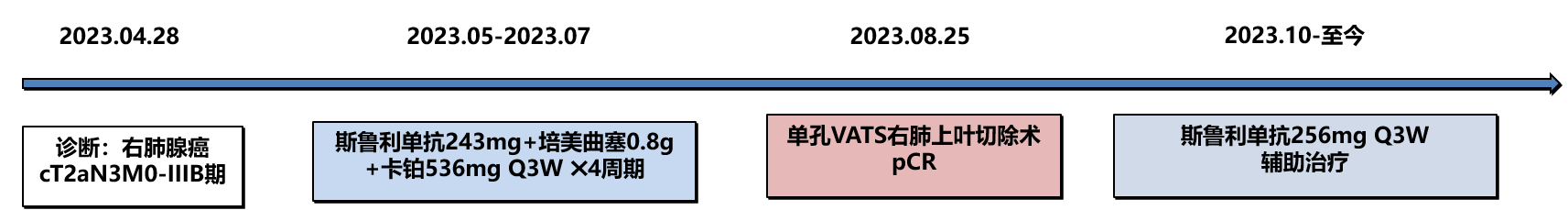 图3 治疗时间线
图3 治疗时间线
该患者初诊为ⅢB期驱动基因阴性肺腺癌,合并高血压、糖尿病等基础疾病,根据《2023年CSCO非小细胞肺癌诊疗指南》,针对不可手术切除的ⅢA~ⅢC期NSCLC患者,Ⅰ级推荐为同步放化疗后行度伐利尤单抗巩固治疗,经诱导治疗后行手术治疗为指南Ⅱ级推荐,旨在为Ⅲ期不可切除患者增加可手术治疗的机会。该患者行斯鲁利单抗+培美曲塞+卡铂方案进行新辅助治疗,4周期后患者PET-CT及胸部CT提示病灶较前缩小,综合评估患者身体状况后进行手术治疗,术后病理结果显示未查见肿瘤细胞,免疫联合化疗新辅助治疗疗效达pCR,患者术后恢复良好,患者治疗过程中出现≥3级的不良反应为骨髓抑制,对症处理后缓解,患者整体耐受性良好。术后同患者充分沟通后,继续给予斯鲁利单抗单药辅助治疗,期待能带给患者长久的生存获益。
专家点评:
肺癌是最常见的恶性肿瘤之一,全球最新的数据显示肺癌死亡率居恶性肿瘤首位,发病率占恶性肿瘤第二位,其中非小细胞肺癌发病人数远超于小细胞肺癌[1],免疫药物在非小细胞肺癌治疗中占据重要地位。CheckMate-816研究开辟了免疫联合化疗新辅助治疗可切除非小细胞患者的新征程[2],NEOSTAR等研究初步探索双免方案新辅助治疗的可行性[5]。PACIFIC研究证实同步放化疗后免疫巩固治疗可为不可切除Ⅲ期非小细胞肺癌患者带来显著生存获益(mPFS,16.8个月vs 5.6个月,P<0.001)[6],GEMSTONE-301研究填补了不可手术Ⅲ期肺癌患者序贯放化疗后免疫治疗的空白[7]。然而针对Ⅲ期NSCLC患者治疗,不论哪种免疫治疗模式,都无法取代外科手术切除的治疗价值。
Ⅲ期肺癌患者异质性强,需要临床医生结合患者情况开展个性化诊疗。随着新辅助治疗的广泛应用,肿瘤降期后行手术治疗,或许能为Ⅲ期不可切除非小细胞肺癌患者治疗提供新的选择。目前对于Ⅲ期不可切NSCLC患者免疫新辅助治疗研究探索极少,多数研究入组患者为初治可切除患者(大多为ⅠB-ⅢA期),且新辅助治疗未能明显缩小可切除肺癌患者手术范围[8] 。2022ESMO-IO报道的一项Ⅱ期SHR-1701-205研究,旨在解答不可手术Ⅲ期肺癌能否转化为可手术的临床问题,结果表明,不可手术患者经术前免疫治疗后,手术转化率为25.2%,手术患者的MPR率和pCR率分别为44.4%和25.9%[9],期待后续有更大样本量的研究进一步解答疑惑。
PD-1抑制剂斯鲁利单抗在肺癌研究领域深耕,凭借ASTRUM-005研究的优异结果,2023年1月17日,NMPA批准斯鲁利单抗联合卡铂和依托泊苷一线治疗广泛期小细胞肺癌(ES-SCLC)的适应症,《2023年CSCO小细胞肺癌诊疗指南》也将斯鲁利单抗+依托泊苷+卡铂作为ES-SCLC的Ⅰ级推荐(优选,1A类)治疗方案。在非小细胞肺癌领域,ASTRUM-004研究中斯鲁利单抗同样表现出优异的疗效及安全性,2022年11月1日,NMPA批准斯鲁利单抗联合卡铂和白蛋白紫杉醇用于一线治疗不可手术切除的局部晚期或转移性鳞状非小细胞肺癌(sqNSCLC)适应症,《2023年CSCO非小细胞肺癌诊疗指南》也将白蛋白紫杉醇+铂类联合斯鲁利单抗以Ⅰ级推荐用于驱动基因阴性肺鳞癌患者的一线治疗。正在进行的ASTRUM-002研究,旨在探索斯鲁利单抗联合化疗±贝伐珠单抗一线治疗非鳞非小细胞肺癌(nsqNSCLC)的疗效和安全性,预计2024年披露研究数据。基于治疗晚期肺癌患者的优异数据,斯鲁利单抗也在积极布局肺癌围术期研究。
该患者为ⅢB期PD-L1高表达、驱动基因阴性肺腺癌,考虑到患者强烈的手术意愿,经MDT讨论,给予斯鲁利单抗联合化疗新辅助治疗后进行手术的治疗方案,疗效达pCR,而且安全性良好,未见额外的手术并发症,该病例表明新辅助免疫治疗能够为不可切除ⅢB期非小细胞肺癌提供可手术的机会,免疫治疗前移是否能为Ⅲ期不可切肺癌患者带来更长生存获益,值得进一步探索。该病例证明斯鲁利单抗能为Ⅲ期不可切肺腺癌患者治疗提供依据,扩大了斯鲁利单抗真实世界的用药人群,为更多的肺癌患者带来更有效、更多样化的治疗选择。
[1]Siegel RL, Miller KD, Jemal A. Cancer statistics, 2020. CA Cancer J Clin. 2020 Jan;70(1):7-30.
[2] FORDE PM, SPICER J, LU S, et al. Neoadjuvant nivolumab plus chemotherapy in resectable lung cancer. N Engl J Med, 2022, 386 (21): 1973-1985.
[3]中国临床肿瘤学会指南工作委员会.中国临床肿瘤学会(CSCO)小细胞肺癌诊疗指南2023.
[4]Deng H,Liu J,Cai X.Radical Minimally Invasive Surgery After Immuno-chemotherapy in Initially-unresectable Stage IIIB Non-small cell Lung Cancer. Ann Surg.2022 Mar 1;275(3):e600-e602.
[5] Cascone T, William W N, Weissferdt A, et al. Neoadjuvant nivolumab or nivolumab plus ipilimumab in operable non-small cell lung cancer: the phase 2 randomized NEOSTAR trial[J]. Nature medicine, 2021, 27(3): 504-514.
[6]ANTONIA SJ, VILLEGAS A, DANIEL D, et al. Durvalumab after chemoradiotherapy in stage III non-small-cell lung cancer. N Engl J Med, 2017, 377 (20): 1919-1929.
[7] ZHOU Q, CHEN M, JIANG O, et al. Sugemalimab versus placebo after concurrent or sequential chemoradiotherapy in patients with locally advanced, unresectable, stage ITT non-small-cell lung cancer in China (GEMSTONE-301): Interim results of a randomised, double-blind, multi centre, phase 3 trial. Lancet Oncol, 2022, 23 (2): 209-219.
[8] Mountzios G, et al. Nat Rev Clin Oncol,2023 Jul 24.
[9] Wu Y. A Phase 2 Study of Neoadjuvant SHR-1701 with or without Chemotherapy Followed by Surgery or Radiotherapy in Stage III Unresectable NSCLC. ESMO IO. 2022.
病例作者
同济大学附属上海市肺科医院胸外科
点评专家
同济大学附属上海市肺科医院胸外科主任医师
同济大学外科学副教授、博士研究生导师,博士后合作导师
中华医学会器官移植分会肺移植学组委员
中华器官移植杂志编委
中国康复医学会器官移植专委会委员
上海市医学会器官移植分会青年委员和中国医促会胸外科分会青年委员
具有20余年的胸外科临床经验,擅长运用单孔胸腔鏡技术和开放技术治疗早中期及可手术的局部晚期肺部恶性肿瘤,以及肺部良性疾病和各类纵隔疾病。擅长肺癌的早期诊断,肺部磨玻璃结节(影)及其它肺部结节的诊治;擅长终末期肺病的肺移植治疗;擅长气管肿瘤、狭窄等气道疾病的外科治疗。2011年6月-2012年6月在麻省总医院访问学习胸部肿瘤外科技术和气管外科技术。
排版编辑:DND











 苏公网安备32059002004080号
苏公网安备32059002004080号


