近日,全球最负盛名和最具影响力的肿瘤学会议之一——欧洲肿瘤内科学会(ESMO)大会在西班牙马德里盛大落幕。诸多前沿进展在本届大会中公布了最新成果,其中百泽安®(替雷利珠单抗)联合含铂双药化疗用于可切除非小细胞肺癌(NSCLC)“新辅助+辅助”治疗的Ⅲ期注册临床研究——RATIONALE-315研究以高手术率、病理完全缓解(pCR)率、以及主要病理缓解(MPR)率而备受瞩目,为NSCLC“新辅助+辅助”围术期全程免疫治疗模式再添力证。在此,【肿瘤资讯】特别邀请RATIONALE-315研究PI同济大学附属上海市肺科医院张鹏教授深入解析该研究的结果及其临床意义。
主任医师,教授,博士生导师
副院长
中华医学会胸心血管外科学分会青委会副主任委员
中国抗癌协会青年理事会理事
中国生理协会呼吸专业委员会副主任委员
擅长肺部小结节的诊断及微创治疗,对于局部晚期非小细胞肺癌的新辅助治疗和辅助治疗有独到的体会。发起和参加了多项局部晚期非小细胞肺癌的免疫新辅助和靶向新辅助临床研究,取得了良好的临床治疗效果。科学研究专注于肺癌免疫治疗和靶向治疗免疫微环境的变化以及肺癌发生发展机制的探索。
近年来作为通讯作者(含共同)的文章发表于Genome Biology, Journal of Thoracic Oncology, Nature Communications, Nucleic Acids Research, The Annals of thoracic surgery等权威期刊,获得了国家自然科学基金委员会杰出青年基金、面上项目,上海市科学委员会青年优秀学术带头人等项目课题的资助。以第一完成人获得第十七届上海医学科技奖三等奖。
RATIONALE-315研究脱颖而出,数据惊艳亮相ESMO
RATIONALE-315研究在本届ESMO大会中吸引了全球研究者的关注。作为该研究的PI,请您分享一下该研究的数据亮点?
张鹏教授:RATIONALE-315研究是一项随机、双盲、安慰剂对照的Ⅲ期临床研究【1】,旨在评估可切除Ⅱ-ⅢA期NSCLC患者接受替雷利珠单抗联合含铂双药化疗“新辅助+辅助”围术期免疫全程治疗的疗效和安全性(图1)。全国近五十家研究中心参与该研究,最终入组453例中国患者,是迄今为止纳入中国患者最多的肺癌围术期免疫治疗Ⅲ期临床研究,广泛覆盖了II-III期患者,获益人群更广。
 图1 RATIONALE-315研究设计
图1 RATIONALE-315研究设计
RATIONALE-315研究取得了令人惊艳的结果。在病理缓解方面,替雷利珠单抗联合化疗组的pCR率达41%,较单纯化疗组提升35%。同时,替雷利珠单抗联合化疗组的MPR率达56%,较单纯化疗组提升41%。亚组分析显示,无论患者PD-L1表达水平、组织类型,患者均可从替雷利珠单抗联合化疗的治疗中显著获益(图2)。
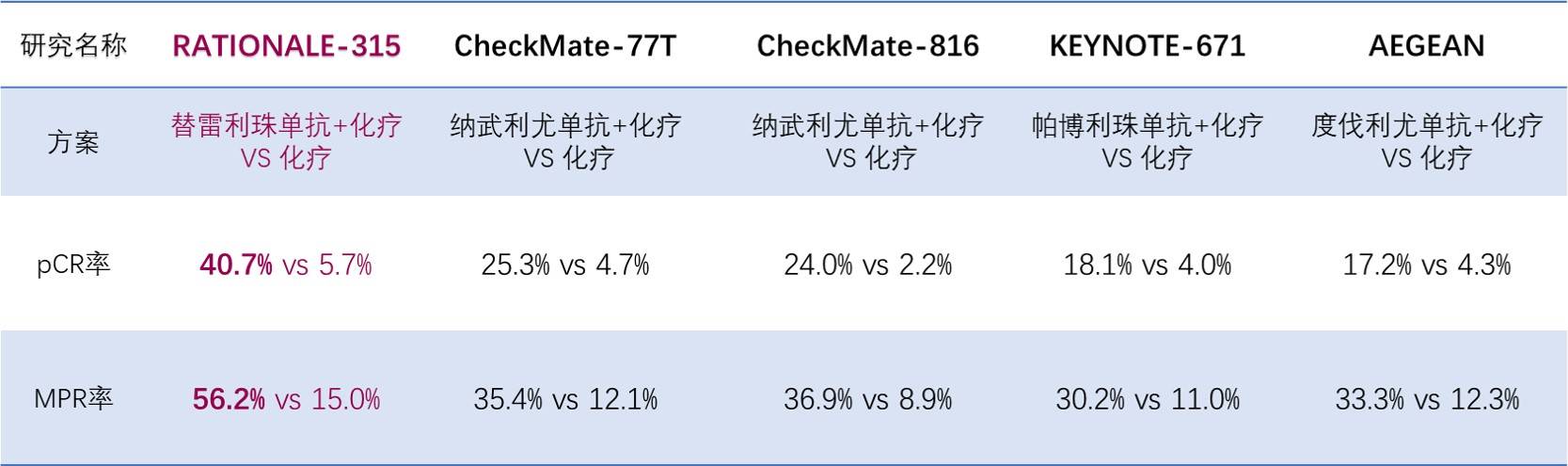 图2 NSCLC围术期领域Ⅲ期临床研究总览——pCR率、MPR率[1-5](非头对头研究,仅供参考)
图2 NSCLC围术期领域Ⅲ期临床研究总览——pCR率、MPR率[1-5](非头对头研究,仅供参考)
我们中心参与了RATIONALE-315研究,并成功入组了15例患者,入组患者总体疗效优异,即使在盲态下,全部受试者的客观缓解率也达到了60.0%,pCR率为33.3%,以及MPR率为58.3%,均达到较高水准,最终的研究结果也印证了我们的临床感受。此外相较于既往新辅助治疗经验,入组患者的总体不良反应并未增加,免疫联合化疗新辅助不良反应甚至更为轻微,临床用药更为安心。
pCR是最直观反映新辅助治疗阶段疗效的临床指标之一,其定义为在切除的肿瘤组织和区域淋巴结进行完整评估后没有任何残留的肿瘤细胞,亦可直接反应药物对肿瘤的深度缓解能力,被视为免疫激活的金标准。同时,pCR率和MPR率与患者的长期生存密不可分,围术期免疫治疗能够将原位肿瘤转变为“自体疫苗”进而激活抗肿瘤免疫反应,活化的肿瘤特异性CD8+ T细胞通过机体迁移持续寻找并消灭肿瘤微病灶,从而实现更长的EFS和OS。随着替雷利珠单抗RATIONALE-315研究的MPR和EFS双终点全面报阳,让我们对其未来在临床实践中为患者带来更长的EFS及OS充满信心,让更多患者实现治愈!
此外,手术切除仍然是现阶段治愈肺癌的唯一手段,最大化提升根治性手术率是我们开展围术期免疫治疗的重要目标之一。RATIONALE-315研究手术率为84%,因新辅助治疗期间疾病进展或发生治疗相关不良反应取消手术的比例仅为4.9%。同时,新辅助替雷利珠单抗联合化疗组患者发生严重不良事件(SAE)的发生率与单纯化疗组相当(11.1% vs 10.6%),其中与替雷利珠单抗相关的SAE仅4.9%,充分证实了替雷利珠单抗全面兼顾了卓越疗效与优异安全性,最大化患者接受根治性手术的机会,为更多NSCLC患者走向治愈保驾护航!
RATIONALE-315研究立足中国临床实践,创新围术期免疫全程管理模式
在众多NSCLC围术期免疫治疗研究中,RATIONALE-315研究设计有何特点,对临床有哪些重要的意义和价值?
张鹏教授:在获得如此优异疗效的基础上,RATIONALE-315研究还有着极具巧思的方案设计,有望为临床带来创新治疗方案选择。
在新辅助治疗阶段,RATIONALE-315研究前瞻性地采用了3-4周期方案,这样的设计更符合新辅助治疗的初衷,不仅可以最大程度激活抗肿瘤免疫反应,在术前有效缩瘤降期,同时也充分满足了临床实践中针对每位患者个体情况灵活选择最佳手术时机的需求。
在术后辅助治疗阶段,RATIONALE-315研究创新性地采用了6周间隔给药(400mg Q6W 8周期)的辅助治疗方案,与既往研究3周或4周间隔给药模式截然不同,让辅助治疗阶段仅需用药8次,可降低患者就医次数和负担。替雷利珠单抗400mg,Q6W的方案前期已经过暴露-反应 (E-R) 研究分析以及3项临床研究(BGB-A317-001、BGB-A317-102、BGB-A317-203)的充分验证,均显示400mg、Q6W与200mg、Q3W方案的疗效与安全性相当【6-8】。总的来说6周间隔给药方案在不影响患者用药安全性和有效性的前提下,实现给药间隔延长,有利于提高患者持续治疗的依从性和生活质量,也为临床治疗和长期随访带来了便利,具有极高临床创新价值。
随着对肿瘤生物学特性探索的不断深入,围术期治疗方案的不断更新,我们相信“新辅助+辅助”围术期免疫全程治疗模式将成为主流的围术期治疗模式,而RATIONALE-315研究在此基础上独具匠心的研究设计,成功为Ⅱ/Ⅲ期NSCLC患者提供了一个更符合临床需求以及疗效更优的围术期免疫全程治疗方案,相信这将极大地改善中国早期NSCLC患者的生存获益。
以独特结构优化为基础,引领肺癌领域开拓新纪元
您认为RATIONALE-315研究之所以可以取得如此优异成绩,是否与替雷利珠单抗的结构特点相关?未来您对于替雷利珠单抗的临床探索还有哪些期待?
张鹏教授:免疫检查点抑制剂虽然都作用于PD-1/PD-L1,但不同药物的结构设计也会产生差异,并最终体现为疗效或安全性上的差异。替雷利珠单抗通过对抗体Fc段进行结构优化,减少了与FcγR的结合,消除了抗体依赖细胞介导的吞噬作用(ADCP),显示出较强的抗肿瘤活性;此外,替雷利珠单抗抗体Fab段与PD-1结合位点面大,与PD-1的亲和力更高,解离速率低,能较为持久地阻断PD-1与PD-L1的结合。结构优化为替雷利珠单抗带来独特的药学优势,使更多T细胞被激活和保留,从而发挥强效抗肿瘤作用。替雷利珠单抗能在RATIONALE-315研究中取得优异缓解表现与该药学优势密不可分,同时肺癌领域的多项III期研究中均一致验证了替雷利珠单抗独特的药学优势(图3)带来的卓越疗效及良好的安全性。
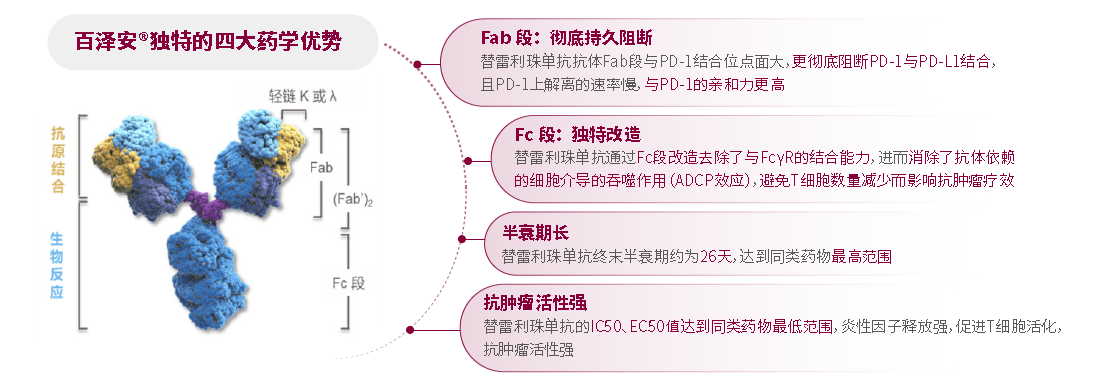 图3 替雷利珠单抗药学特性
图3 替雷利珠单抗药学特性
在肺癌领域,替雷利珠单抗全面布局,五大Ⅲ期研究均取得成功。此前RATIONALE-307、RATIONALE-304、RATIONALE-303三项晚期NSCLC的Ⅲ期研究均获得成功,替雷利珠单抗在晚期NSCLC实现了全线全人群获益、独家适应症及医保全面覆盖,并通过RATIONALE-312研究将获益人群从NSCLC进一步拓展到了SCLC。RATIONALE-315研究的成功更是让替雷利珠单抗成为全球唯一实现肺癌免疫治疗从晚期到早期全人群获益大满贯的PD-(L)1单抗,并让NSCLC围术期免疫治疗的疗效实现了质的飞跃!
就在上个月,欧洲药品管理局(EMA)人用药品委员会(CHMP)批准了替雷利珠单抗治疗食管癌适应症在欧洲上市,替雷利珠单抗作为首个成功出海的PD-(L)1单抗,实现中国实体肿瘤抗癌药出海零的突破。同时,美国食品药品监督管理局(FDA)也已受理了替雷利珠单抗的上市申请。替雷利珠单抗不仅品质获国际认证且价格惠民,患者接受替雷利珠单抗新辅助免疫单次治疗费用不到三千元,完成全程围术期治疗也仅需5万元左右,大大降低了患者用药负担,惠及更多中国患者。
未来,随着检测技术和新型药物的持续发展、创新治疗模式的持续探索,在肺癌领域,我们还将看到更多创新治疗方案进一步延长患者的生存获益。基于替雷利珠单抗独特的结构优化以及在肺癌领域所取得的优异疗效,我相信在更多以PD-(L)1单抗为基础的联合治疗探索中,替雷利珠单抗也将持续“发光发热”,取得更多的循证医学证据,持续拓展免疫治疗边界,为肺癌患者延长更久生存,创造更多治愈可能。期待替雷利珠单抗进一步拓展在肺癌治疗中的应用,并不断登上国际学术舞台,向全世界展示我国原研药物的强大实力!
[1] Dongsheng Yue,et al. LBA58 - Pathological response to neoadjuvant tislelizumab (TIS) plus platinum-doublet (PtDb) chemotherapy (CT) in resectable stage Ⅱ-ⅢA NSCLC patients (pts) in the phase Ⅲ (Ph3) RATIONALE-315 trial. 2023 ESMO.
[2] Shun Lu, Lin Wu, Wei Zhang, et al. Perioperative toripalimab + platinum-doublet chemotherapy vs chemotherapy in resectable stage Ⅱ/Ⅲ non-small cell lung cancer (NSCLC): Interim event-free survival (EFS) analysis of the phase Ⅲ NEOTORCH study. 2023 ASCO Annual Meeting. Abstract #8501.
[3] Forde P M, Spicer J, Lu S, et al. Neoadjuvant nivolumab plus chemotherapy in resectable lung cancer[J]. New England Journal of Medicine, 2022, 386(21): 1973-1985.
[4] Wakelee H A, Liberman M, Kato T, et al. KEYNOTE-671: Randomized, double-blind, phase 3 study of pembrolizumab or placebo plus platinum-based chemotherapy followed by resection and pembrolizumab or placebo for early stage NSCLC[J]. 2023.
[5] John V. Heymach, et al. AEGEAN: A phase 3 trial of neoadjuvant durvalumab + chemotherapy followed by adjuvant durvalumab in patients with resectable NSCLC. 2023 AACR, Abs CT005.
[6]J. Desai, S. Deva, J.S. Lee, et al.
Phase IA/IB study of single-agent tislelizumab, an investigational anti-PD-1 antibody, in solid tumors
J Immunother Cancer, 8 (2020), Article e000453
[7]L. Shen, J. Guo, Q. Zhang, et al.
Tislelizumab in Chinese patients with advanced solid tumors: an open-label, non-comparative, phase 1/2 study
J Immunother Cancer, 8 (2020), Article e000437
[8]Song Y., et al. Treatment of relapsed or refractory classical Hodgkin lymphoma with the anti-PD-1, tislelizumab: results of a phase 2, single-arm, multicenter study.
Leukemia. 2020; 34: 533-542
排版编辑:肿瘤资讯- Olivia











 苏公网安备32059002004080号
苏公网安备32059002004080号


