2019年欧洲肿瘤内科学会亚洲年会(ESMO ASIA)于11月22~24日在新加坡隆重召开。本次大会特别设置了“Challenge Your Expert Session”环节,专家与听众近距离接触,就预设的热点话题与观众面对面地互动交流。在讨论主题为“胃食管癌免疫治疗的现在和未来”的环节,由来自日本的Kei Muro教授担任主席,德国莱比锡大学癌症中心的Florian Lordick教授带来主题演讲,分享胃食管癌免疫治疗的研究进展和未来方向。大会同时展开专家面对面现场互动,为听众解答临床实践中的挑战和疑惑。
主题演讲:胃食管癌免疫治疗的现在和未来

Florian Lordick教授做主题演讲
晚期胃食管癌包括晚期食管癌和胃癌。食管鳞癌的治疗和头颈部鳞癌相似。2014年TCGA胃癌分子分型将胃癌分为4种类型:EBV感染型、MSI型、GS型、CIN型,这4种不同的分子分型对应不同的治疗策略。
食管鳞癌治疗
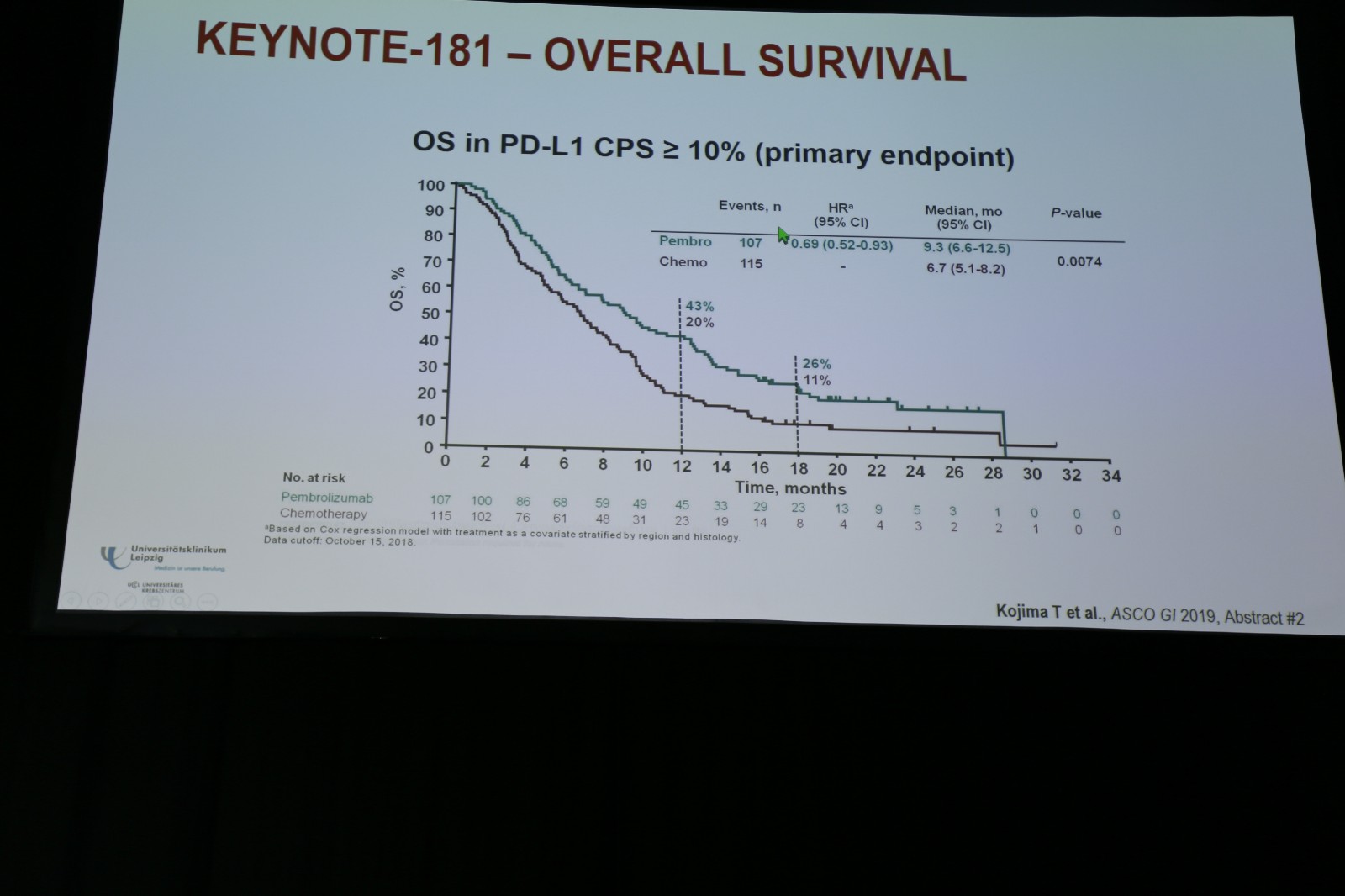
KEYNOTE-181研究入组了一线治疗进展的晚期转移性食管腺癌或鳞癌以及Ⅰ型胃食管结合部(GEJ)腺癌,按1∶1随机接受帕博利珠单抗或研究者选择的化疗。研究达到主要终点,在PD-L1 CPS≥10%的患者中,帕博利珠单抗对比化疗显著延长总生存期(OS),降低了31%的疾病死亡风险(图1)。在食管鳞癌患者中,帕博利珠单抗组的OS也有临床意义上的改善。基于此,2019年7月FDA批准帕博利珠单抗用于PD-L1 CPS≥10%的复发性、局部晚期或转移性食管鳞癌患者的二线或以上治疗。
ATTRACTION-3研究证实,纳武利尤单抗在经治食管鳞癌患者中,较化疗显著改善OS,死亡风险降低23%,OS绝对获益2.5个月(图2)。且纳武利尤单抗组的安全性更好,患者的生活质量得到显著改善。基于这一研究数据,纳武利尤单抗可以作为晚期食管鳞癌的二线治疗新标准。
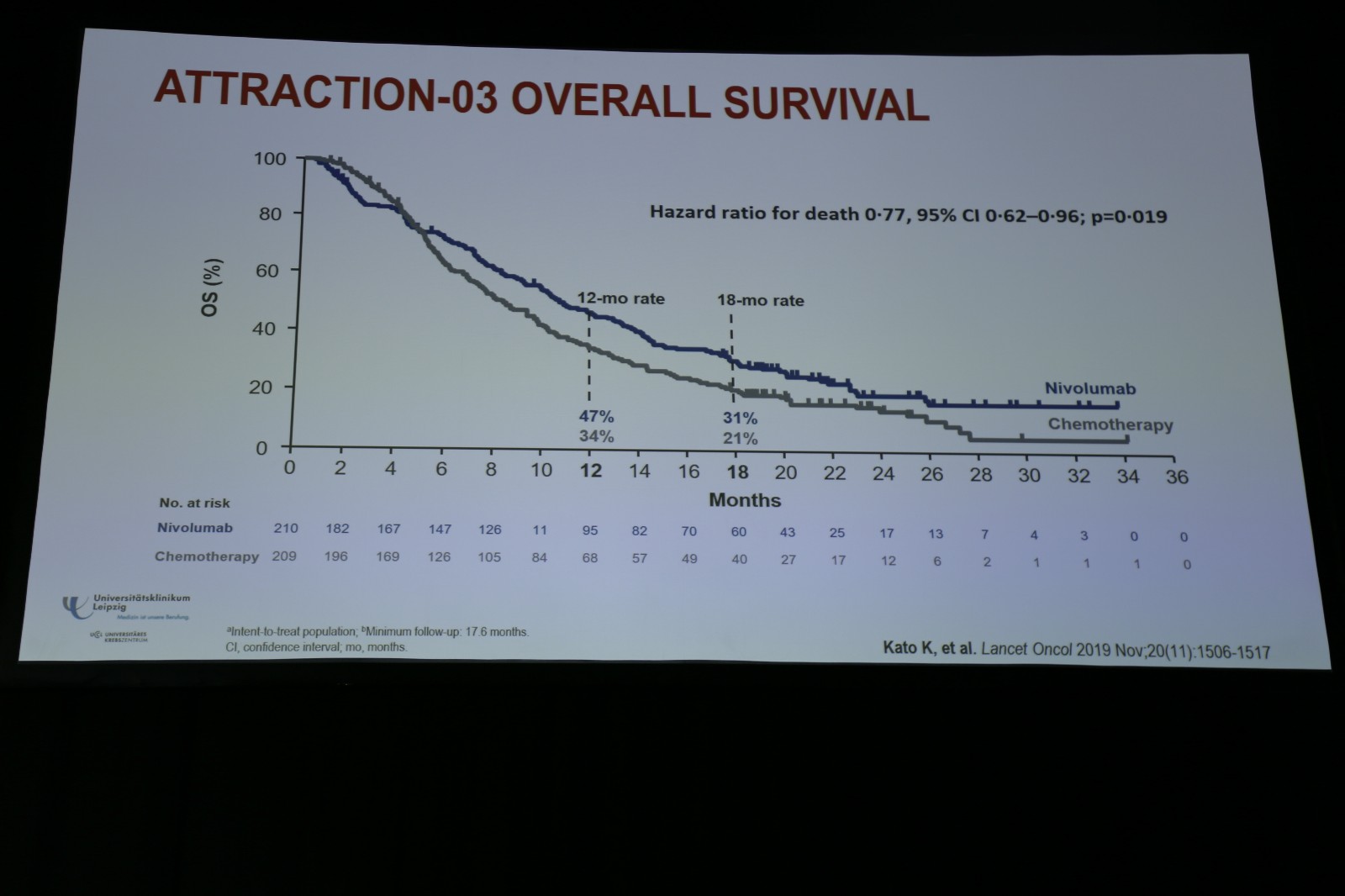
图2. ATTRACTION-03研究OS结果
局部晚期胃癌的治疗
欧洲肿瘤内科学会(ESMO)指南中,对于分期>T1N0的可切除早期胃癌,建议优选新辅助化疗-手术-辅助化疗的模式。微卫星高度不稳定(MSI-H)型胃癌表现为高突变率,个体数据的荟萃分析显示,MSI-H型患者较微卫星稳定(MSS)/微卫星低度不稳定(MSI-L)型患者预后更优,但MSI-H型患者不能从辅助化疗中获益。那么对于这类肿瘤,是否应该规避化疗?对于可切除患者,未来是否应该接受单纯免疫治疗?目前,在局部晚期胃癌中,也开展了多项围术期免疫治疗的研究探索。如EORTC 1707-VESTIGE研究入组了可切除胃癌,患者接受了至少6周铂类和氟尿嘧啶类的新辅助化疗,术后病理为ypN+和/或R1切除,随机分配接受辅助治疗,分别为纳武利尤单抗联合伊匹木单抗治疗1年和术后辅助化疗,主要研究终点为无病生存(DFS)。其他正在进行的围术期研究包括DANTE和KEYNOTE-585。DANTE研究探索围术期Atezolizumab联合FLOT(5-FU+奥沙利铂+多西他赛)治疗;KEYNOTE-585研究探索围术期帕博利珠单抗联合FP(5-FU+顺铂)或FLOT治疗。
晚期胃食管癌一线或维持治疗
ESMO指南中,对于晚期胃癌,主要根据患者的HER2状态分为HER2阳性和HER2阴性型,这两类患者的标准一线治疗分别为化疗联合或不联合曲妥珠单抗。
KEYNOTE-062研究入组了HER2阴性、PD-L1阳性(CPS≥1%)的局部晚期不可切除或转移性胃/胃食管结合部腺癌,按1∶1∶1随机分配,给予帕博利珠单抗单药、帕博利珠单抗联合化疗或单纯化疗。主要研究终点为无进展生存(PFS)和OS。结果显示,在CPS≥1%的晚期胃癌/胃食管结合部癌患者中,帕博利珠单抗对比化疗用于一线治疗,可以取得相似的OS获益;且在CPS≥10%的患者中,帕博利珠单抗组的OS显著优于化疗组(图3)。安全性对比显示帕博利珠单抗的耐受性更优。在帕博利珠单抗基础上联合化疗,获益有限,但安全性可管理。此外,单独分析MSI-H型患者,结果显示帕博利珠单抗组的OS显著优于化疗,无论是在CPS≥1%还是≥10%的患者(图4)。另一项Ⅲ期研究CheckMate-649在晚期胃/胃食管结合部癌中评估了纳武利尤单抗联合伊匹木单抗、纳武利尤单抗联合化疗或单纯化疗,目前研究仍在进行中。
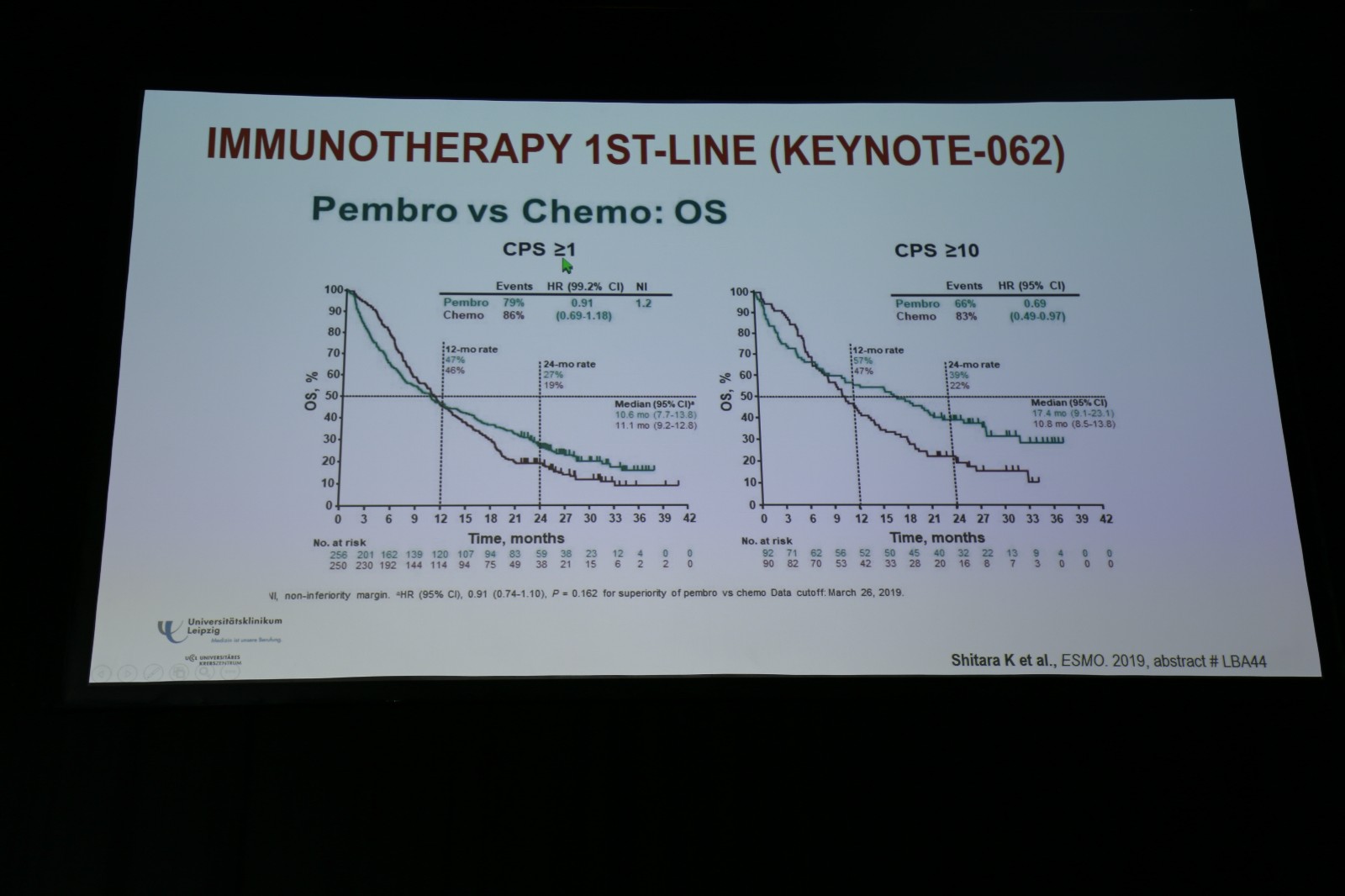
图3. KEYNOTE-062研究帕博利珠单抗对比化疗的OS结果
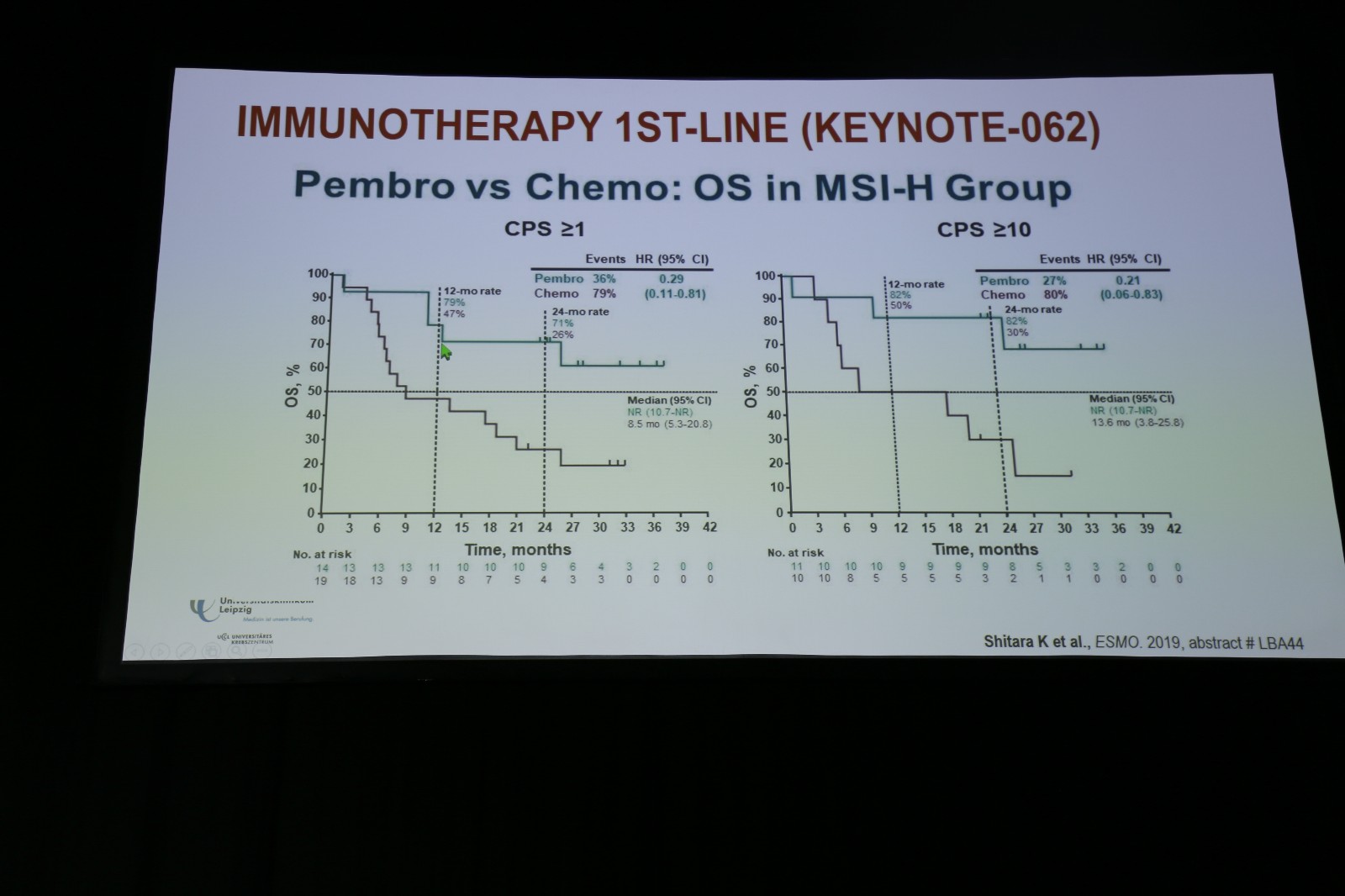
图4. KEYNOTE-062 MSI-H亚组的OS结果
JAVELIN100研究入组了初治不可切除的局部晚期或转移性胃癌/胃食管结合部癌患者,HER2阴性,无论PD-L1表达水平如何。入组患者接受12周的FOLFOX(5-FU+奥沙利铂)或CAPOX(卡培他滨+奥沙利铂)方案一线诱导化疗,未出现疾病进展者按1∶1随机分为2组:第一组继续采用一线化疗维持或最佳支持治疗,第二组接受Avelumab 10mg/kg,q2w治疗直至疾病进展、出现不可耐受的毒性或患者要求出组,主要终点为OS和PFS。然而,研究未达到主要终点,Avelumab维持治疗并不能改善OS和PFS。
对于HER2阳性晚期胃癌/胃食管结合部患者的一线治疗,也开展了一些研究探索。一项Ⅱ期研究在HER2阳性(IHC3+或FISH+)晚期胃食管癌患者中探索了帕博利珠单抗+曲妥珠单抗联合化疗。患者首先接受1个周期的曲妥珠单抗8mg/kg联合帕博利珠单抗200mg诱导治疗,之后再接受卡培他滨+奥沙利铂联合曲妥珠单抗和帕博利珠单抗治疗。主要终点为6个月的PFS率。在可评估疗效的32例患者中,28例(87%)取得疾病缓解,其中完全缓解(CR)和部分缓解(PR)患者分别为3例(9%)和25例(71%),疾病控制率达到100%;中位PFS为11.4个月(图5)。基于上述研究的数据,一些大型Ⅲ期研究也正在开展中,如KEYNOTE-811研究在HER2阳性胃癌患者中评估帕博利珠单抗+曲妥珠单抗联合化疗对比曲妥珠单抗联合化疗,计划入组732例患者。另一项探索性研究INTEGA计划在HER2阳性胃癌患者中探索去化疗方案,即采用纳武利尤单抗+伊匹木单抗+曲妥珠单抗治疗。
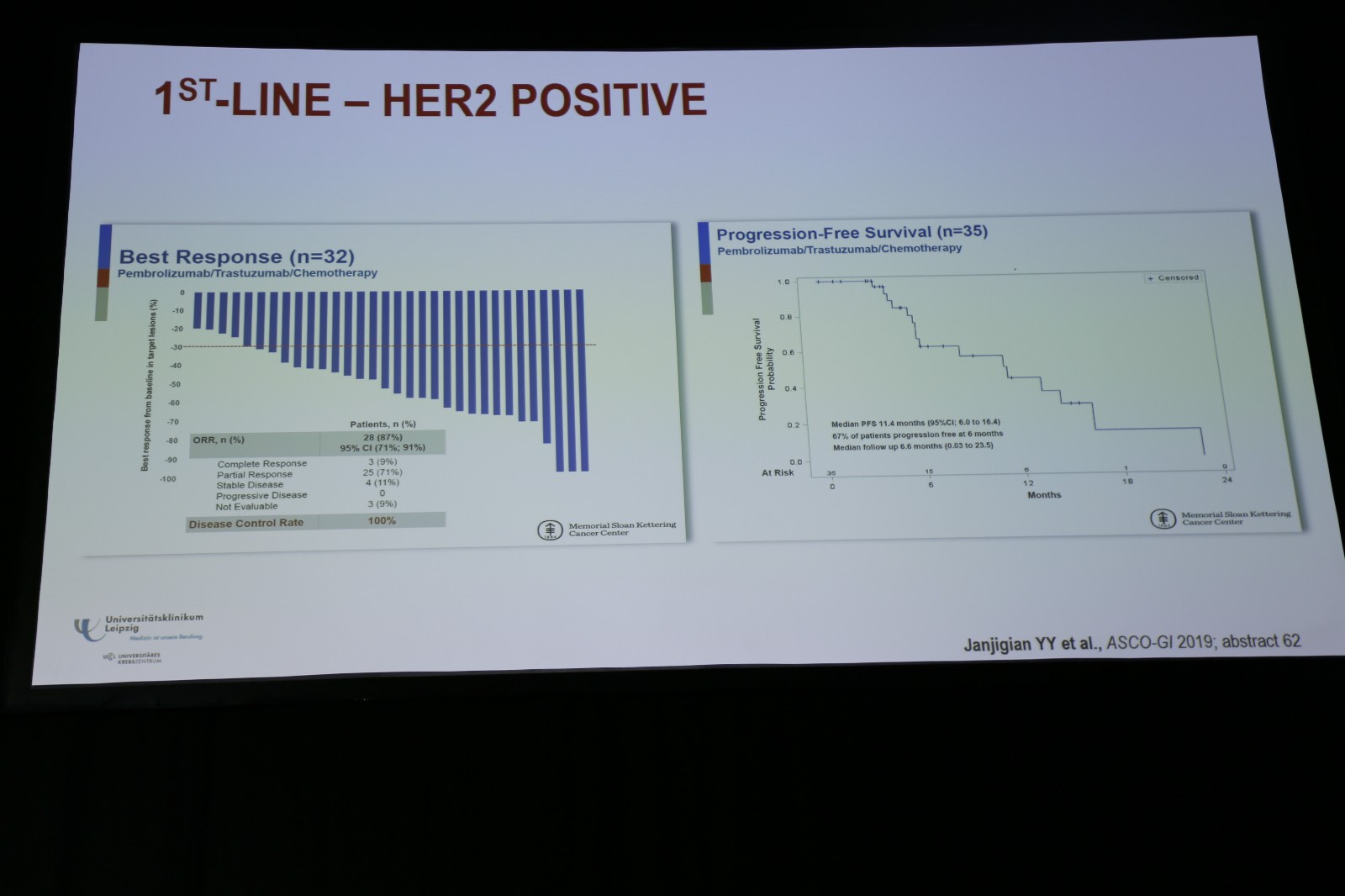
图5. 帕博利珠单抗+曲妥珠单抗联合化疗用于HER2阳性晚期胃食管癌患者的Ⅱ期研究结果
晚期胃食管癌二线治疗
ESMO指南中,对于晚期胃癌的二线治疗,推荐根据患者的ECOG PS状态评分选择不同的治疗方案。PS评分0~1分的患者可以考虑紫杉醇联合雷莫芦单抗;PS评分0~2分的患者可以考虑雷莫芦单抗单药或伊立替抗单药或紫杉醇单药;PS 2~4分的患者则以最佳支持治疗为主。
KEYNOTE-061研究在既往接受过铂类和氟尿嘧啶类方案一线治疗进展的局部晚期或转移性胃或胃食管结合部腺癌患者中对比了帕博利珠单抗和紫杉醇单药化疗,主要终点为CPS≥1%分患者的OS和PFS。结果显示,帕博利珠单抗较紫杉醇单药化疗组延长了不到1个月的OS(9.1 个月对比8.3 个月,HR 0.82,P =0.042),但帕博利珠单抗组的安全性更好。亚组分析显示,在PD-L1 CPS≥10%的患者中,帕博利珠单抗较紫杉醇观察到OS获益的趋势。探索性分析发现,在MSI-H型患者中,帕博利珠单抗组的OS明显优于紫杉醇组。
晚期胃食管癌三线治疗
ATTRACTION-02研究入组了既往接受过二线或以上治疗的患者,按2∶1随机分配接受纳武利尤单抗和安慰剂治疗,结果显示,纳武利尤单抗较安慰剂显著延长OS,由此奠定了纳武利尤单抗的三线治疗地位。
创新性的免疫联合研究
在胃癌/胃食管结合部癌领域,PD-1/PD-L1单抗还开展了多项联合治疗的探索。如Ⅱ期FRACTION研究评估了5种不同联合方案,纳武利尤单抗+relatimab,纳武利尤单抗+BMS-986205,纳武利尤单抗+rucaparib,伊匹木单抗+rucaparib,纳武利尤单抗+伊匹木单抗+rucaparib,对比纳武利尤单抗+伊匹木单抗用于胃癌/胃食管结合部癌患者一线或以上治疗。Ⅰ/Ⅱ期MORPHEUS研究在一线治疗中评估不同的Atezolizumab联合方案,包括Atezolizumab + cobimetinib + mFOLFOX6 (5-FU + 奥沙利铂)、Atezolizumab + mFOLFOX6 → Atezolizumab + cobimetinib,以及Atezolizumab + mFOLFOX6,以mFOLFOX6方案为对照。Ⅱ期LEAP-005研究和NCT03609359分别在胃癌二线或以上治疗和一线/二线治疗中探索帕博利珠单抗联合仑伐替尼治疗(图6)。
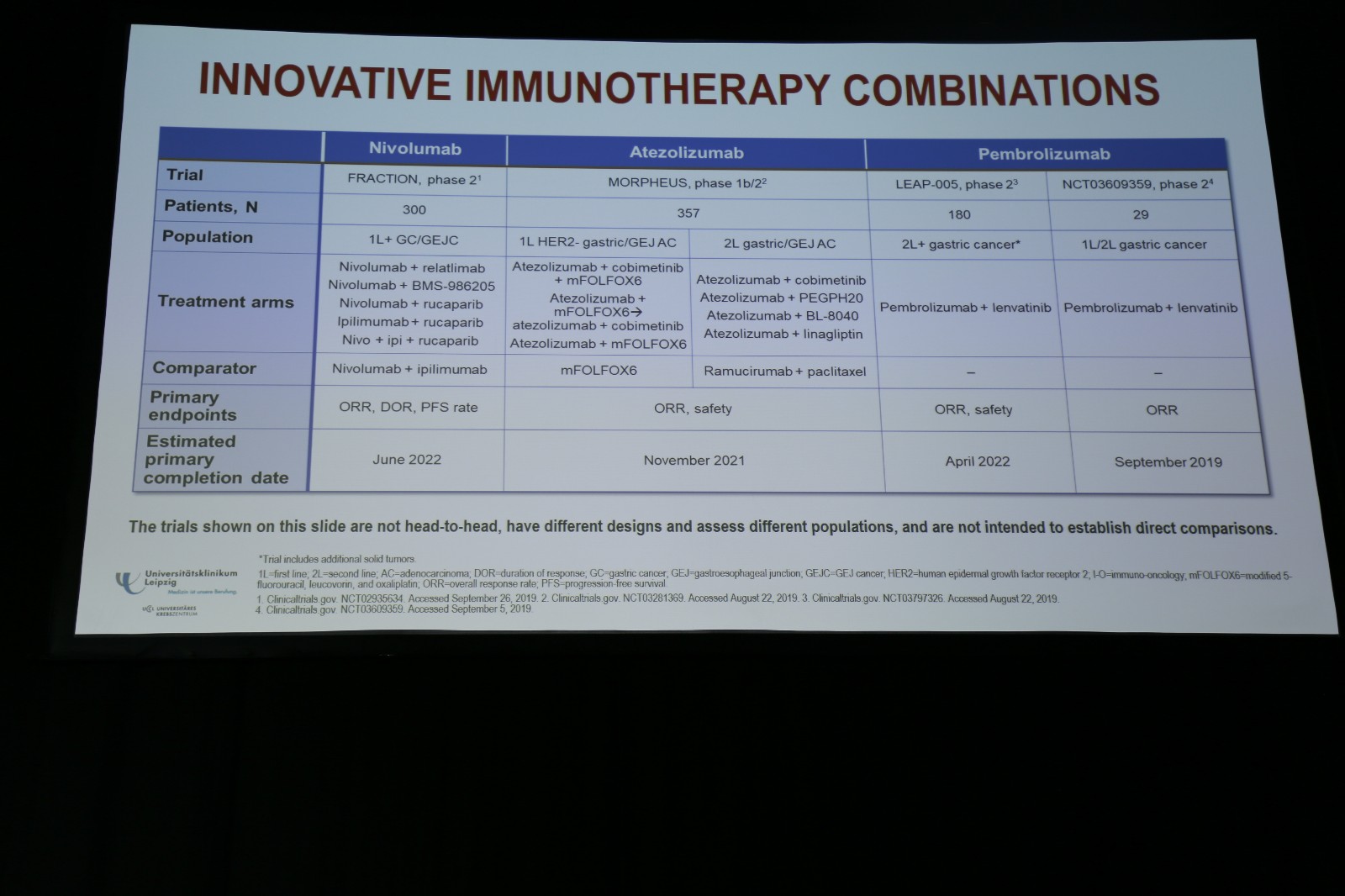
图6. 创新性的免疫联合研究
胃食管癌免疫治疗的疗效预测标志物
2014年TCGA胃癌分子分型将胃癌分为4种类型:EBV感染型、MSI型、GS型、CIN型,这四种不同的分子分型对应不同的治疗策略。其中EBV感染型患者,表现为PIK3CA高突变、PD-L1/2过表达以及免疫细胞浸润。研究发现,MSI-H型、EBV阳性和/或PD-L1阳性患者接受免疫治疗的疗效更优,可能是免疫治疗潜在的疗效预测标志物。
观众提问:与黑色素瘤或肺癌等肿瘤相比,胃癌的免疫治疗疗效相对欠佳,其可能的原因是什么?
Florian Lordick教授:一方面可能是因为胃癌表现为免疫抑制性,即所谓的“冷”肿瘤;另一方面,胃癌是一类异质性很大的肿瘤,尤其是瘤内异质性。
观众提问:胃癌免疫治疗的潜在的标志物包括EBV感染、TMB、MSI-H,PD-L1表达等,您如何看待PD-L1表达对免疫治疗疗效的预测作用?
Florian Lordick教授:PD-L1表达在胃癌中并不是一个非常好的预测标志物。因为胃癌是一个瘤内异质性很大的肿瘤,小的活检组织并不能反映肿瘤的全貌。因此,在胃癌中,PD-L1 CPS评分并不是一个很好的预测标志物。
观众提问:KEYNOTE-062研究中,在PD-L1 CPS≥1和CPS≥10的晚期胃/胃食管结合部癌患者中,帕博利珠单抗联合化疗对比单纯化疗,并未取得显著更优的OS;但在CPS≥1的晚期胃/胃食管结合部癌患者中,帕博利珠单抗单药对比化疗用于一线治疗,可以取得相似的OS的获益。在您的临床实践中,是否会考虑选择帕博利珠单抗作为一线治疗?
Florian Lordick教授:毫无疑问,帕博利珠单抗是一个非常好的药物,在多个瘤种中都观察到不错的疗效。临床上,对于需要快速缓解症状的患者,可能会考虑选择化疗,但是对于一些一般状态较好,且PD-L1 CPS评分较高的患者,可以考虑接受帕博利珠单抗一线治疗。需要注意的是,这类患者并不是特别多,仅占15%左右。
观众提问:在胃癌领域,免疫治疗联合化疗的疗效一般,您如何看待免疫联合治疗的前景?
Florian Lordick教授:从今年公布的研究数据来看,免疫联合化疗的效果的确不够理想,我们需要思考两者联合的作用机理,以及考虑联合不同的化疗方案。但是不要灰心,明年会有更多结果公布,如免疫+免疫,值得期待。
免疫治疗的进展突飞猛进,在胃食管癌中的研究已经从后线推进到一线,乃至局部晚期的围手术期治疗;在用药方案上,也在从单药向联合治疗探索。免疫治疗的安全性好,疗效持续时间长,随着免疫治疗基础和临床研究的深入,分子生物标志物的发现,优势人群的筛选,相信这一疗法将为更广大的胃食管癌人群提供新的选择。











 苏公网安备32059002004080号
苏公网安备32059002004080号


