
第67例
HER2阳性乳腺癌的生长高度依赖HER2蛋白,在靶向治疗未问世之前,这类乳腺癌进展快、易复发转移且预后不良。自1998年曲妥珠单抗问世以来,针对抗HER2治疗的研究进展不断,20年来靶向治疗取得了显著成绩。目前,以曲妥珠单抗为基础的抗HER2治疗已经彻底改变了这类乳腺癌患者的疾病进程,在晚期乳腺癌治疗阶段,坚持持续抗HER2治疗,有望为患者带来长期生存。

广州中医药大学第一附属医院乳腺科主任、学科带头人、医学博士
广东省中西医结合学会乳腺病专业委员会主任委员
中华中医药学会乳腺病防治协会委员
从事乳腺专科临床工作20余年,擅长开展各种类型的乳腺手术,尤其是乳腺微创手术及整形手术。在中西医结合治疗乳腺肿瘤性疾病、乳腺增生性疾病、炎症性疾病方面积累了丰富的经验。中医理论根基深厚,拜四川省名中医刘方柏为师,对运用中医经典防治乳腺疾病方面有独到的体会。
主持多项省部级课题。

广州中医药大学第一附属医院 乳腺科
毕业于广州中医药大学,研究方向中医外科乳腺疾病。
师从广州中医药大学第一附属医院乳腺科黄梅教授,发表多项学术论文及实用新型发明专利,参与广中医一附2019年创新强院二期工程之临床专项研究。
参加多个学术交流,擅长中西医结合治疗乳腺肿瘤,急性乳腺炎,肉芽肿性乳腺炎,乳腺增生等常见乳腺疾病及中医特色疗法在乳腺癌全程管理中的运用并擅长多种乳腺手术。在中医治疗乳癖、乳核、乳痈疾病方面培养了一定的中医独特思维。
基本情况
患者女性,41岁,未绝经,发现右乳肿块3个月就诊。既往史、家族史无特殊。
既往手术及辅助治疗
2010年1月29日入院,专科检查:右乳上方可触及一大小约4cm×3cm肿物,质地硬,边界欠清,活动度差,与皮肤基底无黏连,右腋下可触及1cm×2cm肿大淋巴结,质地硬,边界尚清,活动度差。乳腺彩超示:右乳12点异常回声,大小约25mm×23mm,边界尚清,形态不规则,呈分叶状,其内血流信号丰富,右腋下见淋巴结回声,大小约12mm×10mm,纵横比失常。左乳未见明显异常。右乳CA待排。肝胆、子宫、胸部CT、心脏彩超、相关抗原等血液学检查均未见明显异常。
2010年2月1日,患者行右乳癌改良根治术,术后病理:①右侧乳房浸润性导管癌,III级,癌肿大小约3cm×2.5cm×2.5cm;②根治术标本底切缘、侧切缘、乳头均未见癌浸润;③癌组织内及癌周围未见脉管内癌栓;④第1站淋巴结未见癌转移(0/15),第2站淋巴结未见癌转移(0/4),第3站淋巴结未见癌转移(0/6);⑤免疫组化检测:ER(-),PR(-),HER2(3+)-约50%细胞强阳性,Ki-67(+++,约40%细胞强阳性)。
2010年2月9日—5月25日,行TEC方案化疗6次 (T,多西他赛75mg/m2,d1,q21d;E,表柔比星50mg/m2,d1,q21d;C,环磷酰胺500 mg/m2 d1,q21d)。因个人经济原因未行靶向治疗。
第一次进展
2012年2月13日,右乳癌术后2年余,定期复查发现左乳肿物。专科检查:右乳缺如,右胸壁见一长约15cm的伤口,伤口愈合良好。左乳内上象限腺体边缘可触及一大小约3cm×3cm肿块,质韧,边界尚清,活动度一般,与皮肤基底无粘连。左腋下可触及一大小约2cm×1cm肿大淋巴结,质韧,边界不清楚,活动度差。乳腺彩超示:左乳内上象限异常回声,大小约33mm×25mm,边界尚清,形态不规则,呈分叶状,其内血流信号丰富,左腋下见淋巴结回声,大小约10mm×15mm,内未见明显皮髓质。左乳癌待排。其他检查:肝胆、子宫、心脏、胸部CT、颅脑MR、血液学癌标未见明显异常。
2012年2月16日行左乳癌改良根治术,术后病理:①“左乳”浸润性导管癌III级;②根治标本底切缘、侧切缘、皮肤及乳头均未见癌浸润;③Ⅰ、Ⅱ、Ⅲ站淋巴结均可见癌转移(13/21,3/6,1/2);最大淋巴结约直径1.5cm,癌组织浸润整个淋巴结;④免疫组化标记:ER(-),PR(-),HER2(3+)约100%细胞强阳性,Ki-67(+++)约70%细胞强阳性,P53(+++)约80%细胞强阳性,E-ca(+++)约100%细胞强阳性。结合2013版乳腺肿瘤学双侧原发乳腺癌和对侧转移性乳腺癌的鉴别要点,患者肿瘤位于近中线对侧乳腺周围,双乳病理组织类型完全相同且癌组织分化一致,双侧乳腺癌未找到原位癌成分,考虑左侧乳腺癌为对侧转移。
患者于2012年2月13日开始TXH方案治疗(多西他赛6个周期,卡培他滨8个周期联合曲妥珠单抗治疗1年),同时接受放疗。2013年3月开始停用曲妥珠单抗治疗,定期复查未见复发转移征象,综合疗效评价为CR。
第二次进展
2014年5月底,患者发现“左胸壁结节”。专科检查:双乳术后缺如,双侧胸壁分别见一长约15cm的疤痕,左胸壁近约第4肋间胸骨处可及一结节,大小约1cmx1cm,边界欠清,活动度差,质硬。乳腺彩超:双乳癌术后,前正中线稍偏左侧胸壁后方见低回声区,范围约10mm×8mm,边界欠清,内回声不均匀。胸壁低回声性质待定。胸部CT、ECT、颅脑MR等未见明显异常。2014年6月12日,行左胸壁结节切除术,术后病理示:①符合“左乳房”浸润性导管癌,Ⅲ级,胸壁复发,并见脉管内癌栓;②“底切缘、上、下切缘”均未见癌浸润;③癌组织免疫组化标记:ER(-)、PR(-)、HER2(+++),约90%细胞强阳性。继续给予曲妥珠单抗治疗联合吉西他滨化疗8个周期。2014年6月10日—2018年4月,给予曲妥珠单抗靶向治疗维持,期间考虑病情稳定间断停药共6个月,综合疗效评价评估CR。
第三次进展
2018年5月6日,复查胸部CT示:双肺外带新增多发结节,长径3-11mm不等,转移瘤待排(图1)。颅脑MR、ECT未见癌转移。评价为PD,未行穿刺活检,继续曲妥珠单抗治疗。
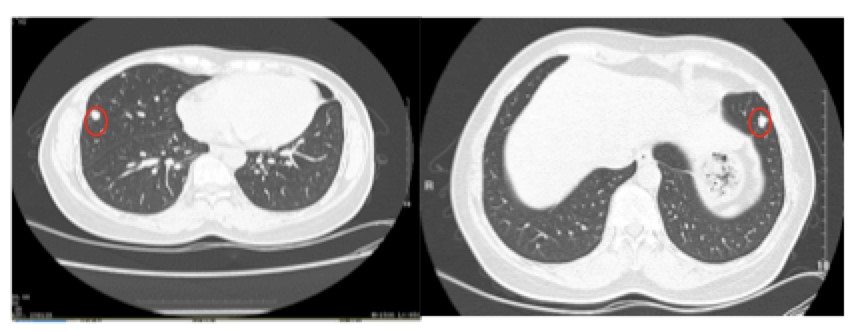
图1 第三次进展,发现肺部转移瘤
2018年8月27日,复查胸部CT(图2)示:双肺多发结节普遍较前轻度增大,如右肺中叶外侧段结节长径约12mm(原约10mm),评价为SD,继续曲妥珠单抗治疗。

图2. 给予曲妥珠单抗治疗后,肺部转移瘤维持稳定
第四次进展
2018年11月22日,胸部CT(图3):发现双肺多发结节普遍较前轻度增大,新增结节,如右肺中叶外侧段结节长径约15mm(原约12mm),评价为PD,给予曲妥珠单抗联合卡培他滨(1500 mg bid po)治疗。
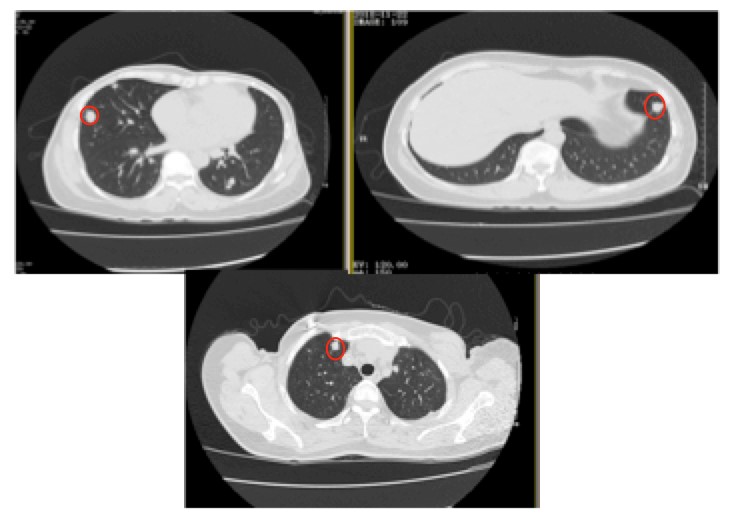
图3. 第四次进展,新发肺部转移瘤
2019年4月6日复查胸部CT示:双肺多发结节大小较前似变化不大,轻度强化;双肺转移瘤,较前变化不大(图4)。继续给予HX方案治疗。患者目前仍继续接受曲妥珠单抗治疗,维持单药卡培他滨治疗,定期复查随访(表1)。
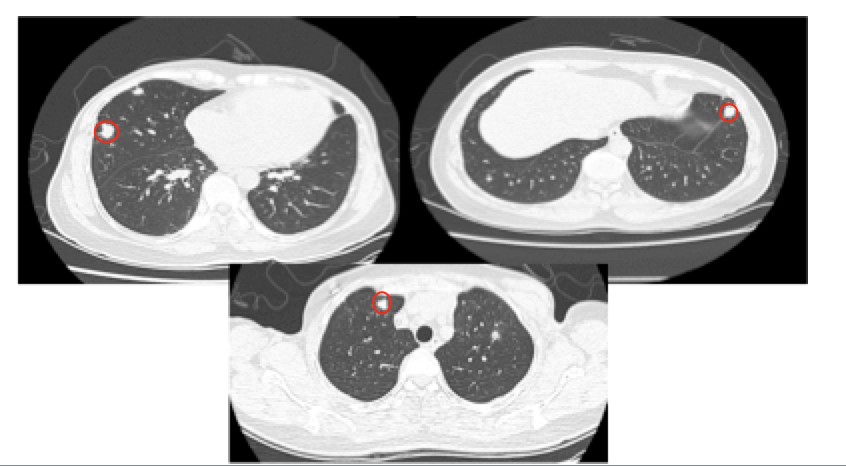
图4. 给予曲妥珠单抗联合卡培他滨治疗后,肺部转移瘤维持稳定
表1 患者定期复查随诊对比

点评专家

江苏省肿瘤医院肿瘤内科病区主任
中国抗癌协会乳腺癌专业委员会委员
江苏省肿瘤防治联盟乳腺癌专家委员会委员
江苏省医学会肿瘤化疗与生物治疗分会乳腺癌学组副组长
从事肿瘤内科临床、科研及教学工作30余年擅长乳腺癌的内科治疗
点评
该患者右乳HER2阳性癌(T2N0M0)术后,因经济原因未行规范的抗HER2辅助治疗,对疗效有不利影响;两年后出现左乳腺癌,虽然双乳病理类型及免疫组化一致,且未找到原位癌成分,但左乳癌术前检查未发现左乳及左腋窝以外部位的转移,且双侧乳癌的间隔时间已有2年,因此左乳癌为原发或转移癌均有可能。当时未发现左乳及左腋窝以外部位的转移,行手术治疗为合理治疗。另外,该患者接受左乳癌手术切除以及左胸壁结节切除后,不宜使用CR来评估疗效,而是应观察其DFS或者PFS。
患者从早期乳腺癌发展为复发转移性乳腺癌,期间接受了多次手术、化疗和靶向治疗。尤其是在患者发展为晚期疾病以后,坚持使用抗HER2靶向治疗,给患者带来了很大的获益。结合此病例,对于HER2阳性乳腺癌的患者,在晚期疾病治疗过程中应注意以下关键环节:
1. 以曲妥珠单抗为基础联合化疗的方案是HER2阳性晚期乳腺癌一线治疗标准方案
《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南(2019)》中推荐,对于既往未接受过曲妥珠单抗辅助治疗的HER2 阳性复发转移乳腺癌,以曲妥珠单抗为基础联合化疗的方案是这部分患者晚期一线治疗标准方案。HERMINE研究[1]对HER2阳性晚期乳腺癌的分析显示,越早使用曲妥珠单抗(即一线使用),患者的临床获益越大。在ABC4指南中也明确提出,所有HER2阳性晚期乳腺癌患者应尽早开始使用抗HER-2治疗。以曲妥珠单抗单靶治疗的基础上,CLEOPATRA研究[2]进一步评估了曲妥珠单抗联合帕妥珠单抗的双靶方案,结果显示,与单靶向相比,双靶向联合化疗总生存提高了15.7个月,达到56.5个月;且帕妥珠单抗不增加心脏事件发生率,妥妥双靶方案的心脏安全性良好,可以显著改善患者生活质量。2019年ASCO大会上公布了CLEOPATRA III期研究随访8年的OS结果(中位随访99个月),显示妥妥双靶方案对比单靶方案,显著延长了16.3个月的OS(中位OS:57.1个月 vs 40.8个月),死亡风险显著降低31%(HR=0.69,95%CI: 0.58-0.82,P<0.0001)[3]。研究中仅1例患者发生了心衰事件。此外,在2019年ASCO大会上,还公布了在中国进行的桥接试验——PUFFIN研究[4],再次验证妥妥双靶在中国患者的疗效与安全性。妥妥双靶方案对比单靶方案,患者的ORR分别为79% vs 69.1%;中位PFS分别为14.5个月 vs 12.4个月,降低了31%复发风险。目前,NCCN指南,ABC4指南以及CSCO乳腺癌诊疗指南,均推荐帕妥珠单抗+曲妥珠单抗+紫杉作为HER2阳性晚期乳腺癌一线治疗方案,在NCCN指南中更是将这一方案作为一线治疗优选方案。
鉴于目前帕妥珠单抗在中国尚未获批晚期一线治疗适应证,因此,患者可以选择曲妥珠单抗为基础的一线治疗。CHAT研究[5]证实,HTX可以作为HER2阳性晚期乳腺癌可选择的一线治疗方案,可以用于能够耐受双药化疗,尤其适用于考虑维持治疗。这例患者在一线治疗上选择了HTX方案治疗,然而,患者仅接受了1年曲妥珠单抗治疗就停药,这并不符合指南规定。目前,国际国内各项指南均推荐,曲妥珠单抗晚期一线治疗应该用药至疾病进展。这例患者可能因为经济原因或用药依从性问题,未坚持使用曲妥珠单抗治疗,这也是导致患者后续出现疾病进展的原因。
2. 二线治疗曲妥珠单抗也是合理选择
目前,国际指南推荐,对于HER2阳性乳腺癌二线治疗,推荐使用T-DM1;而T-DM1尚未在中国上市。因此,CSCO指南推荐,抗HER2二线治疗可以考虑继续选择曲妥珠单抗或其他靶向治疗。HERMINE研究是评估曲妥珠单抗持续治疗关键研究,结果显示,相比于中断治疗,一线治疗进展后继续曲妥珠单抗可显著延长OS,中位OS延长16.7个月。EGF 104900研究[6]证实,在曲妥珠单抗治疗进展后,继续使用曲妥珠单抗+拉帕替尼双靶治疗较单拉帕替尼能显著提高PFS及OS。上述这例患者在一线曲妥珠单抗治疗进展后,二线及后续治疗继续使用曲妥珠为基础的治疗,取得了较好的疗效,这一治疗策略值得肯定。尤其是在第四次进展后,采用了曲妥珠单抗联合卡培他滨的方案,口服的化疗药物卡培他滨,单药治疗有效、相对低毒、便于长期使用,是维持化疗的理想选择。患者目前仍继续接受曲妥珠单抗联合卡培他滨治疗,且观察到临床获益,且耐受性好,推荐坚持使用,以期获得较好生存。
[1]Extra JM, Antoine EC, Vincent-Salomon A, Delozier T, Kerbrat P, Bethune-Volters A, et al. Efficacy of trastuzumab in routine clinical practice and after progression for metastatic breast cancer patients: the observational Hermine study. Oncologist 2010;15(8):799-809.
[2]Swain SM, Baselga J, Kim SB, Ro J, Semiglazov V, Campone M, et al. Pertuzumab, trastuzumab, and docetaxel in HER2-positive metastatic breast cancer. N Engl J Med 2015;372(8):724-34.
[3]End-of-study analysis from the phase III, randomized, double-blind, placebo (Pla)-controlled CLEOPATRA study of first-line (1L) pertuzumab (P), trastuzumab (H), and docetaxel (D) in patients (pts) with HER2-positive metastatic breast cancer (MBC). 2019 ASCO,abs1020.
[4]A phase III, randomized, double-blind, placebo (Pla)-controlled study of pertuzumab (P) + trastuzumab (H) + docetaxel (D) versus Pla + H+ D in previously untreated HER2-positive locally recurrent/metastatic breast cancer (LR/MBC) (PUFFIN). 2019 ASCO,abs1026.
[5]Wardley Andrew M,Pivot Xavier,Morales-Vasquez Flavia et al. Randomized phase II trial of first-line trastuzumab plus docetaxel and capecitabine compared with trastuzumab plus docetaxel in HER2-positive metastatic breast cancer.[J] .J. Clin. Oncol., 2010, 28: 976-83.
[6]Blackwell KL, Burstein HJ, Storniolo AM, Rugo HS, Sledge G, Aktan G, et al. Overall survival benefit with lapatinib in combination with trastuzumab for patients with human epidermal growth factor receptor 2-positive metastatic breast cancer: final results from the EGF104900 Study. J Clin Oncol 2012;30(21













 苏公网安备32059002004080号
苏公网安备32059002004080号


