
本篇为龙哥查房病历3的后续讨论
地点:广东省人民医院伟伦楼十四楼
时间:2017-10-11 星期三 15:00
专家:
吴一龙(教授、主任医师、博导)、张绪超(研究员、硕导)、杨衿记(主任医师、博导)、杨学宁(主任医师)、钟文昭(主任医师、博导)、周清(主任医师、博导)、马东(主任医师)、涂海燕(副主任医师)、陈晓明(主任医师、硕导)、李伟雄(主任医师)、潘燚(副主任医师)、陈华军(副主任医师)、汪斌超(副主任医师)、王震(副主任医师)、陈观娣(副主任医师)、徐崇锐(主治医师)、廖日强(主治医师)、董嵩(主治医师)、江本元(医师)、白晓燕(医师)、孙月丽(医师)、陈志勇(医师)、李安娜(医师)、郑明英(医师)、林嘉欣(医师)、白晓燕(医师)、林辉(医师)、黄婕(医师);全体在读研究生。
病例汇报人:广东省人民医院肺一科 胥冰菲医生
患者病史
MKM,女,56岁,PS 1分;非吸烟者,无肿瘤家族史
主诉:确诊卵巢癌2年余,肺部结节进行性增大1年
现病史:
1. 2015-7-17因“卵巢肿物”于深圳市宝安区人民医院行全子宫+双附件+大网膜+阑尾切除+盆腔淋巴结清扫术,术后诊断卵巢粘液性腺癌IIIC期。
2. 2015-7-31至2015-11-19于中山大学附属第三医院行6周期泰素+卡铂方案化疗。化疗前行胸部CT提示肺部多发结节,无特殊治疗;化疗期间及化疗后定期复查,提示肺部结节稳定(未见复查CT片,具体不详)。
3. 2016-6患者无明显诱因出现刺激性干咳,体重下降6公斤,胸部CT提示右肺中叶病灶较前增大,未行进一步诊治。2015-10至2017-8复查CT片详见图1、图2。
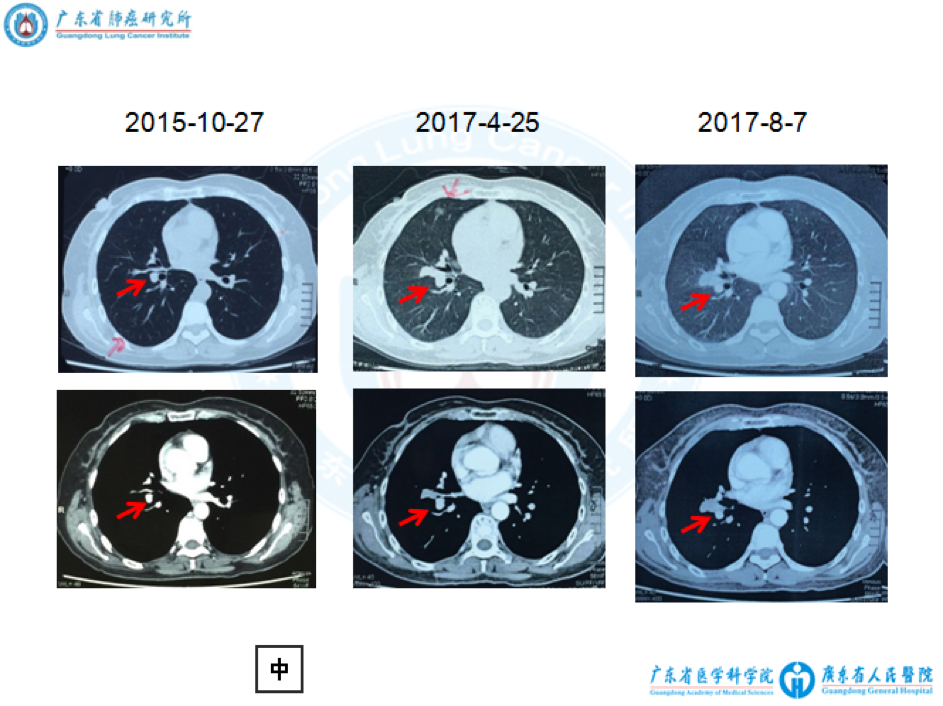
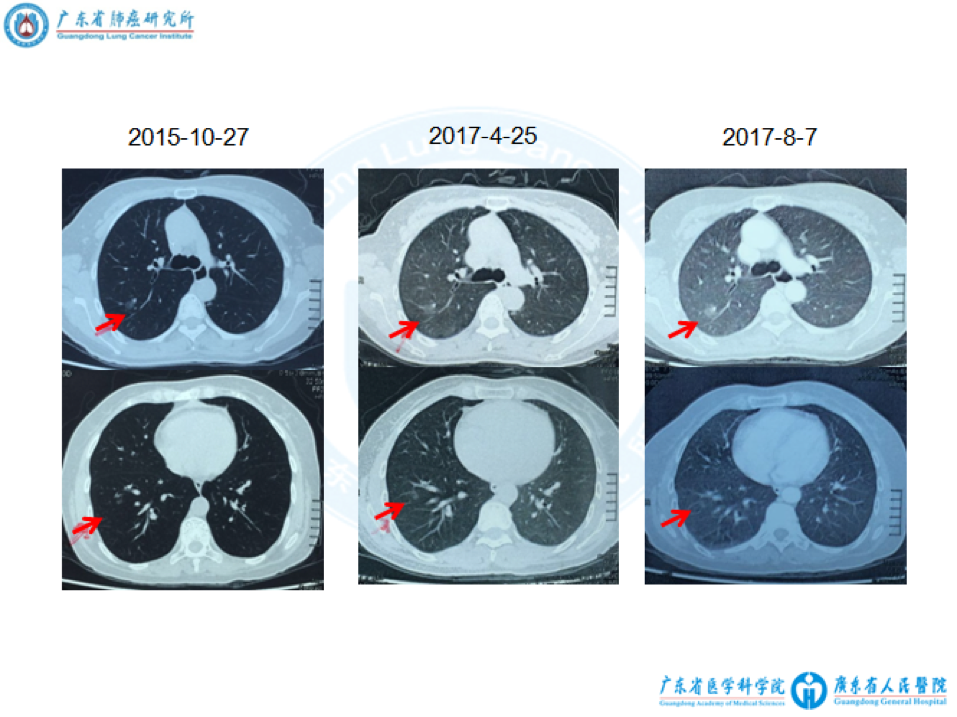
4. 2017-8-21复查PET/CT提示:盆腔直肠右侧软组织结节,代谢活跃,SUVmax=9.7,大小21*12mm,考虑肿瘤复发;右肺中叶软组织影,代谢活跃,SUVmax=10.9,大小约26*17mm,纵隔、右侧腋窝及右肺门见数个肿大淋巴结影,代谢活跃;双肺数个磨玻璃样小结节,代谢未见异常,右肺上叶结节较前增大(详见下图)。
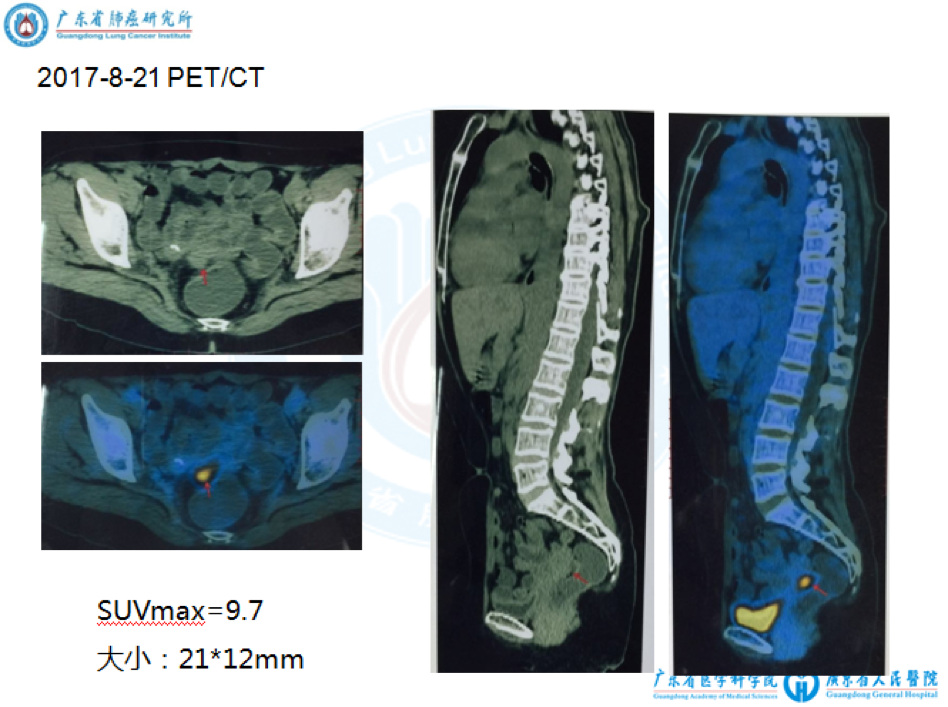
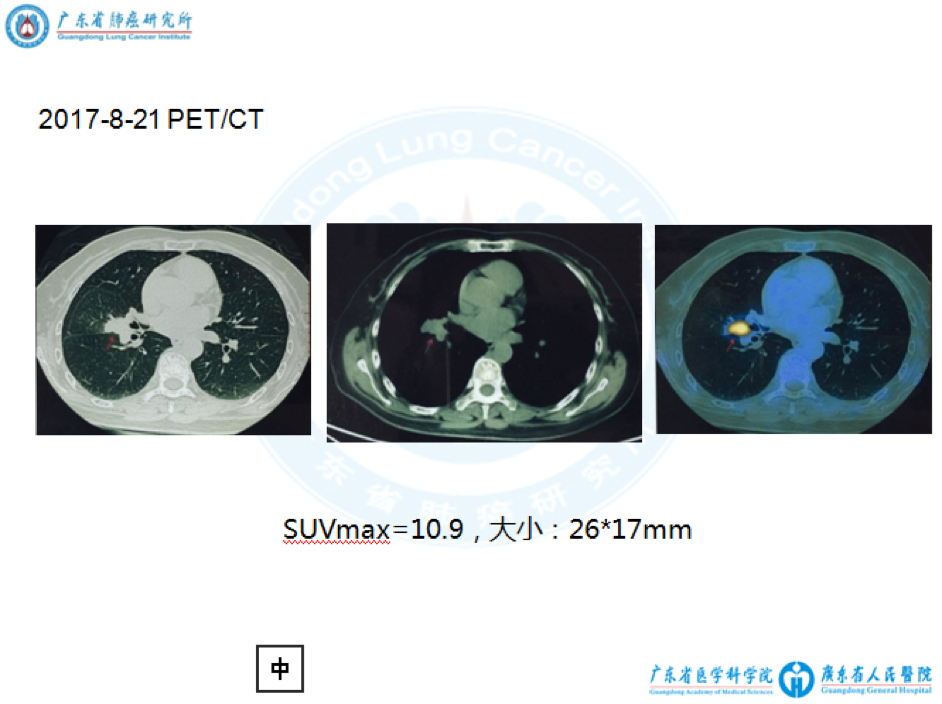
5. 支气管镜病理活检:少许肺及支气管粘膜组织,上皮未见增生,间质少量炎性细胞浸润,未见特征性病变。
6. 外周血EGFR基因检测:未见突变。
7. 妇产科会诊意见:目前该病人暂无手术指征,可行化疗。
入院诊断:
(1)卵巢恶性肿瘤术后(右侧卵巢粘液性腺癌Ⅲc期)局部复发
(2)肺肿物(右中肺肿瘤:原发?转移?)
原发:右中肺肺癌cT1cN2M0,IIIA3期?
转移:卵巢癌术后2年局部复发及右中肺、纵隔淋巴结转移?
病史小结
• 中年女性,非吸烟者,PS评分1分;
• 卵巢粘液腺癌根治术后,术后行6周期泰素+卡铂辅助化疗,2017-8复查PET/CT提示肿瘤复发,DFS=2年;
• 肺部结节影,化疗期间及化疗后病灶维持稳定;2016-8复查胸部CT提示右肺病灶增大,未行进一步诊治;
讨论要点
诊疗小组内的诊断及治疗意见:
1.卵巢癌肺转移可能性大,建议按妇科肿瘤复发治疗。
2.不能完全排除原发肺癌,是否考虑外科干预确认。
MDT讨论回顾
2017年9月20日,进行第一次MDT讨论:讨论要点为明确诊断及制定下一步诊疗方案。
第一次MDT讨论意见:通过病理活检,判断是肺内肿物原发或转移病灶,可以先做EBUS,无法明确诊断时再考虑纵隔镜取活检。如果是原发肺癌,需要明确病理分期,按照肺癌诊疗规范进行治疗;另外可考虑结合妇科意见、是否需要行卵巢复发肿瘤的减瘤手术。如果是转移性病灶,卵巢复发肿瘤的减瘤手术意义不大,需要转至妇科进行化疗。
2017年10月11日第二次MDT讨论,反馈第一次MDT讨论意见执行情况,并制定下一步治疗方案。
第一次MDT讨论意见执行:2017年09月29日行EBUS淋巴结活检,结果为(右中叶LN)转移性分化差的腺癌,免疫表型提示肺来源。
2017年10月11日第二次MDT讨论意见:建议患者进行同步放化疗,在化疗方案的选择上,可以兼顾到卵巢癌的治疗,如使用紫衫类的药物联合。同时,放疗科在制定放疗方案的时候,也可以考虑卵巢病灶,评估是否可以一起治疗。
2017年11月1日第三次MDT讨论,反馈第二次MDT讨论意见执行情况,并制定下一步治疗方案。
第二次MDT讨论意见执行:
1. 将EBUS获取的肿瘤组织标本送检NGS检测,结果显示EGFR 21外显子L858R突变,以及TP5310号外显子移码突变、EGFR 扩增(CN=19.61)、MET 扩增(CN=3.33)、BRAF 扩增(CN=3.05)、PIK3R1 扩增(CN=3.27)。外周血基因检测的结果为EGFR21外显子L858R突变,TP538号外显子错译突变,肿瘤突变负荷较低。
2. 患者拒绝进行同步放化疗,强烈要求靶向治疗。对于EGFR21外显子突变伴多个受体酪氨酸激酶扩增的IIIA3期的肺腺癌,合并卵巢癌术后两年复发的患者,接下来的治疗策略。
病例讨论
肺内科汪斌超医生:这个病人是典型的双原发的肿瘤,影像学和病理上都已经得到诊断。之前已经进行了两次MDT讨论,这次肿瘤中心大讨论,期望把这个复杂问题简单化。即患者的生命周期中,肺癌占的权重大还是卵巢癌权重大。请妇科的陈观娣主任把卵巢方面的治疗做一个解读。
妇科陈观娣医生:这个患者卵巢癌术后分期是IIIC,术后中位的DFS是18个月左右,这个病人的情况基本符合。对于复发的卵巢癌患者,如果复发病灶比较局限,根据临床医生评估,如果能够完整切除,首选还是手术切除,然后再进行化疗,效果比较好。但病人是黏液性腺癌,这类肿瘤的特点是,盆腔里面病灶很广泛,不容易局限,整个盆腹腔都有可能蔓延。黏液性腺癌的复发,二次手术的机会是比较少的。如果不能选择手术治疗,就只选择化疗。患者2015年8月份化疗到现在,复发时间超过半年,说明患者是一个铂敏感的病人,化疗方案的选择上建议用TC方案。如果经济条件许可,可以在TC方案的基础上做一些变化,如采用剂量密集型的TC方案,因为传统的TC是三周一个周期的,密集型方案,泰素采用周疗,病人的生活质量更高一点,副反应更小一点,在此基础上再加用一个靶向靶向治疗,如抗血管生成的药物贝伐珠单抗。经济条件好的患者可以进行BRCA基因检测,突变的患者可以选择奥拉帕尼治疗。
肺内科杨衿记医生:假如不考虑患者是否合并肺癌,单纯的IIIC期卵巢癌患者,术后DFS 2年,目前出现局部复发,再接受正规的治疗以后,中位生存是多长?5年的OS率大概是多少?
妇科陈观娣医生:一般而言,对于III-IV期卵巢癌患者,又出现复发的,5年生存率为10%左右。对于复发后患者的中位生存统计,目前并没有很详细的数据。但考虑到这个病人但病理类型为粘液腺癌,这类病人的治疗效果不好,很容易出现复发。
肺内科杨衿记医生:请教放疗科的医生,对于IIIA期不能手术切除的患者,在进行了标准的化放疗之后,中位的OS有多长,5年生存率多高?
放疗科燚医生:局部晚期NSCLC接受标准的放化疗后,中位的OS是22-26个月,5年生存率一般为16%左右。
胃肠肿瘤内科马东医生:患者为卵巢粘液腺癌术后,接受辅助化疗后的患者,DFS为两年,对于预后不是太好的黏液性癌而言,患者应该属于治疗反应相对比较好的。对这个病人来说,肺癌的威胁更大,我们应该针对肺癌进行治疗,在治疗方案的选择上,尽量可以覆盖到卵巢癌。我个人不建议再用紫杉类的药物,因为患者在卵巢癌辅助化疗使用TC方案的时候,肺部已经有病灶,但辅助化疗过程中,肺的病灶没有变化的,因此紫杉醇方案估计对这个患者肺癌的疗效不是太好,可以选用其它的方案,如吉西他滨也可以覆盖到卵巢癌,抗血管生存治疗,也可以同时覆盖肺癌和卵巢癌。可以考虑在化疗结束后,再进行妇科手术。
肺内科汪斌超医生:马主任的意见和我们第二次MDT讨论的观点是一致的。目前卵巢癌和肺癌,当务之急应该是肺癌,所以我们接下来主要讨论肺癌的治疗。目前,患者的临床分期是IIIA3期,这是一类异质性非常大的群体,这个群体的最佳治疗模式,都处于积极的摸索之中。在这一方面,肺一科的陈华军副主任医师做了一些工作,正在进行前瞻性的临床研究。请陈华军医师介绍一下这方面的研究进展,并结合患者的特征,做一些治疗方面的建议。
肺内科陈华军医生:目前,局部晚期NSCLC的标准治疗是化放疗,但不管从病人还是从医生的角度来讲,都对这种治疗方法有不满意的地方。第一,患者的生存远远没有我们想像的那么好。不管是同期还是序贯放化疗,大概的中位生存期为1年至一年半;第二,治疗的耐受性。10年前,在《循证医学》杂志上发表了一篇荟萃分析,总结局部晚期NSCLC接受同步放化疗的毒性。研究呈现的数据和我个人的临床实践体会还是蛮贴切的。接受同步放化疗的患者,绝大部分人都有3-4度的骨髓抑制,1/5的患者有3度或者以上的食管炎。序贯放化疗的病人稍好一点,但是在做化放疗期间,有超过一半的病人需要接受粒细胞刺激因子的治疗,放射性食管炎的发生率为10%左右。这是十年前的数据。在过去10多年里,化放疗做了很多的研究,包括标准化放疗之前的诱导,后续的巩固,还有放疗方式的改变,超分割,大分割,和很多药物的组合,但是整体的效果都处于平坦期,总体的毒副作用还是偏大的。在当前精准医学的背景下,这样的副作用,我们是很难接受的。目前,在晚期NSCLC中,有8个前瞻性的临床试验已经证实了EGFR TKI的地位,耐受性也远远优于化疗。在晚期患者中,TKI的毒副作用发生率为2%-3%左右,所以,在毒性方面是很有优势的。现在问题是,这一治疗策略能不能适用于局部晚期的患者。对于这类局部晚期的病人,化放疗里的化疗是否又能去掉,而用毒副作用更低的TKI取代。目前,这方面,我缺乏前瞻性的数据。鉴于此,我们针对局部晚期合并基因突变的患者,开展了一个研究者发起的研究,这个研究是采用TKI诱导之后再加上放疗的一个单中心II期研究。主要的终点指标为ORR;次要的指标包括1年和3年的生存率和患者的生活质量。研究入组的是初治的非小细胞肺癌,外科评估不可以切除的III期患者,合并EGFR敏感突变,先用厄洛替尼诱导治疗12周,其实6周的时候就评估一次,第12周再做一次评估,确认之后的DCR的病人加局部的放疗,局部放疗之后再次用6个月的厄洛替尼,然后停掉进行随访。研究从启动到现在已经有半年,但入组速度较慢,目前共入组了两例患者。第1例患者接受了12周的特罗凯诱导治疗之后,疗效评价为PR,后给予60Gy胸部放疗,目前继续接受放疗后的特罗凯治疗。副作用较小,2度的皮疹,正在继续的研究和随访过程中。
肺内科杨衿记医生:上一次MDT讨论结果是考虑采用化疗,方案的选择上,可以采用紫杉类联合铂类,同时覆盖到卵巢癌和肺癌。但回到真实世界,患者治疗的个人意愿很重要,患者不愿意接受化疗。目前,NGS的检测结果提示为EGFR 21外显子L898R敏感突变,同时合并酪氨酸激酶的扩增或突变。请分子生物学方面的专家张绪超所长作简单的介绍,根据患者的NGS检测结果,对EGFR TKI的治疗是否敏感?
分子诊断张绪超医生:患者组织NGS的测序,结果比较复杂,第一个为L858R点突变,这个点突变比例非常高(92.7%),从肿瘤分子突变的空间分布来看,说明大部分的肿瘤细胞都含有这一变异,同时伴随的现象是EGFR的扩增。另一个主要的突变就是P53突变,比例达到38.9%。在过去的研究当中提示,TP53突变对TKI有一定的影响,是不良的影响。另外,从肿瘤的克隆性分布来看,患者还合并有三个重要的基因的扩增,一个是BARF,一个Met,还有一个PIK3CA。MET和BRAF同时分布在7号染色体的长臂上,EGFR是在7号染色体的短臂上,所以,Met跟BRAF的扩增是不是跟EGFR的扩增来自于同一个细胞,但MET和BRAF的扩增拷贝数的量非常低,分别为3.33和3.05,和EGFR的拷贝数19.61相比,还是小了很多,也就是说明只是在一部分细胞群当中有,不是大部分细胞群。我个人觉得BARF和CMET的扩增对患者的治疗影响并不大,接受EGFR TKI治疗还是非常有效的,因为它的突变丰度通路特别高,而且拷贝数也非常高。当然它有一个不良的因素,就是TP53突变,这是组织检测的结果。
肺内科杨衿记医生:我想补充一点有关TP53的基本认识,以往讲的TP53是一个抑癌基因,目前没有一个特异性的抑制剂来治疗,在肺癌的预后上有一定的价值。在今年刚刚结束的WCLC会议上,王洁教授和吴一龙教授共同牵头进行的BENIFIT研究,评估采用外周血ctDNA测出来EGFR敏感突变的病人一线接受TKI治疗的疗效。在研究的后续探索性分析中,根据患者NGS的结果进行了进一步分析:单纯是EGFR单纯突变的患者,接受易瑞沙治疗的中位的PFS是13个月,超过了IPASS研究的9.5个月;第二组患者,EGFR敏感突变合并TP53的突变,中位PFS 是9.3个月,中等疗效,和IPASS结果类似的;第三组患者,EGFR敏感突变同时合并第二个或第三个驱动基因,如Met,Her2,BRAF等基因,这类患者的中位PFS只有5.4个月。根据这个最新研究的的证据,请吴院长解读一下,这一结果会不会影响我们临床上TKI的使用?
吴一龙医生:经过前几次的讨论,我们对卵巢癌有了一些初步的认识,它的生物学行为就是在局部,减瘤手术放在首位的。对于这一患者,又没有机会进行二次手术。患者在随访过程中,是发现了肺部的病灶,之后进行评估,才发现了盆腔的病灶,那么,卵巢的病灶是否有可能是肺转移的?
妇科陈观娣医生:如果暂且不考虑肺癌,这个病人在临床上,一定要做过妇检,如果是腹部柔软的,疤块又是局限的,还是可以。但前提是有一定难度,黏液性腺癌的患者,从我们的临床处理经验来看,即使影像学上看不到广泛的转移病灶,但整个盆腔都有可能肠粘连。可以进行尝试,但需要和病人充分沟通。此外,这个病人应该不太可能是肺转移到卵巢,患者第一次手术后,卵巢子宫附件都已经全切了,这种复发更多是局部的复发。真正肺转移到盆腔局部的可能性还是很小。所以盆腔的病灶,应该还是原发卵巢癌的复发。
吴一龙医生:我们在讨论的时候应该先把大的策略定下来,然后再去讨论细节的问题。目前,这个病人是一个双原发的肿瘤,从刚刚讨论的数据来看,目前患者的生命周期中,肺癌和卵巢癌的预后差别不大。结合患者的个人治疗意愿和具体的肺部疾病特征,可以考虑这一临床试验的治疗模式,之后再分别考虑局部的干预。
回到NGS的问题上,目前NGS做的非常多,这些结果也带来新的问题,究竟如何看待这些东西?目前,对于EGFR突变的患者,我们有 9大临床试验的结果证实了其治疗地位。在这些研究中,我们的伴随诊断的工具是什么?就只有一个指标——EGFR突变,我们没有去检测P53突变或其他基因的扩增。9大临床试验非常清楚的告诉我们,EGFR突变的病人接受一线EGFR TKI治疗的有效率为70%—80%之间,疾病控制率达到90%,大概10%左右的是原发性耐药。那么,这些临床试验的患者,是不是就不存在TP53突变?不是,他们也存在,只不过我们没有去检测。今天,我们进行了NGS的检测,发现了一些问题,但是目前他们还不足以改变临床实践。
如何评价BENEFIT这个临床试验?大家知道BENEFIT的主要终点是什么?评估血液检测的敏感性突变,然后来指导我们的治疗。我们BENEFIT用的检测的方法是什么?一个是PCR,一个是ddPCR。NGS不是BENEFIT研究设计里面要求的,而是后来我们加进去的。从临床试验的角度来讲,这种加进去的探索性分析,它的可信度不够高,这只是一个Explore,这个Explore告诉我们,未来可能要考虑这些问题。然而,完全不可以作为一个证据来左右我们目前的临床实践。BENEFIT探索性NGS分析的结果,给我们提示了非常好的信号,以后要重视整个,但是今天仍然不能用来决定我们该如何治疗的。
如何看待临床试验的结果非常的重要的。对于这个患者,我们医生心中应该有数,有可能,只是可能,这个病人用EGFR TKI的PFS不会很长。只能用可能这个词,为什么可能?两个理由,第一个理由,比合并多基因突变更重要,患者是一个21外显子突变,按照现在所有的数据来讲,它的PFS是短于19外显子缺失的,这是所有的试验都证实的一点。如果再考虑到患者合并这么多其他基因的突变,也有可能会影响到患者的PFS。在这个时候,就变成是另外一个问题了。如果进行治疗选择的话,如选择TKI,选择什么样的TKI?是选第一代还是第二代?第二代的TKI,特别是Dacomitinib的研究结果,19外显子突变和L858R突变的患者是有区别,L858R突变的患者接受Dacomitinib的PFS达到12.3个月。第二,这个病人合并EGFR扩展,二代TKI也可以兼顾到。为什么第二代的效果比第一代好,有可能就是它同时覆盖HER 1-4,疗效比较稳定。阿法替尼的几个临床试验,PFS都是11个月,说明这个药的质量很好,效果非常稳定的。根据这些基因检测更新的结果,我们可以考虑将第二代放在前面。但这时候必须马上想到另外一个问题了,药物的副作用是否能承受不,此外,第一代有很多进入医保了,患者的家庭经济能够承受二代TKI。将这些因素全部综合起来,如果患者觉得副作用可以耐受,经济也可以承受,我推荐选择二代TKI。是选一代应该选二代。用药一段事件后再来评估肺部的卵巢的病灶。
最近,在很多场合我经常提到,肺癌的患者有EGFR突变和没有EGFR突变是两个完全不同的病,它的预后、治疗、生物学,完全不一样的。时代走到了今天,对EGFR突变的晚期的病人,建立了非常好的治疗方式。早期的病人我们也开始有了证据,如ADJUVANT和EVAN研究,如果日本的研究可以重复这个结果,我们觉得早期的病人,辅助靶向治疗是肯定的。唯一缺的一点就是局部晚期的病人,局部晚期就有EGFR突变的跟没有EGFR突变的,从目前的角度来讲,我个人来讲应该是不同的疾病,但是我们今天仍然把它当成一个同样的疾病来治疗。所以才有了陈华军博士的这一研究,针对IIIA期EGFR突变的患者,把化疗取代的这样一个临床试验。这个临床试验,开期挺不错的,因为第一个病人缩小50%,而化疗缩小50%是极少的,而且患者的副作用较轻。今天这个病人,把这些东西综合起来,可以得出几点:第一,我认为说这个病人可以考虑先用TKI,然后化疗做准备。TKI可以选用第二代药物,在TKI治疗同时,观察肺部的病变跟盆腔的病变。在计划把放疗的介入进去的时候,请我们的外科,妇科和放疗科医生,一起讨论,盆腔的肿瘤是外科切掉还是放疗。在积极诱导治疗的同时,观察局部治疗介入的时机和局部治疗的手段,期望达到比较完美的结局。













 苏公网安备32059002004080号
苏公网安备32059002004080号


