(以下内容仅供医学药学专业人士阅读参考,如您非前述专业人士,请离开本页。)
BRAF V600E突变与甲状腺癌:探索预后不确定性与治疗机遇
BRAF V600E in thyroid cancer: navigating prognostic uncertainty and therapeutic opportunity.
Garcilaso Riesco-Eizaguirre et al.
Eur Thyroid J
IF = 4.3
本综述探讨BRAF V600E在甲状腺癌中的作用,重点分析其存在争议的预后价值、显著的分子异质性以及作为治疗靶点的潜力。
作为甲状腺乳头状癌最常见的致癌驱动突变,BRAF V600E通过激活MAPK通路并抑制碘代谢和分化相关基因表达发挥作用。虽然该突变与甲状腺外侵犯、淋巴结转移、复发和死亡率等不良特征相关,但其作为独立预后标志物的临床价值仍存争议。对于1-4厘米的孤立性甲状腺内肿瘤和低风险微小癌,BRAF V600E检测可能有助于优化手术决策,但相关证据(尤其对<2厘米肿瘤)尚不一致。该突变还可能导致放射性碘难治性,但并非所有BRAF突变肿瘤都呈现相同生物学行为。转录组和基因组异质性(包括甲状腺分化评分差异、基因共突变和miRNA特征)调控着治疗反应。
针对BRAF V600E的靶向治疗已衍生出新策略。选择性BRAF和MEK抑制剂在晚期甲状腺癌中展现疗效。此外,利用MAPK抑制剂恢复RAI摄取的再分化策略显示出前景,尤其对特定患者群体。这些进展强调需将BRAF突变状态置于更广泛的分子和临床背景中解读,以指导个体化有效治疗。
点评专家
专家介绍
华中科技大学同济医学院附属同济医院核医学科主任
中国医学影像技术研究会常务理事及核医学分会副主任委员
中华医学会核医学分会委员及PET学组副组长
中国医师协会核医学分会常务委员及诊疗一体化学组副组长
中国核学会核医学分会常务理事
中国医院协会医学影像中心分会常务委员
中国生物物理学会分子影像学分会委员
武汉医学会核医学分会主任委员
湖北省医学会核医学分会副主任委员
湖北省核学会副理事长
湖北省医师协会核医学分会副主任委员
美国ACNM Fellow
中德医学会核医学专业委员会副主任委员
国际肝胆胰MDT专业委员会常务委员
《中华核医学及分子影像杂志》等多个行业期刊编委
承担国家自然基金项目6项,发表SCI收录论文(第一或通讯)50余篇,编写专著及教材多部,湖北省自然科学奖三等奖(第一完成人),武汉英才硚楚人才行业拔尖人才
这篇综述全面探讨了BRAF V600E突变在甲状腺癌中的双重角色:有争议的预后标志物和明确的治疗靶点。它为临床医生在处理这一常见分子事件时面临的困惑提供了清晰的梳理。
在甲状腺癌诊疗的临床实践中,我们经常面临这样的问题:发现BRAF V600E突变,是否必然意味着预后更差?是否应该据此采取更积极的治疗?这篇综述给出了一个较为平衡的答案。一方面,多项大型回顾性研究和荟萃分析(meta-analysis)显示,BRAF V600E与甲状腺外侵犯、淋巴结转移和复发风险增加相关[1-3]。特别是在1-4厘米的孤立性甲状腺内肿瘤(solitary intrathyroidal PTC)这一特定人群中,BRAF状态对手术方式(甲状腺叶切除术 vs. 全甲状腺切除术)的选择可能具有指导意义,因为研究表明突变阳性患者的复发风险显著高于阴性患者[4]。但另一方面,近期的前瞻性及高质量研究也提示我们不宜过度解读BRAF的独立预后价值。例如,ESTIMABL2研究的分子分析显示,在低危(肿瘤≤2 cm)甲状腺癌患者中,BRAF突变状态与3年无事件生存并无显著相关性[5]。此外,一些研究也未能证实BRAF突变与高危病理特征或疾病特异性生存的独立相关性[6]。
综上,个人认为BRAF V600E是一个重要的临床参考指标,尤其是在评估1-4 cm单发肿瘤时可能为手术决策提供增量信息,但不宜作为独立的、决定性的预后判读工具。更重要的可能是将其置于更完整的分子背景下考量,例如结合TERT启动子、TP53等共突变状态,以及患者的年龄、性别、淋巴结转移等传统临床病理因素。Xing团队近期发表于《Lancet Oncology 》的研究提示,将BRAF与TERT突变状态结合,可显著改善AJCC/TNM分期系统对死亡风险的预测能力[7],这指向了多基因组合评估的未来方向。
如果说BRAF的预后价值尚有争议,那么其作为治疗靶点的地位则已非常明确。综述中系统梳理了MAPK通路靶向治疗在晚期甲状腺癌中的应用,包括选择性BRAF抑制剂和MEK抑制剂。这些靶向药物在临床研究中展现了双重价值。
在放射性碘难治性分化型甲状腺癌(RAIR-DTC)中,靶向治疗策略包括直接的抗肿瘤作用和旨在恢复碘摄取的“再分化”治疗。对于前者,已有临床研究证实,针对BRAF V600E的靶向治疗能为经治的RAIR-DTC患者提供有效的治疗选择。而“再分化”策略则提供了另一种思路:通过短期应用MAPK通路抑制剂(如BRAF/MEK抑制剂组合),部分患者的肿瘤可恢复对放射性碘的摄取能力,从而使后续的放射性碘治疗重新变得有效。这一策略提示,对于部分RAIR-DTC患者,我们或可尝试通过靶向治疗暂时逆转碘难治状态,为患者争取宝贵的治疗机会。
在未分化甲状腺癌(ATC)这一预后极差的亚型中,针对BRAF V600E的靶向治疗(特别是BRAF/MEK抑制剂联合方案)取得了突破性进展。相关研究显示,与传统的化疗时代相比(中位总生存期约5个月),靶向治疗为BRAF V600E突变型ATC患者带来了显著且具有临床意义的生存改善。基于这些数据,相关靶向治疗方案已在一些国家和地区获批用于此类患者。因此,对于新诊断的ATC患者,常规进行BRAF V600E检测已成为重要的临床实践,一旦发现突变,应考虑相应的靶向治疗策略。
当然,目前仍存在未满足的临床需求,例如如何精准筛选对“再分化”治疗敏感的患者、如何克服靶向治疗耐药以及优化治疗组合等,这些问题有待更多转化研究和临床试验探索。
总之,这篇综述客观、全面地总结了BRAF V600E在甲状腺癌中的研究现状,强调了在预后评估中需结合多维度信息。相比之下,BRAF作为治疗靶点的价值更具临床可操作性,尤其体现在晚期疾病中的靶向治疗和再分化治疗策略上,为临床医生的决策提供了有价值的参考框架。
BRAF V600E 与 TERT 启动子突变在分化型甲状腺癌放射性碘抵抗及复发中预后意义[8]
Prognostic significance of BRAF V600E and TERT promoter mutations in radioiodine resistance and recurrence of differentiated thyroid cancer
Nhung LTT, et al.
Medicine (Baltimore)
IF = 1.6
摘要
甲状腺癌是最常见的内分泌恶性肿瘤,而分化型甲状腺癌(DTC)对放射性碘治疗的耐药性呈上升趋势。BRAF V600E 突变与 TERT启动子突变在甲状腺乳头状癌中协同驱动肿瘤复发与死亡。本研究旨在探讨上述两种突变在越南放射性碘难治性分化型甲状腺癌(RAIR-DTC)患者中,与摄碘能力丧失、临床特征的相关性及其预后价值。
研究纳入 2021 年 1 月至 2024 年 12 月期间接受甲状腺全切术及 ¹³¹I 治疗的 144 例 DTC 患者,分析 BRAF V600E 与 TERT 启动子突变的诊断及预后价值。
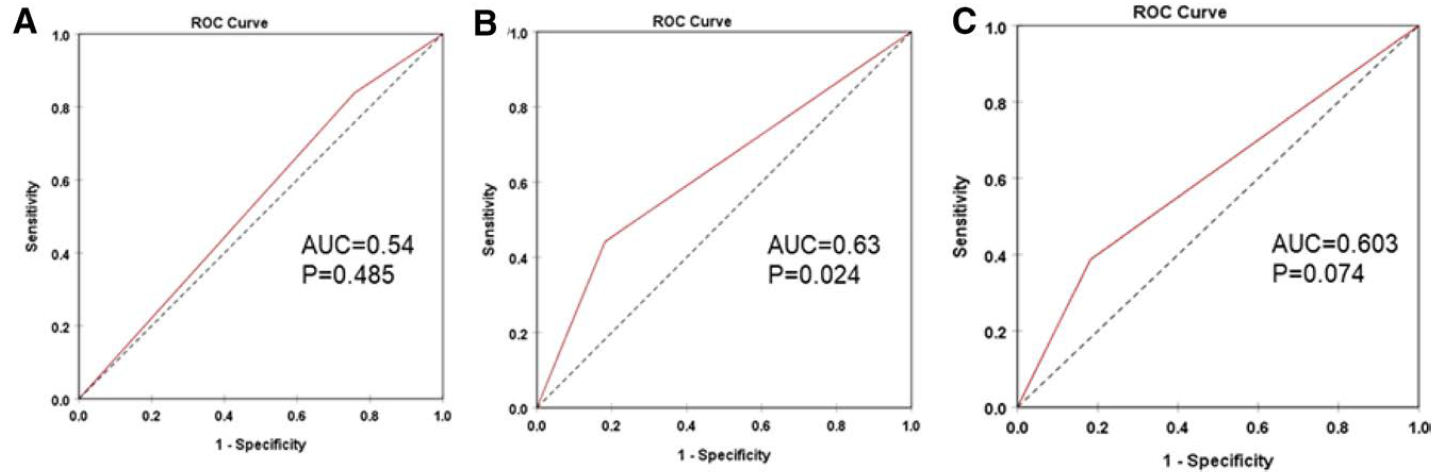
结果显示,BRAF V600E 突变检出率为 81.9%(118/144),TERT 启动子突变检出率为 38.2%(55/144)。TERT 突变在 RAIR-DTC 患者中更为常见,可显著增加摄碘能力丧失风险(OR=3.6,P=0.007),而单纯 BRAF V600E 突变则无显著影响。BRAF V600E 与 TERT 共突变可独立升高摄碘能力丧失风险(OR=4.8,P=0.009)。两种突变均与肿瘤大小、甲状腺球蛋白水平、复发 / 转移及更高复发风险相关,共突变状态可加速肿瘤复发。TERT 突变可有效区分 RAIR-DTC 与碘敏感型 DTC(AUC=0.63),并对复发具有中等预测效能(AUC=0.72),与共突变的预测价值相近(AUC=0.69)。共突变患者术后无复发生存期(10.5 个月)短于 BRAF 野生型组(11.3 个月)及仅 BRAF 突变组(11.8 个月),差异具有统计学意义(P<0.05)。
本研究提示,TERT 启动子突变与 DTC 患者放射性碘治疗失败风险升高相关,可作为预测放射性碘耐药的早期生物学标志物。
表1 BRAF V600E、TERT 突变与分化型甲状腺癌患者碘摄取功能丧失的相关性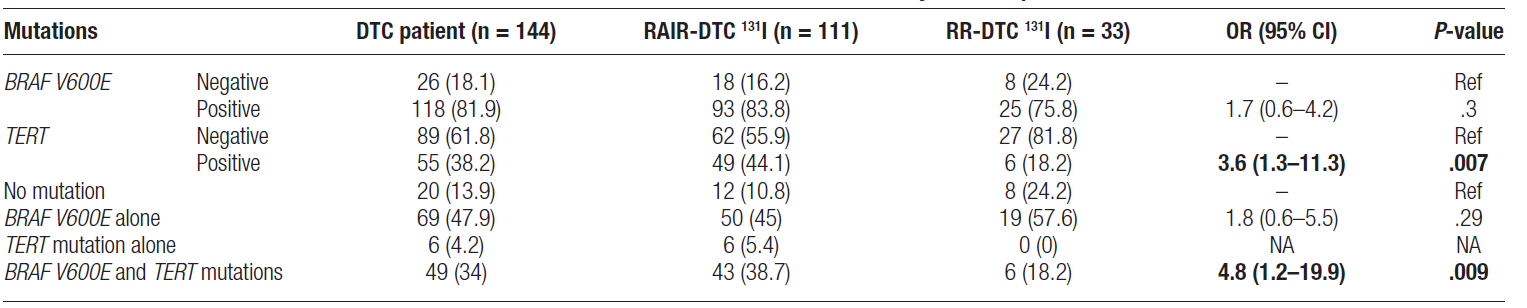
点评专家
专家介绍
江苏省人民医院甲状腺外科主任
中国医师协会外科医师分会甲状腺外科专家工作组专家委员
海医会台海医学发展委员会甲状腺微创美容外科学组副组长兼秘书长
中华医学会外科分会甲状腺和代谢外科学组腔甲联盟副主席兼秘书长
中国研究型医院学会甲状腺疾病专业委员会委员
国家癌症中心甲状腺癌质控专家委员会委员
中国人体健康科技促进会甲状腺肿瘤专业委员会常务委员
海医会台海医学发展委员会委员
江苏省研究型医院学会甲状腺疾病专业委员会副主任委员
江苏省医师协会微无创医学专业委员会委员
浙江省抗癌协会甲状腺肿瘤专业委员会常委兼青委主委
浙江省康复医学会甲状腺专委会副主任委员
国际内分泌肿瘤整形外科医师协会(ISOPES)学术委员
临床诊疗中,诸多临床医师十分关注:BRAF 与 TERT 共突变是否会加剧分化型甲状腺癌患者碘抵抗风险、增加复发概率?这项亚洲人群队列研究,便针对这一临床疑点给出了客观解答。放射性碘难治性分化型甲状腺癌(RAIR DTC)是临床诊疗难点,有效预测碘抵抗与复发风险、实现精准分层,是优化治疗策略、改善患者预后的核心环节。BRAF V600E 作为甲状腺乳头状癌最常见的驱动突变,已被证实与甲状腺外侵犯、淋巴结转移等因素相关[9];TERT 启动子突变则通过核糖体生物合成途径促进肿瘤进展,二者的协同作用已成为甲状腺癌分子预后评估的重要方向[10]。
该研究以越南人群分化型甲状腺癌队列为研究对象,系统探讨了 BRAF V600E、TERT 启动子突变及二者共突变与碘摄取丧失、复发风险的关联,为亚洲人群分子预后分层提供了证据。研究明确,TERT 启动子突变是碘抵抗的危险因素(OR=3.6,P=0.007),而BRAF V600E 联合 TERT 启动子共突变可进一步显著升高碘抵抗风险(OR=4.8,P=0.009),并成为术后二次复发的强独立预测因子,同时显著缩短患者无复发生存期,提示共突变是叠加高危信号[8]。
本研究结果提示BRAF 联合 TERT 突变检测能更精准地识别出易发生碘抵抗、早期复发的超高危患者,弥补传统临床病理分期对预后判断的不足,为治疗决策提供关键依据。Tan等[11]的研究结果同样也证明了BRAF 联合 TERT共突变患者进展为RAIR-DTC的速度更快,与该研究结果一致。这些研究结果均提示我们对于共突变阳性患者,可提前规避无效、反复放射性碘治疗,更早启动靶向治疗等替代方案,显著提升诊疗效率与患者获益。
总体而言,该研究明确阐释了 BRAF V600E 与 TERT 启动子突变在碘抵抗及肿瘤复发中的独立作用与协同效应,进一步完善了不同人群的分子预后证据体系。研究结果证实,将二者联合检测纳入分化型甲状腺癌常规分子评估,可有效助力风险分层、治疗决策及长期随访管理,对推进甲状腺癌精准诊疗落地具有重要临床价值与实践意义。因此,临床工作中应重视分化型甲状腺癌患者的基因筛查,强化 BRAF V600E 合并 TERT 启动子双突变高危人群的个体化全程管理与密切随访,从而全面提升此类患者的精准诊疗水平。
[1] Kim KB, et al. Clinical responses to vemurafenib in patients with metastatic papillary thyroid cancer harboring BRAFV600E mutation. Thyroid 2013 23 1277–1283.
[2] Zhang Q, et al. Meta-Analyses of Association Between BRAFV600E Mutation and Clinicopathological Features of Papillary Thyroid Carcinoma. Cell Physiol Biochem 2016 38 763–776.
[3] Liu C, et al. Associations between BRAFV600E and prognostic factors and poor outcomes in papillary thyroid carcinoma: a meta-analysis. World J Surg Oncol 2016 14 241.
[4] Huang Y, et al. BRAF V600E mutation-assisted risk stratification of solitary intrathyroidal papillary thyroid cancer for precision treatment. J Natl Cancer Inst 2018 110 362–370.
[5] Leboulleux S, et al. Thyroidectomy without radioiodine in patients with low-risk thyroid cancer. N Engl J Med 2022 386 923–932.
[6] Yasuhiro I, et al. BRAF mutation in papillary thyroid carcinoma in a Japanese population: its lack of correlation with high-risk clinicopathological features and disease-free survival of patients. Endocr J 2009 56 89–97.
[7] Xing M, et al. Genetic modification of the AJCC classification of papillary thyroid cancer: an international, multicentre, retrospective cohort study. Lancet Oncol 2025 26 1382–1392.
[8] Nhung LTT, et al. Prognostic significance of BRAF V600E and TERT promoter mutations in radioiodine resistance and recurrence of differentiated thyroid cancer. Medicine (Baltimore). 2025 Sep 19;104(38):e44540.
[9] Caronia LM, et al. Role of BRAF in thyroid oncogenesis. Clin Cancer Res. 2011 Dec 15;17(24):7511-7.
[10] Yu PC, et al. TERT accelerates BRAF mutant-induced thyroid cancer dedifferentiation and progression by regulating ribosome biogenesis. Sci Adv. 2023 Sep;9(35):eadg7125.[11] Tan GX, et al. TERT promoter mutations contribute to adverse clinical outcomes and poor prognosis in radioiodine refractory differentiated thyroid cancer. Sci Rep. 2024 Oct 10;14(1):23719
排版编辑:C Y X











 苏公网安备32059002004080号
苏公网安备32059002004080号


