2026年5月,国际顶尖医学期刊《新英格兰医学杂志》(NEJM)在线发表了一项具有里程碑意义的临床研究结果。该研究由美国丹娜-法伯癌症研究所Brian M. Wolpin教授团队牵头,报道了RAS(ON)多选择性抑制剂Daraxonrasib(RMC-6236)在既往经治的RAS突变晚期胰腺导管腺癌(PDAC)患者中的安全性与初步疗效。同期,莱恩伯格综合癌症中心Channing J. Der教授与Jen Jen Yeh教授发表了题为“Advances in RAS Therapeutics for Pancreatic Cancer”的社论,对该研究的突破性意义进行了深度评述,并客观分析了面临的挑战与未来方向。

研究背景与临床需求
胰腺导管腺癌(PDAC)是一种高度致死的癌症,多数患者确诊时已处晚期。转移性PDAC中位总生存期(OS)不足1年,5年OS率仅3%。二线化疗客观缓解率(ORR)不足10%,中位OS仅5~7个月,临床获益极为有限。
超过90%的PDAC存在KRAS突变,其中G12D(42%)、G12V(31%)、G12R(15%)最为常见。KRAS作为小GTP酶,在活性GTP结合态(ON)与失活GDP结合态(OFF)之间循环。突变导致GTP酶活性受损,驱动持续性致癌信号。长期以来RAS被视为“不可成药”,但共价KRAS G12C(OFF)抑制剂的开发——通过共价结合将KRAS G12C突变蛋白锁定在“关闭”状态,证明了直接靶向RAS是可行的。然而KRAS G12C突变在PDAC中不足2%,且OFF态抑制剂对活性态RAS作用有限、易产生耐药。因此,靶向活性态RAS并覆盖多种RAS变异体的治疗方法成为迫切需求。
Daraxonrasib的作用机制
Daraxonrasib是一种口服、非共价RAS(ON)多选择性抑制剂。其机制借鉴“分子胶”原理:先与环孢素A形成二元复合物,再与GTP结合态RAS结合为三重复合物,空间位阻阻断RAS与下游效应分子(如RAF)结合,抑制MAPK信号通路。该药可同时抑制KRAS、HRAS和NRAS三种亚型的突变型及野生型蛋白的活性态,实现全面RAS抑制。临床前研究显示其在PDAC模型中呈深度、持久的抗肿瘤效应。
研究设计核心
RMC-6236-001为多中心、开放标签I~II期试验(16个美国中心)。纳入携带RAS(12、13、61位点)突变的晚期实体瘤患者,PDAC患者需经氟尿嘧啶或吉西他滨的化疗后进展。
主要终点为安全性,次要终点包括药代动力学及抗肿瘤活性。剂量递增阶段(10~400 mg每日一次),基于安全性、PK和疗效选择300 mg为III期研究推荐剂量。该次报告重点分析了168例既往接受过治疗的RAS突变PDAC患者(剂量≤300 mg)。
核心数据
1. 患者基线
168例患者中位年龄65岁(30~86岁),68% ECOG评分0或1分,均处IV期。RAS G12突变占89%:KRAS G12D(39%)、G12V(31%)、G12R(17%);非G12突变包括Q61H(14例)、Q61R(2例)、Q61K(2例)、G13D(1例)。中位既往治疗线数2(1~6),58%接受过≥2线治疗。既往化疗:吉西他滨+白蛋白紫杉醇(60%)、FOLFIRINOX或改良FOLFIRINOX(43%)。
2. 安全性
168例中任何级别的治疗相关不良事件(TRAE)发生率为96%,≥3级TRAE发生率为30%,未观察到5级事件。最常见TRAE(任意级别)为皮疹、腹泻、恶心、口腔炎或黏膜炎。严重TRAE发生率为6%(腹泻2%)。
300 mg剂量组(83例):≥3级TRAE发生率为34%(皮疹和贫血各占7%)。剂量调整率为48%(43%停药、30%减量),未出现因不良事件停药。皮疹和胃肠道事件可通过常规干预(局部糖皮质激素、抗生素、止泻治疗等)管理。平均相对剂量强度为86%,因TRAE而导致的累计剂量中断的中位持续时间为16天。
3. 抗肿瘤活性
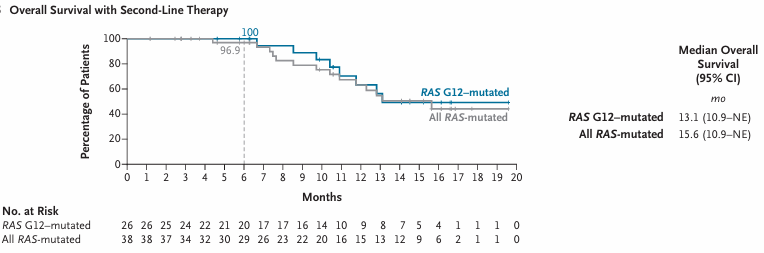
二线治疗RAS G12突变亚组(26例,300 mg):ORR达35%(95%CI,17%~56%),疾病控制率92%(95%CI,75%~99%)。中位至缓解时间2.6个月,中位缓解持续时间8.2个月(95%CI,3.8个月~不可评估)。中位随访时间为17个月(10.3~24.6个月)时,中位无进展生存期(PFS)8.5个月(95%CI,6.7~10.5个月),中位OS 13.1个月(95%CI,10.9个月~不可评估)。
二线治疗全RAS突变人群(38例,G12/G13/Q61):ORR为29%(95%CI,15%~46%),疾病控制率95%(95%CI,82%~99%)。中位缓解持续时间8.2个月(95%CI,3.8~8.8个月);中位随访时间为17个月(10.3~24.6个月)时,中位PFS 8.1个月(95%CI,5.9~10.1个月),中位OS 15.6个月(95%CI,10.9个月~不可评估)。
三线及以上治疗:G12突变组(38例)ORR 21%,全RAS突变组(45例)ORR 20%,中位PFS均为4.3个月,中位OS分别为8.6和9.0个月。
社论指出,35%的ORR和8.2个月的中位缓解持续时间是实质性突破,疗效显著优于历史二线化疗数据。
深度思考
机制突破:从RAS(OFF)到RAS(ON)
社论指出,KRAS G12C抑制剂(Sotorasib/Adagrasib)通过结合GDP结合态(OFF)的开关-II口袋发挥作用,但该突变在PDAC中频率不足2%。相比之下,Daraxonrasib创新性地靶向GTP结合态(ON)的活性RAS,通过形成“药物-环孢素A-RAS”三重复合物,阻断RAS与下游效应子(如RAF激酶)的结合。该策略可同时抑制突变型和野生型RAS蛋白,实现广谱覆盖。
耐药机制的初步揭示
社论提及,尽管Daraxonrasib单药疗效显著,但大多数患者最终因疾病进展而停药。通过对治疗进展患者的循环肿瘤DNA(ctDNA)或肿瘤组织分析,发现了获得性基因组改变,包括错义突变、缺失、截断突变、融合基因及扩增(总体检出率52%,PDAC中为59%)。这些改变提示RAS通路再激活是耐药的重要机制。
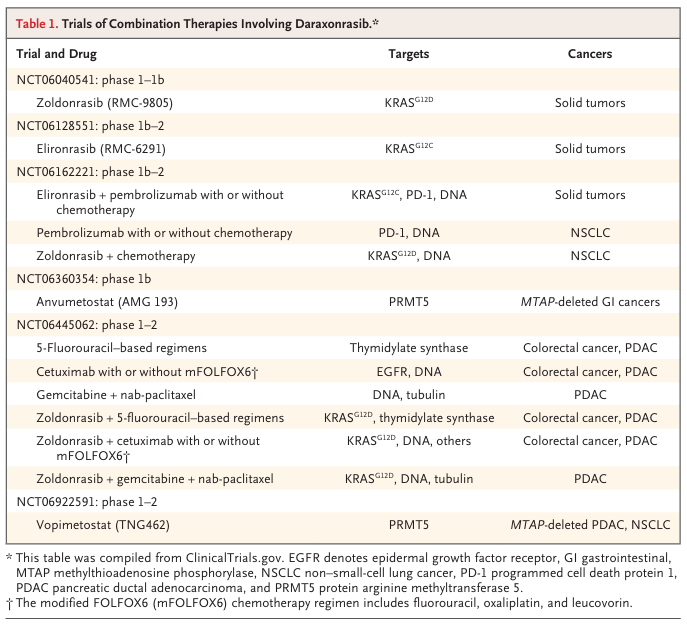
克服耐药需要合理设计联合治疗策略,目前正在评估的联合方案包括:与KRAS G12D抑制剂(Zoldonrasib)、KRAS G12C抑制剂(Elironrasib)、免疫检查点抑制剂(帕博利珠单抗)、PRMT5抑制剂(Anvumetostat、Vopimetostat)以及化疗(5-氟尿嘧啶方案、吉西他滨+白蛋白紫杉醇等)的联合应用。
毒性管理与治疗指数
300 mg剂量组≥3级TRAE发生率为34%,约半数患者需要剂量中断或减量,但无患者因不良事件终止治疗。社论认为,该药物的治疗指数可能得益于其对活性GTP结合态RAS的选择性、PDAC对持续通路信号传导的依赖性,以及相对于正常组织的肿瘤内优先蓄积。
总结与展望
RMC-6236-001研究证实,在既往经治RAS突变PDAC中,Daraxonrasib(300 mg每日一次)展现出具有临床意义的抗肿瘤活性(ORR 29%~35%,中位OS 13.1~15.6个月),显著优于历史二线化疗。治疗相关≥3级不良事件发生率30%~34%,以皮疹和胃肠道反应为主,可经常规干预管理。
社论评价其为首个在PDAC中证实RAS(ON)多选择性抑制剂明确临床获益的研究,标志着RAS靶向治疗从“不可成药”走向临床应用的又一里程碑。比较Daraxonrasib与标准化疗作为转移性PDAC二线治疗的疗效的全球随机III期RASolute 302研究也将在2026 ASCO会议上公布数据结果。同时,如何通过合理联合策略克服耐药、优化患者筛选、平衡疗效与毒性,是未来重要方向。该研究为RAS突变PDAC患者带来新希望,为RAS靶向药物发展奠定坚实基础。
[1] Wolpin BM, Park W, Garrido-Laguna I, et al. Daraxonrasib in Previously Treated Advanced RAS-Mutated Pancreatic Cancer. N Engl J Med, 2026, 394(18): 1790-1802.
[2] Der CJ, Yeh JJ. Advances in RAS Therapeutics for Pancreatic Cancer. N Engl J Med, 2026, 394(18): 1803-1806.
排版编辑:肿瘤资讯-ZJN











 苏公网安备32059002004080号
苏公网安备32059002004080号


