胆道恶性肿瘤(BTC)是一种起源于胆管上皮、具有高度异质性的恶性肿瘤,其发病率与死亡率仍在逐年增加1-2。手术切除是早期BTC的唯一根治手段,但超过半数患者确诊时已失去手术机会1。即使是接受手术切除的患者,其术后长期生存仍面临巨大挑战。
随着精准诊疗理念的深入,BTC的分层诊疗体系不断完善,系统治疗方案也持续迭代,其中,以IDH1抑制剂为代表的精准靶向药物,为突破BTC治疗瓶颈、改善患者长期生存带来了新希望。本期特邀陆军军医大学第一附属医院唐腾骞教授围绕边界可切除BTC新辅助治疗和转化治疗,以及靶免联合方案的临床进展等热点话题进行深度解读与点评,为BTC的临床实践带来更多前沿的学术见解。
CSCO指南率先提出边界可切除BTC概念,为新辅助和转化治疗提供重要依据
BTC具有高度侵袭性和异质性,仅依靠外科手段难以突破长期生存的瓶颈。即使是边界可切除人群,其术后5年复发率高达60%~70%3。目前,围手术期治疗策略已被证实可改善多种实体瘤的远期预后,其在BTC领域的研究亦逐步展开。然而,BTC新辅助治疗和转化治疗尚缺乏标准方案与高质量循证证据,适应人群界定不明确4。2023年,《中国临床肿瘤学会(CSCO)胆道恶性肿瘤诊疗指南》(以下简称“《指南》”)率先提出“边界可切除”BTC的定义,明确划定了边界可切除与不可切除的分层界限5。《指南》将边界可切除肝内胆管癌定义为:①肿瘤单个直径>5cm;②肿瘤数目≥3个或者合并卫星灶;③门静脉或肝静脉侵犯;④区域淋巴结转移;⑤术前CA19-9>200U/ml。边界可切除肝门部胆管癌定义为:①区域淋巴结多发转移或伴融合;②肿瘤侵犯单侧或双侧门静脉或肝动脉;③FLR虽未符合安全肝切除决策体系,但预期通过门静脉栓塞术等治疗措施可达标者5。这一概念的提出,进一步细化了可切除BTC、边界可切除BTC和不可切除BTC的概念,为临床针对不同的BTC患者进行新辅助治疗和转化治疗提供了指导。
在明确人群分层的基础上,如何提高根治性切除率、降低术后复发率,寻找更有效的新辅助治疗方案和转化治疗方案,仍是亟待解决的临床难题。
靶免联合治疗为突破BTC患者生存困境带来新希望
长期以来,吉西他滨联合顺铂(GC)方案是晚期BTC的标准一线化疗方案,但其带来的生存获益十分有限,中位总生存期(mOS)仅为11.7个月6。近年来,免疫治疗的兴起为晚期BTC治疗带来了更多新选择。TOPAZ-1、KEYNOTE-966两项Ⅲ期临床研究的成功,证实免疫联合化疗可改善mOS,但这一提升的幅度仅为1.6~1.8个月,未达到真正意义上的延长患者生存的目标,绝大多数患者仍面临着疾病进展的现实问题6。
目前,靶免治疗与化疗的三联策略,凭借三者协同增效的特点,成为BTC治疗领域的研究热点。从机制上看,化疗可诱导肿瘤细胞凋亡、降低肿瘤负荷,同时改善肿瘤间质纤维化,提升靶向药物穿透性。靶向药物可逆转化疗耐药、抑制肿瘤细胞增殖的同时,上调程序性死亡配体1(PD-L1)的表达,增加肿瘤浸润淋巴细胞的密度,将“冷肿瘤”转化为“热肿瘤”。此外,联合用药还可通过多通路阻断,降低耐药克隆的生存概率6。
近年来,已有多项研究证实了靶免联合化疗的三联方案具有良好的疗效和应用前景:一项全球多中心1b/2期临床研究(NCT06501625),旨在评估艾伏尼布联合度伐利尤单抗+GC方案一线治疗IDH1突变晚期胆管癌的安全性与疗效,其1b期安全导入期数据已在2026年ASCO GI大会公布。结果显示,7例入组患者中,1例达到部分缓解(PR),4例实现疾病稳定(SD),展现了该靶免联合化疗的三联方案在IDH1突变BTC人群中良好的抗肿瘤活性,6例患者仍在持续接受治疗。研究证实,艾伏尼布联合度伐利尤单抗及GC的毒性谱与既往各报道一致,安全性可控,并确定以艾伏尼布500mg QD为推荐剂量,扩展阶段预计招募40例患者7。这项研究提示,艾伏尼布联合免疫和化疗有望为IDH1突变BTC患者的治疗提供新选择。此外,一项多中心、前瞻性、Ⅱ期临床试验,评估了替雷利珠单抗联合仑伐替尼和吉西他滨+奥沙利铂(GEMOX)化疗在不可切除胆道癌患者中的疗效与安全性,结果显示,中位随访至19.5个月时,总人群的R0切除率为63%,客观缓解率(ORR)为49%,疾病控制率(DCR)为90%。该研究证实,"靶向+免疫+化疗"的三联方案在胆道癌中具有一定的应用潜力,为局部晚期胆道癌提供了一种潜在可行的转化治疗方案8。

艾伏尼布在IDH1野生型BTC中可逆转化疗耐药,增强抗肿瘤效果
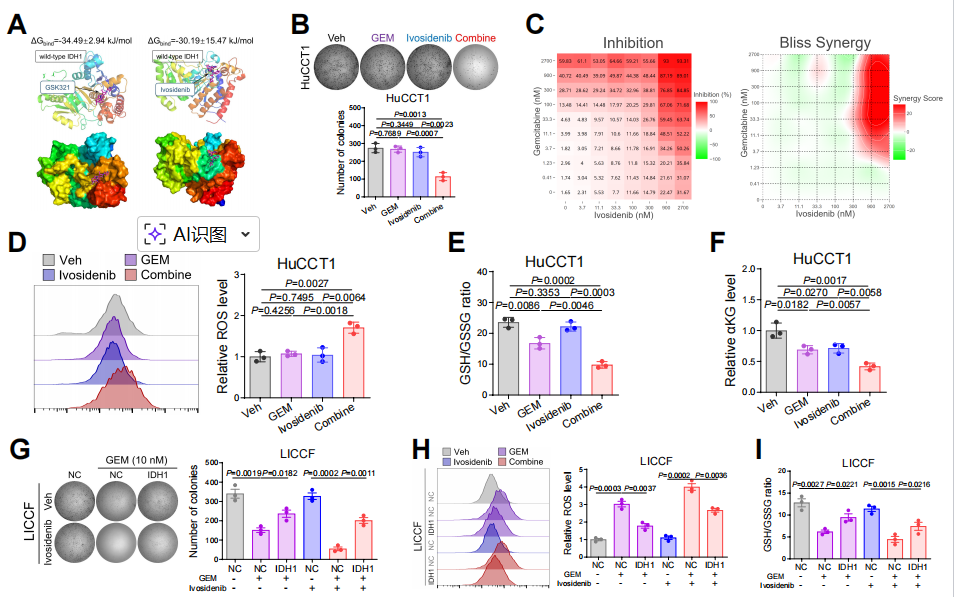
作为全球首个获批的IDH1抑制剂,艾伏尼布已在IDH1突变型BTC的治疗中展现出明确的临床获益,而最新的基础研究进一步拓展了其临床应用边界,证实其在IDH1野生型(wt-IDH1)BTC中同样具有重要的治疗价值9。
2026年3月,中山大学研究团队在《Journal of Clinical Investigation》发表的一项重磅研究,深入探索了艾伏尼布在wt-IDH1肝内胆管癌中的抗肿瘤作用与机制。研究结果显示,在wt-IDH1肝内胆管癌的临床前模型中,艾伏尼布可逆转wt-IDH1介导的吉西他滨化疗耐药性,并显著增强吉西他滨的抗肿瘤效果9,为其在更广泛BTC人群中的应用提供了坚实的理论依据。
该研究进一步证实,艾伏尼布可直接与wt-IDH1的催化结构域稳定结合,对wt-IDH1具有抑制作用。在携带wt-IDH1的模型中,wt-IDH1可催化异柠檬酸氧化,生成α-酮戊二酸与还原型烟酰胺腺嘌呤二核苷酸磷酸(NADPH),从而中和吉西他滨诱导的氧化应激,维持细胞氧化还原稳态,最终导致肿瘤细胞对吉西他滨产生化疗耐药性。值得关注的是,艾伏尼布在生理条件下可通过加剧细胞内氧化应激,在wt-IDH1肝内胆管癌临床前模型中,与吉西他滨展现出协同抗肿瘤活性。尤为关键的是,研究证实,肝内胆管癌肿瘤微环境中存在低水平的镁离子,这一特征为艾伏尼布在肝内胆管癌患者中拓宽治疗窗口提供了生理基础:镁离子会与艾伏尼布竞争性结合wt-IDH1的变构口袋,高水平镁离子环境下会阻碍艾伏尼布的结合与抑制作用,而肝内胆管癌因肿瘤组织血供差、营养灌注不足,其肿瘤微环境内游离镁离子水平显著低于外周血与正常肝组织、胆管组织,这一特性使得艾伏尼布可在肿瘤组织内有效抑制wt-IDH1,发挥抗肿瘤作用,同时在镁离子水平较高的正常组织中,不影响细胞的正常生理功能,在保障疗效的同时兼具良好的安全性9。
专家点评
唐腾骞教授:
长期以来,BTC的治疗始终面临着手术切除机会少、复发率高、患者长期生存获益有限等多重困境。近年来,随着精准诊疗理念的普及与临床研究的深入,BTC的诊疗格局正在发生深刻变革。
2023版CSCO胆道癌指南率先提出的“边界可切除”BTC的概念,不仅规范了BTC中可切除、不可切除和边界可切除的评估标准,更为围手术期治疗的应用划定了清晰的人群范围。而如何为这部分患者选择高效、安全的新辅助/转化治疗方案,正是当前临床研究的重要方向。
免疫联合化疗虽然为晚期BTC带来了生存获益的改善,但其提升幅度仍不尽如人意,主要原因在于BTC特有的“冷肿瘤”免疫微环境与高度异质性。因此,基于靶点的精准靶向药物联合免疫、化疗的三联方案,成为突破当前治疗瓶颈的核心思路。IDH1是BTC的重要驱动靶点,艾伏尼布作为高选择性IDH1抑制剂,已在临床研究中证实了其联合免疫和化疗的抗肿瘤活性,为IDH1突变BTC患者提供了重要的治疗选择。
值得关注的是,最新的临床前研究证实,艾伏尼布在wt-IDH1 BTC中可逆转化疗耐药,增强化疗药物的抗肿瘤疗效,这一发现打破了IDH1抑制剂适用人群的固有认知,拓展了其临床应用前景。这意味着,艾伏尼布有望不再局限于IDH1突变的人群,而是成为BTC联合治疗方案中的重要组成部分,为更多BTC患者带来生存获益。
小结
BTC的诊疗已进入精准分层与联合治疗的新时代,《中国临床肿瘤学会(CSCO)胆道恶性肿瘤诊疗指南(2023版)》提出边界可切除BTC的概念,为新辅助治疗和转化治疗的应用奠定了基础;而以艾伏尼布为代表的精准靶向药物的研发与临床探索,则为突破BTC治疗瓶颈提供了动力。从IDH1突变人群中靶免联合化疗的三联方案的抗肿瘤活性,到IDH1野生型人群中逆转化疗耐药,与化疗协同增效的突破性发现,艾伏尼布凭借其精准的靶点调控与免疫微环境重塑作用,不断拓宽自身的临床应用边界,为BTC患者的治疗提供了更多优选方案。
未来,随着临床研究的不断深入与诊疗体系的持续完善,以靶向药物为核心的精准联合治疗方案,将为更多BTC患者点燃长期生存的希望,推动我国BTC诊疗水平的进一步提升。
肝胆外科 副主任医师、副教授、医学博士
国际肝胆胰协会中国分会胆道肿瘤专委会委员
国际肝胆胰协会中国分会肝胆胰MDT专委会委员
中国临床肿瘤学会(CSCO)胆道肿瘤专委会委员
中国医师协会外科医师分会胆道外科青年专家委员会副主任委员
中国医师协会外科医师分会肝胆青年专家工作组专家委员
中国医师协会肝癌专业委员会青年工作组委员
中华医学会消化内镜学分会胆囊协作组委员
重庆市外科学会肝胆胰临床研究专委会副主任委员
重庆市抗癌协会肿瘤内镜学专业委员会委员
重庆市医学会肿瘤MDT专委会委员兼肝胆胰肿瘤学组顾问
重庆市医学会肝胆胰外科分会胆道外科学组委员
重庆市医学会肝胆胰外科分会内镜外科学组委员兼秘书
1. 李鑫, 敖建阳, 王敬晗, 等. 胆道恶性肿瘤的免疫治疗现状及研究进展[J]. 临床肝胆病杂志, 2025, 41(12): 2447-2452
2. 李相成,黄彬,长江.晚期胆道恶性肿瘤免疫与靶向治疗的现状与进展[J].中华消化外科杂志,2025,24(7):832-839.
3. 蓝晨露,曾智明,朱广志,等. 胆道恶性肿瘤新辅助治疗和转化治疗的临床研究进展[J]. 中华外科杂志,2025,63(10):904-910.
4. 陈诗雨,吴向嵩,龚伟. 胆道恶性肿瘤围手术期化疗及联合治疗策略的进展[J]. 中国实用外科杂志,2025,45(7):835-840.
5. 中国临床肿瘤学会指南工作委员会. 中国临床肿瘤学会(CSCO)胆道恶性肿瘤诊疗指南[M]. 北京:人民卫生出版社,2023.
6. 余立钦,王坚.靶免时代胆道恶性肿瘤治疗的困境与希望[J].腹部外科,2026,39(1):17-23.
7. Do-Youn Oh, et al. 2026 AS0O GI. abstract 558.
8. Shi G, et al. Conversion therapy of tislelizumab plus lenvatinib and GEMOX in unresectable locally advanced biliary tract cancer (ZSAB-TransGOLP): a multicentre, prospective, phase 2 study. Lancet Oncol. 2025 Oct;26(10):1334-1345.
9. Li X, et al. The allosteric IDH1 inhibitor ivosidenib overcomes chemoresistance in intrahepatic cholangiocarcinoma models expressing wild-type IDH1. J Clin Invest. 2026 Mar 17:e199730.
免责声明:
本资料的内容仅作为科学信息参考,仅用于医疗卫生专业人士的学术交流,请勿用于任何其他用途。若您不是医疗卫生专业人士,请勿观看和/或传播此资料。
本资料可能会出现某些药品信息,但该药品/适应症可能尚未获得国家药品监督管理局的注册批准。医疗卫生专业人士做出的任何与治疗有关的决定应根据患者的具体情况并应参照国家药品监督管理局批准的药品说明书。对于本资料可能提到的相关诊断、治疗方法,请遵守国家卫生健康委员会以及相关部门批准使用的指南或规定。
审批号:M-TIBS0-CN-202604-00009











 苏公网安备32059002004080号
苏公网安备32059002004080号


