
本次分享的文章于2025年12月发表在Cancer Letters(Q1/1区,IF 10.1),题目为“Updated Clinical practice guidelines for the management of adult diffuse gliomas”,本指南由 中国脑胶质瘤协作组(CGCG) 、 中国神经肿瘤学会(SNO-China) 与 中国脑胶质瘤协会(CBCA) 联合委员会组织制定。在编撰过程中,国内外同行专家对指南全文进行了严格的审阅与修订。该指南系统检索了自1990年1月1日起发表的英文文献,文献检索截止于 2025年1月 。本次指南更新积极纳入并评估了最新的高级别循证医学证据,特别是近年来在胶质瘤分子机制与治疗领域的重要发现。
第一部分 背景
新版中国脑胶质瘤诊疗指南,紧跟国际新分类,为临床治疗提供新依据, 其逻辑如下:
背景与动因 :WHO在2021年更新了中枢神经系统肿瘤分类,对常见的成人弥漫性胶质瘤进行了分子层面的简化分型(分为3种主要亚型)。 指南行动 :为跟进这一国际更新,中国的三大专业学术组织联合制定了新版《胶质瘤临床实践指南》。 指南内容 :指南聚焦于 分子与病理诊断 ,以及 手术、放疗、化疗和靶向治疗 等核心治疗手段,并纳入了前沿的新疗法临床试验成果。 目标与意义 :旨在为相关医疗专业人员提供实用指导,并为医保等机构在费用管理方面提供知识依据,服务于中国乃至全球的医疗实践。
简单来说 :国际分类变了(为什么做)→ 所以我们更新了指南(做了什么)→ 指南涵盖了诊断与治疗的关键内容(内容是什么)→ 希望指导临床并影响医疗决策(目的是什么)
第二部分 流行病学与生存状况
一、流行病学核心数据
全球与中国现状 :脑肿瘤是全球重要疾病负担。 中国是发病与死亡率最高的三个国家之一 。2022年,中国估计新增恶性脑肿瘤约8.75万例,死亡约5.66万例。 胶质瘤地位 :是 最常见 的原发性恶性脑肿瘤,全球年发病率约5-6/10万人。 性别差异 :男性发病率约为女性的 1.5-1.6倍 。
二、主要生存影响因素
经典预后因素 :患者年龄、体能状态、肿瘤恶性程度、手术切除范围是明确的预后指标。 分级与生存 :肿瘤分级是生存的关键决定因素。数据中位总生存期(OS)分别为:WHO 2级(78.1个月)、3级(37.6个月)、4级(14.4个月),级别越高,生存期越短。 分子标志物 :IDH1/2突变、1p/19q共缺失和MGMT启动子甲基化等 分子特征对预后有极大影响 ,通常预示着更有利的预后。
结论 :本节通过宏观流行病学数据定位了疾病负担,并明确了影响患者生存的 临床 与 分子 两大层面的关键因素,为后续诊断和治疗决策的讨论奠定了基础。
第三部分 影像诊断
一、检查手段与价值
CT与MRI 是常规影像工具。 MRI优于CT ,能提供更详细的解剖、肿瘤形态与功能信息。 CT作用 :快速显示钙化、出血、囊变等 结构特征 。 MRI核心 :常规序列(T1、T2、FLAIR、增强)显示肿瘤 位置、信号、边界、水肿及强化模式 ,是诊断基础。
二、高低级别胶质瘤的影像特征对比
| 特征 | 低级别胶质瘤 | 高级别胶质瘤 |
|---|---|---|
| 信号与边界 | ||
| 水肿与占位效应 | ||
| 内部结构 | ||
| 强化特点 |
三、多模态MRI的功能与价值
功能评估 : DWI高信号 → 提示细胞密度高( 高级别 特征)。 PWI高灌注 → 提示血流量增加( 高级别 特征)。 MRS(Cho↑,Cho/NAA↑) → 与肿瘤级别 正相关 。 手术规划关键 : DTI 与 BOLD-fMRI 能清晰显示肿瘤与 重要功能区及纤维束 的关系,为 手术保护脑功能 提供直接依据。
总结 :影像诊断的核心是 通过常规MRI初步判断级别,利用多模态MRI进行功能评估与手术规划 。它为后续的病理与分子诊断提供定位依据,并直接指导治疗策略(尤其是手术)的制定。
第四部分 核心分子标志物
本节强调,现代胶质瘤诊断已从 单纯看病理切片 ,升级为 结合分子特征进行精准分型 。以下是关键标志物及其核心用途:
一、诊断与分型的“基石”标志物 这类标志物是 确定肿瘤类型 的核心依据。
IDH1/2突变 :成人型弥漫性胶质瘤的 核心分类标志 。存在突变即可归类为预后相对较好的“IDH突变型”肿瘤。 1p/19q共缺失 :在IDH突变的基础上,若存在共缺失,则确诊为 少突胶质细胞瘤 ;若不存在,则指向 星形细胞瘤 。 ATRX缺失/TP53突变 :是IDH突变型 星形细胞瘤 的特征,可用于辅助诊断及鉴别。
二、用于分级与判定恶性的标志物 在确定类型后,这些标志物帮助判断肿瘤的恶性程度。
CDKN2A/B纯合缺失 :在IDH突变型星形细胞瘤和少突胶质细胞瘤中,是提示 高级别(4级) 的关键分子指标。 TERT启动子突变、+7/-10、EGFR扩增 :对于IDH野生型肿瘤,即使病理切片未看到典型高级别特征,只要存在其中之一,即可诊断为 胶质母细胞瘤 。它们是“分子层面”的恶性证据。
三、指导治疗与预后的“实用”标志物 这类标志物直接关联治疗方案选择和疗效预测。
MGMT启动子甲基化 :最重要的 疗效预测标志物 。甲基化阳性的胶质母细胞瘤患者对 替莫唑胺化疗更敏感 ,预后更好。 EGFRvIII突变 :是 潜在的靶向治疗靶点 ,见于部分胶质母细胞瘤。 MET变异/融合 :在特定亚型(如婴儿型)中用于诊断,在IDH突变型星形细胞瘤中提示预后较差,且是 靶向药 的潜在作用靶点。 PTEN突变/缺失、+7/-10 :在IDH野生型胶质瘤中,提示 预后不良 。
总结逻辑 :分子诊断遵循 “先分型,再分级,后定策” 的路径:
分型 :用IDH、1p/19q、ATRX/TP53确定基本类型。 分级 :用CDKN2A/B、TERT等判断恶性级别。 定策 :依据MGMT、EGFR、MET等制定个体化治疗方案并预测预后。
第五部分 整合病理诊断
一、核心理念 诊断已从 传统形态学 转向 “组织学 + 分子表型”的整合诊断 。2021年WHO第5版分类是当前诊断的核心依据。
二、诊断路径(逻辑树)
第一步:两大分类 成人型弥漫性胶质瘤 (主要见于成人,儿童亦可发生) 儿童型弥漫性胶质瘤 (主要见于儿童,青少年/年轻成人亦可发生) 第二步:成人型诊断流程(核心看IDH) 具有 坏死或微血管增生 的典型病理特征 → 胶质母细胞瘤,IDH野生型 。
即使缺乏上述典型特征,只要存在 TERT启动子突变、EGFR扩增、+7/-10 任一分子特征 → 同样可诊断为 胶质母细胞瘤,IDH野生型 。
伴 1p/19q共缺失 → 少突胶质细胞瘤,IDH突变型
无1p/19q共缺失,但有 ATRX突变/缺失 → 星形细胞瘤,IDH突变型
分级关键 :对于IDH突变型星形细胞瘤,出现 坏死/微血管增生 或 CDKN2A/B纯合缺失 → 即可诊断为 4级 。
第三步:儿童型诊断特点(更复杂,核心看分子) 低级别 :主要特征为 MYB/MYBL1改变 或 MAPK通路基因 (如BRAF, FGFR1)改变。 高级别 :主要特征为 组蛋白H3突变 (如H3 K27突变见于中线,H3 G34突变见于大脑半球)。 对于 IDH与H3均为野生型 的高级别肿瘤(多见于婴幼儿/儿童/青年),需依据其他分子改变(如MET)和甲基化谱进一步分型。
三、病理报告规范 报告必须采用 标准化、分层式 格式,整合以下四要素:
整合诊断 (最终诊断) 组织学分型 CNS WHO分级 分子信息 (包括检测方法与具体变异)
总结 :本节描绘了清晰的诊断决策树。其核心逻辑是 先通过IDH状态区分成人型与儿童型主线,再依据特定分子标记进行精准分型与分级 ,最终生成一份整合了所有关键信息的标准化报告。这确保了诊断的精确性和治疗指导的有效性。
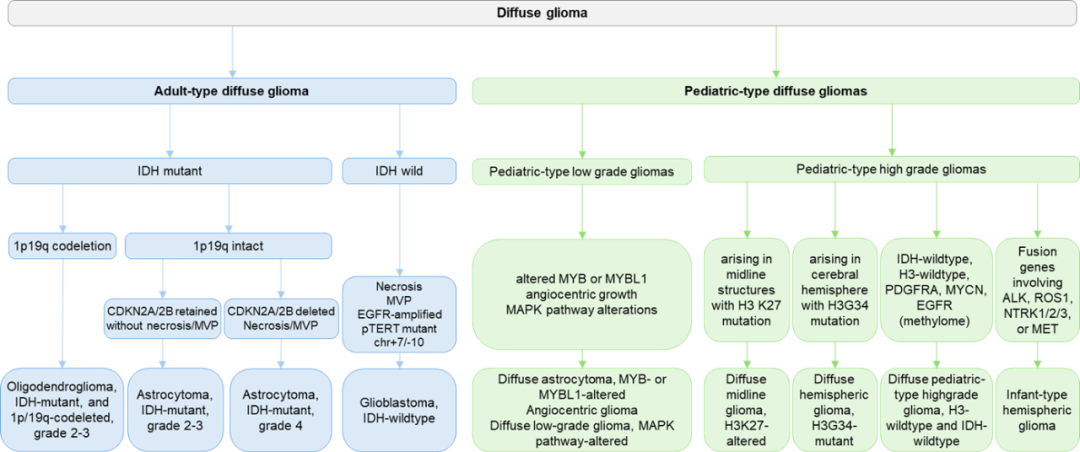
图1 弥漫胶质瘤的分类
第六部分:疾病管理
本节是全指南的 核心实践部分 ,系统构建了从治疗决策到随访评估的完整临床路径。
一、 总体原则:精准整合决策
治疗必须基于 多学科整合策略 ,核心决策依据是两大支柱:
患者因素 :年龄、体能状态(KPS评分)。 肿瘤因素 : 分子病理特征 (IDH、1p/19q等)是最关键的预后和治疗预测指标。
二、 核心支柱一:神经外科手术
目标 : 最大范围安全切除 ,在保护功能的前提下尽可能切除肿瘤。
术前 :标准MRI评估。功能区肿瘤必须进行 神经心理及功能磁共振 评估,为手术“导航”。 术中 :运用 神经导航、术中MRI、5-ALA荧光 等辅助技术,以提升切除率、降低损伤。 术后 : 48-72小时内 行MRI评估切除范围。 分子指导 :切除策略因分型而异(如少突胶质细胞瘤需积极全切),但 底线是绝不能牺牲神经功能 。
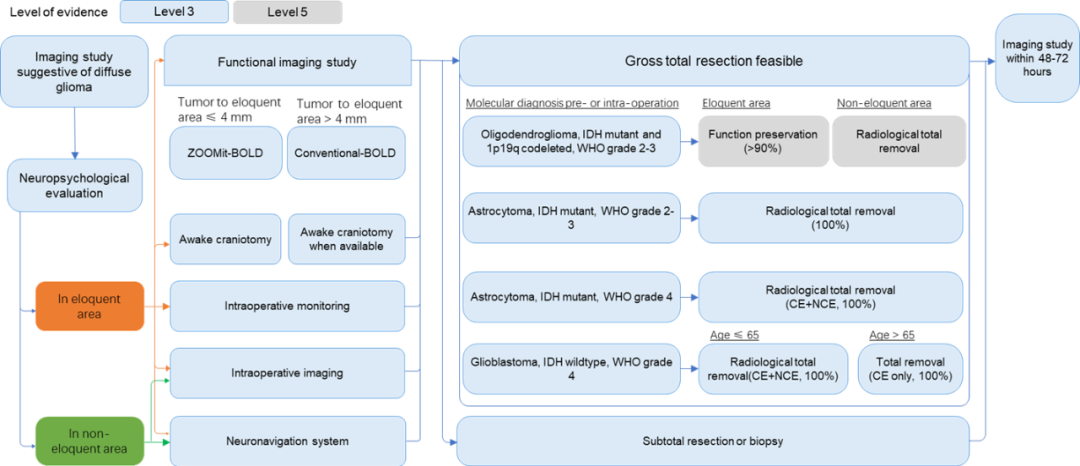
图2 弥漫胶质瘤的外科治疗策略
三、 核心支柱二:基于新分类的辅助治疗
辅助治疗(放疗/化疗/靶向)方案完全由 肿瘤的分子分型与分级 决定,并需结合患者的 体能状态(KPS评分) 进行个体化调整。
1. 少突胶质细胞瘤(IDH突变,1p/19q共缺失)
2级肿瘤 :若全切且患者状态良好(KPS≥60),可采取 “观察等待” 策略。对于未全切或存在其他高风险因素者,推荐 标准放疗联合辅助化疗 (PCV方案或TMZ)。 IDH抑制剂 对残留或复发的2级肿瘤显示出治疗潜力。 3级肿瘤 : 标准方案为放疗联合PCV化疗 (PCV疗效证据更充分)。放疗联合TMZ是备选方案。对于体能状态较差者(KPS<60),可采用 短程放疗±TMZ 。
2. 星形细胞瘤(IDH突变)
2级肿瘤 :治疗策略与同级少突胶质细胞瘤类似。全切且状态佳者可观察;高风险或残留者推荐 放疗联合辅助化疗 (PCV或TMZ)。 IDH抑制剂 同样是重要选择。 3级与4级肿瘤 : 标准治疗为放疗联合替莫唑胺 。对于4级肿瘤, 放疗同步并辅助TMZ联合肿瘤电场治疗 是备选强化方案。 关键提示 :一旦出现 坏死/微血管增生 或 CDKN2A/B纯合缺失 ,即应按4级方案治疗。
3. 胶质母细胞瘤(IDH野生型)
标准治疗 :即 Stupp方案 (最大安全切除后,进行 放疗同步并辅助TMZ化疗 )。 老年/体弱患者 :可采用 短程放疗(40Gy/15次)± TMZ ,尤其在MGMT启动子未甲基化时。 重要进展 :在Stupp方案基础上,联合 肿瘤电场治疗 已成为新的标准治疗之一,可进一步延长生存期。
总体原则 :
积极治疗 :适用于分子分型预后较好(如IDH突变)或肿瘤级别高,且患者体能状态良好(KPS≥60)的情况。 缓和方案 :对于体能状态较差(KPS<60)的患者,核心目标是控制肿瘤、维持生活质量,常采用 短程放疗±化疗 或最佳支持治疗。 治疗强度 遵循 “分型定方向,分级定强度,体能定耐受” 的决策逻辑。
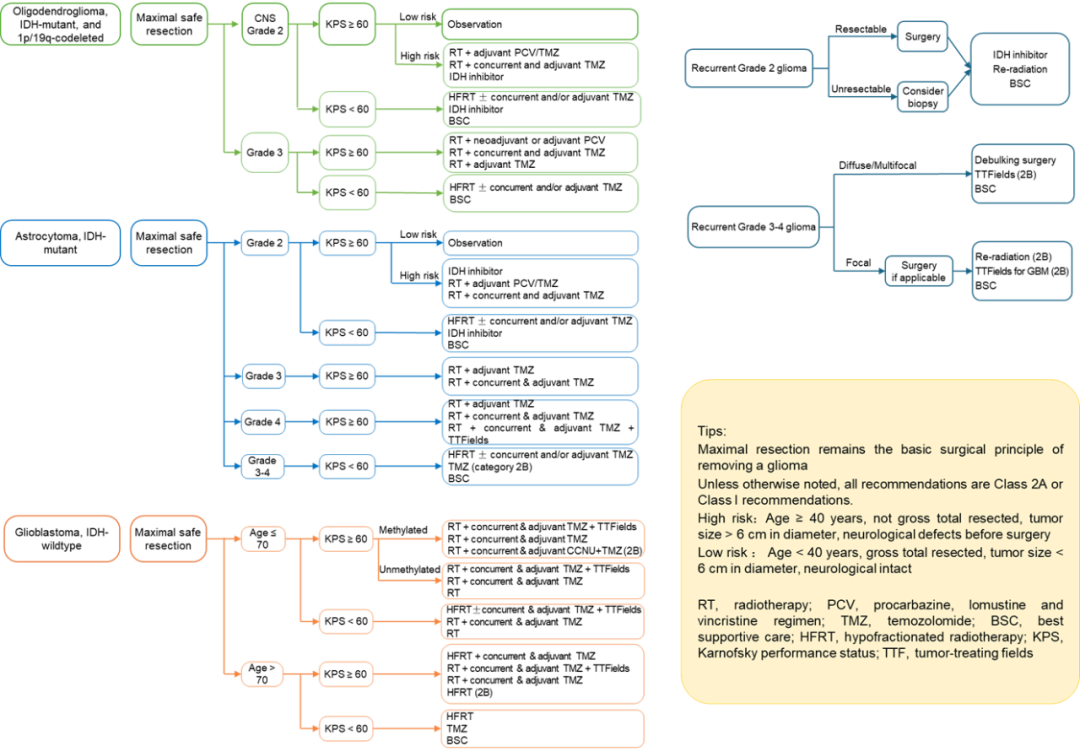
图3 弥漫胶质瘤的辅助治疗
四、 肿瘤复发/进展的治疗
原则 :无标准方案,需个体化选择。 选项 : 再次手术 (适用于局灶性复发)、 再次放疗 (需间隔12个月以上且病灶在原野外)、 系统治疗 (换用洛莫司汀、贝伐珠单抗等)。
五、 贯穿始终的支持治疗
癫痫 :长期治疗首选 左乙拉西坦 。不推荐无癫痫史者常规预防用药。 水肿 :类固醇应 最低剂量、最短疗程 使用,并尽快减停,以减少感染、高血糖等副作用。 血栓 :患者为高危人群,确诊后需 长期抗凝 (通常用低分子肝素)。 康复与姑息 :强烈推荐早期整合 认知康复 与姑息治疗,管理症状,提高生活质量。
六、 疗效评估与随访
标准 :采用 RANO 2.0标准 。 关键变化 : 放疗后MRI 定为评估基线(而非术后MRI)。 随访 :治疗后每 3-6个月 复查MRI。 两大难点 :
总结 :“疾病管理”部分构建了一个 “以分子分型为纲、以患者状态为目”的精准整合治疗体系 ,并强调了支持治疗和精准评估在全程管理中的核心地位。
第七部分:新型疗法解读
本节概述了超越传统放化疗的三大前沿方向:靶向治疗、IDH抑制与免疫治疗。
一、 分子靶向治疗:精准打击,方兴未艾
现状 :尽管大量药物在研发,但能成功应用于临床的仍属少数。核心挑战是单一靶向药难以显著延长总生存期。 主要方向 :
FGFR融合 :见于部分IDH野生型胶质瘤。早期临床试验显示靶向药对特定患者有持续疾病控制作用。 MET融合 :是重要治疗靶点。 伯瑞替尼 已在中国获批,用于治疗携带PTPRZ1-MET融合的复发IDH突变型4级星形细胞瘤,临床试验显示其能显著降低死亡风险。 贝伐珠单抗 :用于复发胶质母细胞瘤,主要价值在于 短期控制症状、减轻水肿和激素依赖 ,虽延长无进展生存期,但未显著改善总生存。 瑞戈非尼 :在复发胶质母细胞瘤中显示出优于传统化疗的生存获益。
前景 :靶向治疗未来的希望在于与标准治疗联合的 多模式治疗 策略。
二、 IDH靶向治疗:变革低级别胶质瘤的治疗范式
原理 :直接针对IDH突变这一驱动基因,抑制其异常代谢产物。 重大突破 :针对残留/复发的2级IDH突变型胶质瘤,III期临床试验证实 伏西地尼 能 显著延长无进展生存期、推迟下次干预时间,并更好地控制癫痫 ,且不影响生活质量与认知。 结论 :IDH抑制剂已成为此类患者 早期干预 的重要推荐,尤其对于高风险患者。
三、 免疫治疗:积极探索,尚未破局
现状 :多种策略在胶质母细胞瘤中积极研究,但尚未确立标准疗法。 主要策略 : 1. 疫苗 :以树突状细胞疫苗为代表,最新研究显示在标准治疗基础上加用可延长生存。 2. 溶瘤病毒 :通过激活免疫系统攻击肿瘤,早期临床试验显示出希望。 3. 免疫检查点抑制剂 :在胶质瘤中疗效有限。 术前新辅助使用 (即手术前用药)是当前有潜力的探索方向。 4. CAR-T细胞疗法 : 最具前景 的策略之一。已证实CAR-T细胞能浸润肿瘤并产生持续抗肿瘤反应。当前研究重点在于寻找最佳靶点、克服抗原逃逸(如双靶点CAR-T),以及与其它疗法联合。 未来方向 :核心在于 不同免疫疗法的联合 ,或 免疫与放化疗的联合 ,以期产生协同效应。
总结 :新型疗法正从不同角度改写胶质瘤的治疗格局。其中, IDH抑制剂已确立其在低级别突变型肿瘤中的治疗地位;靶向MET融合的药物已获批应用;而CAR-T等免疫疗法则代表了最具潜力的未来方向 。
参考文献
Jiang T, Nam DH, Ram Z, et al. Updated Clinical practice guidelines for the management of adult diffuse gliomas. Cancer Lett . Published online December 1, 2025. doi:10.1016/j.canlet.2025.218185











 苏公网安备32059002004080号
苏公网安备32059002004080号


