液态活检技术,尤其是循环肿瘤DNA(ctDNA)检测技术的突破性进展,正重塑实体肿瘤精准诊疗的整体格局。然而,在以高侵袭性、高异质性为特征的三阴性乳腺癌(TNBC)领域,ctDNA技术的临床转化始终面临技术可行性与临床证据支撑的双重挑战。近日,《Clinical Cancer Research》期刊公布了TRICIA试验的核心研究成果。该研究聚焦新辅助化疗(NAC)后未达到病理完全缓解(non-pCR)的高危TNBC人群,借助自主研发的肿瘤知情微滴式数字PCR(ddPCR)技术,对患者手术前后及卡培他滨辅助治疗全周期进行了连续ctDNA动态追踪。作为目前针对该特定人群规模最大的ctDNA动态监测队列研究之一,TRICIA试验系统性验证了ctDNA在复发风险分层与疗效监测中的临床应用价值,为乳腺癌辅助治疗的精准升降阶梯决策提供了明确的科学依据。

研究背景
三阴性乳腺癌因缺乏雌激素受体、孕激素受体及人表皮生长因子受体2(HER2)的表达,化疗长期以来是其核心治疗手段。在早期TNBC的规范化治疗中,新辅助化疗(NAC)为首选方案,但约50%的患者术后仍存在残留肿瘤病灶(non-pCR)。此类患者预后不佳,约35%会在术后两年内出现疾病复发。
针对这一临床痛点,经典CREATE-X试验已证实,对non-pCR患者在术后使用卡培他滨辅助化疗可改善其无病生存期。但该标准治疗方案存在显著的过度治疗问题:仅约15%的患者能真正从卡培他滨治疗中获益,其余85%的患者在承受手足综合征等严重化疗毒副作用后,并未获得生存获益。目前临床中广泛依赖的残余肿瘤负荷(RCB)评分,仅能静态评估手术切除时的局部病灶范围,无法精准区分哪些患者体内仍存在微小残留病变(MRD)并最终导致复发。
尽管ctDNA被认为是检测MRD的有效工具,但TNBC领域仍存在显著的科学空白。其一,针对non-pCR这一超高危人群,NAC结束后、术前这一关键时间点的ctDNA预后价值缺乏大样本独立验证;其二,在卡培他滨辅助治疗全程,ctDNA的动态演变规律及其与药物疗效的关联缺乏系统性研究数据;其三,TNBC存在极高的基因突变异质性(除TP53外极少有共性突变),当前固定基因检测极易出现漏检,临床亟需兼具高灵敏度与高适配性的个性化检测方案。
研究方法
TRICIA是一项在加拿大三家医疗中心开展的多中心真实世界队列研究,共纳入92例经标准新辅助化疗后证实为non-pCR的TNBC患者。为系统评估ctDNA的临床价值,研究设定了四个核心采血时间点:T1(NAC结束后/手术前)、T2(术后早期/辅助治疗启动前)、T3(卡培他滨治疗期间)及T4(术后晚期/辅助治疗结束后)。
在检测技术层面,研究团队在学术医院实验室内自主研发了一套肿瘤知情定制化ddPCR检测方案。首先对每位患者切除的肿瘤组织进行全外显子测序(WES),结合外周血白细胞测序结果剔除克隆性造血相关干扰,随后为每位患者精准筛选出5个专属的体细胞突变位点(共设计467个突变靶点,92%的靶点基因为该患者专属)。在仅提取2mL血浆游离DNA的基础上,增加一轮靶向预扩增步骤,再上机进行ddPCR检测。该策略有效克服了TNBC高异质性导致的漏检风险,在变异等位基因频率(VAF)≥0.1%的区间内实现了97%的检测敏感性和99%的特异性。
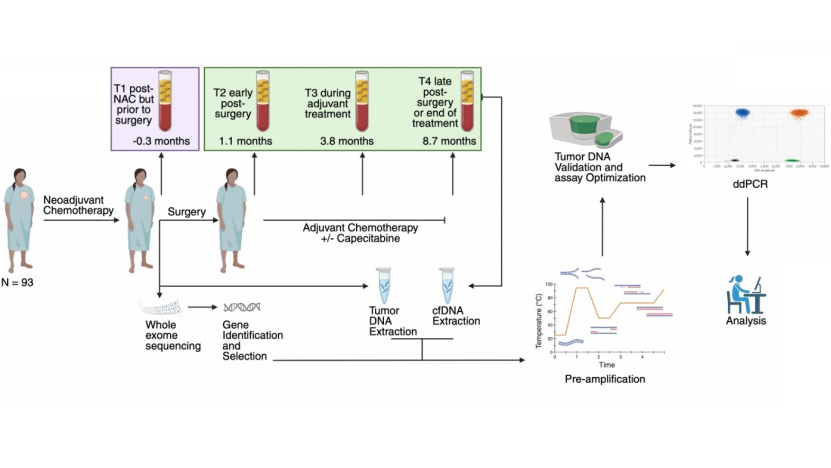
研究结果
通过对262份血浆样本的系统性追踪与分析,研究全面证实了ctDNA在non-pCR TNBC患者中的临床价值:
1. T1时间点(NAC后/术前)ctDNA检测具备极强的预后分层能力
在64份T1时间点检测样本中,ctDNA阳性患者的复发率达64%,而ctDNA阴性患者仅为5%(P<0.001)。该时间点对复发预测的敏感性为97%、特异性为54%、阴性预测值(NPV)高达95%(图2)。生存数据分析显示,T1 ctDNA阴性患者的5年无复发生存率(RFS)和总生存率(OS)均达95%(死亡风险降低94%,HR=0.06,P=0.0001);而ctDNA阳性患者的5年OS仅为35%。
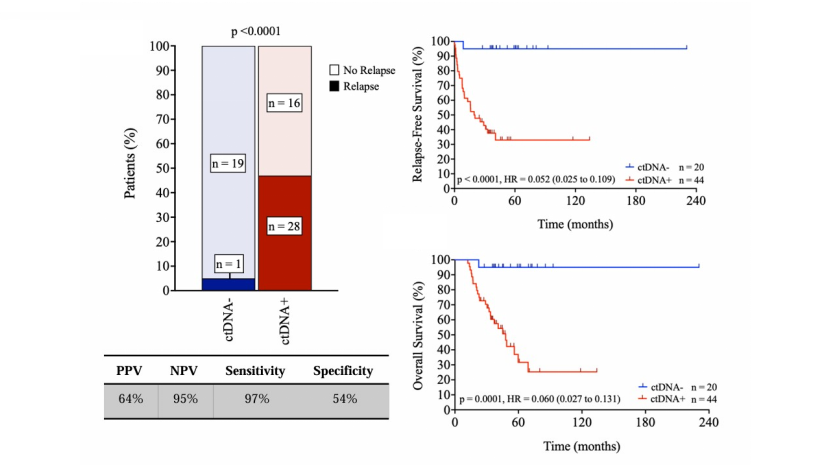
2. ctDNA可在RCB评分基础上进一步精准分层中高危
患者在预后最差的RCB 3级(广泛残留病变)患者中,ctDNA检测效能达100%:所有T1 ctDNA阳性患者均出现复发,所有ctDNA阴性患者均无病生存。在合并分析RCB 2级和RCB 3级患者时,T1 ctDNA阴性患者的5年OS为90%,而阳性患者仅为10%,证实ctDNA可有效识别残留病灶广泛但无生物学侵袭性的患者亚群。(图3)
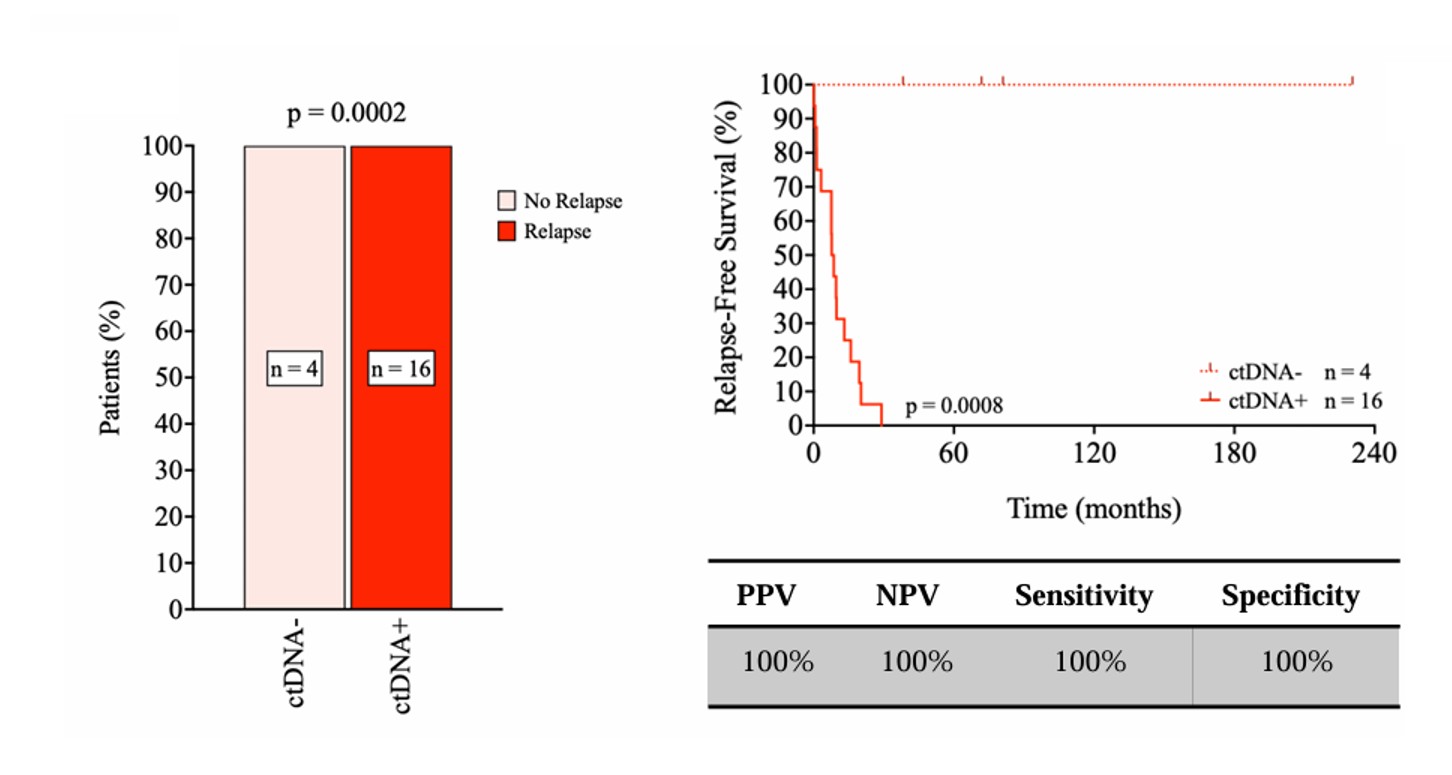
3. 手术可显著降低ctDNA水平,术后早期检测易受手术创伤干扰
在T1/T2配对样本分析中,术后ctDNA丰度较术前整体下降91%,下降幅度与RCB分级呈负相关。但研究同时发现,手术创伤会导致正常组织释放大量游离DNA(cfDNA),稀释原本低丰度的ctDNA信号,致使术后早期(T2)ctDNA检测的灵敏度和预测效能均弱于T1时间点。
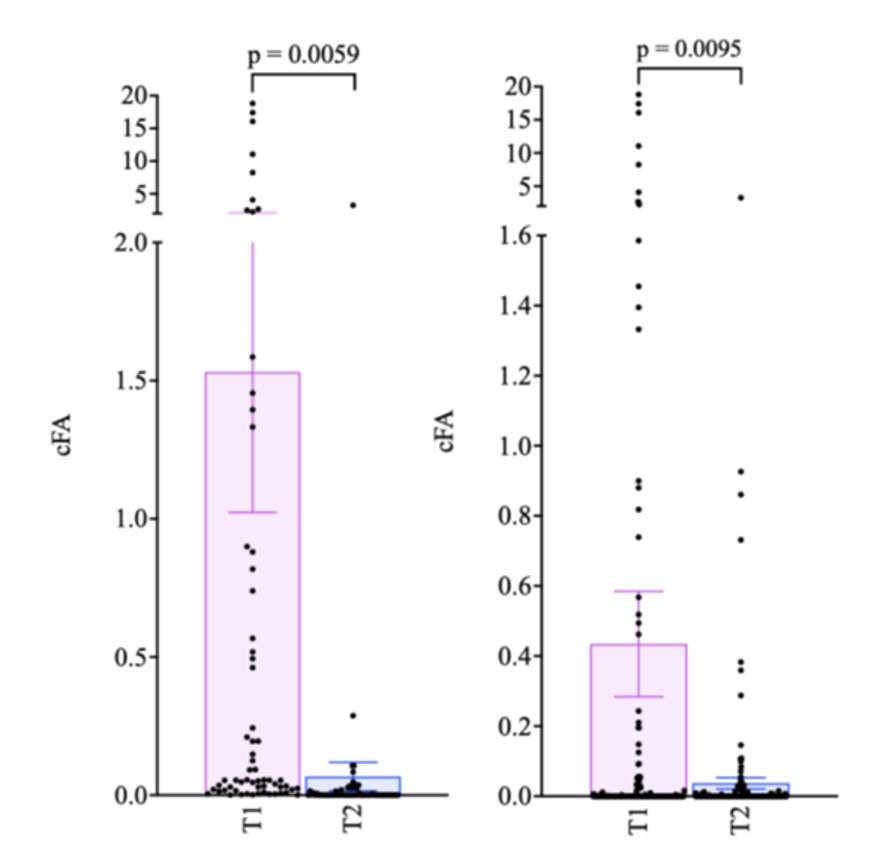
4. 术后ctDNA可提前12个月预测复发,辅助治疗后(T4)检测价值最高
术后任意时间点ctDNA阳性对复发预测的敏感性达92%,且较临床复发中位提前12个月检出,为临床早期干预提供了关键窗口期。在术后各时间点中,T4(辅助治疗结束后)的预后评估价值最强:ctDNA阳性患者复发率为36%,阴性患者仅11%;且T4 ctDNA阴性患者的5年OS达100%。在整个随访周期中,97%的复发患者在临床确诊复发前均可检测到ctDNA阳性。
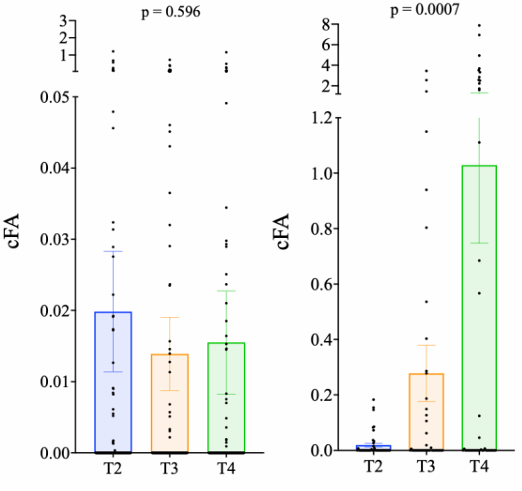
5. ctDNA状态是non-pCR TNBC患者最强的独立预后因素
多因素Cox回归分析显示,在校正RCB评分、是否接受卡培他滨辅助治疗等变量后,T1时间点ctDNA阳性是患者复发的最强独立预后因素(HR=24.7,95%CI 3.20-191.34,P=0.002)。
6. 卡培他滨可诱导ctDNA清除,清除状态与良好预后高度相关
在T2 ctDNA阳性的患者中,接受卡培他滨治疗的患者有41%在T4时间点实现ctDNA完全清除,而未接受该药物治疗的患者清除率仅9%(P<0.0001)。从预后角度看,卡培他滨治疗后实现ctDNA清除的患者复发率仅15%,5年OS达100%(图6);而ctDNA持续阳性的患者复发率为37%,5年OS仅52%。在未实现ctDNA清除的患者中,最终复发者的ctDNA丰度在治疗期间呈持续显著升高趋势。
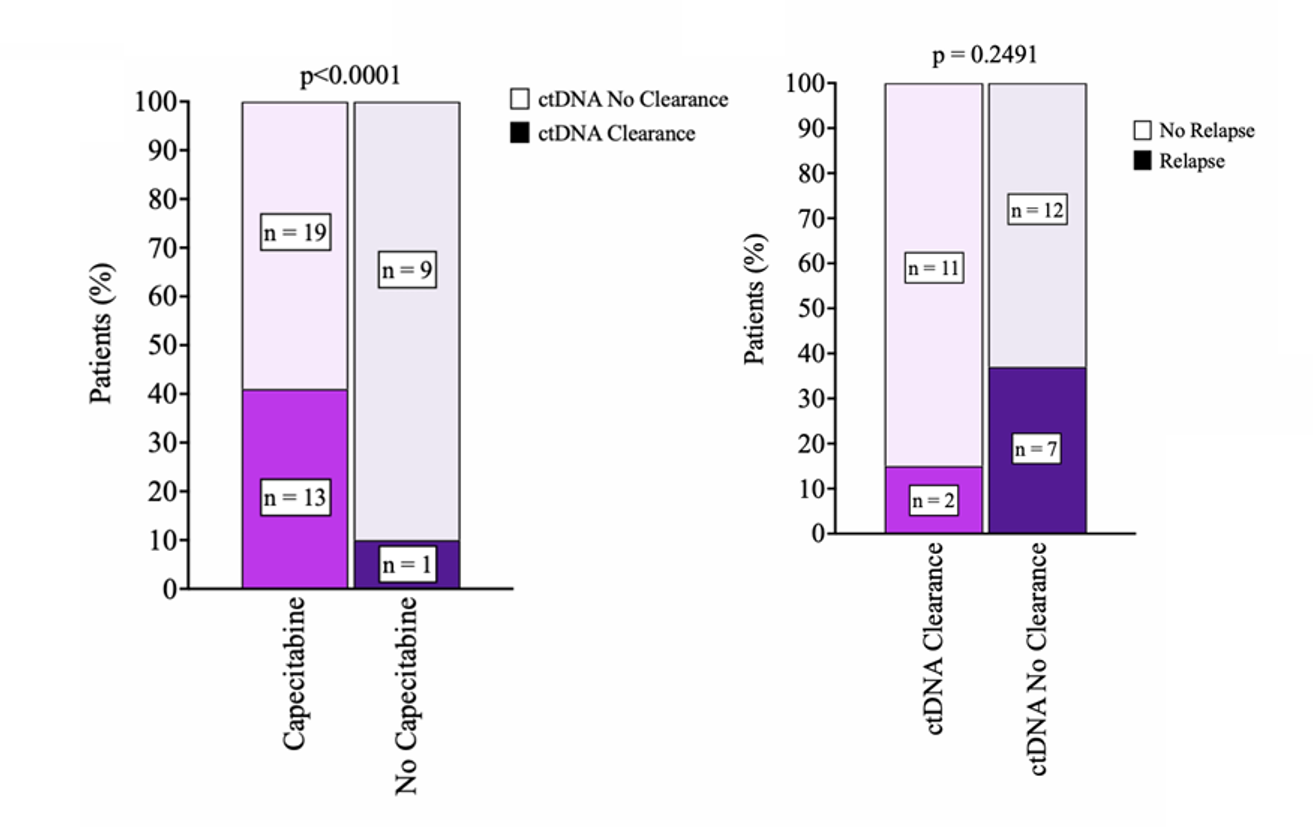
讨论
TRICIA试验的研究结果为优化TNBC临床治疗路径提供了直接依据,解决了长期以来non-pCR患者辅助治疗过度与疗效不足并存的临床痛点。
在临床决策层面,该研究为辅助治疗的降阶梯策略提供了循证医学证据。鉴于T1 ctDNA阴性的non-pCR患者复发风险极低(阴性预测值达95%),该部分患者未来有望豁免卡培他滨辅助化疗,从而避免85%无法获益的患者承受严重的药物毒性。同时,对于T1 ctDNA阳性、尤其是RCB 2/3级的患者,其极高的复发风险提示需进一步采取治疗升阶梯策略。此外,ctDNA的动态清除轨迹可作为卡培他滨辅助治疗疗效的早期替代终点,助力临床医生尽早评估治疗有效性,为治疗无效的患者及时更换其他治疗方案提供决策依据。
在技术层面,该研究验证了一套可落地且性价比高的个体化ctDNA检测方案。TNBC缺乏高频复发突变,商业化固定基因检测的漏检风险较高(既往研究显示其在同类人群中的敏感性仅约60%)。该研究采用的“定制化WES+靶向预扩增+5个突变位点ddPCR”模式,不仅将检测敏感性提升至97%,且单患者四个时间点的检测总成本控制在约4500美元,检测周期缩短至6-7周,高度契合临床常规应用需求。
尽管该研究成果显著,但仍存在一定局限性:其一,肿瘤知情检测策略无法识别治疗压力下新进化的耐药克隆突变;其二,预扩增步骤在提升极低丰度ctDNA检出率的同时,可能引入微量聚合酶扩增错误,需在未来进一步优化阳性判定阈值;其三,该研究为观察性队列研究,虽证实了ctDNA的预后与监测价值,但未来仍需开展基于ctDNA状态指导治疗决策的前瞻性干预性随机对照试验,以最终确立其临床应用的标准。此外,未来还可探索将ctDNA动态变化与RCB评分、影像学特征及分子亚型深度整合,构建多维度联合预后模型。
小结
TRICIA试验首次系统性验证了基于靶向预扩增的个体化ddPCR ctDNA检测技术,在non-pCR三阴性乳腺癌患者全程治疗中的预后评估与疗效预测价值。该研究明确了新辅助化疗后至术前(T1)是预后评估的最佳窗口期,并证实辅助治疗期间ctDNA的动态清除状态可准确反映卡培他滨在体内的抗肿瘤活性。该研究为三阴性乳腺癌从标准化辅助治疗模式,向基于ctDNA指导的个体化精准治疗模式转变提供了高质量的临床证据。
Roseshter T, Klemantovich A, Lafleur J, et al. Clinical Validation of Digital PCR-based ctDNA detection for risk stratification in residual triple negative breast cancer: TRICIA trial results. Clin Cancer Res. Published online February 9, 2026.
排版编辑:肿瘤资讯-slb











 苏公网安备32059002004080号
苏公网安备32059002004080号


