混合表型急性白血病(MPAL)是一种罕见且高度侵袭性的白血病亚型,约占成人急性白血病的2%~5%。相较于急性淋巴细胞白血病(ALL)和急性髓系白血病(AML),MPAL患者的死亡风险分别高出59%和26%。由于高比例的不良细胞遗传学异常,成人MPAL的治疗选择仍十分有限。对于无法耐受标准化疗或无法接受异基因造血干细胞移植(allo-HSCT)的患者,预后较差。此外,多数非费城染色体阳性(Ph+)MPAL患者缺乏可靶向的基因突变,临床治疗中仍存在显著未满足的需求。
维奈克拉(Ven)作为一种BCL-2抑制剂,已在AML治疗中得到广泛应用。然而,其在MPAL中的应用仍以个案报告为主,尤其是在新发T/髓系MPAL中尚无相关记录。近期,河南省肿瘤医院魏旭东教授团队在Frontiers in Oncology发表了一项回顾性研究[1],分析了4例采用Ven联合去甲基化药物(HMAs)治疗的新发MPAL患者,所有患者均在单疗程治疗后达到完全缓解(CR)。【肿瘤资讯】现将核心内容整理如下,以期为临床提供参考。

病例1:合并新冠感染的T/髓系MPAL,Ven联合阿扎胞苷实现有效诱导缓解
患者为43岁男性,因乏力入院,血常规示白细胞(WBC)94.48×10⁹/L,血红蛋白(HGB)67g/L,血小板(PLT)151×10⁹/L,外周血原始细胞占85%。骨髓穿刺提示增生极度活跃,原始细胞占87.2%,免疫表型显示异常原始细胞占79.83%,表达HLA-DR、CD117等髓系及T系抗原,确诊为T/髓系MPAL。
入院时患者合并新型冠状病毒感染,伴持续高热及严重肺部感染,基础状况较差,无法耐受标准化疗(图1)。2023年7月27日起予VA方案(Ven每日递增至400mg,阿扎胞苷100mg d1~7)诱导治疗。第15天复查骨髓提示原始细胞降至10.5%,多参数流式细胞术(FCM)检测到可测量的微小残留病灶(MRD),其中异常原始细胞占4.9%。治疗期间合并持续高热、重症肺炎及胸腔积液,经积极抗感染及支持治疗后病情控制。
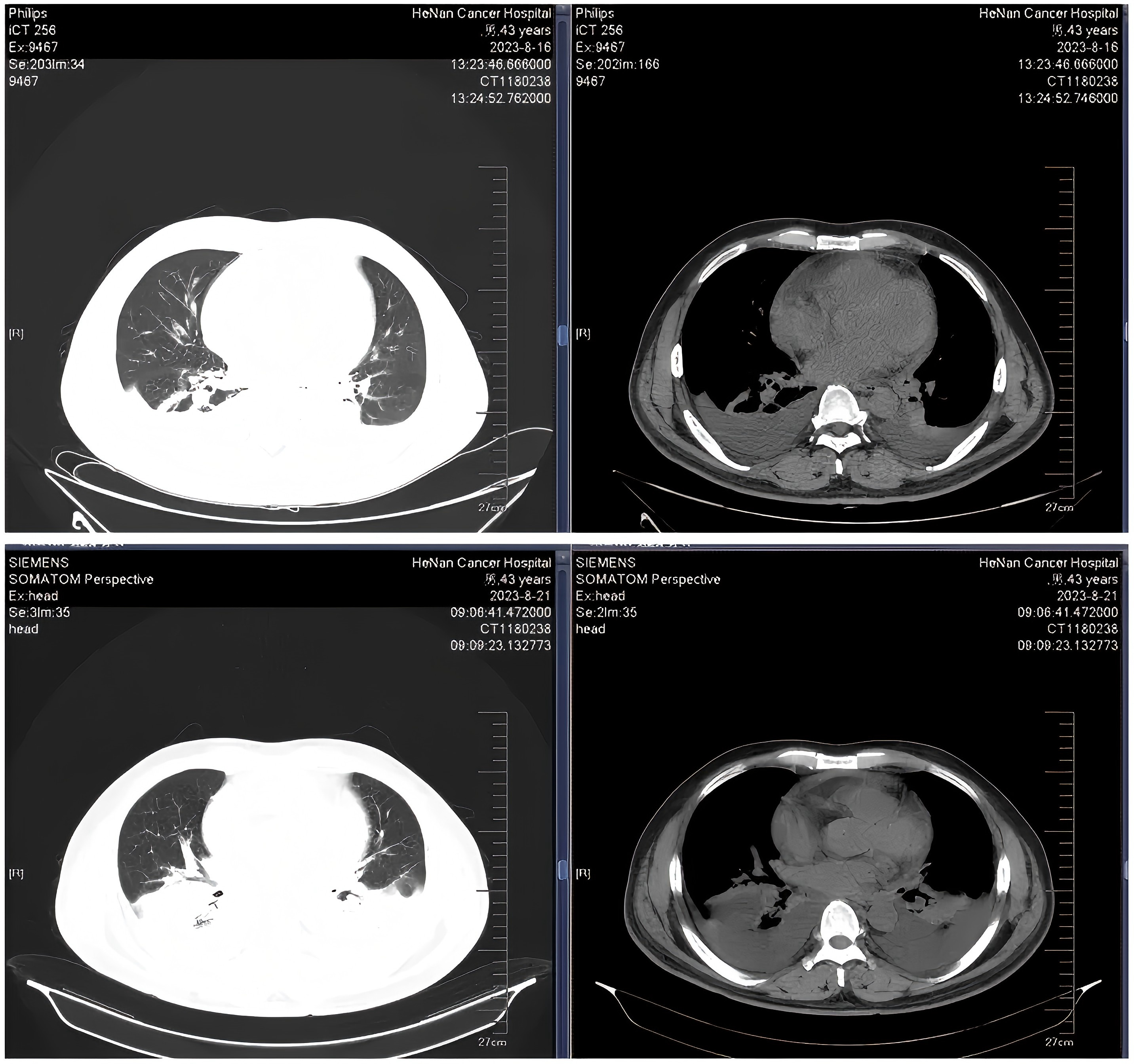
第29天骨髓检查提示CR,MRD阴性,基因检测未发现CEBPA基因突变。首个周期骨髓抑制持续26天。患者后续接受1周期VA方案巩固,并接受全相合亲缘供者allo-HSCT,但移植后2天因毛细血管渗漏综合征导致多器官功能衰竭去世(图2)。
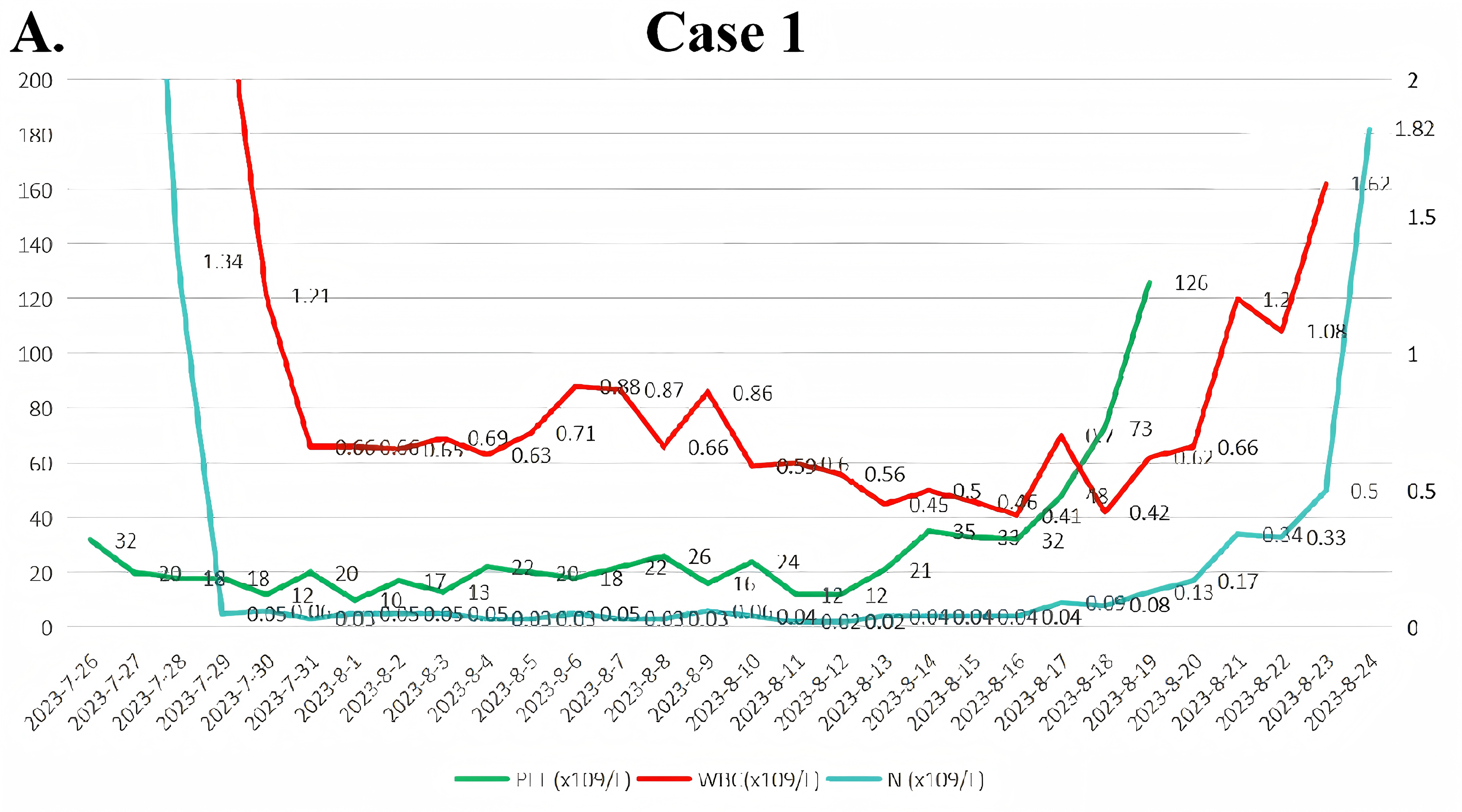
病例2:乳腺癌化疗后继发B/髓系MPAL,Ven联合地西他滨实现安全缓解
患者为51岁女性,有乳腺癌病史,曾接受多周期阿霉素联合环磷酰胺化疗。2024年5月因常规复查入院,血常规示WBC 1.57×10⁹/L,HGB 107g/L,PLT 160×10⁹/L,外周血原始细胞占3%。骨髓穿刺示原始细胞占60%,POX染色53%阳性,PAS染色88%阳性,免疫表型提示异常细胞占52.44%,兼具早期髓系和B淋系特征,确诊为B/髓系MPAL。
因既往多周期化疗史,患者拒绝强化疗,于2024年7月接受VD方案(Ven剂量递增至400mg,地西他滨25mg d1~10)诱导治疗。治疗期间仅出现短暂中性粒细胞减少伴发热,无明显不适。第22天骨髓检查示原始细胞0.6%,MRD示CD19异常表达的早期髓系细胞占0.02%,达到CR,首个周期骨髓抑制持续21天。
患者后续接受1周期VD方案巩固,因经济原因拒绝allo-HSCT,目前仍在规律巩固治疗中,总生存期(OS)已达16个月(图3)。
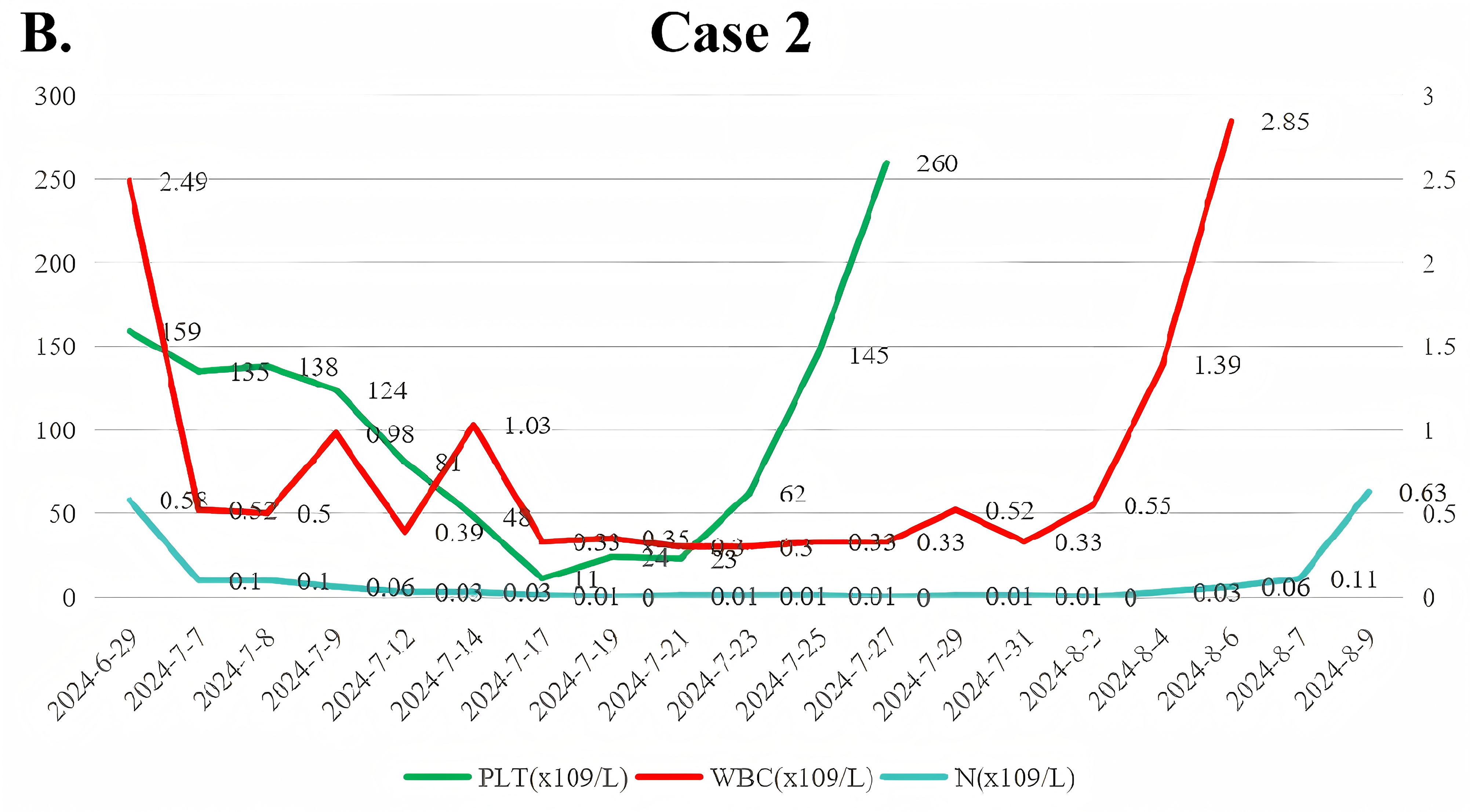
病例3:BCR::ABL1阳性B/髓系MPAL,三联方案实现分子学完全缓解并维持长期无病生存
患者为40岁女性,因白细胞增多就诊,外周血WBC 24.90×10⁹/L,HGB 127g/L,PLT 211×10⁹/L。外院骨髓示原始细胞占53.5%,入院后复查提示幼稚淋巴细胞占11.6%,原始+幼稚单核细胞占43.3%,免疫表型显示异常幼稚B淋巴细胞及髓系原始细胞分别占22.34%和11.6%,融合基因检测示BCR::ABL1(p190)阳性(18.88%),确诊为BCR::ABL1阳性B/髓系MPAL。
2023年9月起予奥雷巴替尼联合VA方案(Ven剂量同前,阿扎胞苷100mg d1~7,奥雷巴替尼40mg隔日口服)。治疗14天骨髓未见原始细胞,MRD示异常原始细胞0.25%,BCR::ABL1(p190)占6.85%;治疗28天BCR::ABL1(p190)降至3.39%,单疗程后达CR,MRD阴性且融合基因转阴,实现完全分子学缓解。
患者后续接受全相合亲缘供者allo-HSCT,目前移植后1年余,仍维持MRD阴性CR状态,OS已达25个月(图4)。
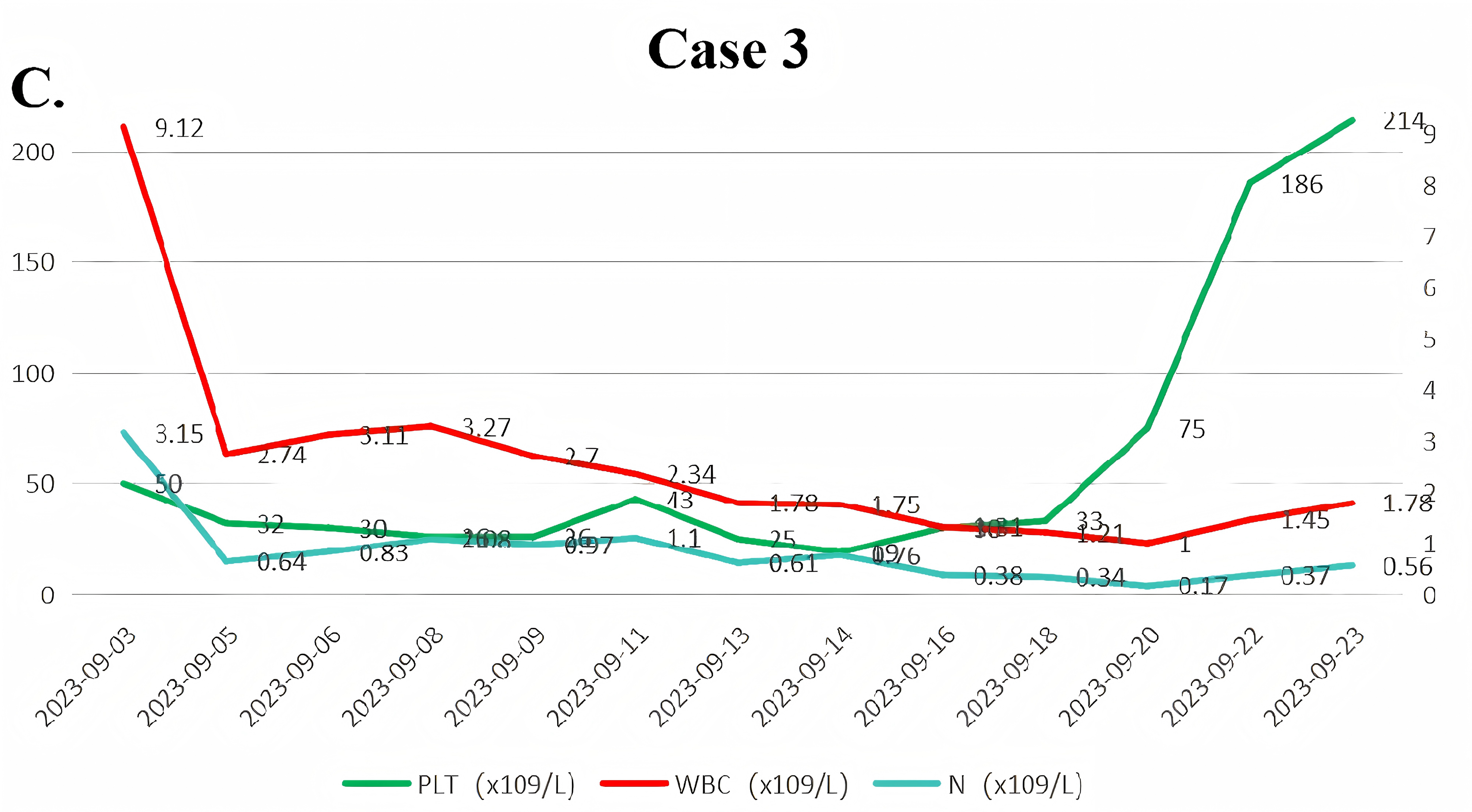
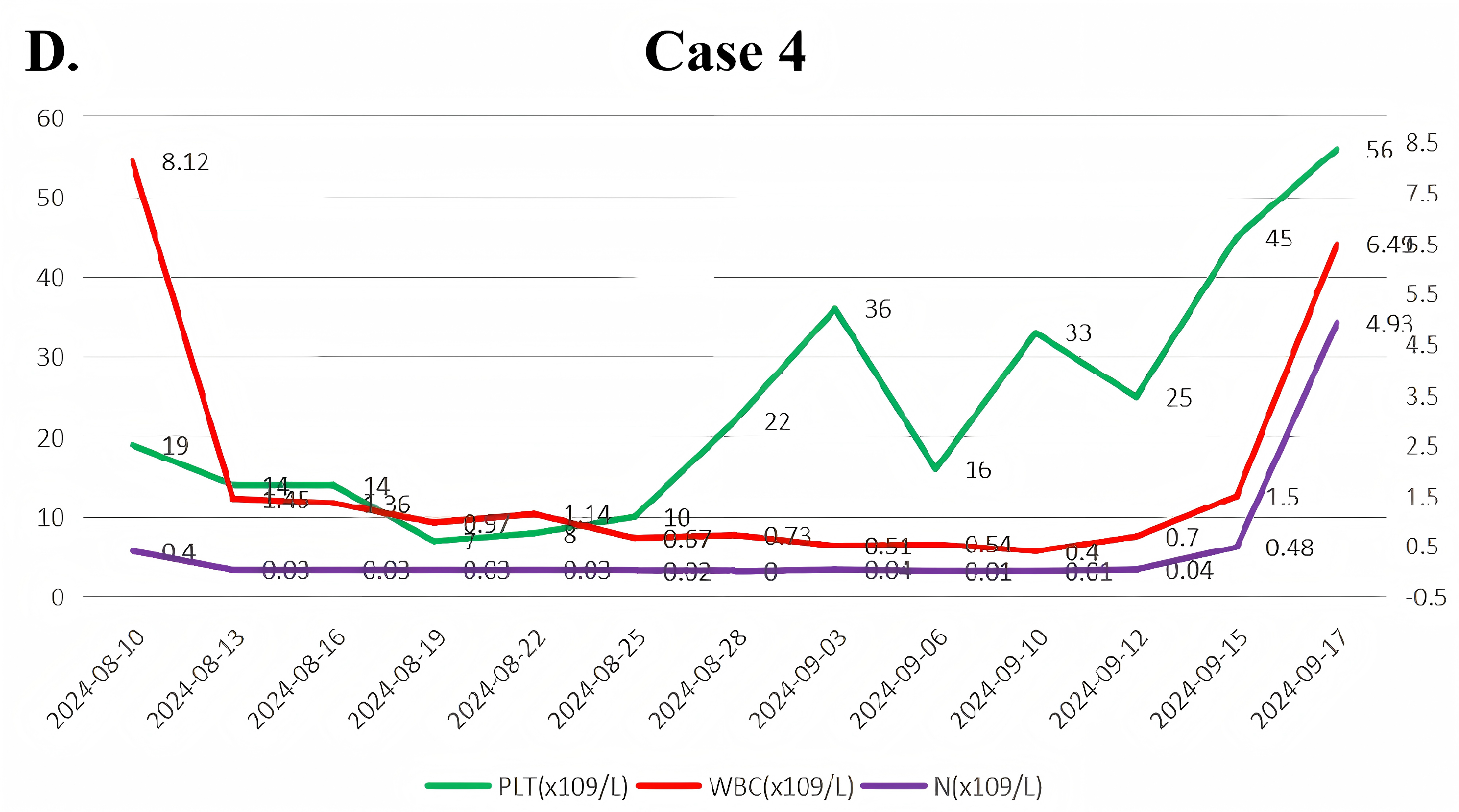
病例4:高龄B/髓系MPAL,个体化Ven联合方案实现持续缓解超12个月
患者为80岁男性,因全血细胞减少伴发热入院,血常规示WBC 1.99×10⁹/L,HGB 37g/L,PLT 6×10⁹/L,外周血原始细胞占45%。骨髓检查示原始细胞占78.4%,免疫表型提示髓系原始/幼稚细胞约占51.4%,幼稚B细胞前体占22.6%,伴TET2基因突变,确诊为B/髓系MPAL。
因高龄及家属拒绝化疗,于2024年8月起予个体化VA方案(Ven100mg d1~21,阿扎胞苷0.1g d1~5)诱导治疗。第16天骨髓示原始细胞17.2%,MRD示髓系原始/幼稚细胞2.4%、幼稚B细胞前体0.3%。首个周期骨髓抑制持续36天,为4例患者中最长,期间予抗感染及成分血输注支持。
2024年10月骨髓检查示原始细胞0.5%,造血恢复,达到CR。2024年11月复查MRD阴性。目前患者一般状况良好,已维持CR超12个月,并规律接受VA方案巩固治疗(Ven疗程缩短至10~14天)(图5)。
总结
该研究系统报告Ven联合HMAs在新发MPAL中的应用,纳入的4例患者涵盖T/髓系、B/髓系(含BCR::ABL1阳性)亚型,且均因合并新冠感染、既往化疗史或高龄等原因无法耐受标准化疗。所有患者在接受Ven联合阿扎胞苷/地西他滨(部分联合TKI)方案后,均于单疗程内达到CR,展现出较高的缓解率。
安全性方面,主要不良反应为骨髓抑制(中位持续26天,范围7~36天),病例1和病例4在骨髓抑制期合并感染,经积极治疗后控制;病例2和病例3耐受良好,未见严重不良事件。相较于传统强化疗方案,Ven联合HMAs展现出较好的安全性特征。尤其是病例4,通过个体化疗程调整,实现长期缓解,提示该方案在老年或脆弱人群中亦具可行性。
既往MPAL治疗多借鉴ALL或AML方案,虽ALL样诱导方案缓解率较高,但复发风险高,长期生存率低;混合方案则因毒性叠加而预后更差。维奈克拉作为BCL-2抑制剂,在AML和ALL中均显示出良好活性,其与HMAs的协同作用为MPAL治疗提供了新思路。该研究进一步验证了该组合在MPAL中的有效性,包括此前未见报道的新发T/髓系MPAL。
未来应开展更多前瞻性研究,以明确该方案的最佳用药剂量、疗程安排,及其与allo-HSCT、其他靶向药物的联合策略,进一步优化MPAL治疗体系,改善患者预后。
关于维奈克拉联合去甲基化药物治疗新发混合表型急性白血病(MPAL)的临床应用,下列哪项叙述最正确?
A.该方案仅适用于B/髓系MPAL,对T/髓系MPAL无治疗效果
B.合并BCR::ABL1阳性的MPAL患者,需联合酪氨酸激酶抑制剂才能实现完全缓解
C.对于高龄MPAL患者,可通过缩短维奈克拉疗程实现疗效与耐受性的平衡D.该方案治疗后骨髓抑制持续时间均超30天,且易引发无法控制的严重感染
上一期《【寻根溯源】腮腺肿胀背后的“伪装者”——套细胞淋巴瘤病例分享》的答案为C。
[1] Mi R, Guo S, Yang W, et al. Case Report: Venetoclax combined with hypomethylating agents for the treatment of newly diagnosed with mixed-phenotype acute leukemia and a literature review[J]. Front Oncol, 2025,15:1693061.
排版编辑:Grady











 苏公网安备32059002004080号
苏公网安备32059002004080号


