近日,2026年美国临床肿瘤学会泌尿生殖系统肿瘤研讨会(ASCO GU)召开,液体活检技术再次成为焦点。随着分子生物学检测技术的迭代,循环肿瘤DNA(ctDNA)已从单纯的预后生物标志物,逐渐演变为能够指导临床决策的关键工具。与此同时,尿液肿瘤DNA(utDNA)作为一种无创的新兴标志物,展现出了与ctDNA互补的独特优势。
本文将结合会议公布的三项重磅研究——IMvigor011、NIAGARA及HCRN GU 20-444的最新数据,探讨液体活检如何重新定义MIBC的临床管理路径。
Abs 633:ctDNA指导的阿替利珠单抗辅助治疗MIBC:IMvigor011试验中ctDNA动力学的探索性分析
第一作者:Thomas Powles,巴茨癌症研究所,国家健康研究院生物医学研究中心
研究背景
在随机、双盲的III期IMvigor011试验(NCT04660344)中,对于MIBC患者,在根治性膀胱切除术(RC)后,与安慰剂相比,采用ctDNA指导的辅助阿替利珠单抗治疗在研究者评估的无病生存期(INV-DFS)和总生存期(OS)方面均带来了统计学上显著的改善。阿替利珠单抗组中,在第3周期(C3)或第5周期(C5)实现ctDNA清除的患者比例更高;而安慰剂组中所有实现ctDNA清除的患者,其基线ctDNA浓度均较低(Powles, 新英格兰医学杂志 2025)。本文报告了在监测期间ctDNA阳性(+)患者的ctDNA出现时间和浓度,以及随机化患者的治疗中ctDNA动力学(包括与临床结局的相关性)的探索性分析。
研究方法
在RC术后6-24周内,纳入无影像学疾病证据的MIBC患者进入监测阶段。在RC术后一年内,每6周进行一次连续的ctDNA监测,每12周进行一次影像学检查。在任何时间点检测为ctDNA阳性的患者,均被筛选进入治疗阶段。符合条件的患者按2:1的比例随机分配接受阿替利珠单抗或安慰剂治疗,每4周一次,共12个周期或最多1年。在监测期间检测为ctDNA阳性的所有患者(n = 379)中,评估了首次出现ctDNA阳性的时间和基线ctDNA浓度;在未接受积极辅助治疗的患者(n = 212)中,评估了其与INV-DFS的相关性。在接受至少1剂阿替利珠单抗(n = 165)或安慰剂(n = 83)的患者中,评估了治疗期间的ctDNA动力学,包括其与INV-DFS和OS的关联。
研究结果
在监测期间检测为ctDNA阳性的患者中,首次阳性检测时的ctDNA浓度范围为0.01-613.8平均肿瘤分子数/mL(中位数,0.27平均肿瘤分子数/mL)。大多数患者(n = 281,74.1%)在RC术后24周内检测为ctDNA阳性。早期ctDNA阳性和较高的基线ctDNA浓度与RC术后更高的肿瘤分期和/或淋巴结阳性状态,以及更短的INV-DFS相关。晚期ctDNA阳性与较低的基线ctDNA浓度相关(R = -0.28;P< 0.001)。在随机化患者中,阿替利珠单抗使ctDNA水平在C1至C3期间下降(log2倍数变化 -0.4),而安慰剂组则升高(log2倍数变化 0.5;Wilcoxon检验 P= 0.009)。在C3或C5时实现ctDNA清除与改善的DFS和OS相关;阿替利珠单抗治疗组患者的DFS率和OS率数值上更高。
研究结论
对于大多数通过RC术后连续ctDNA监测被识别为ctDNA阳性的患者,其阳性结果在≤24周内即可显现。早期阳性和高基线浓度是负性预后因素。阿替利珠单抗治疗阻止了在安慰剂组中观察到的ctDNA水平快速升高,并提高了ctDNA清除率,这与更优的临床结局相关。
表 基于C3或C5 ctDNA清除状态的DFS和OS
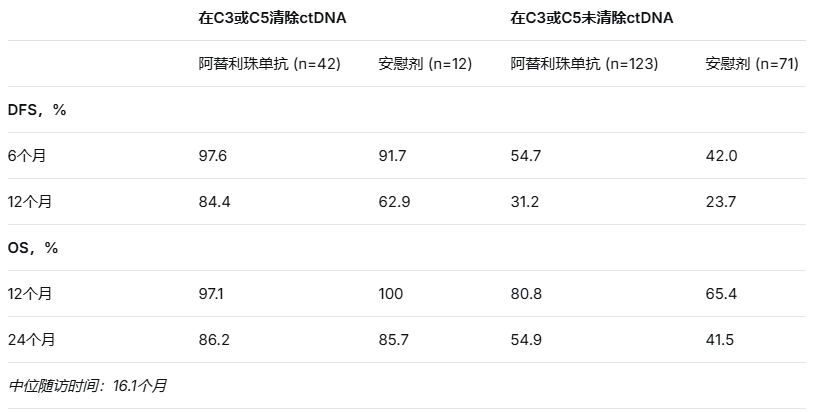
Abs 636:NIAGARA研究中接受度伐利尤单抗围手术期治疗的MIBC患者的utDNA和ctDNA分析
第一作者:Michiel S. Van Der Heijden,荷兰阿姆斯特丹,荷兰癌症研究所
研究背景
在NIAGARA研究(NCT03732677)中,对于MIBC患者,在新辅助化疗(NAC)和根治性膀胱切除术(RC)的基础上增加围手术期度伐利尤单抗治疗,与单独使用NAC和RC相比,显著改善了无事件生存期(EFS)和总生存期,并提高了病理学完全缓解(pCR)率(数值上)。在先前的一项探索性分析中,新辅助治疗后、RC术前(pre-RC)的血浆ctDNA阴性状态与延长的EFS相关,但与pCR无关。本文在此背景下评估utDNA作为补充方法的价值。
研究方法
符合顺铂治疗条件的MIBC患者(cT2-T4aN0/1M0)按1:1的比例随机分配接受围手术期度伐利尤单抗联合NAC(顺铂+吉西他滨)和RC(D组),或仅接受NAC和RC(对照组[C组])。双重主要终点是EFS和pCR。使用个体化检测系统(Natera, Inc, Austin, TX, USA)在基线(BL;n=205)和RC术前(pre-RC;n=183)完成了utDNA和ctDNA的探索性分析。
研究结果
在1063名患者中,265名(25%)构成了生物标志物可评估人群(BEP;D组134名;C组131名)。在基线时,较低的utDNA水平与较长的EFS相关(低utDNA vs 高utDNA HR 0.65,95% CI 0.40-1.04)。从基线到RC术前,utDNA阳性率从85%下降到55%。utDNA清除与更长的EFS相关(HR 0.24,95% CI 0.09-0.62),且D组的utDNA清除率比C组高12%(39% vs 27%)。RC术前utDNA状态与pCR相关(utDNA阴性;72% [55/76] vs utDNA阳性;18% [17/96])。RC术前utDNA和ctDNA状态与RC术后的疾病分期呈现不同的相关性,utDNA阳性与非肌层浸润性疾病(<T2N0M0)相关,而ctDNA阳性与肌层浸润性疾病(≥T2N0M0)或全身性播散(N+和/或M+)相关(见表)。RC术前双重阴性的患者(utDNA阴性 ctDNA阴性)估计24个月EFS率最高(90%,95% CI 83-97),其次是仅utDNA阳性的患者(utDNA阳性 ctDNA阴性;75%,95% CI 65-87),而双重阳性的患者(utDNA阳性 ctDNA阳性)EFS率最低(55%,95% CI 41-75)。
研究结论
分析表明,较低的基线水平和RC术前utDNA的清除与更好的EFS相关,并且显示在NAC基础上增加度伐利尤单抗可提高utDNA清除率。与先前关于ctDNA状态的研究结果相比,RC术前utDNA状态与pCR的相关性更密切。结合RC术前ctDNA和utDNA分析与EFS相关,并可能为RC术后的疾病分期提供互补信息。utDNA状态可以提供关于原发膀胱肿瘤的临床相关信息,特别是在ctDNA阴性的患者中,这凸显了联合utDNA和ctDNA为未来MIBC的管理提供信息的潜在价值。
表 RC术前utDNA和ctDNA与RC术后疾病分期的相关性
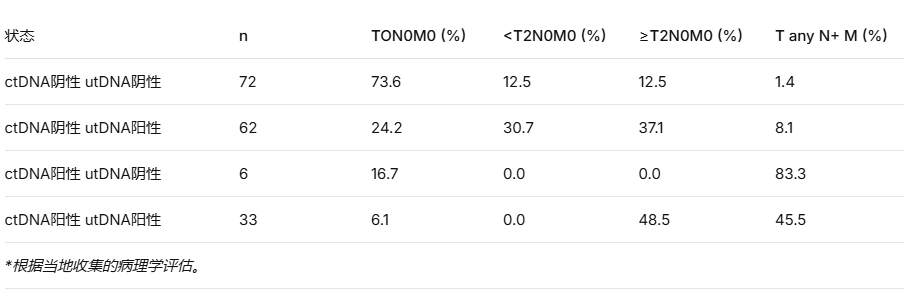
Abs 737:帕博利珠单抗联合基于疗效评估的膀胱保留疗法治疗MIBC的II期试验(HCRN GU 20-444)
第一作者:Jonathan F. Anker,美国纽约,西奈山蒂施癌症中心
研究背景
许多MIBC患者不适合进行根治性膀胱切除术(RC)和/或倾向于保留膀胱的替代方案。在TURBT后进行新辅助化疗(NAC)可使一部分患者达到病理学完全缓解(pCR),这表明并非所有患者都需要RC才能实现治愈。我们之前的研究表明,TURBT后接着进行基于顺铂的NAC联合PD-1阻断,可使43%的患者达到严格定义的临床完全缓解(cCR),并且此类患者中约2/3避免了立即行RC,获得了持久的保留膀胱生存期(Galsky, Nat Med, 2023)。然而,约50%的MIBC患者不适合顺铂治疗,且新辅助PD-1阻断单药治疗可产生30-40%的pCR率。HCRN GU 20-444评估了对MIBC患者进行TURBT后,使用帕博利珠单抗单药治疗并依据反应指导保留膀胱策略的疗效。
研究方法
符合条件的患者为cT2-3N0M0期尿路上皮癌,且拒绝或不适合顺铂治疗。在最大程度TURBT后,患者接受2个周期帕博利珠单抗治疗(每6周给药一次),随后通过MRI/CT、尿液细胞学和膀胱镜检查(含活检)进行临床再分期。达到cCR的患者省略确定性局部治疗,并接受最多7个额外周期的帕博利珠单抗治疗。未达到cCR的患者接受确定性局部治疗(RC或放化疗)。通过肿瘤和血浆的全基因组测序结合基于人工智能的模式识别,对ctDNA进行连续评估,以超灵敏检测残留病灶。主要终点是cCR率。关键的次要和探索性终点包括2年无转移生存期(MFS)、总生存期(OS)和ctDNA状态。
研究结果
从2022年7月至2024年12月,共入组46名患者;中位年龄为74岁(24%的患者年龄≥80岁)。cCR率为43%(95% CI 29% - 59%)。中位随访时间为11个月(范围2.4-33.5个月)。在达到cCR的患者中,所有患者均未行立即RC,且均未出现转移性疾病;1/20的患者因新发前列腺癌接受了延迟性膀胱前列腺切除术(膀胱癌病理分期pT0N0);2/20的患者因非癌症原因死亡。不良事件与帕博利珠单抗的毒性特征一致。在达到cCR和未达到cCR的患者中,第1周期(C1)ctDNA不可检出率分别为90%和55%(Mann-Whitney检验 P = 0.01)。C1 ctDNA不可检出与改善的MFS(HR 11.2,95% CI 2.2-57,log-rank检验 P = 0.0003)和OS(HR 11.4,95% CI 1.3-103,P = 0.007)相关。在达到cCR的患者中,第2周期(C2)ctDNA不可检出率为100%。在未达到cCR的患者中,C2 ctDNA不可检出与改善的MFS相关(HR 14.8,95% CI 1.4-2000,P = 0.02)。
研究结论
对于达到严格定义cCR的患者,TURBT联合帕博利珠单抗单药治疗可带来有前景的保留膀胱无转移生存期。在C1或C2时ctDNA不可检出的患者,即使省略RC,其发生转移性复发的风险也极低。仅6周帕博利珠单抗治疗后的ctDNA状态即可区分未达到cCR患者的结局。这些发现凸显了cCR状态与ctDNA相结合的潜力,有望重新定义MIBC中基于反应指导的个体化治疗路径。
讨论
纵观2026 ASCO GU的这三项研究,我们可以看到MIBC诊疗模式已经发生改变:
1. 从解剖分期到分子分期: ctDNA/utDNA提供了比传统TNM分期更动态、更微观的预后信息。
2. 从被动随访到主动干预: 液体活检不再仅仅是预后判断的工具,而是直接指导辅助治疗启用、监测治疗反应和决定手术去留的决策依据。
3. 多维度评估的必要性: NIAGARA研究提示,单一维度的检测可能存在局限,血液与尿液的联合检测将是未来提升检测敏感性的重要方向。
虽然目前液体活检在标准化检测流程、成本控制及临界值设定上仍需进一步探索,但基于ctDNA/utDNA指导的精准医疗已不再是遥远的未来,而是正在发生的现实。对于临床医生而言,理解并适时应用这一工具,将是优化患者全程管理、改善生存获益的关键。
2026 ASCO GU官网
排版编辑:肿瘤资讯-小编











 苏公网安备32059002004080号
苏公网安备32059002004080号


