对于不可切除的III期非小细胞肺癌(NSCLC)患者,标准治疗模式是根治性放化疗。PACIFIC研究提示了在此类患者中,接受同步放化疗后应用免疫巩固治疗为患者带来的获益,然而,对于NSCLC中占比较高的EGFR突变患者,该模式带来的获益较为有限。研究提示,三代EGFR-TKI的巩固治疗有望为EGFR突变的不可切除III期NSCLC患者带来获益。近期发表的一项研究[1],在真实世界中评估了EGFR突变的III期不可切除NSCLC患者的基因检测、治疗模式及治疗结局,以为三代EGFR-TKI在巩固治疗中的临床应用提供重要参考。
研究背景
约20-30%的NSCLC患者在确诊时处于III期,即局部晚期疾病,其中约60-90%为不可切除。这些患者中,接近三分之一携带EGFR突变。对于不可切除的III期NSCLC患者,标准治疗模式为同步或序贯放化疗后序贯免疫检查点抑制剂的巩固治疗,然而EGFR突变患者接受免疫巩固治疗的获益有限。
三代EGFR-TKI此前已经成为了EGFR突变晚期NSCLC患者一线治疗和术后辅助治疗的标准用药。在III期LAURA研究(NCT03521154)中,对于不可切除的III期EGFR突变(19del或21L858R)NSCLC患者,在根治性同步或序贯放化疗后接受奥希替尼治疗,对比安慰剂显示出统计学显著且具有临床意义的无进展生存期(PFS)获益(中位PFS:39.1个月 vs 5.6个月;HR 0.16;95%CI 0.10–0.24;p < 0.001)。在LAURA研究中,奥希替尼相比安慰剂也在CNS PFS(HR 0.17;95% CI 0.09–0.32;p < 0.001)和至死亡或远处转移时间(HR 0.21;95% CI 0.11–0.38)方面显示出具有临床意义的改善。此外,尽管有高比例(78%)停用安慰剂的患者后续接受了奥希替尼治疗,但奥希替尼同样显示总生存期(OS)的获益趋势。在POLESTAR研究中,三代EGFR-TKI阿美替尼同样显示了在不可切除的III期EGFR突变(19del或21L858R)NSCLC患者,根治性同步或序贯放化疗后巩固治疗中为患者带来的获益,研究中阿美替尼组基于独立评审委员会评估的中位PFS达到30.4个月,对照组仅为3.8个月(HR 0.20),在所有预设亚组中均观察到阿美替尼组的获益趋势。
鉴于此,需要进一步了解这些患者在真实世界中接受EGFR-TKI治疗的情况,分析该患者群体的治疗模式和结局可能有助于进一步理解真实世界临床实践的复杂性和可变性,从而掌握未满足的临床需求,并为临床决策提供参考。因此,研究者报告了一项全球性、回顾性、真实世界研究结果,该研究评估了EGFR-TKI巩固治疗获批前、接受放化疗作为标准治疗的不可切除III期EGFR突变NSCLC患者的突变检测模式、治疗模式和临床结局。
研究方法
这项全球性、回顾性、真实世界观察性研究评估了从奥地利、日本、韩国、中国台湾、英国和美国肿瘤中心患者病历中提取的数据。这些患者在2016年1月至2019年12月期间被诊断为不可切除的III期NSCLC,并从其索引日期开始随访,直至最后一次可用随访、死亡或2022年12月31日(以先发生者为准)。
纳入患者经组织学和实验室确诊为不可切除III期NSCLC,且携带至少一种EGFR敏感突变(19del或21L858R),可切除状态基于医生的评估,允许既往在索引日期前三个月内完成I-II期的手术切除,且在索引日期后未进行手术。合格患者还须在索引日期后接受过放化疗作为标准治疗。主要研究终点是真实世界无进展生存期(rwPFS)。次要终点包括基线患者人口统计学和临床特征、突变检测模式、索引日期后的治疗模式、真实世界至下次治疗或死亡时间(rwTTNTD)、OS、真实世界第二次无进展生存期(rwPFS2)和真实世界至第二次下次治疗或死亡时间(rwTTNTD2)。
研究结果
患者特征
研究总计纳入了172例不可切除III期EGFR突变NSCLC患者的病历数据。患者的中位年龄为67岁(IQR 60-74),62%(n=107)为女性,ECOG PS评分为0分和1分的患者占比分别为42%(n=73)和49%(n=84)。此外,63%(n=109)的患者从不吸烟,94%(n=162)为腺癌。从索引日期(患者被诊断为不可切除III期NSCLC的日期)起,中位随访时间为45.7个月(IQR 26.6-62.0)。
突变检测模式
172例患者总计记录了194次EGFR突变检测,其中56%(108次检测)使用了单基因检测法,10%(19次检测)使用了多基因检测法,35%(67次检测)的检测方法未知。从索引日期到样本采集的中位时间为1天(IQR 1-2),从样本采集到获得检测结果的中位时间为12天(IQR 6-21)。少数患者存在除Ex19del或L858R之外的EGFR突变。
PD-L1表达方面,高表达(≥50%)患者占比为16%(27/172),低表达(1-49%)患者占为16%(27/172),PD-L1阴性患者占比为30%(52/172),另有38%(66/172)的患者结果不确定或未知。
接受其他基因检测的患者中,ALK重排(0/142)、BRAF突变(0/23)、RET重排(0/19)或HER2外显子20插入(0/11)检测均无阳性。KRAS突变、ROS-1重排和TP53突变的发生率分别为8%(2/26)、3%(2/77)和79%(11/14)。
治疗模式
从索引日期到开始首次放化疗的中位时间为0.7个月(IQR 0.4-1.0)。134例患者(78%)接受了单纯放化疗,31例患者(18%)接受放化疗后度伐利尤单抗巩固治疗,6例患者(3%)接受放化疗后EGFR-TKI巩固治疗(2例使用厄洛替尼,阿法替尼、吉非替尼、奥希替尼或厄洛替尼加吉非替尼各1例),1例患者(1%)接受放化疗联合帕博利珠单抗作为首次治疗。
在首次治疗中,130例患者(76%)接受了同步放化疗,42例患者(24%)接受序贯放化疗。同步放化疗中最常用的化疗方案是卡铂+紫杉醇,占比为22%(29/130),序贯放化疗中最常用的方案是顺铂+紫杉醇,占比为69%(29/42)。
大多数患者(n=104, 60%)接受了调强放疗(IMRT)或容积旋转调强放疗(VMAT),另外分别有26例(15%)、21例(12%)和5例(3%)接受了三维适形放疗、质子治疗和其他类型的放疗(9%未知)。放疗中位剂量为64 Gy(IQR 60-66),放疗中位分割次数为30次(IQR 30-32)。总共115例患者(67%)完成了首次治疗。在57例未完成首次治疗的患者中,首次治疗中止的原因包括(患者可能有一个以上的中止原因)不良反应(33/57, 58%)、医生决定(24/57, 42%)、疾病进展(16/57, 28%)和患者拒绝治疗(9/57, 16%)。
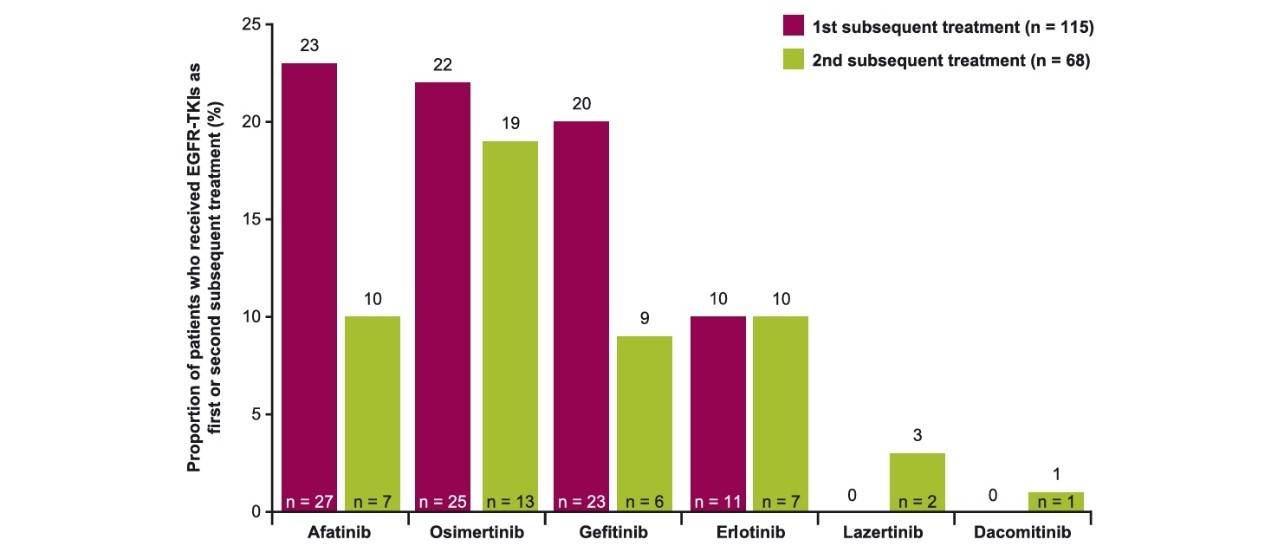
172例患者中有133例(77%)出现疾病进展并可以接受后续的治疗,其中115例患者(86%)接受了首次后续治疗,这其中86例患者(75%)接受了EGFR-TKI治疗,其余患者接受了单纯化疗(13%)、单纯放疗(10%)或免疫治疗±化疗(3%)。首次后续治疗的中位停药时间总体为11.5个月(95% CI 7.5-13.0),接受含第一/第二代EGFR-TKI方案的患者为12.0个月(95% CI 9.3-13.0),接受含第三代EGFR-TKI方案的患者为22.7个月(95% CI 14.3-NE),接受单纯化疗的患者为1.0个月(95% CI 0.7-1.9),接受单纯放疗的患者为1.0天(95% CI NE-NE),接受含免疫治疗方案的患者为1.9个月(95% CI 1.4-NE)。
总体而言,115例接受首次后续治疗的患者中有76例(66%)出现进展,其中76例中有68例(89%)接受了第二次后续治疗,其中36例(36/68, 53%)接受了EGFR-TKI治疗。
表1 患者接受后续治疗的情况
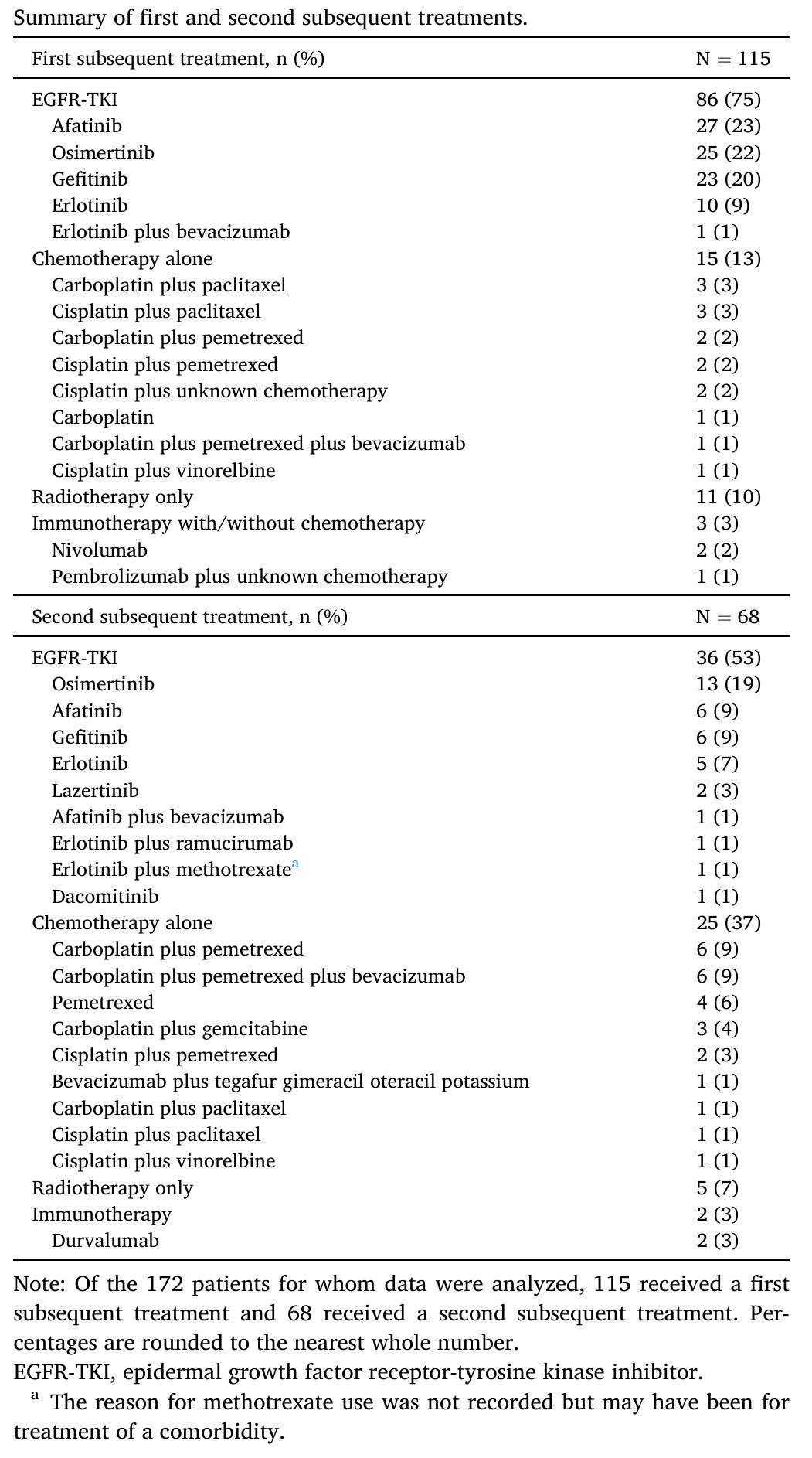
临床结局
患者的中位rwPFS为8.3个月(95% CI 6.3-9.5)。6个月和12个月PFS率分别为62%(95% CI 54-69)和33%(95% CI 26-41)。在134例接受单纯放化疗作为首次治疗的患者中,共发生112例(84%)rwPFS事件(中位rwPFS 6.7个月 [95% CI 6.0-9.0])。在接受单纯放化疗作为首次治疗的患者中,6个月和12个月的PFS率分别为56%(95% CI 46-64)和28%(95% CI 20-36)。接受同步放化疗的患者6个月和12个月PFS率分别为53%(95% CI 41-63)和30%(95% CI 20-40),接受序贯放化疗的患者6个月和12个月PFS率分别为63%(95% CI 45-76)和24%(95% CI 12-39)。31例接受放化疗后度伐利尤单抗巩固治疗作为首次治疗的患者中发生了21例(68%)rwPFS事件(中位rwPFS 11.9个月 [95% CI 9.1-24.0])。6个月和12个月PFS率分别为79%(95% CI 60-90)和48%(95% CI 28-65)。所有患者中共发生114例(66%)rwTTNTD事件,中位rwTTNTD为13.1个月(95% CI 10.4-18.9)。
OS方面,总体的中位OS为66.9个月(95% CI 56.9-76.7),五年OS率为58%。接受单纯放化疗作为首次治疗的患者中位OS为68.6个月(95% CI 60.9-NE),五年OS率为60%,其中,接受同步放化疗的患者未达到中位OS(95% CI 68.6-NE),接受序贯放化疗的患者中位OS为52.9个月(95% CI 36.9-64.9),两组的五年OS率分别为68%和42%。接受放化疗后度伐利尤单抗巩固治疗的患者中位OS为52.8个月(95% CI 48.9-NE)。
研究结论
这项真实世界研究表明,在不可切除的III期EGFR突变NSCLC患者中,放化疗是首选的初始治疗方案,而EGFR-TKI则是最常见的后续治疗方案。尽管rwPFS相对较短,但患者的OS却相当可观,这可能归因于后续EGFR-TKI的应用。
小编点评
这项全球性、回顾性、真实世界观察性研究评估了2016年至2019年间诊断为不可切除III期EGFR突变NSCLC的172例患者的突变和治疗模式以及临床结局。大多数患者接受单纯放化疗作为首次治疗,其余患者接受放化疗后度伐利尤单抗巩固治疗或放化疗后EGFR-TKI巩固治疗。在接受首次后续治疗的患者中,大多数接受了EGFR-TKI治疗。
本研究中的大多数患者(78%)接受单纯放化疗作为首次治疗,18%的患者接受放化疗后度伐利尤单抗巩固治疗,这反映了研究的时间背景,在当时基于PACIFIC研究,度伐利尤单抗的巩固治疗模式成为了不可切除III期NSCLC在同步放化疗后的标准治疗模式。在本研究中,接受放化疗后度伐利尤单抗巩固治疗作为首次治疗的患者的中位rwPFS为11.9个月,长于仅接受单纯放化疗的患者,这些结果虽然提示了免疫巩固治疗可能在EGFR突变NSCLC的治疗中发挥一定作用,但为患者带来的获益较为有限。考虑到患者的后续治疗以EGFR-TKI为主,且患者的OS时间较长,更加凸显了LAURA模式的临床价值。
尽管无法与随机试验的数据进行直接比较,但这项真实世界研究的临床结局结果提供了进一步的支持性证据,提示了EGFR-TKI巩固治疗有望为EGFR突变III期不可切除NSCLC患者带来更长的获益,同时,也强调了在NSCLC治疗中的所有阶段(包括不可切除III期)都应该进行EGFR检测,以确保患者在放化疗后接受最合适的巩固治疗。
本研究存在一定局限性,包括不同治疗方案在不同地区的可及性差异,主要纳入了亚洲人群数据,部分亚组样本量较低等,因此应谨慎解读数据。
但总之,这项真实世界研究结果提供了进一步的证据,支持在不可切除III期EGFR突变NSCLC患者中放化疗后使用EGFR-TKI进行巩固治疗,并支持实施常规EGFR检测的重要性,以确保在疾病早期阶段为患者确定合适的治疗方案。
[1] Ahn MJ, Lin SH, Yang CT, Lee JB, Neal JW, Okishio K, Nishino K, Smith D, Rauter M, Jimenez M, Nasirova F, Kim Y. Mutation testing, treatment patterns, and outcomes in patients with unresectable stage III EGFR-mutated non-small cell lung cancer treated with chemoradiotherapy: Final analysis of a global real-world study. Lung Cancer. 2025 Nov;209:108748. doi: 10.1016/j.lungcan.2025.108748.
本材料由阿斯利康提供支持,仅供医疗卫生专业人士参考,不可用于推广目的。
审批编号:CN-172091
过期日期:2026-02-20
排版编辑:肿瘤资讯-邓文普











 苏公网安备32059002004080号
苏公网安备32059002004080号


