滤泡性淋巴瘤(FL)作为成人最常见的惰性非霍奇金淋巴瘤亚型,临床特征呈现显著异质性。在过去数十年中,以蒽环类或苯达莫司汀为基础的免疫化疗(ICT)是FL的标准治疗方案。然而,ICT治疗存在两大核心局限:其一,现有研究证实ICT无法降低FL患者的总体死亡风险;其二,ICT的长期毒性累积效应显著,多次治疗后感染、第二原发肿瘤等并发症风险升高,尤其在老年或合并基础疾病的患者中耐受性较差。
近年来,随着靶向治疗与免疫治疗技术的快速发展,以双特异性抗体、布鲁顿酪氨酸激酶(BTK)抑制剂、嵌合抗原受体T细胞(CAR-T)疗法为代表的“chemo-free”方案逐渐崭露头角,为FL治疗带来了范式转变的可能。近日,一项发表于British Journal of Haematology杂志的综述,基于全球范围内1990~2025年的临床研究数据,系统梳理了FL“chemo-free”治疗的演进历程,明确了不同治疗线数下的方案选择依据,为临床实践提供了兼具循证依据与实操性的指导框架。
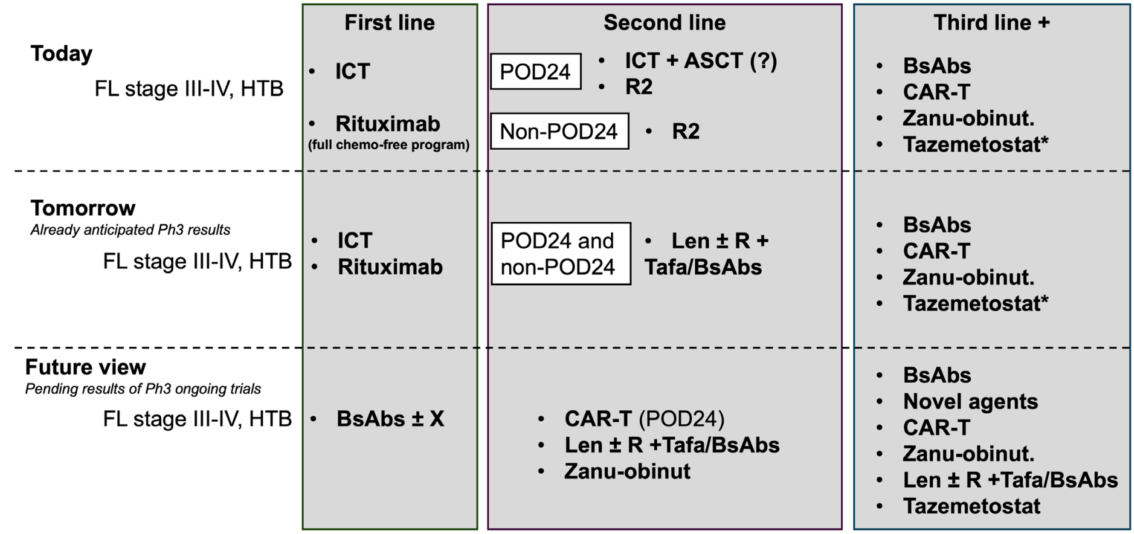
图1. FL不断发展的治疗范式

初治FL的 “chemo-free”探索:从单药到联合治疗的渐进式突破
目前初治FL的“chemo-free”方案仍处于临床验证阶段,尚未完全替代ICT,但以利妥昔单抗为基础的治疗已形成明确的适用场景。
2000年后,利妥昔单抗单药治疗成为首个获批用于FL的“chemo-free”方案,其疗效与安全性在多项临床试验中得到证实:在低肿瘤负荷患者中,对比“观察等待”策略,利妥昔单抗单药可显著延长无进展间隔时间(中位延长3~4年)、推迟二线治疗需求,且3~4级不良反应发生率低于5%;即使在高肿瘤负荷患者中,长期随访数据显示,45%患者经利妥昔单抗单药治疗后缓解状态可维持8年以上,约1/3患者在中位随访10年内无需额外治疗。
需注意的是,利妥昔单抗单药的疗效仍低于传统ICT方案,其CR率(45%~50%)与PFS(5~6年)均显著低于利妥昔单抗联合化疗(CR率80%、PFS超8 年),因此目前主要适用于三类人群:老年(≥75岁)或体能状态较差(ECOG PS 2分及以上)患者、拒绝化疗的患者,以及作为向后续更有效“chemo-free”方案过渡的桥梁治疗。
利妥昔单抗联合来那度胺(R2方案)是初治FL“chemo-free”领域的重要突破。Ⅲ期RELEVANCE试验纳入1030例初治晚期FL患者,对比R2方案与利妥昔单抗联合化疗(R-化疗)的疗效,结果显示两组6年PFS率(60% vs 59%)与OS率(均为89%)无统计学差异;尽管R-化疗组的CR率(53% vs 48%)与总缓解率(OR/R,65% vs 61%)略高,但差异未达到临床意义,且R2方案的3~4级血液学毒性发生率(28% vs 45%)显著更低。基于该数据,部分国家(如美国、法国)已将R2方案纳入初治FL的一线治疗选项,更多地区则将其定位为二线治疗的标准方案。
此外,新型“chemo-free”联合方案的一线探索正在推进。例如,EZH2抑制剂他泽司他联合R2方案在Ⅰ/Ⅱ期试验中显示出协同效应,EZH2突变患者的OR/R达71%,野生型患者达50%;双抗(如莫妥珠单抗)单药或联合来那度胺的早期数据显示,初治FL患者的CR率超过60%,且毒性可控,相关Ⅲ期试验(如NCT06337318比较莫妥珠单抗与利妥昔单抗单药)正在进一步验证其一线疗效。
二线复发/难治性(R/R)FL:“chemo-free”方案成为标准选择
二线治疗是FL“chemo-free”方案的核心应用场景,目前已有多款方案获得欧美药品监管机构批准,其中R2方案和他法西他单抗联合R2(Tafa-R2)方案的证据最为充分。
表 1. 目前批准的R/R FL的chemo-free方案
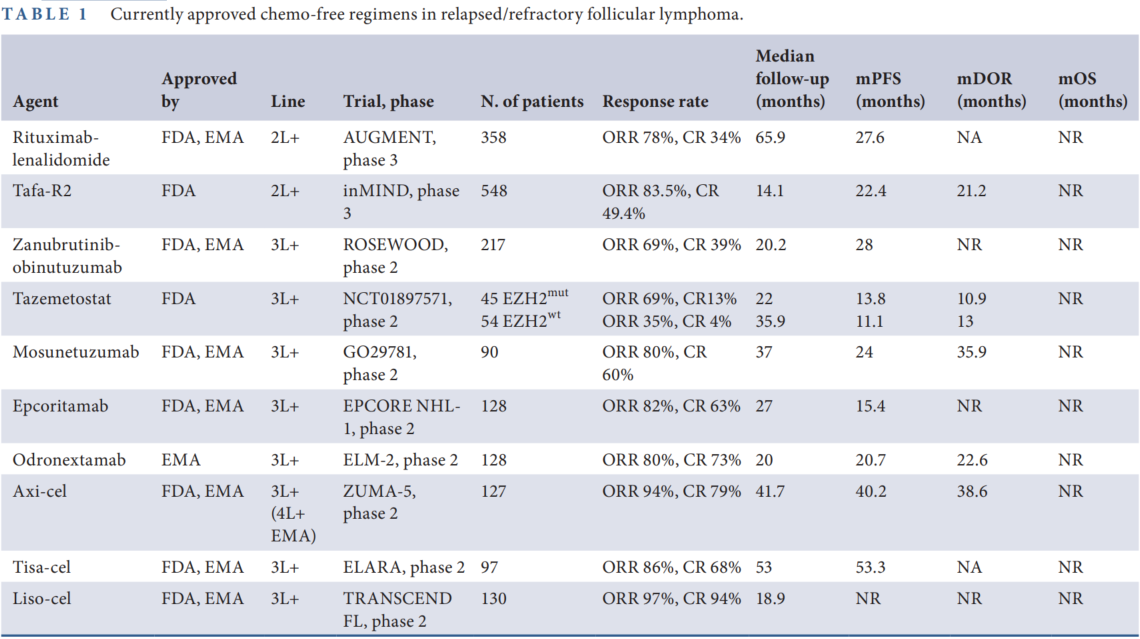 R2 方案的疗效在Ⅲ期AUGMENT试验中得到确证:该试验纳入358例二线R/R FL患者,对比R2方案与利妥昔单抗联合安慰剂,结果显示R2组ORR达78%(CR率34%),中位PFS延长至27.6个月(安慰剂组仅11.8个月),且5年随访数据显示OS仍未达到,证实其长期获益。真实世界研究进一步验证了R2方案的有效性,即使在存在bulky病灶(≥7.5cm)或利妥昔单抗耐药的患者中,OR/R仍可维持在65%~70%,中位PFS达22个月。
R2 方案的疗效在Ⅲ期AUGMENT试验中得到确证:该试验纳入358例二线R/R FL患者,对比R2方案与利妥昔单抗联合安慰剂,结果显示R2组ORR达78%(CR率34%),中位PFS延长至27.6个月(安慰剂组仅11.8个月),且5年随访数据显示OS仍未达到,证实其长期获益。真实世界研究进一步验证了R2方案的有效性,即使在存在bulky病灶(≥7.5cm)或利妥昔单抗耐药的患者中,OR/R仍可维持在65%~70%,中位PFS达22个月。
Tafa-R2方案在R2基础上进一步提升疗效,成为二线R/R FL的新选择。Ⅲ期inMIND试验纳入548例二线R/R FL患者,其中32%为POD24患者、43%为抗CD20抗体耐药患者,结果显示Tafa-R2组的代谢CR率(49.4% vs 39.8%)与中位PFS(22.4个月 vs 13.9个月)均显著优于R2组,疾病进展或死亡风险降低57%;安全性方面,两组3~4级不良反应发生率无显著差异(35% vs 32%),仅Tafa-R2组的输注相关反应发生率略高(18% vs 8%),但多为1~2级。基于该数据,Tafa-R2方案于2024年获美国FDA批准用于二线R/R FL治疗。
需注意的是,目前二线“chemo-free”方案尚未与ICT开展头对头比较,但基于间接证据,“chemo-free”方案的安全性优势已十分明确:R2和Tafa-R2方案的3~4级血液学毒性发生率不足30%,远低于ICT方案(如利妥昔单抗联合苯达莫司汀的45%~50%),且感染、第二原发肿瘤等长期毒性风险显著降低。此外,BTK抑制剂联合方案也为二线治疗提供了补充选择,如Ⅲ期ROSEWOOD试验显示,泽布替尼联合奥妥珠单抗治疗二线R/R FL的ORR达69%(CR 率39%),中位PFS达28个月,适合无法耐受免疫调节剂(来那度胺)的患者。
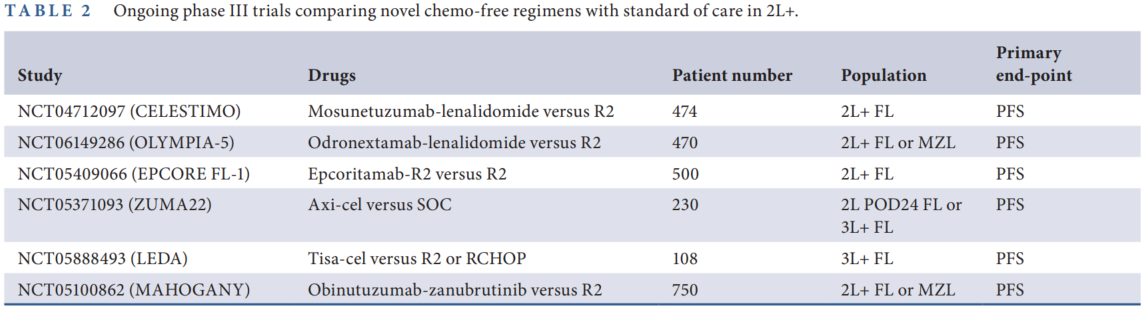
表2. 正在进行的Ⅲ期试验,将新型chemo-free方案与2L+治疗标准进行比较
≥3线R/R FL:双抗与CAR-T疗法主导治疗格局
≥3线R/R FL患者多经过多线治疗,体能状态较差、治疗选择有限,“chemo-free”方案已成为该人群的主要治疗手段,目前形成以双抗、CAR-T疗法为核心,EZH2抑制剂为补充的治疗格局。
双抗:快速缓解与门诊可及性的平衡
双抗通过同时靶向B细胞表面抗原(CD20或CD19)与T细胞表面CD3分子,激活T细胞介导的肿瘤细胞裂解,具有起效快、可门诊给药的优势,目前已有3款双抗获批用于≥3线R/R FL:
莫妥珠单抗(CD20×CD3):首个获FDA与EMA批准用于治疗FL的双抗,其疗效基于Ⅱ期GO29781试验,该试验纳入90例中位经3线治疗的R/R FL患者,结果显示ORR达80%(CR率60%),3年PFS率43%,中位缓解持续时间(DOR)达35.9个月;安全性方面,44%患者出现1~2级细胞因子释放综合征(CRS),无3级以上CRS发生,3~4级中性粒细胞减少发生率为27%,且采用固定疗程(8个周期)给药,患者依从性较高。
Epcoritamab(CD20×CD3):采用皮下注射给药,可显著降低CRS风险(65%为1~2级,仅2%达3级)。Ⅱ期EPCORE NHL-1试验纳入128例≥3线R/R FL患者,结果显示ORR达82%(CR率63%),中位PFS尚未达到,且联合R2方案时ORR提升至98%(CR率 87%),无论患者是否存在POD24或双耐药(抗CD20+化疗耐药)均能获益。
Odronextamab(CD20×CD3):Ⅱ期ELM-2试验显示,其治疗≥3线R/R FL的ORR达80%(CR率73%),中位PFS为20.7个月,中位DOR为22.6个月;需注意的是,该试验期间受COVID-19疫情影响,3~5级感染发生率较高(41%),其中约1/3与疫情相关,后续真实世界研究需进一步验证其感染风险。
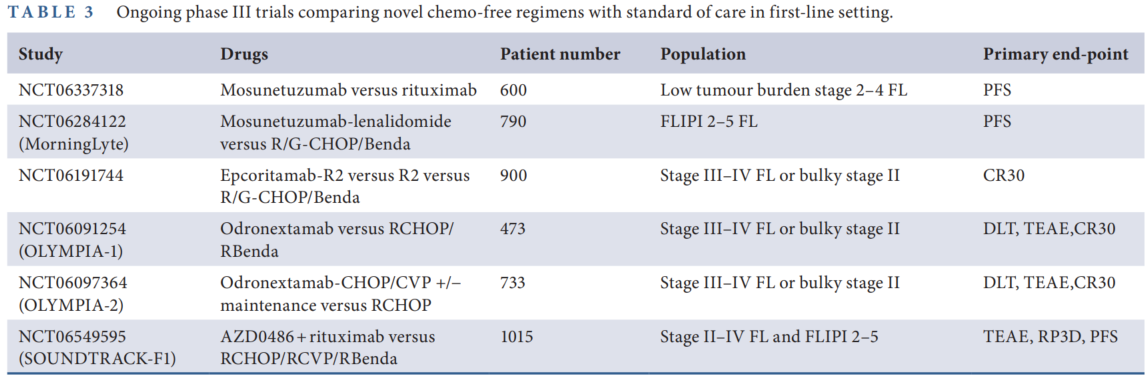
表3. 正在进行的Ⅲ期试验比较了新型chemo-free方案和一线标准治疗方案
CAR-T疗法:深度缓解与长期获益的优选
CAR-T疗法作为具有“一次性治疗”潜力的方案,在≥3线R/R FL中展现出卓越的深度缓解效果,目前已有3款CD19靶向CAR-T产品获批:
Axicabtagene ciloleucel(axi-cel):Ⅱ期ZUMA-5试验纳入127例≥3线R/R FL患者,结果显示ORR达94%(CR率79%),中位随访41.7个月,中位PFS达40.2个月,3年OS率75%;安全性方面,6%患者出现3级以上CRS,15%出现3级以上神经毒性,需住院监测治疗。
Tisagenlecleucel(tisa-cel):Ⅱ期ELARA试验中位随访53个月,结果显示ORR达86%(CR率69%),45个月PFS率为52.9%,即使是POD24患者也达45%;安全性更优,仅49%患者出现1~2级CRS,3级以上神经毒性发生率仅1%,适合老年或体能状态较差的患者。
Lisocabtagene maraleucel(liso-cel):Ⅱ期TRANSCEND-FL试验是目前最大规模的FL相关CAR-T研究,纳入130例≥3线R/R FL患者,结果显示ORR达97%(CR率94%),中位随访18.9个月,PFS与DOR均未达到,且13%患者可在门诊完成治疗,显著提升了治疗可及性。
EZH2抑制剂:精准靶向特定亚型患者
EZH2抑制剂他泽司汀为存在EZH2突变的R/R FL患者提供了精准治疗选择。Ⅱ期NCT01897571试验显示,他泽司汀治疗EZH2突变患者的ORR达69%(CR率13%),中位PFS达13.8个月;即使在EZH2野生型患者中,也能达到35%的ORR与11.1个月的中位PFS。安全性方面,他泽司汀的耐受性良好,3~4级不良反应主要为血液学毒性(血小板减少18%、中性粒细胞减少15%),无治疗相关死亡发生,适合无法耐受免疫疗法或CAR-T的患者。
结论
该综述基于1990~2025年全球FL治疗研究数据,明确了“chemo-free”方案已成为FL治疗的重要发展方向,不同治疗线数下的方案选择呈现清晰格局:二线R/R FL患者优先推荐R2或Tafa-R2方案,三线及以上患者则根据病情风险、治疗可及性及患者意愿,选择双抗或CAR-T疗法,初治患者的“chemo-free”方案仍需等待Ⅲ期试验验证。
与传统ICT方案相比,“chemo-free”方案在疗效与安全性上实现了双重优化:二线Tafa-R2方案使疾病进展风险降低57%,三线双抗的ORR普遍超过80%,CAR-T疗法的中位PFS可达40个月以上;同时,“chemo-free”方案的3~4级毒性发生率降低30%-50%,长期感染、第二原发肿瘤风险显著下降,显著改善了患者的生活质量。尤其值得关注的是,“chemo-free”方案对POD24、抗CD20耐药等高危患者仍具有明确疗效,打破了这类患者既往“治疗选择有限”的困境。
然而,FL“chemo-free”治疗仍需解决三大关键问题:其一,缺乏双抗与CAR-T疗法的头对头比较数据,方案顺序(如双抗失败后是否可序贯CAR-T)需进一步验证;其二,现有预后评分(如FLIPI、PRIMA-PI)无法精准预测患者对“chemo-free”方案的治疗反应,需整合分子标志物(如EZH2 突变、MYC基因状态)与微小残留病(MRD)监测,实现个体化治疗;其三,部分“chemo-free”方案(如CAR-T)存在成本高、制备周期长等问题,限制了基层医疗机构的推广应用,需通过技术优化与政策支持提升可及性。
未来,随着多项Ⅲ期试验结果的公布,双抗联合免疫调节剂有望成为二线治疗的新标准;而一线“chemo-free”方案的临床验证,或将推动FL治疗进入“全周期chemo-free”时代。同时,真实世界研究与长期随访数据的积累,将进一步明确“chemo-free”方案的长期疗效与毒性,为FL患者构建更精准、更安全的治疗体系提供循证依据。
Luminari S, Barbieri E, Nizzoli M E. Towards a chemo‐free approach for follicular lymphoma[J]. British Journal of Haematology, 2025.
排版编辑:mathilda











 苏公网安备32059002004080号
苏公网安备32059002004080号


