重庆大学附属肿瘤医院 乳腺肿瘤中心
主治医师,中山大学外科学博士,重庆大学博士后
重庆市医学青年拔尖人才。
长期从事乳腺肿瘤的临床及基础转化研究,主要方向为新辅助治疗疗效分子标志物及乳腺癌靶向治疗耐药的分子机制,主持在研课题5项,发表SCI论文多篇,研究成果于SABCS、JSCO、CBCS及CSCO等国内外会议壁报展示
ASCO解读文献
Abstract LBA1000
Vepdegestrant, a PROTAC estrogen receptor (ER) degrader, vs fulvestrant in ER-positive/human epidermal growth factor receptor 2 (HER2)–negative advanced breast cancer: Results of the global, randomized, phase 3 VERITAC-2 study.
Vepdegestrant(一种蛋白水解靶向嵌合体[PROTAC]雌激素受体降解剂)对比氟维司群治疗ER+/HER2-晚期乳腺癌的全球随机3期VERITAC-2研究结果
摘要
研究背景
对于HR+/HER2-晚期乳腺癌患者,一线CDK4/6i联合内分泌治疗后,仍有大量患者因获得性耐药进展,是临床亟待解决的问题。传统选择性雌激素受体降解剂(SERD)代表药物如氟维司群因水溶性差、肌注剂型及对ER降解效率有限,临床应用受限。Vepdegestrant(ARV-471)作为首个进入III期临床验证的PROTAC(Proteolysis Targeting Chimera)ER降解剂,其通过泛素-蛋白酶体途径高效靶向降解ER蛋白,兼具口服、降解效率高等特点,有望突破既往SERD的治疗瓶颈。此前I/II期研究已展现出良好耐受性和抗肿瘤活性(NCT04072952)。
研究设计
VERITAC-2为一项全球多中心、随机、双盲、III期临床研究(NCT05654623),旨在评估口服PROTAC ER降解剂Vepdegestrant对比氟维司群在HR+/HER2-晚期乳腺癌(ABC)患者中的疗效与安全性。纳入标准包括:年龄≥18岁,ER+/HER2- 晚期或转移性乳腺癌;既往接受过一线CDK4/6抑制剂联合内分泌治疗,且使用内分泌药物不超过1种;未接受过任何SERD类治疗;晚期或转移阶段未接受化疗。
入组患者按1:1比例随机分配,28天为一周期,接受Vepdegestrant(200 mg,口服,每日一次)或氟维司群(500 mg,肌注,第一周期的第1天和第15天,后续每周期的第1天)治疗。研究设定盲法独立中心评估(BICR)为主要评估方式,首要终点为ESR1基因突变(ESR1m)人群及所有患者的无进展生存期(PFS)。关键次要终点为总生存期(OS),其它次要终点包括客观缓解率(ORR)、临床获益率(CBR)以及不良事件(AEs)发生率。
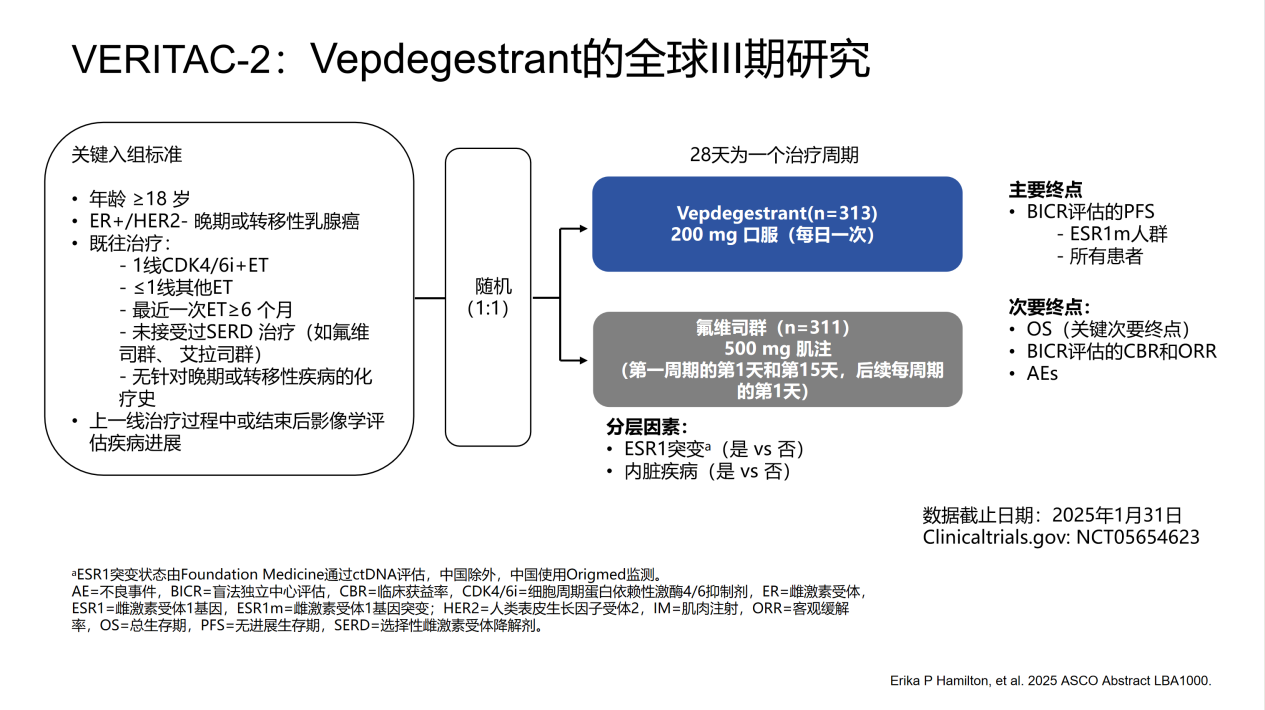
研究结果
本研究共计纳入624例患者,其中43%携带ESR1m,Vepdegestrant组313人(136人携带ESR1m),氟维司群组311人(134人携带ESR1m),两组基线特征基本平衡,入组患者中位年龄为60岁,其中约80%既往接受一线治疗,约20%既往接受二线治疗。
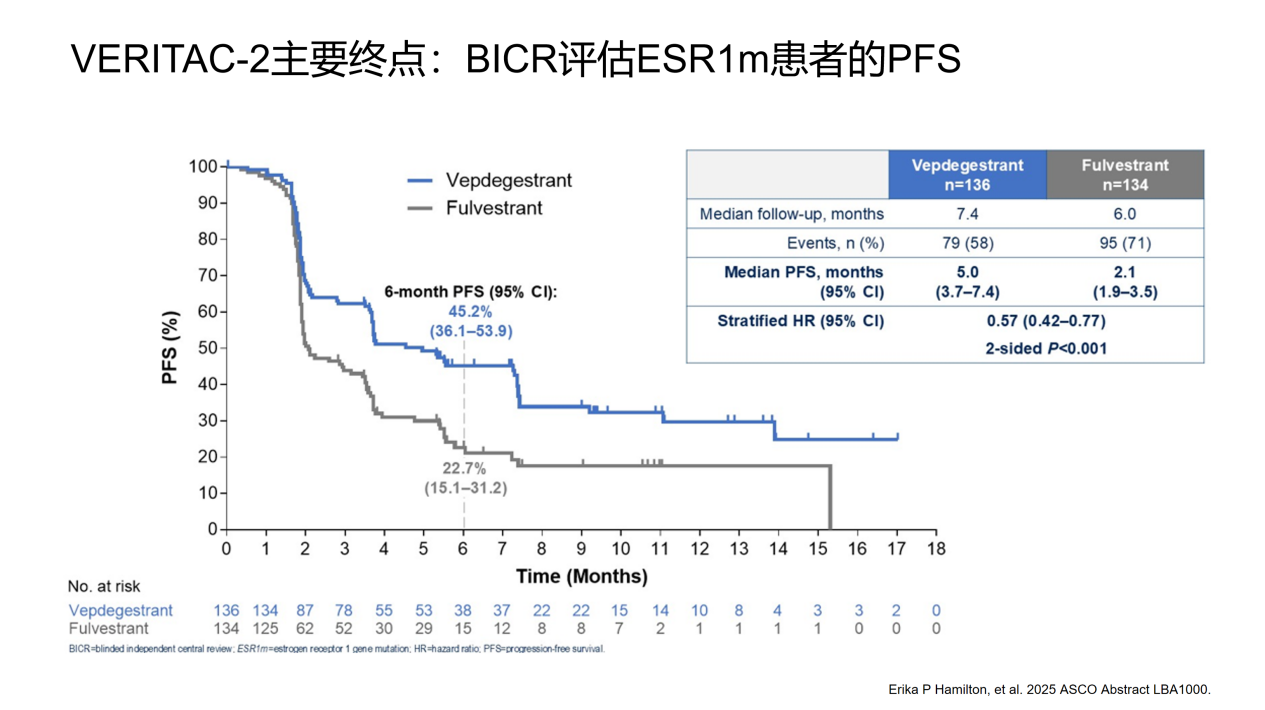
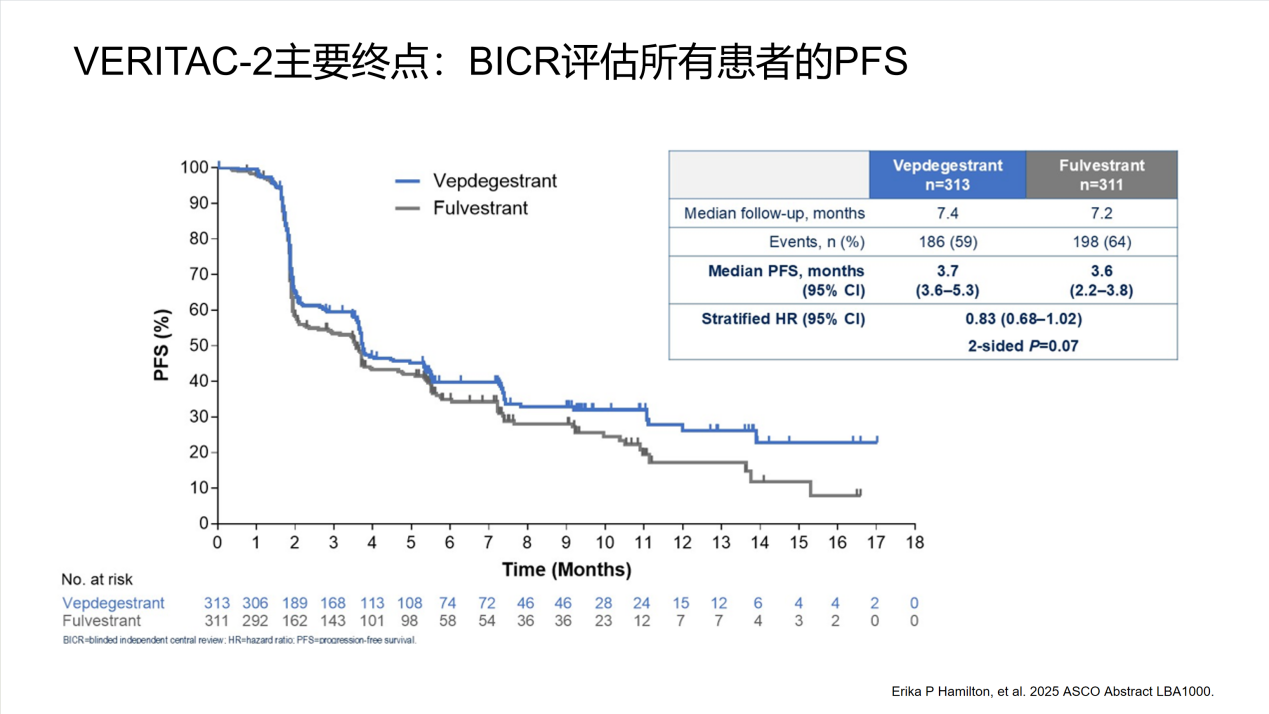
在ESR1m人群中,Vepdegestrant在主要终点PFS上表现出显著延长,中位PFS为5.0个月(对比氟维司群2.1个月),疾病进展风险降低43%(HR=0.57;95% CI:0.42-0.77,P<0.001);在所有患者中未达到统计学显著差异,中位PFS为3.7个月vs 3.6个月(HR=0.83;95% CI:0.68-1.02,P=0.07)。
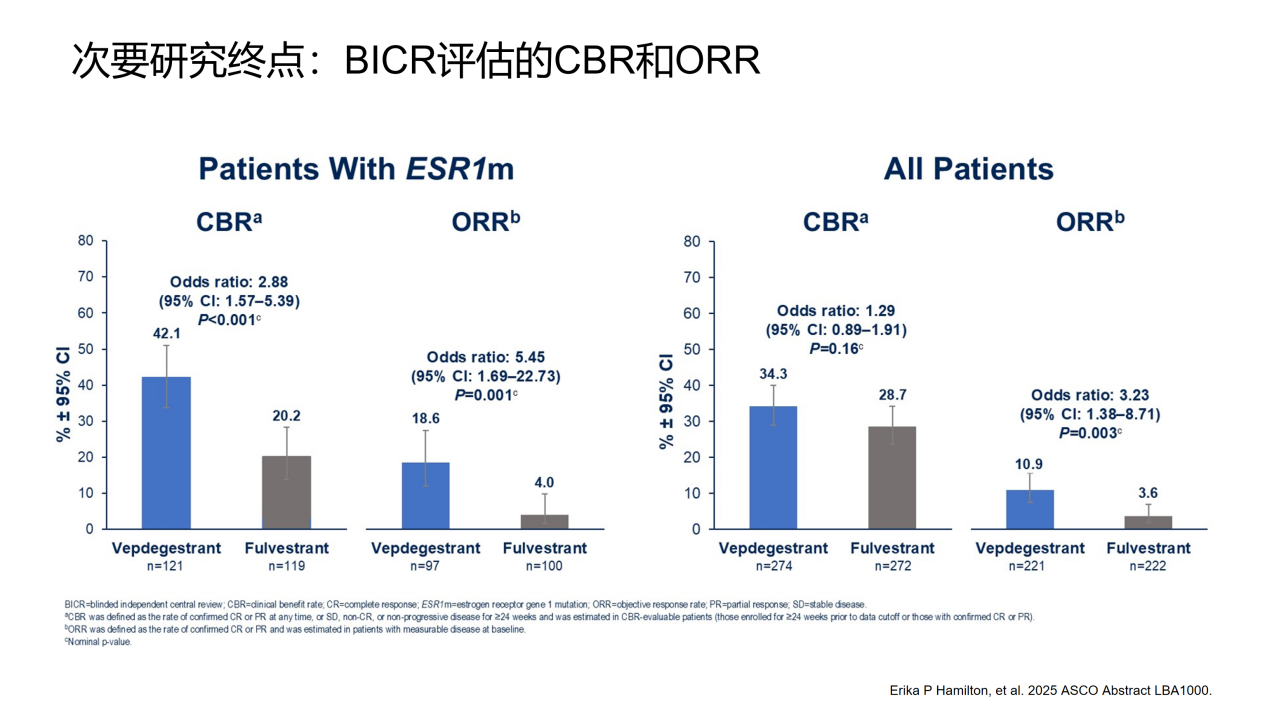
次要终点的结果,Vepdegestrant组ORR为18.6%,显著高于对照组的4.0%(OR 5.45,95% CI:1.69-22.73,P = 0.001);CBR为42.1%,亦优于氟维司群组的20.2%(OR 2.88,95% CI:1.57-5.39,P<0.001)。累计观察到80例死亡,其中43例为ESR1m患者,OS数据尚不成熟。
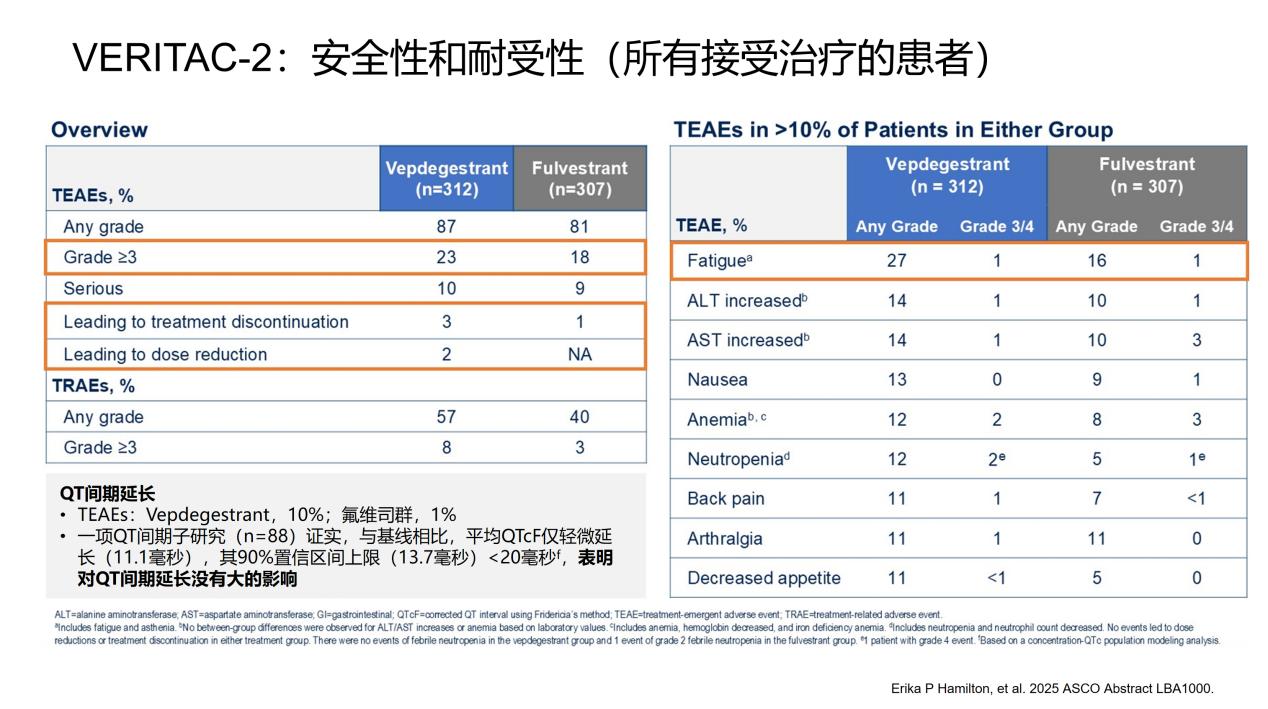
安全性方面,Vepdegestrant组≥3级AEs发生率为23%,高于氟维司群组的18%。最常见不良反应为疲劳(27% vs 16%)、ALT升高(14% vs 10%)、AST升高(14% vs 10%)以及恶心(13% vs 9%),治疗期间出现的不良事件(TEAEs)导致的停药率为(3% vs 1%)。
结论
Vepdegestrant在ESR1突变(ESR1m)患者中显著改善PFS,耐受性良好,研究结果支持Vepdegestrant作为CDK4/6抑制剂经治的ESR1m ER+/HER2-晚期乳腺癌患者的潜在治疗选择。
解读
CDK4/6抑制剂进展后治疗现状:尚待突破
CDK4/6抑制剂联合内分泌治疗已成为HR+/HER2-晚期乳腺癌一线标准,但一旦进展,治疗选择匮乏。现有研究结果不甚理想。II期MAINTAIN研究探索了哌柏西利治疗进展后更换至瑞波西利联合方案的可行性,结果尽管对比单纯内分泌治疗取得了PFS的显著改善,但中位PFS也仅延长了2.5个月[1];postMONARCH研究显示阿贝西利联合氟维司群对比安慰剂联合氟维司群,PFS绝对获益仅0.7个月(6.0个月vs 5.3个月)[2];II期PACE研究(中位PFS:4.6个月vs 4.8个月,HR=1.11,P=0.62)与PALMIRA研究(中位PFS:4.2个月vs 3.6个月,HR=0.8,P=0.21)设计相似,分别探索了基于哌柏西利的不同联合治疗方案在哌柏西利经治患者中的疗效,均未能取得理想结果[3, 4]。
总体而言,CDK4/6抑制剂进展后缺乏标准治疗方案,凸显出在耐药人群中治疗策略的局限,亟需更具创新机制的药物来打破治疗瓶颈。
PROTAC:从概念到临床的革命性创新
PROTAC技术由耶鲁大学Craig Crews 教授团队在2001年首次提出,是一种利用细胞内泛素-蛋白酶体途径选择性降解目标蛋白的创新机制[5]。与传统小分子药物只阻断靶蛋白活性不同,PROTAC通过双功能分子,一端结合靶蛋白,另一端招募E3泛素连接酶,将靶蛋白标记为“待降解”对象,最终送入蛋白酶体彻底清除[6]。
相比传统药物,PROTAC带来三大潜在优势:(1)作用更彻底:直接清除靶蛋白,而不是仅抑制其活性;(2)克服耐药:可靶向野生型或突变型蛋白;(3)拓展靶点:可靶向传统小分子药物难以作用的蛋白,如缺乏活性结合位点的靶点。近十余年,PROTAC从实验室逐步进入临床,Vepdegestrant正是全球首个进入III期临床的ER靶向PROTAC药物,凭借对野生型和ESR1突变型ER的高效降解能力,为HR+/HER2-晚期乳腺癌带来了新的希望。
HR+/HER2-晚期乳腺癌治疗进入PROTAC时代——Vepdegestrant的突破
ESR1突变属于获得性突变,在未经治疗的原发乳腺癌患者中突变率较低(约3%)。随着治疗干预,突变率呈现显著升高趋势:接受芳香化酶抑制剂(AI)治疗的患者中,ESR1突变率显著上升;而在晚期乳腺癌患者中,突变频率可达30%~40%。尤其在接受CDK4/6抑制剂治疗的患者中,ESR1突变率可达32%,成为CDK4/6i联合AI治疗耐药的重要机制之一[7]。Vepdegestrant作为口服PROTAC ER降解剂,利用UPS系统,将野生型和ESR1突变型ER蛋白彻底降解,尤其有望解决氟维司群降解效率受限的问题。
VERITAC-2研究共纳入624名既往接受CDK4/6i治疗的HR+/HER2-晚期乳腺癌患者,其中43%携带ESR1突变。ESR1突变人群获益显著:Vepdegestrant中位PFS达5.0个月,显著优于氟维司群的2.1个月(HR=0.57,P<0.001),ORR高达18.6%(对照组仅4.0%),CBR提升至42.1%。然而,在总人群中PFS差距未达统计学显著(3.7月vs 3.6月,HR=0.83,P = 0.07)。这一结果提示ESR1突变仍是关键人群,而野生型ER患者可能由多条旁路通路驱动,需要未来联合治疗探索。
值得强调的是,在VERITAC-2研究的ESR1突变人群中,与已上市的Elacestrant或在研的Imlunestrant[8]等新一代口服SERD相比,Vepdegestrant带来的PFS获益在数值上表现突出(中位PFS 5.0 vs 2.1个月),显示出PROTAC技术的潜在突破价值,但跨研究的比较仍需谨慎。
安全可控,口服剂型更加便利
Vepdegestrant的≥3级不良事件发生率为23%,略高于氟维司群组的18%,但整体可控,最常见为疲劳、转氨酶升高、恶心等。因不良事件导致停药率仅3%,且为口服制剂,相较氟维司群的肌注给药,预期在患者依从性和生活质量上有显著优势。
PROTAC 的未来:或重塑治疗格局
Vepdegestrant是首个在III期临床显示对ESR1突变人群具有明确疗效优势的PROTAC药物,为HR+/HER2-晚期乳腺癌带来机制层面的治疗突破,也验证了PROTAC技术的临床可行性。若后续OS数据显示生存获益,Vepdegestrant有望继CDK4/6抑制剂之后,成为改变HR+/HER2-晚期乳腺癌治疗格局的重要新药。未来两大方向值得期待:(1)联合治疗探索:如与PI3K、AKT/mTOR抑制剂或CDK4/6i联合,以突破野生型ER人群的疗效瓶颈;(2)早期疾病应用:Vepdegestrant或有望在HR+/HER2-高复发风险早期乳腺癌中发挥更大潜力。
综上,VERITAC-2研究不仅让我们看到了Vepdegestrant在ESR1突变人群中的治疗希望,更为整个PROTAC技术的临床应用奠定了重要基础,预示着HR+/HER2-晚期乳腺癌治疗可能迈入全新技术跃迁的时代。
曾晓华教授 重庆大学附属肿瘤医院
屈凡力博士后对2025ASCO会议上VERITAC-2临床研究的解读专业且精准。背景部分清晰点明CDK4/6抑制剂耐药后治疗困境及传统SERD局限,引出Vepdegestrant的临床价值。研究设计介绍详实,从纳入标准到治疗方案、评估终点,条理清晰呈现研究架构,为结果解读筑牢基础。在结果解读上,精准聚焦ESR1突变人群关键数据,Vepdegestrant显著延长中位PFS、降低疾病进展风险,凸显其优势,同时兼顾次要终点,丰富疗效证据。对总人群PFS差距未达显著性的情况,合理分析野生型ER患者耐药机制,为联合治疗探索指明方向,彰显对疾病机制的深刻理解。安全性解读全面客观,如实呈现Vepdegestrant组略高的≥3级AEs发生率,强调整体可控性及低停药率,对比口服剂型与肌注给药的患者依从性及生活质量优势,使读者多维度评估其临床价值。对PROTAC技术的介绍及Vepdegestrant未来应用方向的展望,结合研究结果,合理预测发展路径,为领域研究提供新思路。总体而言,屈凡力博士后的解读逻辑严谨、分析透彻、内容全面,展现扎实专业素养与敏锐学术洞察力,助读者快速深入理解研究价值及药物潜力,对临床实践与未来研究具重要启发意义。
[1] Kalinsky K, Accordino M K, Chiuzan C, et al. Randomized Phase II Trial of Endocrine Therapy With or Without Ribociclib After Progression on Cyclin-Dependent Kinase 4/6 Inhibition in Hormone Receptor-Positive, Human Epidermal Growth Factor Receptor 2-Negative Metastatic Breast Cancer: MAINTAIN Trial[J]. J Clin Oncol, 2023, 41(24): 4004-4013.
[2] Kalinsky K, Bianchini G, Hamilton E P, et al. Abemaciclib plus fulvestrant vs fulvestrant alone for HR+, HER2-advanced breast cancer following progression on a prior CDK4/6 inhibitor plus endocrine therapy: Primary outcome of the phase 3 postMONARCH trial.[J]. Journal of Clinical Oncology, 2024, 42(17_Suppl): Lba1001-Lba1001.
[3] Mayer E L, Ren Y, Wagle N, et al. PACE: A Randomized Phase II Study of Fulvestrant, Palbociclib, and Avelumab After Progression on Cyclin-Dependent Kinase 4/6 Inhibitor and Aromatase Inhibitor for Hormone Receptor-Positive/Human Epidermal Growth Factor Receptor-Negative Metastatic Breast Cancer[J]. J Clin Oncol, 2024, 42(17): 2050-2060.
[4] Llombart-Cussac A, Harper-Wynne C, Perello A, et al. Second-Line Endocrine Therapy With or Without Palbociclib Rechallenge in Patients With Hormone Receptor-Positive/Human Epidermal Growth Factor Receptor 2-Negative Advanced Breast Cancer: PALMIRA Trial[J]. J Clin Oncol, 2025, 43(18): 2084-2093.
[5] Sakamoto K M, Kim K B, Kumagai A, et al. Protacs: chimeric molecules that target proteins to the Skp1-Cullin-F box complex for ubiquitination and degradation[J]. Proc Natl Acad Sci U S A, 2001, 98(15): 8554-8559.
[6] Wang C, Zhang Y, Chen W, et al. New-generation advanced PROTACs as potential therapeutic agents in cancer therapy[J]. Mol Cancer, 2024, 23(1): 110.
[7] Herzog S K, Fuqua S a W. ESR1 mutations and therapeutic resistance in metastatic breast cancer: progress and remaining challenges[J]. Br J Cancer, 2022, 126(2): 174-186.
[8] Bardia A, Bidard F C, Neven P, et al. EMERALD phase 3 trial of elacestrant versus standard of care endocrine therapy in patients with ER+/HER2-metastatic breast cancer: Updated results by duration of prior CDK4/6i in metastatic setting[J]. Cancer Research, 2023, 83(5).
【温馨提示】:如果您觉得屈凡力医生解读的好,请在下方为她点赞并将文章分享给更多的同道!当然,您也可以在下方留下您的个人见解哦!












 苏公网安备32059002004080号
苏公网安备32059002004080号


